2024-2025高二下学期期中考试化学模拟卷(含答案)
文档属性
| 名称 | 2024-2025高二下学期期中考试化学模拟卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-11 18:50:56 | ||
图片预览




文档简介
2024-2025高二下学期期中考试 化学模拟卷
一、单选题
1.2024年11月30号,神舟十九号载人飞船发射取得圆满成功。下列说法错误的是
A.硬铝合金作航天飞船材料的原因是硬铝合金密度小,硬度大
B.煤油和液氧作火箭的发射推进剂,煤油、氧气都是纯净物
C.航天飞船的太阳能电池板的主要材料是Si
D.酚醛树脂作飞船返回舱外壳烧蚀材料,酚醛树脂是有机高分子
2.下列说法正确的是
A. 与含有相同的官能团,互为同系物
B.属于醛类,官能团为
C.的名称为:乙基丁烯
D.乙醚与乙醇互为同分异构体
3.下列实验目的对应的实验方案、现象和结论都正确的是
选项 实验目的 实验方案 现象和结论
A 探究食品脱氧剂中还原铁粉是否变质 取少量样品溶于盐酸,滴加KSCN溶液 溶液未变红,说明铁粉未变质
B 证明乙烯的氧化反应 将乙烯通入盛有溴水的试管中 溴水褪色,说明乙烯被溴水氧化
C 检验某纯净气体是否为 将该纯净气体通入盛有品红溶液的试管中 品红溶液褪色,说明该纯净气体是
D 比较、的大小 向溶液中滴加2滴同浓度的溶液,振荡后再加入4滴同浓度的KI溶液 先产生白色沉淀,后白色沉淀转变成黄色沉淀,说明
A.A B.B C.C D.D
4.下列说法正确的是
A.与发生加成反应后的产物具有手性
B.有机物最多有9个原子在同一平面上
C.某烃的键线式为,该烃和 按物质的量之比为1:1加成时,所得产物有5种
D.1-丁烯和2-丁烯属于位置异构,和属于官能团异构
5.下列物质结构与性质或物质性质与用途具有对应关系的是
A.乙二醇易溶于水,可用作汽车防冻液
B.分子间存在氢键,的热稳定性强于
C.甲苯易挥发,可用于制备2,4,6-三硝基甲苯
D.有机物能形成分子间氢键,熔沸点高于
6.设表示阿伏加德罗常数的值,下列说法正确的是
A.苯中碳碳双键的数目为
B.甲基中含有的电子数为
C.己烷中含有的极性键数目为
D.标准状况下,氯仿中所含有的原子数目为
7.下列说法不正确的是
A.只含有一种等效氢的,可命名为2,二甲基丙烷
B.的一氯代物有4种
C.甲基己烯存在顺反异构。
D.二环丁烷()的二溴代物有4种(不考虑立体异构)
8.车叶草苷酸是传统消炎药材闭花耳草的活性成分之一,其结构简式如图所示.下列有关该物质的说法错误的是
A.含有4种含氧官能团
B.可用酸性高锰酸钾溶液检验该物质中存在碳碳双键
C.分子中含有9个手性碳原子
D.该物质与足量钠反应可生成
9.化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列反应制得。
下列有关X、Y、Z的说法不正确的是
A.1molX分子中采取杂化的碳原子数目为7mol
B.Y与足量反应生成的有机化合物中含有手性碳原子
C.1molZ中含有3mol碳氧键
D.X、Y、Z分子中碳原子的轨道杂化类型都既有杂化又有杂化
10.某化学兴趣小组的同学为了检验某种一卤代乙烷中卤素原子的种类,设计了如图所示的实验。该实验设计的错误有
A.1处 B.2处 C.3处 D.4处
11.下列有关DNA和RNA的叙述,正确的是
A.细胞中的DNA通常为双链结构,HIV中的RNA为单链结构
B.组成DNA的碱基与组成RNA的碱基完全不同
C.核苷酸之间的连接方式不同
D.真核细胞中,DNA全部分布在细胞核中,RNA全部分布在细胞质中
12.室温下,下列实验方案能达到相应目的的是
选项 目的
A 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加溶液,观察溶液颜色变化 探究食品脱氧剂样品中有无价铁
B 用计测量等物质的量浓度的醋酸、盐酸的,比较溶液大小 证明是弱电解质
C 向浓中插入红热的炭,观察生成气体的颜色 证明炭可与浓反应生成
D 向淀粉溶液中加适量溶液,加热,冷却后加溶液至碱性,再加少量碘水,观察溶液颜色变化 探究淀粉溶液在稀硫酸和加热条件下是否水解
A.A B.B C.C D.D
13.目前,外科手术常用一种化学合成材料——医用胶代替传统的手术缝合线。某种医用胶的结构简式为(俗称504),下列关于该医用胶的说法错误的是
A.氰基、酯基具有较强的极性,对碳碳双键基团具有活化作用
B.把 504 医用胶结构修饰变为有利于增大降解速率
C.504医用胶在常温下受到人体组织中的水的引发,可较快聚合,该聚合反应为缩聚反应
D.新型医用胶分子()含有两个碳碳双键,可发生交联聚合,形成体型高聚物
14.有一种功能性的聚合物,合成路线如下:
已知:
下列说法不正确的是
A.的分子式为 B.的结构简式是
C.降解后可得到和 D.合成的反应是加聚反应
15.氧化石墨烯在能源、材料等领域具有重要的应用前景。用强氧化剂在石墨层间引入大量基团(如、等)削弱层间作用力得到氧化石墨烯。下列说法正确的是
A.氧化石墨烯有一定的亲水性 B.石墨是一种有机高分子材料
C.石墨层内导电性和层间导电性相同 D.石墨转化成氧化石墨烯是物理变化
16.人造海绵的主要成分是聚氨酯,合成方法如图,下列说法不正确的是
+nHOCH2CH2OH→
A.M的分子式为C15H10N2O2
B.聚氨酯和蛋白质分子的某些化学性质相似
C.聚氨酯在一定条件下能发生水解反应
D.合成聚氨酯的反应属于缩聚反应
17.可降解聚合物Q可由有机物P和反应制备,转化关系如下:
已知:①;
②的结构式为。
依据上述信息,可知下列说法中不正确的是
A.P分子中的所有碳原子可能在同一平面内
B.Q中的官能团为
C.由P制备Q的反应为加聚反应且原子利用率为100%
D.P、Q在一定条件下均能水解且所得产物相同
18.实验室提取桂花精油的流程如下。下列说法错误的是
A.“操作①”所需的玻璃仪器有烧杯、漏斗、玻璃棒
B.“操作②”为过滤,所得的石油醚可循环利用
C.“乙醇洗涤”可提高桂花精油的收率
D.“减压蒸馏”可防止桂花精油在较高温度下变质
二、解答题
19.阿司匹林(乙酰水杨酸)具有解热镇痛、抗风湿等药效,以水杨酸(邻羟基苯甲酸)与乙酸酐为反应物可制取阿司匹林,反应的化学方程式为:
已知反应体系中各物质的性质如下表所示:
物质 相对分子质量 熔点/℃ 沸点/℃ 溶解性
水杨酸 138 158 336 易溶于乙醇,微溶于水
乙酸酐 102 -73 140 易溶于乙醇,溶于水,水解生成乙酸
乙酰水杨酸 180 134 321 溶于乙醇,微溶于冷水,可溶于热水
乙酸 60 — — 与水、乙醇混溶
请回答下列问题。
(1)常温下水杨酸在水中的溶解度(0.2g)小于对羟基苯甲酸(0.5g),从结构角度解释其原因为 。
(2)水杨酸易形成难溶于水的聚合物,该聚合物的结构简式为 。
(3)按下图所示连接装置并加入药品,控制温度80~90℃,加热5~10min。
①仪器a的名称为 。
②三颈烧瓶中3种试剂的加入顺序为 。装置中是否需要加入沸石? (填“是”或“否”)。
③该实验适宜的加热方式为 (填标号)。
A.直接加热 B.水浴加热 C.油浴加热 D.沙浴加热
(4)反应结束后,将反应混合物冷却至室温,再加50mL水,继续在冰水中冷却,直至结晶全部析出为止。减压过滤,洗涤,在空气中放置干燥。
①加水时,发生的主要反应的化学方程式为 。
②洗涤晶体时,应使用的试剂为 。
(5)将上述实验获得的粗品进行提纯,操作名称为 。为了检验提纯后的产品是否仍含有杂质,可取少量结晶加入 (填化学式)溶液中,观察有无显色反应。
(6)实验中使用2.00g水杨酸和5mL乙酸酐(0.05mol),获得xg乙酰水杨酸,则产率为 %(用x表示)。
20.光刻胶是一种应用广泛的光敏材料,其合成路线如图(部分试剂和产物略去):
已知(R1、R2为烃基或氢)
(R3、R4为烃基)
(1)A的化学名称是 ,E的核磁共振氢谱为三组峰,且峰面积之比为3:2:1,E能发生水解反应,则F的结构简式为 。
(2)G分子中所含官能团名称为 ,羧酸X的结构简式为 。
(3)由F到G的反应类型为 。
(4)D和G反应生成光刻胶的化学方程式为 。
(5)C的一种同分异构体满足下列条件:
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②苯环上的一氯取代物只有两种;
该同分异构体的结构简式为 。
21.某芳香烃A是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体G等多种物质。
已知:(1);(2)。
(1)B生成C的反应类型为 ,扁桃酸中官能团的名称 ,其结构中含有 个手性碳。
(2)写出C生成D的化学方程式 。
(3)写出由单体G通过加聚反应所得产物的结构简式 。
(4)扁桃酸有多种同分异构体,同时满足下列条件的同分异构体有 (不考虑立体异构)种。其中核磁共振氢谱有五组峰,且峰面积比为2:2:2:1:1的结构简式为 。
①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
③遇FeCl3溶液显紫色
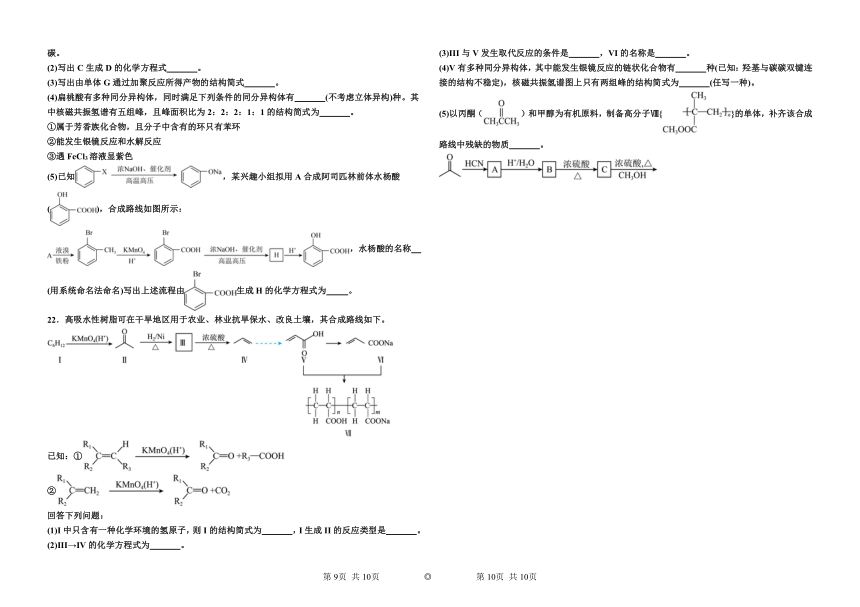
(5)已知,某兴趣小组拟用A合成阿司匹林前体水杨酸(),合成路线如图所示:,水杨酸的名称 (用系统命名法命名)写出上述流程由生成H的化学方程式为 。
22.高吸水性树脂可在干旱地区用于农业、林业抗旱保水、改良土壤,其合成路线如下。
已知:①
②
回答下列问题:
(1)I中只含有一种化学环境的氢原子,则I的结构简式为 ,I生成II的反应类型是 。
(2)III→IV的化学方程式为 。
(3)III与V发生取代反应的条件是 ,VI的名称是 。
(4)V有多种同分异构体,其中能发生银镜反应的链状化合物有 种(已知:羟基与碳碳双键连接的结构不稳定),核磁共振氢谱图上只有两组峰的结构简式为 (任写一种)。
(5)以丙酮()和甲醇为有机原料,制备高分子Ⅷ{}的单体,补齐该合成路线中残缺的物质 。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
《2024-2025高二下学期期中考试 化学模拟卷》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 B C D D D C B B C A
题号 11 12 13 14 15 16 17 18
答案 A B C C A D D B
1.B
【详解】A.硬铝合金具有密度小的特点,这样可以减轻航天飞船的重量,有利于发射,同时硬度大,能保证航天飞船在复杂的太空环境中具有良好的结构稳定性,所以硬铝合金常被用作航天飞船材料,A正确;
B.煤油是石油分馏的产物,是C11~C16烷烃组成的混合物,B错误;
C.硅是一种良好的半导体材料,太阳能电池板主要利用硅将太阳能转化为电能,所以航天飞船的太阳能电池板主要材料是Si,C正确;
D.酚醛树脂是由酚类和醛类通过缩聚反应制成的有机高分子化合物,它具有良好的耐高温等性能,可作飞船返回舱外壳烧蚀材料,D正确;
故选B。
2.C
【详解】
A.属于醇,含醇羟基,属于酚,含酚羟基,两者物质类别不固体,不互为同系物,故A错误;
B.属于酯类,官能团为 COO R,故B错误;
C.主链为含碳碳双键的最长碳链,其名称为: 2 乙基 1 丁烯,故C正确;
D.乙醚是CH3CH2OCH2CH3,乙醇是CH3CH2OH,两者分子式不相同,不互为同分异构体,故D错误;
故答案为C。
3.D
【详解】A.滴加KSCN溶液,溶液未变红,可能是变质的被铁粉还原了,A错误;
B.乙烯与溴水中的溴发生的反应是加成反应,要证明乙烯的氧化反应,应将乙烯通入盛有酸性溶液的试管中,B错误;
C.能使品红溶液褪色的气体不一定是,,等气体也能使品红溶液褪色,C错误;
D.溶液和溶液反应,先生成白色沉淀,由于溶液过量,再加入少量同浓度的溶液,白色沉淀转变成黄色沉淀,说明氯化银转化为碘化银,即可说明,D正确;
故选D。
4.D
【详解】
A.与氢气加成后的产物为,该分子不具有手性,故A错误;
B.有机物中,苯环和碳碳双键(三键)都可以在同一个平面上,中可以有3个原子共面(包含R中一个原子),故最多有22个原子共面,如图所示:,故B错误;
C.和 按物质的量之比为1:1加成时,可以发生1,2-加成,产物为:、、,也可以发生1,4-加成,产物为:,共有4种,故C错误;
D.1-丁烯和2-丁烯,双键位置不一样,属于位置异构,和官能团不一样,属于官能团异构,故D正确;
故选D。
5.D
【详解】A.乙二醇沸点高,熔点低,可以降低水的凝固点,可用作汽车防冻液,与乙二醇易溶于水无关,A不符合题意;
B.和的稳定性与分子内的化学键的键能有关,与分子间氢键无关,B不符合题意;
C.由于受到甲基对苯环的影响,可利用甲苯与浓硝酸发生取代反应制备2,4,6-三硝基甲苯,该性质与甲苯易挥发无关,C不符合题意;
D.有机物能形成分子间氢键,故熔沸点高于,D符合题意;
故选D。
6.C
【详解】A.已知苯分子中六个碳碳键均为介于单键和双键之间独特的键,苯环中不存在双键,故1mol 苯中碳碳双键的数目为0,A错误;
B.已知甲基为不带电的原子团,一个甲基中含有9个电子,则1.5g 甲基中含有的电子数为,B错误;
C.已知己烷的分子式为C6H14,其中含有C-H极性键,即1分子己烷中含有14个极性键,则0.5 mol己烷中含有的极性键数目为0.5mol×14×NAmol-1=7NA,C正确;
D.由于标准状况下,氯仿为液体,故无法计算标准状况下11.2L氯仿中所含有的原子数目,D错误;
故选C。
7.B
【详解】A.有正戊烷、异戊烷和新戊烷三种同分异构体,新戊烷C(CH3)4结构高度对称,只含有一种等效氢,系统命名法为2,2-二甲基丙烷,A正确;
B.分析所给有机物的结构,分子中含有 5 种不同化学环境的氢原子(与甲基相连的碳原子上的氢、甲基上的氢,以及环上 3 种不同位置的氢 ),所以其一氯代物有 5 种,而不是 4 种,B错误;
C.2-甲基-3-己烯的结构简式为 ,碳碳双键两端的碳原子均连接不同的原子或原子团,存在顺反异构,C正确;
D.二环[1.1.0] ()丁烷的结构中,两个溴原子的取代情况:① 两个溴原子在同一个碳原子上,有 1 种;② 两个溴原子在不同碳原子上,有 3 种(相邻碳原子间 2 种、相间碳原子间 1 种 ),共 4 种二溴代物(不考虑立体异构 ),D正确;
故选B。
8.B
【详解】A.该物质含有酯基、羟基、羧基、醚键4种含氧官能团,A正确;
B.羟基、碳碳双键均能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故不能用酸性高锰酸钾溶液检验该物质中存在碳碳双键,B错误;
C.连接四个互不相同的原子或原子团的碳原子是手性碳原子,分子中含有9个手性碳原子,,C正确;
D.该物质中只有羟基和羧基能与钠发生反应,该分子中含有5个羟基和1个羧基,所以该物质与足量钠反应可生成,D正确。
故选B。
9.C
【详解】A.X分子中苯环上的6个碳原子和醛基中的碳原子均采取杂化,共7个,所以1molX分子中采取杂化的碳原子数目为7mol,A正确;
B.Y与足量HBr反应时,碳碳双键发生加成反应,生成的有机化合物中与-Br相连的碳原子连有4个不同原子或原子团,是手性碳原子,如图:或,B正确;
C.Z分子中含有1个碳碳双键和1个酯基,酯基中含1个碳氧键,所以1molZ中含有1mol碳氧键,C错误;
D.X、Y、Z分子中苯环及碳碳双键、羰基、酯基上的碳原子采取杂化,和中的碳原子采取杂化,即碳原子的轨道杂化类型都既有杂化又有杂化,D正确;
故选C。
10.A
【详解】为检验一卤代乙烷中卤素原子的种类,将其在醇溶液中加热使之发生消去反应,然后应加入稀硝酸中和,避免与反应干扰卤素原子的检验,该实验设计有1处错误,即滴加硝酸银溶液之前应加入足量的稀硝酸酸化,A项符合题意。
11.A
【详解】A.DNA是双螺旋结构,RNA一般为单链结构,A正确;
B.组成DNA的碱基与组成RNA的碱基部分不同,组成DNA的碱基有A、G、C、T,组成RNA的碱基有A、G、C、U,只有一个碱基不同,B错误;
C.DNA与RNA的核苷酸之间的连接方式相同,均是戊糖和磷酸交替连接,C错误;
D.真核细胞中DNA主要分布在细胞核中,在线粒体和叶绿体中也有少量分布,RNA主要分布在细胞质中,D错误;
故选A。
12.B
【详解】A.食品脱氧剂样品中的还原铁粉可能未完全变质,剩余较多铁粉,溶于盐酸后,多余的铁粉将反应得到的氯化铁还原为二价铁,加入硫氰化钾,溶液无色,方案不能不能检测出三价铁,A选项错误;
B.一元弱酸部分电离,一元强酸全部电离,用计测量等物质的量浓度的醋酸、盐酸的,醋酸溶液较大,存在电离平衡,盐酸pH较小,可证明是弱电解质,B选项正确;
C.浓硝酸见光或者受热会分解生成NO2,不一定是碳单质与浓硝酸的反应,C选项错误;
D.淀粉在酸性条件下加热水解得到葡萄糖,葡萄糖在碱性条件下,可用新制氢氧化铜溶液检验,而不是用碘水检验,D选项错误;
故答案选B。
13.C
【详解】A.氰基、酯基具有较强的极性,使碳碳双键活化从而更易发生加聚反应,A项正确;
B.酯基容易水解,有利于加快医用胶使用后的降解速率,B项正确;
C.504医用胶在常温下受到人体组织中的水的引发,可较快聚合,该聚合反应为加聚反应,C项错误;
D.分子中含有两个碳碳双键,可发生交联聚合,形成体型高聚物,有助于增强医用胶的耐水、耐热、抗冷热交替等性能,D项正确。
故选C。
14.C
【详解】A.由图可知,E的分子式为,A正确;
B.结合E、P结构和题给已知可知,形成高分子化合物P的单体之一F的结构简式是 ,B正确;
C.降解后,其中的酯基发生反应,不能得到E和F,C错误;
D.结合题给已知,E和F反应生成P的过程中没有生成小分子化合物,为加聚反应,D正确;
故选C。
15.A
【详解】A.氧化石墨烯中含有羟基和羧基,能够和水分子形成氢键,有一定的亲水性,A正确;
B.石墨仅由碳原子构成,是无机物,不是有机高分子材料,B错误;
C.在石墨烯中,每个碳原子都贡献出一个未成键的电子,这些电子形成了一个大π键,电子可以在整个层面内自由移动,使得石墨烯在层内具有优异的导电性,石墨烯层与层之间是通过较弱的范德华力相互作用的,这种力不足以支持电子在层间自由传输,石墨烯的层间导电性相对较弱,C错误;
D.石墨转化成氧化石墨烯的过程中生成了新的物质,是化学变化,D错误;
故选A。
16.D
【详解】A.根据M的结构简式,其分子式为C15H10N2O2,A正确;
B.聚氨酯和蛋白质分子中均含有酰胺基,则某些化学性质相似,如水解,B正确;
C.聚氨酯中含有酯基和酰胺基,在一定条件下能发生水解反应,C正确;
D.合成聚氨酯的反应中,M中的碳氮双键与乙二醇中羟基的H原子、O原子发生加成反应,属于加成聚合反应,D错误;
故选D。
17.D
【详解】A.P分子中苯环侧链上的C之间形成的键为单键,可旋转,分子中的所有碳原子可能在同一平面内,A不符合题意;
B.Q中官能团为(酯基),B不符合题意;
C.由P制备高分子Q时,无其他产物生成,反应为加聚反应且原子利用率为100%,C不符合题意;
D.P在一定条件下与水反应生成,Q在一定条件下水解生成、,所得产物不完全相同,D符合题意;
故选D。
18.B
【分析】向桂花中加入石油醚,充分振荡,过滤,分离除去不溶物,得到溶液,然后根据物质沸点的不同,将溶液进行蒸馏,分离出沸点低的石油醚和桂花浸膏,再向桂花浸膏中加入无水乙醇回流1小时,进行抽滤,并用乙醇洗涤固体残渣,充分回收桂花精油,将分离得到溶液进行减压蒸馏,分离得到桂花精油。
【详解】A.“操作①”是分离难溶性固体与可溶性液体混合物的操作,该操作名称为过滤,所需的玻璃仪器有烧杯、漏斗、玻璃棒,A正确;
B.“操作②”为分离互溶的、沸点不同的混合物,名称为蒸馏,所得的沸点较低的石油醚可循环利用,B错误;
C.残留在固体上的桂花精油能够溶于乙醇,“乙醇洗涤”抽滤时的固体残渣,可提高桂花精油的收率,C正确;
D.桂花精油不稳定,高温易变质。利用物质沸点随压强的减小而降低的性质进行“减压蒸馏”就可防止桂花精油在较高温度下变质,D正确;
故合理选项是B。
19.(1)水杨酸中羟基和羧基相邻,易形成分子内氢键,与水分子结合的能力弱于对羟基苯甲酸
(2)
(3) 球形冷凝管 水杨酸、乙酸酐、浓硫酸 否 B
(4) 冷水
(5) 重结晶
(6)
【分析】实验室以水杨酸和乙酸酐为原料合成阿司匹林,取适量水杨酸、乙酸酐和浓硫酸混合摇匀,控制温度加热,冷却反应液、倒入冷水中并用冰水浴冷却、过滤、洗涤得到粗产品。
【详解】(1)水杨酸分子中羟基和羧基相邻,易形成分子内氢键,与水分子结合的能力弱于对羟基苯甲酸,因此水杨酸在水中的溶解度小于对羟基苯甲酸;
(2)水杨酸分子中含有羟基和羧基,可发生缩聚反应生成聚合物,结构简式为;
(3)①图中仪器a的名称为球形冷凝管;
②向三颈烧瓶中加入试剂时,首先应加入固态试剂水杨酸,然后加入液态试剂乙酸酐,再加入浓硫酸并不断搅拌,防止因温度升高而发生副反应。装置中有搅拌棒,不需要加入沸石;
③该实验加热温度为80~90℃,因此适宜的加热方式为水浴加热;
(4)①加水时,乙酸酐发生水解反应生成乙酸,化学方程式为;
②为洗掉乙酸并减小乙酰水杨酸的溶解损失,应使用冷水洗涤晶体;
(5)实验获得的乙酰水杨酸中含有水杨酸,根据二者在不同温度下溶解度的差异,可采用重结晶的方法进行提纯。杂质水杨酸分子中含有羟基,能与溶液发生显色反应,因此可取少量结晶加入溶液中,观察有无显色反应,即可检验产品是否纯净;
(6)实验中使用的乙酸酐过量,则按照水杨酸的用量计算乙酰水杨酸的产率为。
20.(1) 苯甲醛
(2) 羟基 CH3COOH
(3)取代反应或水解反应
(4)
(5)
【分析】
由D的结构可知,A中含有苯环,A与CH3CHO反应得到B,由物质B的分子式及信息Ⅰ,可推知A为,B为,B与银氨溶液或新制氢氧化铜悬浊液发生氧化反应、酸化得到C,则C为。C发生取代反应得到D.结合G的结构可知,乙炔和羧酸X加成生成E,E发生加聚反应得到F,则且结合小问1中关于E的信息:E的核磁共振氢谱为三组峰即分子内有3种氢,且峰面积之比为3:2:1、即氢原子数目之比为3:2:1,E能发生水解反应,则含酯基,E分子中含有碳碳双键,结合分子式可知,X为CH3COOH,E为CH3COOCH=CH2,F为,G与D发生第二个信息反应得到光刻胶,则光刻胶的结构简式为:。
【详解】(1)
据分析,A为,A的名称为:苯甲醛;F的结构简式为。
(2)据分析,G 分子中所含官能团名称为:羟基。羧酸 X的结构简式为CH3COOH。
(3)由F到G为酯基水解,反应类型为取代反应。
(4)
据第二个信息反应,D 和 G 反应生成光刻胶同时得到氯化氢气体,化学方程式为:。
(5)
C的一种同分异构体满足下列条件:①能发生银镜反应,其水解产物之一能与 FeCl3溶液发生显色反应,说明含有甲酸形成的酯基、且水解后生成酚羟基;②苯环上的一氯取代产物只有两种,则有2个不同的取代基处于对位,该同分异构体的结构简式为:。
21.(1) 水解反应或取代反应 羟基和羧基 1
(2)2+O22+2H2O
(3)
(4) 13
(5) 2-羟基苯甲酸 +3NaOH+NaBr+2H2O
【分析】
芳香烃A分子式为C7H8,则A为,则A与氯气在光照条件下发生甲基上的取代反应生成B,根据扁桃酸的结构简式可知B为 ,B水解得到C,C为,C氧化得到D,D为,结合扁桃酸的结构简式和已知(1)的反应可知E为,F的分子式为C8H8O,结合F后面物质的结构可知F为,根据已知(2)的反应可知G的结构简式为。
【详解】(1)
B为 ,C为,B生成C的反应类型为水解反应或取代反应;扁桃酸中官能团的名称为:羟基和羧基;分子中连有4个不同原子或原子团的碳原子为手性碳,故含有1个手性碳,即连羟基和羧基的碳原子;
(2)
C为,C氧化得到D,D为,化学方程式为:2+O22+2H2O;
(3)
G的结构简式为,通过加聚反应生成的产物的结构简式为;
(4)
扁桃酸的结构简式为,其同分异构体满足如下条件:①属于芳香族化合物,且分子中含有的环只有苯环;③遇FeCl3溶液显紫色,说明含有酚羟基;②能发生银镜反应和水解反应,说明含有醛基和酯基;结合O的个数可知应该含有甲酸酯的结构,如果含有-OH和-CH2OOCH两个取代基,则有3种位置,如果是-OH、-OOCH、-CH3三个取代基,共有10种位置,故共有13种同分异构体;其中核磁共振氢谱有五组峰,且峰面积比为2:2:2:1:1,说明为对称结构,且不含有甲基,故符合条件的结构简式为;;
(5)
水杨酸的结构简式为,用系统命名法命名水杨酸为:2-羟基苯甲酸;根据已知的信息,由生成H的化学方程式为+3NaOH+NaBr+2H2O。
22.(1) 氧化反应
(2)
(3) 浓硫酸、加热 丙烯酸钠
(4) 3 (或)
(5)、、
【分析】根据已知信息①知,I中发生氧化反应,则I中含有碳碳双键,再结合问题(1)所给信息知,I为,II和氢气发生加成反应得到III,III为,III→IV发生醇的消去反应,IV经一系列的变化可得到V,V和氢氧化钠反应可得到VI,VI为丙烯酸钠,V和VI发生加聚反应可得到VII。
【详解】(1)I的化学式C6H12,其中含有一种化学环境的氢原子,结合已知信息①知,
I的结构简式为,I→II过程中I被酸性高锰酸钾溶液氧化,反应类型为氧化反应。
(2)II和氢气发生加成反应得到III,III为,III→IV发生醇的消去反应,化学方程式为。
(3)III属于醇类,V属于羧酸类,二者发生取代反应的条件是浓硫酸、加热;VI为,名称是丙烯酸钠。
(4)V为,其同分异构体能发生银镜反应,说明含“-CHO”,共有、、这3种链状化合物符合题意。其中核磁共振氢谱图上只有两组峰的结构简式为(或)。
(5)
合成路线中丙酮和HCN先发生加成反应得到A,A为,在酸性条件下发生水解得到B,B为,在浓硫酸、加热的条件下发生醇的消去反应得到C,C为,最后和甲醇在浓硫酸、加热的条件下发生酯化反应即可得到高分子VIII的单体。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.2024年11月30号,神舟十九号载人飞船发射取得圆满成功。下列说法错误的是
A.硬铝合金作航天飞船材料的原因是硬铝合金密度小,硬度大
B.煤油和液氧作火箭的发射推进剂,煤油、氧气都是纯净物
C.航天飞船的太阳能电池板的主要材料是Si
D.酚醛树脂作飞船返回舱外壳烧蚀材料,酚醛树脂是有机高分子
2.下列说法正确的是
A. 与含有相同的官能团,互为同系物
B.属于醛类,官能团为
C.的名称为:乙基丁烯
D.乙醚与乙醇互为同分异构体
3.下列实验目的对应的实验方案、现象和结论都正确的是
选项 实验目的 实验方案 现象和结论
A 探究食品脱氧剂中还原铁粉是否变质 取少量样品溶于盐酸,滴加KSCN溶液 溶液未变红,说明铁粉未变质
B 证明乙烯的氧化反应 将乙烯通入盛有溴水的试管中 溴水褪色,说明乙烯被溴水氧化
C 检验某纯净气体是否为 将该纯净气体通入盛有品红溶液的试管中 品红溶液褪色,说明该纯净气体是
D 比较、的大小 向溶液中滴加2滴同浓度的溶液,振荡后再加入4滴同浓度的KI溶液 先产生白色沉淀,后白色沉淀转变成黄色沉淀,说明
A.A B.B C.C D.D
4.下列说法正确的是
A.与发生加成反应后的产物具有手性
B.有机物最多有9个原子在同一平面上
C.某烃的键线式为,该烃和 按物质的量之比为1:1加成时,所得产物有5种
D.1-丁烯和2-丁烯属于位置异构,和属于官能团异构
5.下列物质结构与性质或物质性质与用途具有对应关系的是
A.乙二醇易溶于水,可用作汽车防冻液
B.分子间存在氢键,的热稳定性强于
C.甲苯易挥发,可用于制备2,4,6-三硝基甲苯
D.有机物能形成分子间氢键,熔沸点高于
6.设表示阿伏加德罗常数的值,下列说法正确的是
A.苯中碳碳双键的数目为
B.甲基中含有的电子数为
C.己烷中含有的极性键数目为
D.标准状况下,氯仿中所含有的原子数目为
7.下列说法不正确的是
A.只含有一种等效氢的,可命名为2,二甲基丙烷
B.的一氯代物有4种
C.甲基己烯存在顺反异构。
D.二环丁烷()的二溴代物有4种(不考虑立体异构)
8.车叶草苷酸是传统消炎药材闭花耳草的活性成分之一,其结构简式如图所示.下列有关该物质的说法错误的是
A.含有4种含氧官能团
B.可用酸性高锰酸钾溶液检验该物质中存在碳碳双键
C.分子中含有9个手性碳原子
D.该物质与足量钠反应可生成
9.化合物Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列反应制得。
下列有关X、Y、Z的说法不正确的是
A.1molX分子中采取杂化的碳原子数目为7mol
B.Y与足量反应生成的有机化合物中含有手性碳原子
C.1molZ中含有3mol碳氧键
D.X、Y、Z分子中碳原子的轨道杂化类型都既有杂化又有杂化
10.某化学兴趣小组的同学为了检验某种一卤代乙烷中卤素原子的种类,设计了如图所示的实验。该实验设计的错误有
A.1处 B.2处 C.3处 D.4处
11.下列有关DNA和RNA的叙述,正确的是
A.细胞中的DNA通常为双链结构,HIV中的RNA为单链结构
B.组成DNA的碱基与组成RNA的碱基完全不同
C.核苷酸之间的连接方式不同
D.真核细胞中,DNA全部分布在细胞核中,RNA全部分布在细胞质中
12.室温下,下列实验方案能达到相应目的的是
选项 目的
A 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加溶液,观察溶液颜色变化 探究食品脱氧剂样品中有无价铁
B 用计测量等物质的量浓度的醋酸、盐酸的,比较溶液大小 证明是弱电解质
C 向浓中插入红热的炭,观察生成气体的颜色 证明炭可与浓反应生成
D 向淀粉溶液中加适量溶液,加热,冷却后加溶液至碱性,再加少量碘水,观察溶液颜色变化 探究淀粉溶液在稀硫酸和加热条件下是否水解
A.A B.B C.C D.D
13.目前,外科手术常用一种化学合成材料——医用胶代替传统的手术缝合线。某种医用胶的结构简式为(俗称504),下列关于该医用胶的说法错误的是
A.氰基、酯基具有较强的极性,对碳碳双键基团具有活化作用
B.把 504 医用胶结构修饰变为有利于增大降解速率
C.504医用胶在常温下受到人体组织中的水的引发,可较快聚合,该聚合反应为缩聚反应
D.新型医用胶分子()含有两个碳碳双键,可发生交联聚合,形成体型高聚物
14.有一种功能性的聚合物,合成路线如下:
已知:
下列说法不正确的是
A.的分子式为 B.的结构简式是
C.降解后可得到和 D.合成的反应是加聚反应
15.氧化石墨烯在能源、材料等领域具有重要的应用前景。用强氧化剂在石墨层间引入大量基团(如、等)削弱层间作用力得到氧化石墨烯。下列说法正确的是
A.氧化石墨烯有一定的亲水性 B.石墨是一种有机高分子材料
C.石墨层内导电性和层间导电性相同 D.石墨转化成氧化石墨烯是物理变化
16.人造海绵的主要成分是聚氨酯,合成方法如图,下列说法不正确的是
+nHOCH2CH2OH→
A.M的分子式为C15H10N2O2
B.聚氨酯和蛋白质分子的某些化学性质相似
C.聚氨酯在一定条件下能发生水解反应
D.合成聚氨酯的反应属于缩聚反应
17.可降解聚合物Q可由有机物P和反应制备,转化关系如下:
已知:①;
②的结构式为。
依据上述信息,可知下列说法中不正确的是
A.P分子中的所有碳原子可能在同一平面内
B.Q中的官能团为
C.由P制备Q的反应为加聚反应且原子利用率为100%
D.P、Q在一定条件下均能水解且所得产物相同
18.实验室提取桂花精油的流程如下。下列说法错误的是
A.“操作①”所需的玻璃仪器有烧杯、漏斗、玻璃棒
B.“操作②”为过滤,所得的石油醚可循环利用
C.“乙醇洗涤”可提高桂花精油的收率
D.“减压蒸馏”可防止桂花精油在较高温度下变质
二、解答题
19.阿司匹林(乙酰水杨酸)具有解热镇痛、抗风湿等药效,以水杨酸(邻羟基苯甲酸)与乙酸酐为反应物可制取阿司匹林,反应的化学方程式为:
已知反应体系中各物质的性质如下表所示:
物质 相对分子质量 熔点/℃ 沸点/℃ 溶解性
水杨酸 138 158 336 易溶于乙醇,微溶于水
乙酸酐 102 -73 140 易溶于乙醇,溶于水,水解生成乙酸
乙酰水杨酸 180 134 321 溶于乙醇,微溶于冷水,可溶于热水
乙酸 60 — — 与水、乙醇混溶
请回答下列问题。
(1)常温下水杨酸在水中的溶解度(0.2g)小于对羟基苯甲酸(0.5g),从结构角度解释其原因为 。
(2)水杨酸易形成难溶于水的聚合物,该聚合物的结构简式为 。
(3)按下图所示连接装置并加入药品,控制温度80~90℃,加热5~10min。
①仪器a的名称为 。
②三颈烧瓶中3种试剂的加入顺序为 。装置中是否需要加入沸石? (填“是”或“否”)。
③该实验适宜的加热方式为 (填标号)。
A.直接加热 B.水浴加热 C.油浴加热 D.沙浴加热
(4)反应结束后,将反应混合物冷却至室温,再加50mL水,继续在冰水中冷却,直至结晶全部析出为止。减压过滤,洗涤,在空气中放置干燥。
①加水时,发生的主要反应的化学方程式为 。
②洗涤晶体时,应使用的试剂为 。
(5)将上述实验获得的粗品进行提纯,操作名称为 。为了检验提纯后的产品是否仍含有杂质,可取少量结晶加入 (填化学式)溶液中,观察有无显色反应。
(6)实验中使用2.00g水杨酸和5mL乙酸酐(0.05mol),获得xg乙酰水杨酸,则产率为 %(用x表示)。
20.光刻胶是一种应用广泛的光敏材料,其合成路线如图(部分试剂和产物略去):
已知(R1、R2为烃基或氢)
(R3、R4为烃基)
(1)A的化学名称是 ,E的核磁共振氢谱为三组峰,且峰面积之比为3:2:1,E能发生水解反应,则F的结构简式为 。
(2)G分子中所含官能团名称为 ,羧酸X的结构简式为 。
(3)由F到G的反应类型为 。
(4)D和G反应生成光刻胶的化学方程式为 。
(5)C的一种同分异构体满足下列条件:
①能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应;
②苯环上的一氯取代物只有两种;
该同分异构体的结构简式为 。
21.某芳香烃A是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药中间体G等多种物质。
已知:(1);(2)。
(1)B生成C的反应类型为 ,扁桃酸中官能团的名称 ,其结构中含有 个手性碳。
(2)写出C生成D的化学方程式 。
(3)写出由单体G通过加聚反应所得产物的结构简式 。
(4)扁桃酸有多种同分异构体,同时满足下列条件的同分异构体有 (不考虑立体异构)种。其中核磁共振氢谱有五组峰,且峰面积比为2:2:2:1:1的结构简式为 。
①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
③遇FeCl3溶液显紫色
(5)已知,某兴趣小组拟用A合成阿司匹林前体水杨酸(),合成路线如图所示:,水杨酸的名称 (用系统命名法命名)写出上述流程由生成H的化学方程式为 。
22.高吸水性树脂可在干旱地区用于农业、林业抗旱保水、改良土壤,其合成路线如下。
已知:①
②
回答下列问题:
(1)I中只含有一种化学环境的氢原子,则I的结构简式为 ,I生成II的反应类型是 。
(2)III→IV的化学方程式为 。
(3)III与V发生取代反应的条件是 ,VI的名称是 。
(4)V有多种同分异构体,其中能发生银镜反应的链状化合物有 种(已知:羟基与碳碳双键连接的结构不稳定),核磁共振氢谱图上只有两组峰的结构简式为 (任写一种)。
(5)以丙酮()和甲醇为有机原料,制备高分子Ⅷ{}的单体,补齐该合成路线中残缺的物质 。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
《2024-2025高二下学期期中考试 化学模拟卷》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 B C D D D C B B C A
题号 11 12 13 14 15 16 17 18
答案 A B C C A D D B
1.B
【详解】A.硬铝合金具有密度小的特点,这样可以减轻航天飞船的重量,有利于发射,同时硬度大,能保证航天飞船在复杂的太空环境中具有良好的结构稳定性,所以硬铝合金常被用作航天飞船材料,A正确;
B.煤油是石油分馏的产物,是C11~C16烷烃组成的混合物,B错误;
C.硅是一种良好的半导体材料,太阳能电池板主要利用硅将太阳能转化为电能,所以航天飞船的太阳能电池板主要材料是Si,C正确;
D.酚醛树脂是由酚类和醛类通过缩聚反应制成的有机高分子化合物,它具有良好的耐高温等性能,可作飞船返回舱外壳烧蚀材料,D正确;
故选B。
2.C
【详解】
A.属于醇,含醇羟基,属于酚,含酚羟基,两者物质类别不固体,不互为同系物,故A错误;
B.属于酯类,官能团为 COO R,故B错误;
C.主链为含碳碳双键的最长碳链,其名称为: 2 乙基 1 丁烯,故C正确;
D.乙醚是CH3CH2OCH2CH3,乙醇是CH3CH2OH,两者分子式不相同,不互为同分异构体,故D错误;
故答案为C。
3.D
【详解】A.滴加KSCN溶液,溶液未变红,可能是变质的被铁粉还原了,A错误;
B.乙烯与溴水中的溴发生的反应是加成反应,要证明乙烯的氧化反应,应将乙烯通入盛有酸性溶液的试管中,B错误;
C.能使品红溶液褪色的气体不一定是,,等气体也能使品红溶液褪色,C错误;
D.溶液和溶液反应,先生成白色沉淀,由于溶液过量,再加入少量同浓度的溶液,白色沉淀转变成黄色沉淀,说明氯化银转化为碘化银,即可说明,D正确;
故选D。
4.D
【详解】
A.与氢气加成后的产物为,该分子不具有手性,故A错误;
B.有机物中,苯环和碳碳双键(三键)都可以在同一个平面上,中可以有3个原子共面(包含R中一个原子),故最多有22个原子共面,如图所示:,故B错误;
C.和 按物质的量之比为1:1加成时,可以发生1,2-加成,产物为:、、,也可以发生1,4-加成,产物为:,共有4种,故C错误;
D.1-丁烯和2-丁烯,双键位置不一样,属于位置异构,和官能团不一样,属于官能团异构,故D正确;
故选D。
5.D
【详解】A.乙二醇沸点高,熔点低,可以降低水的凝固点,可用作汽车防冻液,与乙二醇易溶于水无关,A不符合题意;
B.和的稳定性与分子内的化学键的键能有关,与分子间氢键无关,B不符合题意;
C.由于受到甲基对苯环的影响,可利用甲苯与浓硝酸发生取代反应制备2,4,6-三硝基甲苯,该性质与甲苯易挥发无关,C不符合题意;
D.有机物能形成分子间氢键,故熔沸点高于,D符合题意;
故选D。
6.C
【详解】A.已知苯分子中六个碳碳键均为介于单键和双键之间独特的键,苯环中不存在双键,故1mol 苯中碳碳双键的数目为0,A错误;
B.已知甲基为不带电的原子团,一个甲基中含有9个电子,则1.5g 甲基中含有的电子数为,B错误;
C.已知己烷的分子式为C6H14,其中含有C-H极性键,即1分子己烷中含有14个极性键,则0.5 mol己烷中含有的极性键数目为0.5mol×14×NAmol-1=7NA,C正确;
D.由于标准状况下,氯仿为液体,故无法计算标准状况下11.2L氯仿中所含有的原子数目,D错误;
故选C。
7.B
【详解】A.有正戊烷、异戊烷和新戊烷三种同分异构体,新戊烷C(CH3)4结构高度对称,只含有一种等效氢,系统命名法为2,2-二甲基丙烷,A正确;
B.分析所给有机物的结构,分子中含有 5 种不同化学环境的氢原子(与甲基相连的碳原子上的氢、甲基上的氢,以及环上 3 种不同位置的氢 ),所以其一氯代物有 5 种,而不是 4 种,B错误;
C.2-甲基-3-己烯的结构简式为 ,碳碳双键两端的碳原子均连接不同的原子或原子团,存在顺反异构,C正确;
D.二环[1.1.0] ()丁烷的结构中,两个溴原子的取代情况:① 两个溴原子在同一个碳原子上,有 1 种;② 两个溴原子在不同碳原子上,有 3 种(相邻碳原子间 2 种、相间碳原子间 1 种 ),共 4 种二溴代物(不考虑立体异构 ),D正确;
故选B。
8.B
【详解】A.该物质含有酯基、羟基、羧基、醚键4种含氧官能团,A正确;
B.羟基、碳碳双键均能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故不能用酸性高锰酸钾溶液检验该物质中存在碳碳双键,B错误;
C.连接四个互不相同的原子或原子团的碳原子是手性碳原子,分子中含有9个手性碳原子,,C正确;
D.该物质中只有羟基和羧基能与钠发生反应,该分子中含有5个羟基和1个羧基,所以该物质与足量钠反应可生成,D正确。
故选B。
9.C
【详解】A.X分子中苯环上的6个碳原子和醛基中的碳原子均采取杂化,共7个,所以1molX分子中采取杂化的碳原子数目为7mol,A正确;
B.Y与足量HBr反应时,碳碳双键发生加成反应,生成的有机化合物中与-Br相连的碳原子连有4个不同原子或原子团,是手性碳原子,如图:或,B正确;
C.Z分子中含有1个碳碳双键和1个酯基,酯基中含1个碳氧键,所以1molZ中含有1mol碳氧键,C错误;
D.X、Y、Z分子中苯环及碳碳双键、羰基、酯基上的碳原子采取杂化,和中的碳原子采取杂化,即碳原子的轨道杂化类型都既有杂化又有杂化,D正确;
故选C。
10.A
【详解】为检验一卤代乙烷中卤素原子的种类,将其在醇溶液中加热使之发生消去反应,然后应加入稀硝酸中和,避免与反应干扰卤素原子的检验,该实验设计有1处错误,即滴加硝酸银溶液之前应加入足量的稀硝酸酸化,A项符合题意。
11.A
【详解】A.DNA是双螺旋结构,RNA一般为单链结构,A正确;
B.组成DNA的碱基与组成RNA的碱基部分不同,组成DNA的碱基有A、G、C、T,组成RNA的碱基有A、G、C、U,只有一个碱基不同,B错误;
C.DNA与RNA的核苷酸之间的连接方式相同,均是戊糖和磷酸交替连接,C错误;
D.真核细胞中DNA主要分布在细胞核中,在线粒体和叶绿体中也有少量分布,RNA主要分布在细胞质中,D错误;
故选A。
12.B
【详解】A.食品脱氧剂样品中的还原铁粉可能未完全变质,剩余较多铁粉,溶于盐酸后,多余的铁粉将反应得到的氯化铁还原为二价铁,加入硫氰化钾,溶液无色,方案不能不能检测出三价铁,A选项错误;
B.一元弱酸部分电离,一元强酸全部电离,用计测量等物质的量浓度的醋酸、盐酸的,醋酸溶液较大,存在电离平衡,盐酸pH较小,可证明是弱电解质,B选项正确;
C.浓硝酸见光或者受热会分解生成NO2,不一定是碳单质与浓硝酸的反应,C选项错误;
D.淀粉在酸性条件下加热水解得到葡萄糖,葡萄糖在碱性条件下,可用新制氢氧化铜溶液检验,而不是用碘水检验,D选项错误;
故答案选B。
13.C
【详解】A.氰基、酯基具有较强的极性,使碳碳双键活化从而更易发生加聚反应,A项正确;
B.酯基容易水解,有利于加快医用胶使用后的降解速率,B项正确;
C.504医用胶在常温下受到人体组织中的水的引发,可较快聚合,该聚合反应为加聚反应,C项错误;
D.分子中含有两个碳碳双键,可发生交联聚合,形成体型高聚物,有助于增强医用胶的耐水、耐热、抗冷热交替等性能,D项正确。
故选C。
14.C
【详解】A.由图可知,E的分子式为,A正确;
B.结合E、P结构和题给已知可知,形成高分子化合物P的单体之一F的结构简式是 ,B正确;
C.降解后,其中的酯基发生反应,不能得到E和F,C错误;
D.结合题给已知,E和F反应生成P的过程中没有生成小分子化合物,为加聚反应,D正确;
故选C。
15.A
【详解】A.氧化石墨烯中含有羟基和羧基,能够和水分子形成氢键,有一定的亲水性,A正确;
B.石墨仅由碳原子构成,是无机物,不是有机高分子材料,B错误;
C.在石墨烯中,每个碳原子都贡献出一个未成键的电子,这些电子形成了一个大π键,电子可以在整个层面内自由移动,使得石墨烯在层内具有优异的导电性,石墨烯层与层之间是通过较弱的范德华力相互作用的,这种力不足以支持电子在层间自由传输,石墨烯的层间导电性相对较弱,C错误;
D.石墨转化成氧化石墨烯的过程中生成了新的物质,是化学变化,D错误;
故选A。
16.D
【详解】A.根据M的结构简式,其分子式为C15H10N2O2,A正确;
B.聚氨酯和蛋白质分子中均含有酰胺基,则某些化学性质相似,如水解,B正确;
C.聚氨酯中含有酯基和酰胺基,在一定条件下能发生水解反应,C正确;
D.合成聚氨酯的反应中,M中的碳氮双键与乙二醇中羟基的H原子、O原子发生加成反应,属于加成聚合反应,D错误;
故选D。
17.D
【详解】A.P分子中苯环侧链上的C之间形成的键为单键,可旋转,分子中的所有碳原子可能在同一平面内,A不符合题意;
B.Q中官能团为(酯基),B不符合题意;
C.由P制备高分子Q时,无其他产物生成,反应为加聚反应且原子利用率为100%,C不符合题意;
D.P在一定条件下与水反应生成,Q在一定条件下水解生成、,所得产物不完全相同,D符合题意;
故选D。
18.B
【分析】向桂花中加入石油醚,充分振荡,过滤,分离除去不溶物,得到溶液,然后根据物质沸点的不同,将溶液进行蒸馏,分离出沸点低的石油醚和桂花浸膏,再向桂花浸膏中加入无水乙醇回流1小时,进行抽滤,并用乙醇洗涤固体残渣,充分回收桂花精油,将分离得到溶液进行减压蒸馏,分离得到桂花精油。
【详解】A.“操作①”是分离难溶性固体与可溶性液体混合物的操作,该操作名称为过滤,所需的玻璃仪器有烧杯、漏斗、玻璃棒,A正确;
B.“操作②”为分离互溶的、沸点不同的混合物,名称为蒸馏,所得的沸点较低的石油醚可循环利用,B错误;
C.残留在固体上的桂花精油能够溶于乙醇,“乙醇洗涤”抽滤时的固体残渣,可提高桂花精油的收率,C正确;
D.桂花精油不稳定,高温易变质。利用物质沸点随压强的减小而降低的性质进行“减压蒸馏”就可防止桂花精油在较高温度下变质,D正确;
故合理选项是B。
19.(1)水杨酸中羟基和羧基相邻,易形成分子内氢键,与水分子结合的能力弱于对羟基苯甲酸
(2)
(3) 球形冷凝管 水杨酸、乙酸酐、浓硫酸 否 B
(4) 冷水
(5) 重结晶
(6)
【分析】实验室以水杨酸和乙酸酐为原料合成阿司匹林,取适量水杨酸、乙酸酐和浓硫酸混合摇匀,控制温度加热,冷却反应液、倒入冷水中并用冰水浴冷却、过滤、洗涤得到粗产品。
【详解】(1)水杨酸分子中羟基和羧基相邻,易形成分子内氢键,与水分子结合的能力弱于对羟基苯甲酸,因此水杨酸在水中的溶解度小于对羟基苯甲酸;
(2)水杨酸分子中含有羟基和羧基,可发生缩聚反应生成聚合物,结构简式为;
(3)①图中仪器a的名称为球形冷凝管;
②向三颈烧瓶中加入试剂时,首先应加入固态试剂水杨酸,然后加入液态试剂乙酸酐,再加入浓硫酸并不断搅拌,防止因温度升高而发生副反应。装置中有搅拌棒,不需要加入沸石;
③该实验加热温度为80~90℃,因此适宜的加热方式为水浴加热;
(4)①加水时,乙酸酐发生水解反应生成乙酸,化学方程式为;
②为洗掉乙酸并减小乙酰水杨酸的溶解损失,应使用冷水洗涤晶体;
(5)实验获得的乙酰水杨酸中含有水杨酸,根据二者在不同温度下溶解度的差异,可采用重结晶的方法进行提纯。杂质水杨酸分子中含有羟基,能与溶液发生显色反应,因此可取少量结晶加入溶液中,观察有无显色反应,即可检验产品是否纯净;
(6)实验中使用的乙酸酐过量,则按照水杨酸的用量计算乙酰水杨酸的产率为。
20.(1) 苯甲醛
(2) 羟基 CH3COOH
(3)取代反应或水解反应
(4)
(5)
【分析】
由D的结构可知,A中含有苯环,A与CH3CHO反应得到B,由物质B的分子式及信息Ⅰ,可推知A为,B为,B与银氨溶液或新制氢氧化铜悬浊液发生氧化反应、酸化得到C,则C为。C发生取代反应得到D.结合G的结构可知,乙炔和羧酸X加成生成E,E发生加聚反应得到F,则且结合小问1中关于E的信息:E的核磁共振氢谱为三组峰即分子内有3种氢,且峰面积之比为3:2:1、即氢原子数目之比为3:2:1,E能发生水解反应,则含酯基,E分子中含有碳碳双键,结合分子式可知,X为CH3COOH,E为CH3COOCH=CH2,F为,G与D发生第二个信息反应得到光刻胶,则光刻胶的结构简式为:。
【详解】(1)
据分析,A为,A的名称为:苯甲醛;F的结构简式为。
(2)据分析,G 分子中所含官能团名称为:羟基。羧酸 X的结构简式为CH3COOH。
(3)由F到G为酯基水解,反应类型为取代反应。
(4)
据第二个信息反应,D 和 G 反应生成光刻胶同时得到氯化氢气体,化学方程式为:。
(5)
C的一种同分异构体满足下列条件:①能发生银镜反应,其水解产物之一能与 FeCl3溶液发生显色反应,说明含有甲酸形成的酯基、且水解后生成酚羟基;②苯环上的一氯取代产物只有两种,则有2个不同的取代基处于对位,该同分异构体的结构简式为:。
21.(1) 水解反应或取代反应 羟基和羧基 1
(2)2+O22+2H2O
(3)
(4) 13
(5) 2-羟基苯甲酸 +3NaOH+NaBr+2H2O
【分析】
芳香烃A分子式为C7H8,则A为,则A与氯气在光照条件下发生甲基上的取代反应生成B,根据扁桃酸的结构简式可知B为 ,B水解得到C,C为,C氧化得到D,D为,结合扁桃酸的结构简式和已知(1)的反应可知E为,F的分子式为C8H8O,结合F后面物质的结构可知F为,根据已知(2)的反应可知G的结构简式为。
【详解】(1)
B为 ,C为,B生成C的反应类型为水解反应或取代反应;扁桃酸中官能团的名称为:羟基和羧基;分子中连有4个不同原子或原子团的碳原子为手性碳,故含有1个手性碳,即连羟基和羧基的碳原子;
(2)
C为,C氧化得到D,D为,化学方程式为:2+O22+2H2O;
(3)
G的结构简式为,通过加聚反应生成的产物的结构简式为;
(4)
扁桃酸的结构简式为,其同分异构体满足如下条件:①属于芳香族化合物,且分子中含有的环只有苯环;③遇FeCl3溶液显紫色,说明含有酚羟基;②能发生银镜反应和水解反应,说明含有醛基和酯基;结合O的个数可知应该含有甲酸酯的结构,如果含有-OH和-CH2OOCH两个取代基,则有3种位置,如果是-OH、-OOCH、-CH3三个取代基,共有10种位置,故共有13种同分异构体;其中核磁共振氢谱有五组峰,且峰面积比为2:2:2:1:1,说明为对称结构,且不含有甲基,故符合条件的结构简式为;;
(5)
水杨酸的结构简式为,用系统命名法命名水杨酸为:2-羟基苯甲酸;根据已知的信息,由生成H的化学方程式为+3NaOH+NaBr+2H2O。
22.(1) 氧化反应
(2)
(3) 浓硫酸、加热 丙烯酸钠
(4) 3 (或)
(5)、、
【分析】根据已知信息①知,I中发生氧化反应,则I中含有碳碳双键,再结合问题(1)所给信息知,I为,II和氢气发生加成反应得到III,III为,III→IV发生醇的消去反应,IV经一系列的变化可得到V,V和氢氧化钠反应可得到VI,VI为丙烯酸钠,V和VI发生加聚反应可得到VII。
【详解】(1)I的化学式C6H12,其中含有一种化学环境的氢原子,结合已知信息①知,
I的结构简式为,I→II过程中I被酸性高锰酸钾溶液氧化,反应类型为氧化反应。
(2)II和氢气发生加成反应得到III,III为,III→IV发生醇的消去反应,化学方程式为。
(3)III属于醇类,V属于羧酸类,二者发生取代反应的条件是浓硫酸、加热;VI为,名称是丙烯酸钠。
(4)V为,其同分异构体能发生银镜反应,说明含“-CHO”,共有、、这3种链状化合物符合题意。其中核磁共振氢谱图上只有两组峰的结构简式为(或)。
(5)
合成路线中丙酮和HCN先发生加成反应得到A,A为,在酸性条件下发生水解得到B,B为,在浓硫酸、加热的条件下发生醇的消去反应得到C,C为,最后和甲醇在浓硫酸、加热的条件下发生酯化反应即可得到高分子VIII的单体。
答案第1页,共2页
答案第1页,共2页
