第三单元 探秘水世界质量评估 (含答案) 初中化学鲁教版九年级上册
文档属性
| 名称 | 第三单元 探秘水世界质量评估 (含答案) 初中化学鲁教版九年级上册 |

|
|
| 格式 | docx | ||
| 文件大小 | 488.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-11 00:00:00 | ||
图片预览




文档简介
第三单元 探秘水世界质量评估
第Ⅰ卷(选择题 共42分)
一、选择题(每小题只有一个选项符合题意;每小题3分,共42分)
1.少量下列物质放入水中充分搅拌后不能形成溶液的是( )
A.白糖 B.白酒 C.白醋 D.花生油
2.发达的农耕文明,先进的农学思想、悠久的重农传统,以及与自然和谐相处的文化理念,多种因素相互作用催生了二十四节气。下列节气的命名与水的三态变化无关的是( )
A.雨水 B.霜降 C.小雪 D.冬至
3.下列说法正确的是( )
A.均一、稳定的液体一定是溶液 B.饱和溶液一定是浓溶液
C.水可以作任何溶液的溶剂 D.将氢氧化钠溶于水,所得溶液的温度升高
4.下列关于冰、水和水蒸气的说法正确的是( )
A.水不可能由固态直接变成气态
B.水蒸气是肉眼可以看见的气体
C.相同条件下,水蒸气比水的分子运动速率大
D.它们是同一物质,因为组成它们的元素相同
5.t ℃时,向硝酸钠的饱和溶液中加入一定量的水后,下列有关该溶液的叙述中,正确的是( )
A.仍为饱和溶液 B.溶液的质量减小
C.溶质的质量不变 D.溶质质量分数不变
6.下列操作后,所得溶液的溶质质量分数一定增大的是( )
A B C D
7.化学教会我们从微观角度去认识宏观现象。下列对生活中宏观现象的微观解释不合理的是( )
A.气体受热膨胀,因为温度升高,分子体积增大
B.氢气和液氢都能燃烧,说明同种分子的化学性质相同
C.缉毒犬能根据气味发现毒品,因为分子在不断地运动
D.一滴水大约有1.6×1021个水分子,说明分子的体积很小
8.下图是某同学模拟自来水厂将长江水净化并最终制得蒸馏水的流程。下列说法错误的是( )
A.物质A可以是明矾
B.操作a和操作b的作用相同
C.液体C和液体D中溶质种类不同
D.净水方法中,蒸馏是净化程度最高的
9.下列说法正确的是( )
A.饱和石灰水溶液放置较长时间后,表面出现了一层白膜(已知水没有减少),该溶液仍是氢氧化钙的饱和溶液
B.饱和溶液析出晶体后就变成不饱和溶液
C.相同温度下,同一物质的饱和溶液中的溶质比不饱和溶液中的溶质多
D.一定温度下,向某蔗糖溶液中加入少量蔗糖,蔗糖逐渐消失,说明原溶液是不饱和溶液
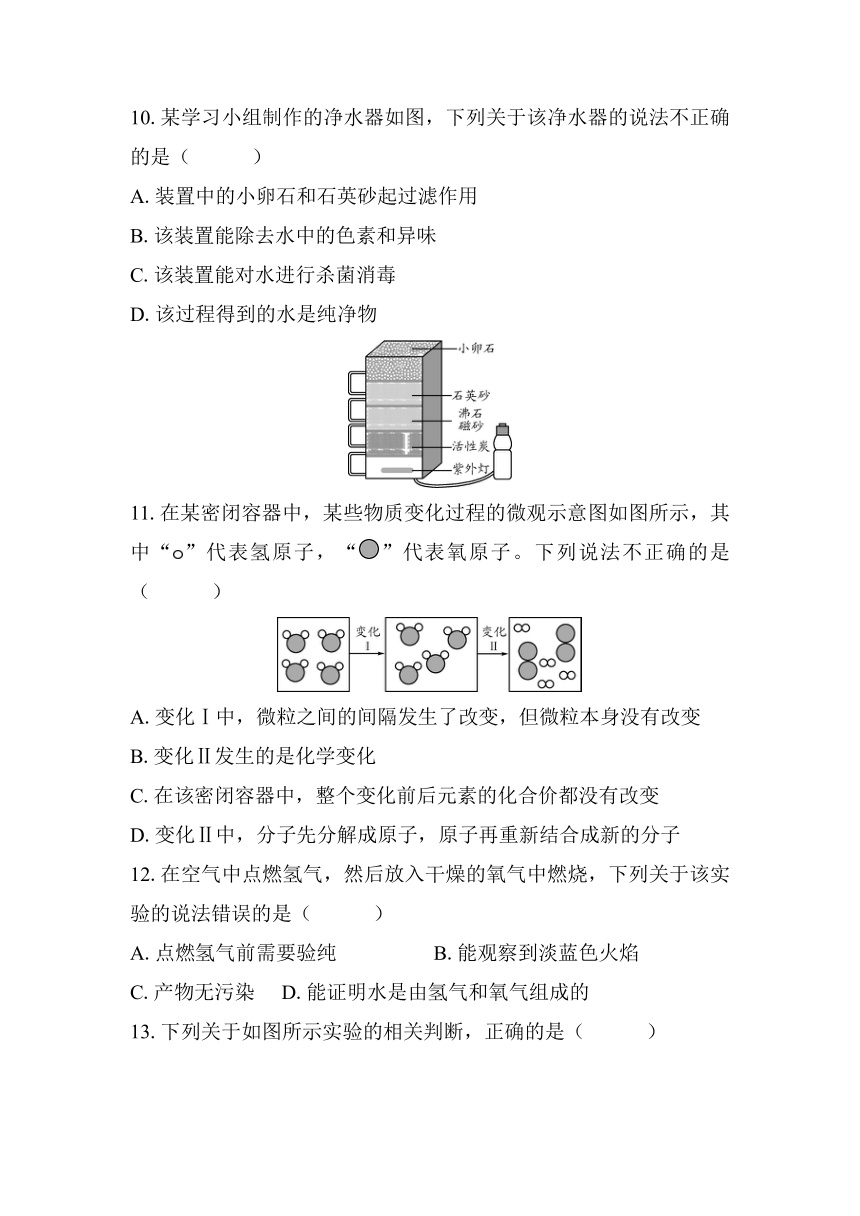
10.某学习小组制作的净水器如图,下列关于该净水器的说法不正确的是( )
A.装置中的小卵石和石英砂起过滤作用
B.该装置能除去水中的色素和异味
C.该装置能对水进行杀菌消毒
D.该过程得到的水是纯净物
11.在某密闭容器中,某些物质变化过程的微观示意图如图所示,其中“”代表氢原子,“”代表氧原子。下列说法不正确的是( )
A.变化Ⅰ中,微粒之间的间隔发生了改变,但微粒本身没有改变
B.变化Ⅱ发生的是化学变化
C.在该密闭容器中,整个变化前后元素的化合价都没有改变
D.变化Ⅱ中,分子先分解成原子,原子再重新结合成新的分子
12.在空气中点燃氢气,然后放入干燥的氧气中燃烧,下列关于该实验的说法错误的是( )
A.点燃氢气前需要验纯 B.能观察到淡蓝色火焰
C.产物无污染 D.能证明水是由氢气和氧气组成的
13.下列关于如图所示实验的相关判断,正确的是( )
A.若Y为硝酸钾,则X可能为氢氧化钠
B.若Y为氢氧化钙,则X可能为硝酸铵
C.③为Y的不饱和溶液
D.Y溶液的溶质质量分数:①=③>②
14.20℃和60℃时,在100g水中KCl的最大溶解量为34g和45.5g,下图所示为KCl的溶解实验。下列分析错误的是( )
A.①中溶液为KCl的饱和溶液
B.②中溶液的质量为25.0g
C.溶液中溶质的质量:①<②=③
D.溶液中溶质的质量分数:①<②=③
第Ⅱ卷(非选择题 共58分)
二、填空题(共30分)
15.(10分)小聪同学将浑浊的湖水样品倒入烧杯中,进行净化处理。
(1)他首先在浑浊的湖水中加入明矾粉末,静置一会儿后,将得到的湖水过滤。过滤是分离 不同的混合物。过滤过程中,使用到玻璃棒,其作用是 。
(2)小聪用如图装置进行过滤,其操作规范的是 (填字母序号)。
A.用玻璃棒引流
B.滤纸边缘高出漏斗
C.漏斗末端紧靠烧杯内壁
D.将滤纸湿润,使其紧贴漏斗内壁
E.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(3)过滤过程中他发现过滤速度太慢,原因可能是 。
(4)过滤后观察发现,滤液仍然浑浊,原因可能是 。
16.(12分)制作“叶脉书签”需用到10%的氢氧化钠溶液,现配制50g溶质质量分数为10%的氢氧化钠溶液。
(1)配制溶液的正确操作顺序为 (填序号,下同),其中操作错误的是 。
(2)若用氢氧化钠固体配制,所需氢氧化钠固体的质量为 g,所需水的体积为 mL。
(3)用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶,还需要 。
(4)下列操作正确的是 (填字母序号)。
A.倾倒液体时,标签朝向手心
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.量取液体后读数时,应仰视液面
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
17.(8分)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)碘酒是临床上常用的一种消毒剂,其溶剂是 ;生理盐水是医疗上常用的一种溶液,若生理盐水密封放置一段时间后出现浑浊现象,可判断其为不合格产品,这是因为溶液具有 性。
(2)稀醋酸可用于除去水壶中的水垢,把30g20%的醋酸稀释为5%的稀溶液,需要加水的质量为 g。
(3)某温度时,向一定量的饱和氢氧化钙溶液中加入少量的生石灰,再恢复到原温度。下列相关量的变化图像正确的是 (填字母序号)。
三、实验探究题(共22分)
18.(10分)化学实践小组的同学们在某河段取河水,设计了一系列实践活动,对水质检测、水的净化、水的组成进行了项目式学习。
任务一 净化水
河水转化为自来水需要经过一系列步骤,但是自来水送到用户过程中仍可能被污染,因此很多公共场所使用直饮机(工作原理如图1所示)。
图1
(1)活性炭罐具有 作用,除去颜色、异味的同时也除去重金属离子。
任务二 验证水的组成
兴趣小组同学利用图2所示装置进行电解水实验。
(2)该反应的符号表达式为 ,b管中得到的气体是 。
图2
【实验拓展】理论上电解水生成氢气与氧气的体积比为2∶1,实际测定结果却往往大于2∶1,这是为什么?
【查阅资料】常温常压下,1L水中最多能溶解约30mL氧气、18mL氢气。
【探究实验】分别选用不同的电极材料进行电解水实验,3分钟后记录实验数据如下表。
电极材料 铜丝 铁丝 保险丝 电阻丝
氢气与氧气的体积比 7.7∶3.3 6.5∶3.2 6.9∶2.9 7.3∶3.4
【实验分析】
(3)下列关于电解水实验的说法中,正确的是 (填字母序号)。
A.进行该实验前,需要先检查装置的气密性
B.铜丝作为电极时,测得的氢气与氧气的体积比最接近2∶1
C.选用不同的电极材料进行实验,可能影响生成气体的体积比
【交流反思】
(4)影响测得的气体体积比的因素除了与电极材料有关外,还可能与 有关。
19.(12分)实验分析和探究是获得化学知识的重要途径。某化学兴趣小组设计并动手完成如图所示的实验,请回答下列问题(已知氨气的密度比空气的小)。
(1)小连同学做了图1所示的对比实验,取两支大小相同的医用注射器,将活塞向外拉,分别吸入等体积的空气和水,用手指顶住注射器末端小孔,将活塞慢慢向内推,发现空气比水更容易被压缩,该实验从微观角度证明了 。
图1
(2)小江同学用图2所示实验探究分子的性质,观察到乙烧杯中的酚酞试液变为红色,甲烧杯中的浓氨水没有变色,该实验说明了 (填字母序号)。
A.浓氨水具有挥发性 B.氨分子在不断地运动
C.氨分子质量很小
图2
(3)小组同学对图2实验进行改进,共同设计了图3所示实验,在实验中观察到 (填“a”或“b”)处的棉花团先变成红色。改进后的优点有 (写一点),为了快速观察到实验现象,可进行的操作是 。
图3
(4)小组同学对氨水的制取产生了兴趣,查阅资料后获悉,氨气溶于水可制得氨水。图4是高温、高压、催化剂条件下反应合成氨气的微观示意图,该反应的符号表达式为 。
图4
四、计算题(共6分)
20.(6分)有100 g 10%的食盐溶液,要使其质量分数变为20%,有以下三种方法,请你分别进行计算:
(1)可加入多少克食盐?
(2)可蒸发多少克水?
(3)将其与质量分数为25%的食盐溶液混合,需要25%的食盐溶液多少克?
参考答案
第三单元质量评估
1.D 2.D 3.D 4.C 5.C 6.C 7.A 8.B
9.D 10.D 11.C 12.D 13.D 14.D
15.(1)溶解性 引流 (2)ACD (3)滤纸没有紧贴漏斗内壁 (4)滤纸破损(合理即可)
16.(1)②①⑤③④ ① (2)5 45 (3)玻璃棒 (4)AD 17.(1)酒精 稳定 (2)90 (3)C
18.(1)吸附 (2)H2OH2+O2 氧气
(3)AC (4)气体在水中的溶解性 19.(1)气体分子间的间隔比液体分子间的间隔大 (2)AB (3)a 更环保(或节约试剂)微热V管处的浓氨水 (4)H2+N2NH3
20.解:(1)设加入食盐的质量为x。
×100%=20% x=12.5 g
(2)设蒸发的水的质量为y。蒸发水时,溶质的质量不变,则:
100 g×10%=(100 g-y)×20% y=50 g
(3)设需要25%的食盐溶液的质量为z。混合后的溶液中溶质质量为混合前两种溶液中溶质质量之和,则:
100 g×10%+25%×z=(100 g+z)×20%
z=200 g
答:(1)可加入12.5 g食盐。(2)可蒸发50 g水。(3)需要25%的食盐溶液200 g。
。
第Ⅰ卷(选择题 共42分)
一、选择题(每小题只有一个选项符合题意;每小题3分,共42分)
1.少量下列物质放入水中充分搅拌后不能形成溶液的是( )
A.白糖 B.白酒 C.白醋 D.花生油
2.发达的农耕文明,先进的农学思想、悠久的重农传统,以及与自然和谐相处的文化理念,多种因素相互作用催生了二十四节气。下列节气的命名与水的三态变化无关的是( )
A.雨水 B.霜降 C.小雪 D.冬至
3.下列说法正确的是( )
A.均一、稳定的液体一定是溶液 B.饱和溶液一定是浓溶液
C.水可以作任何溶液的溶剂 D.将氢氧化钠溶于水,所得溶液的温度升高
4.下列关于冰、水和水蒸气的说法正确的是( )
A.水不可能由固态直接变成气态
B.水蒸气是肉眼可以看见的气体
C.相同条件下,水蒸气比水的分子运动速率大
D.它们是同一物质,因为组成它们的元素相同
5.t ℃时,向硝酸钠的饱和溶液中加入一定量的水后,下列有关该溶液的叙述中,正确的是( )
A.仍为饱和溶液 B.溶液的质量减小
C.溶质的质量不变 D.溶质质量分数不变
6.下列操作后,所得溶液的溶质质量分数一定增大的是( )
A B C D
7.化学教会我们从微观角度去认识宏观现象。下列对生活中宏观现象的微观解释不合理的是( )
A.气体受热膨胀,因为温度升高,分子体积增大
B.氢气和液氢都能燃烧,说明同种分子的化学性质相同
C.缉毒犬能根据气味发现毒品,因为分子在不断地运动
D.一滴水大约有1.6×1021个水分子,说明分子的体积很小
8.下图是某同学模拟自来水厂将长江水净化并最终制得蒸馏水的流程。下列说法错误的是( )
A.物质A可以是明矾
B.操作a和操作b的作用相同
C.液体C和液体D中溶质种类不同
D.净水方法中,蒸馏是净化程度最高的
9.下列说法正确的是( )
A.饱和石灰水溶液放置较长时间后,表面出现了一层白膜(已知水没有减少),该溶液仍是氢氧化钙的饱和溶液
B.饱和溶液析出晶体后就变成不饱和溶液
C.相同温度下,同一物质的饱和溶液中的溶质比不饱和溶液中的溶质多
D.一定温度下,向某蔗糖溶液中加入少量蔗糖,蔗糖逐渐消失,说明原溶液是不饱和溶液
10.某学习小组制作的净水器如图,下列关于该净水器的说法不正确的是( )
A.装置中的小卵石和石英砂起过滤作用
B.该装置能除去水中的色素和异味
C.该装置能对水进行杀菌消毒
D.该过程得到的水是纯净物
11.在某密闭容器中,某些物质变化过程的微观示意图如图所示,其中“”代表氢原子,“”代表氧原子。下列说法不正确的是( )
A.变化Ⅰ中,微粒之间的间隔发生了改变,但微粒本身没有改变
B.变化Ⅱ发生的是化学变化
C.在该密闭容器中,整个变化前后元素的化合价都没有改变
D.变化Ⅱ中,分子先分解成原子,原子再重新结合成新的分子
12.在空气中点燃氢气,然后放入干燥的氧气中燃烧,下列关于该实验的说法错误的是( )
A.点燃氢气前需要验纯 B.能观察到淡蓝色火焰
C.产物无污染 D.能证明水是由氢气和氧气组成的
13.下列关于如图所示实验的相关判断,正确的是( )
A.若Y为硝酸钾,则X可能为氢氧化钠
B.若Y为氢氧化钙,则X可能为硝酸铵
C.③为Y的不饱和溶液
D.Y溶液的溶质质量分数:①=③>②
14.20℃和60℃时,在100g水中KCl的最大溶解量为34g和45.5g,下图所示为KCl的溶解实验。下列分析错误的是( )
A.①中溶液为KCl的饱和溶液
B.②中溶液的质量为25.0g
C.溶液中溶质的质量:①<②=③
D.溶液中溶质的质量分数:①<②=③
第Ⅱ卷(非选择题 共58分)
二、填空题(共30分)
15.(10分)小聪同学将浑浊的湖水样品倒入烧杯中,进行净化处理。
(1)他首先在浑浊的湖水中加入明矾粉末,静置一会儿后,将得到的湖水过滤。过滤是分离 不同的混合物。过滤过程中,使用到玻璃棒,其作用是 。
(2)小聪用如图装置进行过滤,其操作规范的是 (填字母序号)。
A.用玻璃棒引流
B.滤纸边缘高出漏斗
C.漏斗末端紧靠烧杯内壁
D.将滤纸湿润,使其紧贴漏斗内壁
E.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(3)过滤过程中他发现过滤速度太慢,原因可能是 。
(4)过滤后观察发现,滤液仍然浑浊,原因可能是 。
16.(12分)制作“叶脉书签”需用到10%的氢氧化钠溶液,现配制50g溶质质量分数为10%的氢氧化钠溶液。
(1)配制溶液的正确操作顺序为 (填序号,下同),其中操作错误的是 。
(2)若用氢氧化钠固体配制,所需氢氧化钠固体的质量为 g,所需水的体积为 mL。
(3)用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶,还需要 。
(4)下列操作正确的是 (填字母序号)。
A.倾倒液体时,标签朝向手心
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.量取液体后读数时,应仰视液面
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
17.(8分)溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)碘酒是临床上常用的一种消毒剂,其溶剂是 ;生理盐水是医疗上常用的一种溶液,若生理盐水密封放置一段时间后出现浑浊现象,可判断其为不合格产品,这是因为溶液具有 性。
(2)稀醋酸可用于除去水壶中的水垢,把30g20%的醋酸稀释为5%的稀溶液,需要加水的质量为 g。
(3)某温度时,向一定量的饱和氢氧化钙溶液中加入少量的生石灰,再恢复到原温度。下列相关量的变化图像正确的是 (填字母序号)。
三、实验探究题(共22分)
18.(10分)化学实践小组的同学们在某河段取河水,设计了一系列实践活动,对水质检测、水的净化、水的组成进行了项目式学习。
任务一 净化水
河水转化为自来水需要经过一系列步骤,但是自来水送到用户过程中仍可能被污染,因此很多公共场所使用直饮机(工作原理如图1所示)。
图1
(1)活性炭罐具有 作用,除去颜色、异味的同时也除去重金属离子。
任务二 验证水的组成
兴趣小组同学利用图2所示装置进行电解水实验。
(2)该反应的符号表达式为 ,b管中得到的气体是 。
图2
【实验拓展】理论上电解水生成氢气与氧气的体积比为2∶1,实际测定结果却往往大于2∶1,这是为什么?
【查阅资料】常温常压下,1L水中最多能溶解约30mL氧气、18mL氢气。
【探究实验】分别选用不同的电极材料进行电解水实验,3分钟后记录实验数据如下表。
电极材料 铜丝 铁丝 保险丝 电阻丝
氢气与氧气的体积比 7.7∶3.3 6.5∶3.2 6.9∶2.9 7.3∶3.4
【实验分析】
(3)下列关于电解水实验的说法中,正确的是 (填字母序号)。
A.进行该实验前,需要先检查装置的气密性
B.铜丝作为电极时,测得的氢气与氧气的体积比最接近2∶1
C.选用不同的电极材料进行实验,可能影响生成气体的体积比
【交流反思】
(4)影响测得的气体体积比的因素除了与电极材料有关外,还可能与 有关。
19.(12分)实验分析和探究是获得化学知识的重要途径。某化学兴趣小组设计并动手完成如图所示的实验,请回答下列问题(已知氨气的密度比空气的小)。
(1)小连同学做了图1所示的对比实验,取两支大小相同的医用注射器,将活塞向外拉,分别吸入等体积的空气和水,用手指顶住注射器末端小孔,将活塞慢慢向内推,发现空气比水更容易被压缩,该实验从微观角度证明了 。
图1
(2)小江同学用图2所示实验探究分子的性质,观察到乙烧杯中的酚酞试液变为红色,甲烧杯中的浓氨水没有变色,该实验说明了 (填字母序号)。
A.浓氨水具有挥发性 B.氨分子在不断地运动
C.氨分子质量很小
图2
(3)小组同学对图2实验进行改进,共同设计了图3所示实验,在实验中观察到 (填“a”或“b”)处的棉花团先变成红色。改进后的优点有 (写一点),为了快速观察到实验现象,可进行的操作是 。
图3
(4)小组同学对氨水的制取产生了兴趣,查阅资料后获悉,氨气溶于水可制得氨水。图4是高温、高压、催化剂条件下反应合成氨气的微观示意图,该反应的符号表达式为 。
图4
四、计算题(共6分)
20.(6分)有100 g 10%的食盐溶液,要使其质量分数变为20%,有以下三种方法,请你分别进行计算:
(1)可加入多少克食盐?
(2)可蒸发多少克水?
(3)将其与质量分数为25%的食盐溶液混合,需要25%的食盐溶液多少克?
参考答案
第三单元质量评估
1.D 2.D 3.D 4.C 5.C 6.C 7.A 8.B
9.D 10.D 11.C 12.D 13.D 14.D
15.(1)溶解性 引流 (2)ACD (3)滤纸没有紧贴漏斗内壁 (4)滤纸破损(合理即可)
16.(1)②①⑤③④ ① (2)5 45 (3)玻璃棒 (4)AD 17.(1)酒精 稳定 (2)90 (3)C
18.(1)吸附 (2)H2OH2+O2 氧气
(3)AC (4)气体在水中的溶解性 19.(1)气体分子间的间隔比液体分子间的间隔大 (2)AB (3)a 更环保(或节约试剂)微热V管处的浓氨水 (4)H2+N2NH3
20.解:(1)设加入食盐的质量为x。
×100%=20% x=12.5 g
(2)设蒸发的水的质量为y。蒸发水时,溶质的质量不变,则:
100 g×10%=(100 g-y)×20% y=50 g
(3)设需要25%的食盐溶液的质量为z。混合后的溶液中溶质质量为混合前两种溶液中溶质质量之和,则:
100 g×10%+25%×z=(100 g+z)×20%
z=200 g
答:(1)可加入12.5 g食盐。(2)可蒸发50 g水。(3)需要25%的食盐溶液200 g。
。
同课章节目录
