苏教版高中化学选择性必修2专题3微粒间作用力与物质性质总结提升课件(共18张PPT)
文档属性
| 名称 | 苏教版高中化学选择性必修2专题3微粒间作用力与物质性质总结提升课件(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-12 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
专题3 微粒间作用力与物质性质
专题总结提升
第*页
专题归纳提升
第*页
高考素养提升
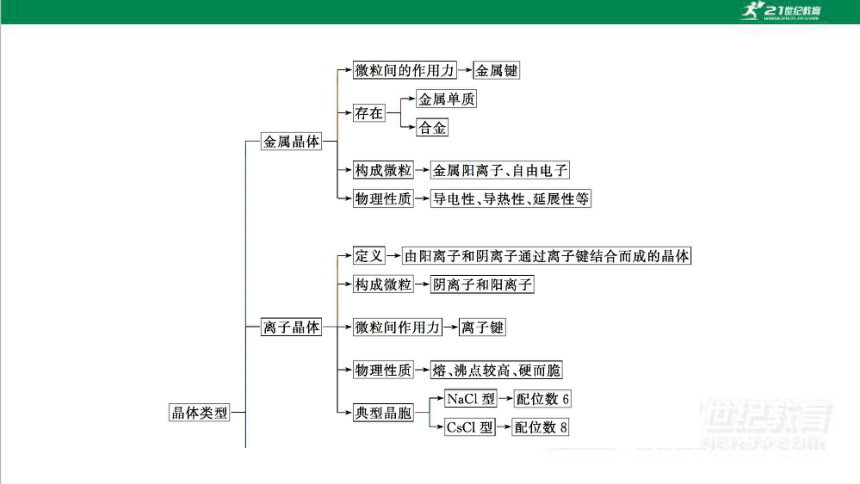
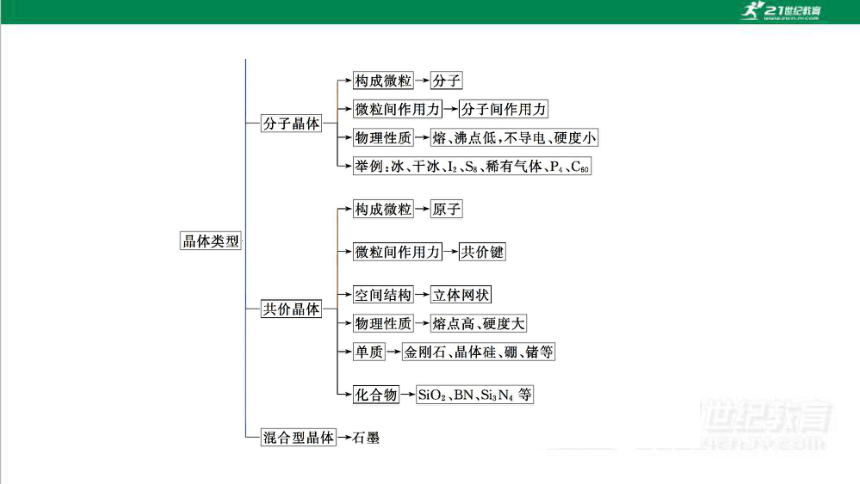
考向一 微粒间作用力与晶体性质
选项 性质差异 结构因素
A 沸点:正戊烷(36.1 ℃)高于新戊烷(9.5 ℃) 分子间作用力
B 熔点:AlF3(1 040 ℃)远高于AlCl3(178 ℃升华) 晶体类型
C 酸性:CF3COOH(p Ka=0.23)远强于CH3COOH(p Ka= 4.76) 羟基极性
D 溶解度(20 ℃):Na2CO3(29 g)大于NaHCO3(8 g) 阴离子电荷
D
1
2
3
4
5
6
7
1
2
3
4
5
6
7
A. 与石墨相比,(CF) x 导电性增强
B. 与石墨相比,(CF) x 抗氧化性增强
C. (CF) x 中C—C的键长比C—F短
D. 1 mol (CF) x 中含有2 x mol共价单键
B
1
2
3
4
5
6
7
解析:石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故 石墨晶体能导电,而(CF) x 中没有未参与杂化的2p轨道上的电子,故与石墨相比, (CF) x 导电性减弱,A错误;(CF) x 中C原子的所有价键均参与成键,没有未参与 成键的孤电子或不饱和键,故与石墨相比,(CF) x 抗氧化性增强,B正确;已知C的 原子半径比F的大,故可知(CF) x 中C—C的键长比C—F长,C错误;由题干结构示 意图可知,在(CF) x 中C与周围的3个碳原子形成共价键,每个C—C键被2个碳原子 共用,和1个F原子形成共价键,即1 mol (CF) x 中含有2.5 x mol共价单键,D错误。
1
2
3
4
5
6
7
考向二 晶胞结构的分析与计算
A. 中心原子的配位数是4
B. 晶胞中配合物分子的数目为2
C. 晶体中相邻分子间存在范德华力
D. 该晶体属于混合型晶体
D
1
2
3
4
5
6
7
A. 该氧化物的化学式为ZrO2
D. 若坐标取向不变,将p点Zr原子平移至原点,则q点Zr原子位于晶胞 xy 面的面心
B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
B. 图1中O原子的配位数为6
C. 图2表示的化学式为LiMg2OCl x Br1- x
D. Mg2+取代产生的空位有利于Li+传导
C
1
2
3
4
5
6
7
1
2
3
4
5
6
7
6. (2023·广东高考)由CoCl2可制备Al x CoO y 晶体,其立方晶胞如图。Al与O最小间 距大于Co与O最小间距, x 、 y 为整数,则Co在晶胞中的位置为 ;晶体中一 个Al周围与其最近的O的个数为 。
体心
12
1
2
3
4
5
6
7
解析:由CoCl2可制备Al x CoO y 晶体,其立方晶胞如图。 x 、 y 为整数,根据图中信息 Co、Al都只有一个原子,而氧(白色)原子有3个,Al与O最小间距大于Co与O最小 间距,则Al在顶角,因此Co在晶胞中的位置为体心;晶体中一个Al周围与其最近的O 原子,以顶角Al分析,面心的氧原子一个横截面有4个,三个横截面共12个,因此晶 体中一个Al周围与其最近的O的个数为12。
1
2
3
4
5
6
7
7. (2023·福建高考)铜的硫化物结构多样。天然硫化铜俗称铜蓝,其晶胞结构 如图。
1
2
3
4
5
6
7
2
2∶1
bc
1
2
3
4
5
6
7
专题3 微粒间作用力与物质性质
专题总结提升
第*页
专题归纳提升
第*页
高考素养提升
考向一 微粒间作用力与晶体性质
选项 性质差异 结构因素
A 沸点:正戊烷(36.1 ℃)高于新戊烷(9.5 ℃) 分子间作用力
B 熔点:AlF3(1 040 ℃)远高于AlCl3(178 ℃升华) 晶体类型
C 酸性:CF3COOH(p Ka=0.23)远强于CH3COOH(p Ka= 4.76) 羟基极性
D 溶解度(20 ℃):Na2CO3(29 g)大于NaHCO3(8 g) 阴离子电荷
D
1
2
3
4
5
6
7
1
2
3
4
5
6
7
A. 与石墨相比,(CF) x 导电性增强
B. 与石墨相比,(CF) x 抗氧化性增强
C. (CF) x 中C—C的键长比C—F短
D. 1 mol (CF) x 中含有2 x mol共价单键
B
1
2
3
4
5
6
7
解析:石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故 石墨晶体能导电,而(CF) x 中没有未参与杂化的2p轨道上的电子,故与石墨相比, (CF) x 导电性减弱,A错误;(CF) x 中C原子的所有价键均参与成键,没有未参与 成键的孤电子或不饱和键,故与石墨相比,(CF) x 抗氧化性增强,B正确;已知C的 原子半径比F的大,故可知(CF) x 中C—C的键长比C—F长,C错误;由题干结构示 意图可知,在(CF) x 中C与周围的3个碳原子形成共价键,每个C—C键被2个碳原子 共用,和1个F原子形成共价键,即1 mol (CF) x 中含有2.5 x mol共价单键,D错误。
1
2
3
4
5
6
7
考向二 晶胞结构的分析与计算
A. 中心原子的配位数是4
B. 晶胞中配合物分子的数目为2
C. 晶体中相邻分子间存在范德华力
D. 该晶体属于混合型晶体
D
1
2
3
4
5
6
7
A. 该氧化物的化学式为ZrO2
D. 若坐标取向不变,将p点Zr原子平移至原点,则q点Zr原子位于晶胞 xy 面的面心
B
1
2
3
4
5
6
7
1
2
3
4
5
6
7
B. 图1中O原子的配位数为6
C. 图2表示的化学式为LiMg2OCl x Br1- x
D. Mg2+取代产生的空位有利于Li+传导
C
1
2
3
4
5
6
7
1
2
3
4
5
6
7
6. (2023·广东高考)由CoCl2可制备Al x CoO y 晶体,其立方晶胞如图。Al与O最小间 距大于Co与O最小间距, x 、 y 为整数,则Co在晶胞中的位置为 ;晶体中一 个Al周围与其最近的O的个数为 。
体心
12
1
2
3
4
5
6
7
解析:由CoCl2可制备Al x CoO y 晶体,其立方晶胞如图。 x 、 y 为整数,根据图中信息 Co、Al都只有一个原子,而氧(白色)原子有3个,Al与O最小间距大于Co与O最小 间距,则Al在顶角,因此Co在晶胞中的位置为体心;晶体中一个Al周围与其最近的O 原子,以顶角Al分析,面心的氧原子一个横截面有4个,三个横截面共12个,因此晶 体中一个Al周围与其最近的O的个数为12。
1
2
3
4
5
6
7
7. (2023·福建高考)铜的硫化物结构多样。天然硫化铜俗称铜蓝,其晶胞结构 如图。
1
2
3
4
5
6
7
2
2∶1
bc
1
2
3
4
5
6
7
