(考点集训)2025年化学中考一轮复习4:自然界的水课件(人教版)
文档属性
| 名称 | (考点集训)2025年化学中考一轮复习4:自然界的水课件(人教版) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-13 22:54:33 | ||
图片预览









文档简介
(共56张PPT)
中考一轮复习 教材同步复习
第四单元 自然界的水
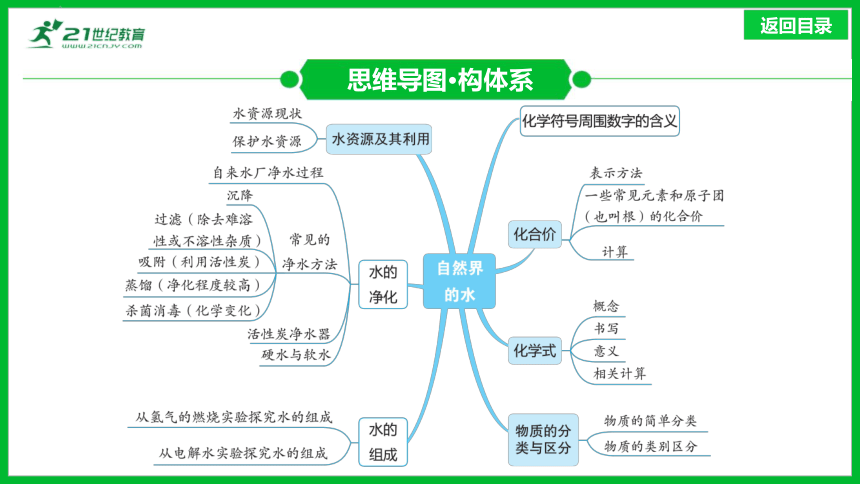
思维导图·构体系
知识精讲·夯基础
真题分点·明趋势
实验分阶·提能力
思维导图·构体系
1.水资源现状:地球上水的储量虽然很大,但大部分是含盐量很高的海水。淡水只约占地球水储量的2.53%。
知识精讲·夯基础
水资源及其利用(近5年4考)
知识点1
2.保护水资源
(1)合理利用水资源
①节约用水:如工业用水重复使用;采用节水
灌溉方式;推广节水器具等。
②合理调配水资源:如通过修建水库和调水工
程等措施改善水资源时空分布不均的局面。
(2)防治水体污染:应用新技术、新工艺减少污染物的产生;对污水进行处理,使之符合排放标准;合理施用农药、化肥。
国家节水标志
判断下列说法的正误。
1.大力开采地下水,缓解水资源短缺。 ( )
2.大量使用含磷洗衣粉会造成水体富营养化。 ( )
易错易混
×
√
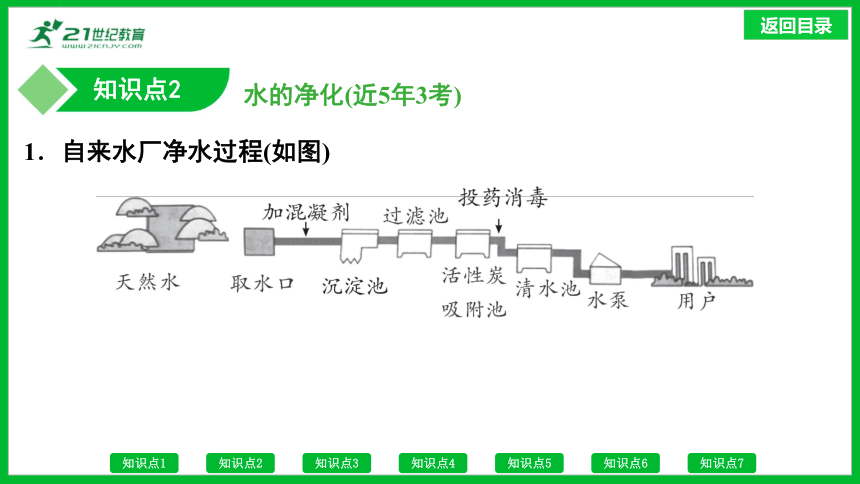
1.自来水厂净水过程(如图)
水的净化(近5年3考)
知识点2
2.常见的净水方法
净水方法 涉及的物质及作用
沉降 加入明矾,加速水中悬浮杂质的沉降
______ 除去水中的难溶性或不溶性杂质
吸附 利用活性炭的______作用除去水中的色素和异味[2022.15(2)]
蒸馏 几乎可以除去水中的所有杂质
杀菌消毒 加入消毒剂,除去水中的细菌和病毒
过滤
吸附
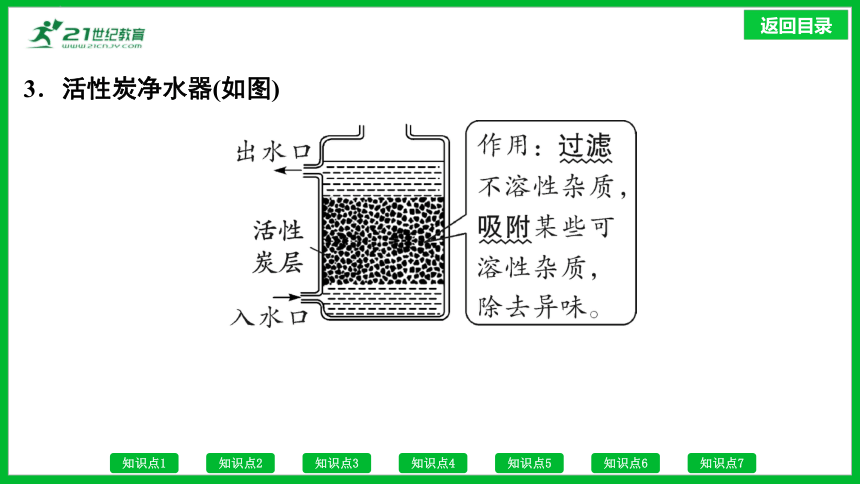
3.活性炭净水器(如图)
4.硬水与软水
(1)概念
①硬水:含有较多可溶性钙、镁化合物的水。
②软水:不含或含较少可溶性钙、镁化合物的水。
(2)硬水的危害:浪费肥皂且洗不净衣物,使衣物变硬;使锅炉内结垢,浪费燃料,损坏管道,可能引起爆炸。
判断下列说法的正误。
1.经过自来水厂净化后的水为纯净物。 ( )
2.过滤可以除去水中所有杂质。 ( )
3.沉降、过滤、吸附、蒸馏、杀菌消毒的过程中,均只发生物理变化。 ( )
4.沉降、过滤、吸附、蒸馏、杀菌消毒是净化水的常用方法,单一操作净化程度较高的方法是蒸馏。 ( )
5.利用活性炭的吸附性能除去水中色素,但不能除去异味。 ( )
6.硬水一定是混合物,软水一定是纯净物。 ( )
易错易混
×
×
×
√
×
×
1.从氢气的燃烧实验探究水的组成
(1)氢气的性质
①物理性质:无色、无臭、____溶于水的气体,密度比空气的____。
②化学性质:a.可燃性,可作______;b.还原性,能与某些金属氧化物发生反应,如CuO+H2 Cu+H2O,可用于冶炼金属。
水的组成(近5年2考)
知识点3
难
小
燃料
(2)检验氢气的纯度
Ⅰ.用拇指堵住集满氢气的试管口 Ⅱ.靠近火焰,移开拇指
从氢气的燃烧实验探究水的组成
【实验原理】______________________(用化学方程式表示)。
【实验装置及现象】
【实验结论】水是由________和________组成的。
教材小实验
淡蓝
2H2+O2 2H2O
氢元素
氧元素
判断下列说法的正误。
1.电解水实验说明水是由氢气和氧气组成的。 ( )
2.电解水时生成氢气与氧气的质量比为2∶1。 ( )
3.混有一定量空气或氧气的H2、CO、CH4等可燃性气体遇明火可能会发生爆炸,因此点燃前一定要检验其纯度。 ( )
易错易混
×
×
√
1.物质的简单分类
物质的分类与区分(近5年5考)
知识点4
2.物质的类别区分
(1)区分混合物与纯净物
分类 混合物 纯净物
概念 由两种或两种以上的物质混合而成的物质 只由一种物质组成的物质
表示 通常不能用一个化学式表示 可以用一个化学式表示
特性 没有固定组成,各成分保持原来的性质 具有固定的组成和性质
判断依据 是否只含有一种物质 联系 纯净物 混合物 (2)区分单质、化合物与氧化物
分类 单质 化合物 氧化物
概念 由同种元素组成的纯净物 含有不同种元素的纯净物 由两种元素组成的化合物中,其中一种元素是氧元素
所含元 素种类 一种 至少两种 两种,且其中一种是氧元素
(3)有机物:通常指含碳元素的化合物,CO、CO2和碳酸盐等除外。
判断下列说法的正误。
1.冰水混合物属于纯净物。 ( )
2.NaHCO3属于氧化物。 ( )
3.单质是由同种元素组成的纯净物,所以由同种元素组成的物质一定是单质。 ( )
易错易混
√
×
×
4.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物。 ( )
5.有机物是含有碳元素的化合物,则含有碳元素的化合物一定是有机物。 ( )
6.酸中都含有氢元素,则含有氢元素的物质一定为酸。 ( )
√
×
×
1.概念:用元素符号和数字的组合表示物质组成的式子。
化学式(近5年5考)
知识点5
2.书写
(1)书写单质的化学式
单质种类 书写方式 举例
稀有气体 用元素符号表示 氦写为He,氖写为Ne
金属和固态非金属 习惯上用元素符号表示 铁写为Fe,碳写为C
气态非金属 在元素符号右下角写上表示分子中所含原子数的数字 氧气写为O2
(2)书写化合物的化学式
①原则:“读前写后,数变角码”,如四氧化三铁写为Fe3O4。
②注意事项
a.当某组成元素的原子个数是1时,1省略不写。
b.氧化物:一般把氧的元素符号写在右边,另一种元素符号写在左边,如CO2。
c.由金属元素与非金属元素组成的化合物:一般把金属的元素符号写在左边,非金属的元素符号写在右边,如NaCl。
【特别提醒】
(1)书写化合物的化学式时,原子个数比一般化为最简整数比,但过氧化物、有机物等除外,如H2O2、C6H12O6。
(2)若化合物中原子团的下角标不为“1”,需要用括号将其括起来,整体加下标,如Ca(OH)2。
3.意义
意义 举例(以“H2O”为例)
宏观 表示该物质的元素组成 表示水由氢元素和氧元素组成
表示一种物质 表示水这种物质
微观 表示该物质一个分子的构成(针对由分子构成的物质) 表示1个水分子由2个氢原子和1个氧原子构成
表示该物质的一个分子或原子 表示 1个水分子
4.相关计算
【特别提醒】计算某元素的质量分数时,计算公式中的“×100%”不能省略。
一、判断下列化学式书写的正误。
1.氦气——He2。 ( )
2.银——AG。 ( )
3.氧化铝——AlO。 ( )
4.四氧化三铁——Fe3O4。 ( )
5.碳酸——HCO3。 ( )
6.氢氧化钾——K(OH)2。 ( )
7.氯化铁——FeCl2。 ( )
8.高锰酸钾——K2MnO4。 ( )
易错易混
×
×
×
√
×
×
×
×
二、判断下列说法的正误。
1.1个C6H12O6分子中含有3个氧分子。 ( )
2.1个H2O2分子由1个氢分子和1个氧分子构成。 ( )
3.C6H12O6中碳、氢、氧元素的质量比为1∶2∶1。 ( )
4.C2H5OH中氢元素质量分数最大。 ( )
5.CH4属于有机物。 ( )
6.C6H12O6的相对分子质量为180 g。 ( )
×
×
×
×
√
×
1.表示方法:通常在元素符号或原子团的正上方用“+n”或“-n”表示,n为1时不能省略。如2O表示水中氢元素的化合价为+1。
化合价(近5年5考)
知识点6
2.一些常见元素和原子团(也叫根)的化合价
(1)常见元素的化合价
H:_____ O:_____ Na:_____
Mg:_____ Al:_____ K:_____
Ca:_____ Zn:_____ Ag:_____
Ba:_____ C:+2、+4 Fe:+2、+3
Cu:+1、+2 S:-2、+4、+6 Cl:-1、+1、+5、+7
+1
-2
+1
+2
+3
+1
+2
+2
+1
+2
【巧学巧记】常见元素的化合价:一价钾钠氯氢银,二价氧钙钡镁锌;三铝四硅五价磷,二三铁、二四碳;二四六硫都齐全,铜汞二价最常见;氢一氧二为标准,单质为零永不变。
(2)常见原子团的化合价
原子团名称 铵根 氢氧根 硝酸根 硫酸根 碳酸根 磷酸根
离子符号 OH-
化合价 _____ _____ _____ _____ _____ -3
【巧学巧记】常见原子团的化合价:负一氢氧硝酸根,负二硫酸碳酸根,负三记住磷酸根,正一价的是铵根。
+1
-1
-1
-2
-2
3.计算(以计算CaCO3中C的化合价为例)
1.H2O2中氧元素的化合价为-2。 ( )
2.CO和CO2中碳元素的化合价相同。 ( )
3. NH4NO3中氮元素显示不同的化合价。 ( )
4.O2和O3中氧元素的化合价都为0。 ( )
5.高锰酸钾中锰元素的化合价可标注为KO4。 ( )
易错易混
×
×
√
√
√
化学符号周围数字的含义(近5年2考)
知识点7
判断下列说法的正误。
1.“2O”表示2个氧元素。 ( )
2.2个镁离子可表示为“2Mg2+”。 ( )
易错易混
×
√
某小组用如图装置探究水的组成及变化,回答下列问题。
实验分阶·提能力
探究水的组成及变化(电解水)(近5年1考)
实验3
例
一阶 基础知识
【实验原理】
(1)电解水的化学方程式为_____________________。
【实验现象】
(2)接通直流电源后,电极表面均出现气泡,一段时间后,两个玻璃管内液面均下降,玻璃管a、b所收集的气体体积比约为______。
2H2O2H2↑+O2↑
2∶1
【生成气体的检验】
(3)正极:用燃着的木条检验产生的气体,观察到________________,说明该气体是_____________。
(4)负极:用燃着的木条检验产生的气体,观察到______________________
____,说明该气体是_____________。
【实验结论】
(5)由该实验得出的结论是水是由________________组成的。
木条燃烧得更旺
氧气(或O2)
气体燃烧并产生淡蓝色
火
氢气(或H2)
氢元素和氧元素
二阶 质疑反思
(6)向水中加入少量NaOH溶液或Na2SO4溶液的作用是____________。
(7)【课标新增·作图】补全电解水实验产生气体的体积和质量关系图。
H2
O2
O2
H2
增强导电性
三阶 拓展延伸
(8)【课标新增·作图】电解水的微观过程模拟示意图如图,请将框内补画完整并回答问题。
①该实验说明1个水分子是由______________________构成的。
②该实验证明了化学反应的实质是__________________________________
______。
2个氢原子和1个氧原子
分子分裂成原子,原子重新组合成新
的分子
(9)【数据分析】学习小组测定两个玻璃管中逸出气体的体积,并记录了如下四组实验数据:
组别 氢气体 积/mL 氧气体
积/mL
甲 5 2.3
乙 10 4.8
丙 15 7.3
丁 20 9.8
同学们发现,每组收集到的氢气与氧气的体积比不同,随着气体量的增加,氧气体积始终比氢气体积的一半少0.2 mL,产生此现象的原因可能是____________________________________________________________________(写1点)。
相同条件下,氧气在水中的溶解度大于氢气在水
中的溶解度(表述合理即可)
测定纯净物元素组成的一般思路与方法
构建模型
1.(安徽真题组合)判断下列说法是否正确:
(1)禁止使用化肥和农药,防止水体污染。 ( )
(2)污水分级处理后再利用。 ( )
(3)生活污水集中处理达标后排放。 ( )
(4)用洗菜的水冲厕所。 ( )
真题分点·明趋势
水资源及其利用(近5年4考)
命题点1
×
√
√
√
2.理论上电解水得到氧气和氢气的体积比约为1∶2,某同学用碳棒作电极进行电解水实验,得到氧气和氢气的体积比小于1∶2,
对产生此现象原因的猜想不合理的是( )
A.部分氧气溶于水
B.部分氧气与碳棒反应
C.部分氧气被碳棒吸附
D.部分氧气与氢气反应重新生成了水
探究水的组成及变化(电解水)(近5年2考)
命题点2
D
3.某自热火锅的发热包成分标识如图所示。下列各组物质
所属类别正确的是( )
物质的分类(近5年5考)
命题点3
D
成分
生石灰、苛性钠、铝粉、活性炭、还原铁粉、碳酸钠
选项 物质 类别
A 生石灰和苛性钠 碱
B 活性炭和碳酸钠 含碳化合物
C 苛性钠和碳酸钠 盐
D 铁粉和铝粉 金属单质
4.端午时节,粽叶飘香。粽叶中的异荭草苷(C21H20O11)具有抗菌、抗病毒、增强免疫力等作用。
下列关于异荭草苷的说法错误的是( )
A.属于有机物
B.由52个原子构成
C.由碳、氢、氧三种元素组成
D.有益于人体健康
化学式的意义及相关计算(近5年5考)
命题点4
B
5.“赠人玫瑰,手留余香”,玫瑰中大马酮(化学式为C13H18O)是其香味的来源。下列有关大马酮的说法,正确的是( )
A.一个分子含有9个H2
B.碳、氢元素的质量比为13∶18
C.属于无机物
D.分子在不断运动
D
6.荷叶中含有的荷叶碱(化学式为C19H21NO2)具有降脂、抑菌等作用。下列有关荷叶碱的说法,正确的是( )
A.含有O2
B.由四种非金属元素组成
C.属于氧化物
D.其中氢元素的质量分数最大
B
7.疫情防控期间用到一种免洗手消毒凝胶,其中含有正丙醇(化学式为C3H8O)。下列有关正丙醇的说法,正确的是( )
A.属于无机物
B.1个分子中含有12个原子
C.相对分子质量为60 g
D.碳、氢元素的质量比为3∶8
B
8.连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为C7H6O5)。下列有关没食子酸的说法,
正确的是( )
A.属于氧化物
B.碳、氢、氧元素的质量比为12∶1∶16
C.含有3个原子
D.完全燃烧生成CO2和H2O
D
9.(4)臭氧的化学式O3的微观意义是____________
______________________________(写1点)。
1个臭氧分子
是由3个氧原子构成的(合理即可)
10.按要求填空:
(1)Fe2O3中铁元素化合价为_____。
(2)从元素角度分析,氯化钠溶液中+1价的元素有_________(填元素符号)。
化合价的计算(近5年5考)
命题点5
+3
Na、H
中考一轮复习 教材同步复习
第四单元 自然界的水
思维导图·构体系
知识精讲·夯基础
真题分点·明趋势
实验分阶·提能力
思维导图·构体系
1.水资源现状:地球上水的储量虽然很大,但大部分是含盐量很高的海水。淡水只约占地球水储量的2.53%。
知识精讲·夯基础
水资源及其利用(近5年4考)
知识点1
2.保护水资源
(1)合理利用水资源
①节约用水:如工业用水重复使用;采用节水
灌溉方式;推广节水器具等。
②合理调配水资源:如通过修建水库和调水工
程等措施改善水资源时空分布不均的局面。
(2)防治水体污染:应用新技术、新工艺减少污染物的产生;对污水进行处理,使之符合排放标准;合理施用农药、化肥。
国家节水标志
判断下列说法的正误。
1.大力开采地下水,缓解水资源短缺。 ( )
2.大量使用含磷洗衣粉会造成水体富营养化。 ( )
易错易混
×
√
1.自来水厂净水过程(如图)
水的净化(近5年3考)
知识点2
2.常见的净水方法
净水方法 涉及的物质及作用
沉降 加入明矾,加速水中悬浮杂质的沉降
______ 除去水中的难溶性或不溶性杂质
吸附 利用活性炭的______作用除去水中的色素和异味[2022.15(2)]
蒸馏 几乎可以除去水中的所有杂质
杀菌消毒 加入消毒剂,除去水中的细菌和病毒
过滤
吸附
3.活性炭净水器(如图)
4.硬水与软水
(1)概念
①硬水:含有较多可溶性钙、镁化合物的水。
②软水:不含或含较少可溶性钙、镁化合物的水。
(2)硬水的危害:浪费肥皂且洗不净衣物,使衣物变硬;使锅炉内结垢,浪费燃料,损坏管道,可能引起爆炸。
判断下列说法的正误。
1.经过自来水厂净化后的水为纯净物。 ( )
2.过滤可以除去水中所有杂质。 ( )
3.沉降、过滤、吸附、蒸馏、杀菌消毒的过程中,均只发生物理变化。 ( )
4.沉降、过滤、吸附、蒸馏、杀菌消毒是净化水的常用方法,单一操作净化程度较高的方法是蒸馏。 ( )
5.利用活性炭的吸附性能除去水中色素,但不能除去异味。 ( )
6.硬水一定是混合物,软水一定是纯净物。 ( )
易错易混
×
×
×
√
×
×
1.从氢气的燃烧实验探究水的组成
(1)氢气的性质
①物理性质:无色、无臭、____溶于水的气体,密度比空气的____。
②化学性质:a.可燃性,可作______;b.还原性,能与某些金属氧化物发生反应,如CuO+H2 Cu+H2O,可用于冶炼金属。
水的组成(近5年2考)
知识点3
难
小
燃料
(2)检验氢气的纯度
Ⅰ.用拇指堵住集满氢气的试管口 Ⅱ.靠近火焰,移开拇指
从氢气的燃烧实验探究水的组成
【实验原理】______________________(用化学方程式表示)。
【实验装置及现象】
【实验结论】水是由________和________组成的。
教材小实验
淡蓝
2H2+O2 2H2O
氢元素
氧元素
判断下列说法的正误。
1.电解水实验说明水是由氢气和氧气组成的。 ( )
2.电解水时生成氢气与氧气的质量比为2∶1。 ( )
3.混有一定量空气或氧气的H2、CO、CH4等可燃性气体遇明火可能会发生爆炸,因此点燃前一定要检验其纯度。 ( )
易错易混
×
×
√
1.物质的简单分类
物质的分类与区分(近5年5考)
知识点4
2.物质的类别区分
(1)区分混合物与纯净物
分类 混合物 纯净物
概念 由两种或两种以上的物质混合而成的物质 只由一种物质组成的物质
表示 通常不能用一个化学式表示 可以用一个化学式表示
特性 没有固定组成,各成分保持原来的性质 具有固定的组成和性质
判断依据 是否只含有一种物质 联系 纯净物 混合物 (2)区分单质、化合物与氧化物
分类 单质 化合物 氧化物
概念 由同种元素组成的纯净物 含有不同种元素的纯净物 由两种元素组成的化合物中,其中一种元素是氧元素
所含元 素种类 一种 至少两种 两种,且其中一种是氧元素
(3)有机物:通常指含碳元素的化合物,CO、CO2和碳酸盐等除外。
判断下列说法的正误。
1.冰水混合物属于纯净物。 ( )
2.NaHCO3属于氧化物。 ( )
3.单质是由同种元素组成的纯净物,所以由同种元素组成的物质一定是单质。 ( )
易错易混
√
×
×
4.化合物是由不同种元素组成的纯净物,则由不同种元素组成的纯净物一定是化合物。 ( )
5.有机物是含有碳元素的化合物,则含有碳元素的化合物一定是有机物。 ( )
6.酸中都含有氢元素,则含有氢元素的物质一定为酸。 ( )
√
×
×
1.概念:用元素符号和数字的组合表示物质组成的式子。
化学式(近5年5考)
知识点5
2.书写
(1)书写单质的化学式
单质种类 书写方式 举例
稀有气体 用元素符号表示 氦写为He,氖写为Ne
金属和固态非金属 习惯上用元素符号表示 铁写为Fe,碳写为C
气态非金属 在元素符号右下角写上表示分子中所含原子数的数字 氧气写为O2
(2)书写化合物的化学式
①原则:“读前写后,数变角码”,如四氧化三铁写为Fe3O4。
②注意事项
a.当某组成元素的原子个数是1时,1省略不写。
b.氧化物:一般把氧的元素符号写在右边,另一种元素符号写在左边,如CO2。
c.由金属元素与非金属元素组成的化合物:一般把金属的元素符号写在左边,非金属的元素符号写在右边,如NaCl。
【特别提醒】
(1)书写化合物的化学式时,原子个数比一般化为最简整数比,但过氧化物、有机物等除外,如H2O2、C6H12O6。
(2)若化合物中原子团的下角标不为“1”,需要用括号将其括起来,整体加下标,如Ca(OH)2。
3.意义
意义 举例(以“H2O”为例)
宏观 表示该物质的元素组成 表示水由氢元素和氧元素组成
表示一种物质 表示水这种物质
微观 表示该物质一个分子的构成(针对由分子构成的物质) 表示1个水分子由2个氢原子和1个氧原子构成
表示该物质的一个分子或原子 表示 1个水分子
4.相关计算
【特别提醒】计算某元素的质量分数时,计算公式中的“×100%”不能省略。
一、判断下列化学式书写的正误。
1.氦气——He2。 ( )
2.银——AG。 ( )
3.氧化铝——AlO。 ( )
4.四氧化三铁——Fe3O4。 ( )
5.碳酸——HCO3。 ( )
6.氢氧化钾——K(OH)2。 ( )
7.氯化铁——FeCl2。 ( )
8.高锰酸钾——K2MnO4。 ( )
易错易混
×
×
×
√
×
×
×
×
二、判断下列说法的正误。
1.1个C6H12O6分子中含有3个氧分子。 ( )
2.1个H2O2分子由1个氢分子和1个氧分子构成。 ( )
3.C6H12O6中碳、氢、氧元素的质量比为1∶2∶1。 ( )
4.C2H5OH中氢元素质量分数最大。 ( )
5.CH4属于有机物。 ( )
6.C6H12O6的相对分子质量为180 g。 ( )
×
×
×
×
√
×
1.表示方法:通常在元素符号或原子团的正上方用“+n”或“-n”表示,n为1时不能省略。如2O表示水中氢元素的化合价为+1。
化合价(近5年5考)
知识点6
2.一些常见元素和原子团(也叫根)的化合价
(1)常见元素的化合价
H:_____ O:_____ Na:_____
Mg:_____ Al:_____ K:_____
Ca:_____ Zn:_____ Ag:_____
Ba:_____ C:+2、+4 Fe:+2、+3
Cu:+1、+2 S:-2、+4、+6 Cl:-1、+1、+5、+7
+1
-2
+1
+2
+3
+1
+2
+2
+1
+2
【巧学巧记】常见元素的化合价:一价钾钠氯氢银,二价氧钙钡镁锌;三铝四硅五价磷,二三铁、二四碳;二四六硫都齐全,铜汞二价最常见;氢一氧二为标准,单质为零永不变。
(2)常见原子团的化合价
原子团名称 铵根 氢氧根 硝酸根 硫酸根 碳酸根 磷酸根
离子符号 OH-
化合价 _____ _____ _____ _____ _____ -3
【巧学巧记】常见原子团的化合价:负一氢氧硝酸根,负二硫酸碳酸根,负三记住磷酸根,正一价的是铵根。
+1
-1
-1
-2
-2
3.计算(以计算CaCO3中C的化合价为例)
1.H2O2中氧元素的化合价为-2。 ( )
2.CO和CO2中碳元素的化合价相同。 ( )
3. NH4NO3中氮元素显示不同的化合价。 ( )
4.O2和O3中氧元素的化合价都为0。 ( )
5.高锰酸钾中锰元素的化合价可标注为KO4。 ( )
易错易混
×
×
√
√
√
化学符号周围数字的含义(近5年2考)
知识点7
判断下列说法的正误。
1.“2O”表示2个氧元素。 ( )
2.2个镁离子可表示为“2Mg2+”。 ( )
易错易混
×
√
某小组用如图装置探究水的组成及变化,回答下列问题。
实验分阶·提能力
探究水的组成及变化(电解水)(近5年1考)
实验3
例
一阶 基础知识
【实验原理】
(1)电解水的化学方程式为_____________________。
【实验现象】
(2)接通直流电源后,电极表面均出现气泡,一段时间后,两个玻璃管内液面均下降,玻璃管a、b所收集的气体体积比约为______。
2H2O2H2↑+O2↑
2∶1
【生成气体的检验】
(3)正极:用燃着的木条检验产生的气体,观察到________________,说明该气体是_____________。
(4)负极:用燃着的木条检验产生的气体,观察到______________________
____,说明该气体是_____________。
【实验结论】
(5)由该实验得出的结论是水是由________________组成的。
木条燃烧得更旺
氧气(或O2)
气体燃烧并产生淡蓝色
火
氢气(或H2)
氢元素和氧元素
二阶 质疑反思
(6)向水中加入少量NaOH溶液或Na2SO4溶液的作用是____________。
(7)【课标新增·作图】补全电解水实验产生气体的体积和质量关系图。
H2
O2
O2
H2
增强导电性
三阶 拓展延伸
(8)【课标新增·作图】电解水的微观过程模拟示意图如图,请将框内补画完整并回答问题。
①该实验说明1个水分子是由______________________构成的。
②该实验证明了化学反应的实质是__________________________________
______。
2个氢原子和1个氧原子
分子分裂成原子,原子重新组合成新
的分子
(9)【数据分析】学习小组测定两个玻璃管中逸出气体的体积,并记录了如下四组实验数据:
组别 氢气体 积/mL 氧气体
积/mL
甲 5 2.3
乙 10 4.8
丙 15 7.3
丁 20 9.8
同学们发现,每组收集到的氢气与氧气的体积比不同,随着气体量的增加,氧气体积始终比氢气体积的一半少0.2 mL,产生此现象的原因可能是____________________________________________________________________(写1点)。
相同条件下,氧气在水中的溶解度大于氢气在水
中的溶解度(表述合理即可)
测定纯净物元素组成的一般思路与方法
构建模型
1.(安徽真题组合)判断下列说法是否正确:
(1)禁止使用化肥和农药,防止水体污染。 ( )
(2)污水分级处理后再利用。 ( )
(3)生活污水集中处理达标后排放。 ( )
(4)用洗菜的水冲厕所。 ( )
真题分点·明趋势
水资源及其利用(近5年4考)
命题点1
×
√
√
√
2.理论上电解水得到氧气和氢气的体积比约为1∶2,某同学用碳棒作电极进行电解水实验,得到氧气和氢气的体积比小于1∶2,
对产生此现象原因的猜想不合理的是( )
A.部分氧气溶于水
B.部分氧气与碳棒反应
C.部分氧气被碳棒吸附
D.部分氧气与氢气反应重新生成了水
探究水的组成及变化(电解水)(近5年2考)
命题点2
D
3.某自热火锅的发热包成分标识如图所示。下列各组物质
所属类别正确的是( )
物质的分类(近5年5考)
命题点3
D
成分
生石灰、苛性钠、铝粉、活性炭、还原铁粉、碳酸钠
选项 物质 类别
A 生石灰和苛性钠 碱
B 活性炭和碳酸钠 含碳化合物
C 苛性钠和碳酸钠 盐
D 铁粉和铝粉 金属单质
4.端午时节,粽叶飘香。粽叶中的异荭草苷(C21H20O11)具有抗菌、抗病毒、增强免疫力等作用。
下列关于异荭草苷的说法错误的是( )
A.属于有机物
B.由52个原子构成
C.由碳、氢、氧三种元素组成
D.有益于人体健康
化学式的意义及相关计算(近5年5考)
命题点4
B
5.“赠人玫瑰,手留余香”,玫瑰中大马酮(化学式为C13H18O)是其香味的来源。下列有关大马酮的说法,正确的是( )
A.一个分子含有9个H2
B.碳、氢元素的质量比为13∶18
C.属于无机物
D.分子在不断运动
D
6.荷叶中含有的荷叶碱(化学式为C19H21NO2)具有降脂、抑菌等作用。下列有关荷叶碱的说法,正确的是( )
A.含有O2
B.由四种非金属元素组成
C.属于氧化物
D.其中氢元素的质量分数最大
B
7.疫情防控期间用到一种免洗手消毒凝胶,其中含有正丙醇(化学式为C3H8O)。下列有关正丙醇的说法,正确的是( )
A.属于无机物
B.1个分子中含有12个原子
C.相对分子质量为60 g
D.碳、氢元素的质量比为3∶8
B
8.连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(化学式为C7H6O5)。下列有关没食子酸的说法,
正确的是( )
A.属于氧化物
B.碳、氢、氧元素的质量比为12∶1∶16
C.含有3个原子
D.完全燃烧生成CO2和H2O
D
9.(4)臭氧的化学式O3的微观意义是____________
______________________________(写1点)。
1个臭氧分子
是由3个氧原子构成的(合理即可)
10.按要求填空:
(1)Fe2O3中铁元素化合价为_____。
(2)从元素角度分析,氯化钠溶液中+1价的元素有_________(填元素符号)。
化合价的计算(近5年5考)
命题点5
+3
Na、H
同课章节目录
