(考点集训)2025年化学中考一轮复习10:课时2 常见的盐课件(人教版)
文档属性
| 名称 | (考点集训)2025年化学中考一轮复习10:课时2 常见的盐课件(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 815.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-13 00:00:00 | ||
图片预览






文档简介
(共33张PPT)
中考一轮复习 教材同步复习
第十单元 常见的酸、碱、盐
课时2 常见的盐
思维导图·构体系
知识精讲·夯基础
真题分点·明趋势
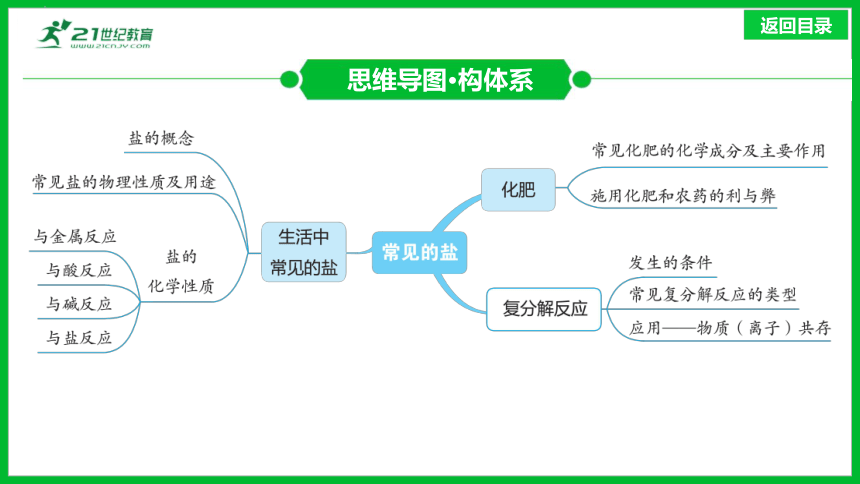
思维导图·构体系
1.盐的概念:指一类组成里含有__________(或__________)和酸根离子的化合物。
知识精讲·夯基础
生活中常见的盐(近5年5考)
知识点1
金属离子
铵根离子
【归纳总结】酸、碱、盐的比较
类别 在水溶液中的特点 举例
酸 阳离子都为______ HCl、H2SO4
碱 阴离子都为________ NaOH、Ca(OH)2
盐 阳离子含有金属离子或铵根离子 Na2CO3、NH4Cl
H+
OH-
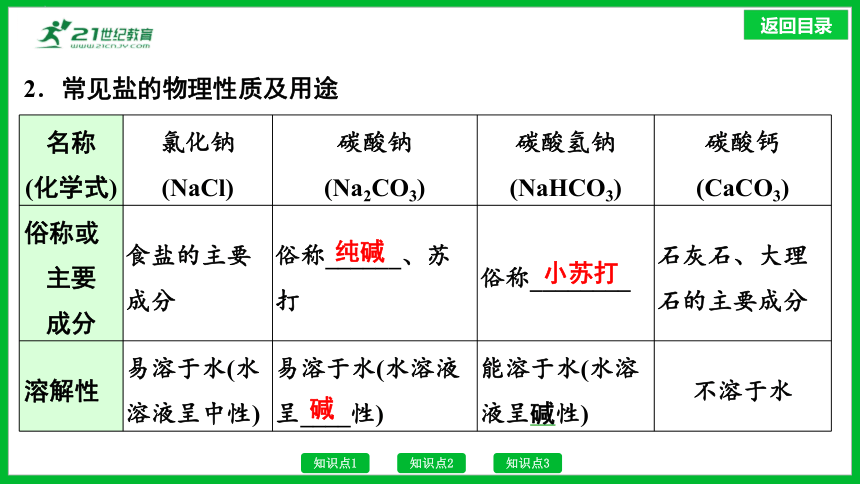
2.常见盐的物理性质及用途
名称 (化学式) 氯化钠 (NaCl) 碳酸钠 (Na2CO3) 碳酸氢钠 (NaHCO3) 碳酸钙
(CaCO3)
俗称或 主要 成分 食盐的主要成分 俗称______、苏打 俗称________ 石灰石、大理石的主要成分
溶解性 易溶于水(水溶液呈中性) 易溶于水(水溶液呈____性) 能溶于水(水溶液呈碱性) 不溶于水
纯碱
小苏打
碱
用途 ①配制生理盐水;②选种;③作工业原料;④曾作融雪剂;⑤作调味品,腌渍食物 广泛用于玻璃、造纸、纺织等行业及洗涤剂的生产 ①制作发酵粉;②治疗胃酸过多症 ①石灰石或大理石作建筑材料;②作补钙剂;③在实验室中常用石灰石或大理石制取CO2
【备考补充】侯德榜发明了“联合制碱法”(又称侯氏制碱法),制碱原理为NH3+H2O+CO2+NaClNH4Cl+NaHCO3↓、2NaHCO3 Na2CO3+H2O+CO2↑。
3.盐的化学性质
(1)化学通性(盐四条)
化学性质 举例 化学方程式 现象
与金属反应(可溶性盐+金属→新盐+新金属,置换反应) 硝酸银溶液与铜反应:_____________ ________________________________ 铜表面有银白色固体析出,溶液由____色变为____色
2AgNO3+Cu
===== Cu(NO3)2+2Ag
无
蓝
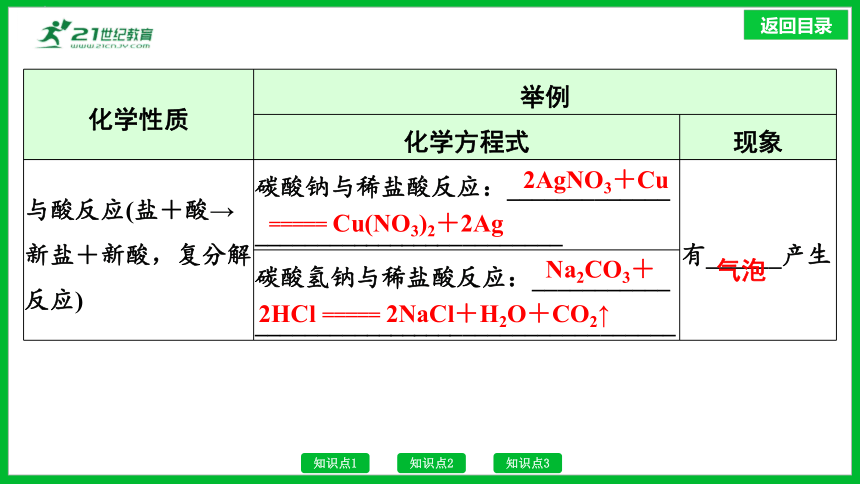
化学性质 举例 化学方程式 现象
与酸反应(盐+酸→新盐+新酸,复分解反应) 碳酸钠与稀盐酸反应:_____________ _________________________ 有______产生
碳酸氢钠与稀盐酸反应:___________ __________________________________ 2AgNO3+Cu
===== Cu(NO3)2+2Ag
Na2CO3+
2HCl ===== 2NaCl+H2O+CO2↑
气泡
化学性质 举例 化学方程式 现象
与碱反应(可溶性盐+可溶性碱→新碱+新盐,复分解反应) 硫酸铜溶液与氢氧化钙溶液反应: __________________________________________ 有__________产生
CuSO4+Ca(OH)2 ===== Cu(OH)2↓
+CaSO4
蓝色沉淀
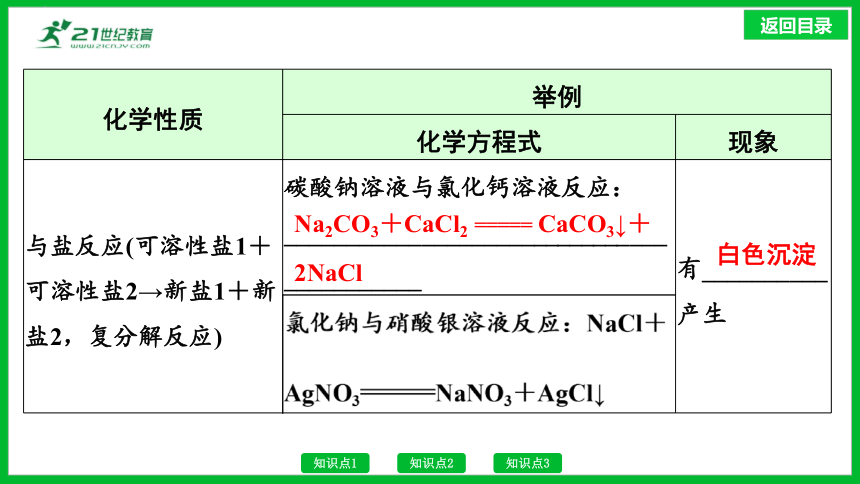
化学性质 举例 化学方程式 现象
与盐反应(可溶性盐1+可溶性盐2→新盐1+新盐2,复分解反应) 碳酸钠溶液与氯化钙溶液反应: __________________________________________ 有__________产生
Na2CO3+CaCl2 ===== CaCO3↓+
2NaCl
白色沉淀
(2)化学特性
①碳酸氢钠加热易分解,化学方程式为2NaHCO3 Na2CO3+H2O+CO2↑。
②碳酸钙在高温下能够分解,化学方程式为CaCO3 CaO+CO2↑(用于工业上制取CO2)。
判断下列说法的正误。
1.盐中一定含有金属元素。 ( )
2.纯碱属于碱。 ( )
3.盐溶液的pH都等于7。 ( )
4.氯化钠溶液中存在自由移动的离子,能导电;蔗糖溶液中不存在自由移动的离子,不能导电。 ( )
易错易混
×
×
×
√
5.侯氏制碱法中的“碱”是指小苏打。 ( )
6.用纯碱溶液洗去铁制品表面的铁锈。 ( )
7.碳酸盐与酸反应能放出气体,则与酸反应放出气体的物质一定是碳酸盐。 ( )
×
×
×
1.发生的条件:两种化合物互相交换成分,有______或有______或有____生成。
2.常见复分解反应的类型:①酸+碱;②酸+盐;③酸+金属氧化物;④可溶性碱+可溶性盐;⑤可溶性盐1+可溶性盐2。
复分解反应(近5年3考)
知识点2
沉淀
气体
水
3.应用——物质(离子)共存
(1)物质共存的条件:物质(即所含离子)之间不会反应生成沉淀或气体或水。
(2)常见不能共存的离子对
【巧学巧记】盐的溶解性记忆口诀:钾钠硝铵溶水快,硫酸盐中钡不溶;氯化物中银不溶,碳酸盐溶钾钠铵。
(3)物质共存的隐含条件
①pH<7的溶液或酸性溶液:溶液中一定存在H+。
②pH>7的溶液或碱性溶液:溶液中一定存在OH-。
③无色溶液:溶液中不存在C(显____色)、Fe(显______色)、Fe(显____色)等。
蓝
浅绿
黄
判断下列说法的正误。
1.复分解反应有沉淀或有气体或有水生成,则有沉淀或有气体或有水生成的反应一定是复分解反应。 ( )
2.MgCl2、NaCl、KCl可在能使无色酚酞溶液变红的溶液中共存。
( )
易错易混
×
×
1.常见化肥的化学成分及主要作用
化肥(近5年5考)
知识点3
分类 化学成分 主要作用
____肥 尿素[CO(NH2)2]、氯化铵(NH4Cl)、硝酸钠(NaNO3)等 可以促进____________________,使叶色浓绿,提高植物蛋白质含量
氮
植物茎、叶生长茂盛
分类 化学成分 主要作用
____肥 磷酸钙[Ca3(PO4)2]等 可以促进作物生长,还可以增强作物的____________能力
____肥 硫酸钾(K2SO4)、氯化钾(KCl)等 可以保证各种代谢过程顺利进行、促进植物生长、增强_______
___________能力
复合肥 磷酸二氢铵(NH4H2PO4)、硝酸钾(KNO3)等 能同时均匀地供给作物几种养分
磷
抗寒、抗旱
钾
抗病虫
害和抗倒伏
【巧学巧记】化肥的作用:钾抗倒伏磷抗旱(寒),叶色发黄要用氮。
2.施用化肥和农药的利与弊
(1)利:提高农作物产量,解决了部分地区粮食短缺的问题。
(2)弊:不合理的施用化肥会造成土壤退化,以及土壤、水和大气环境的污染。
判断下列说法的正误。
1.复合肥是指含有N、P、K三种营养元素的化肥。 ( )
2.目前,施用化肥和农药是提高农作物产量的重要手段,不能禁止施用,应合理施用。 ( )
易错易混
×
√
1.判断说法是否正确:向某固体中加入稀盐酸,有气体产生,则该固体一定是Na2CO3。 ( )
2.(4)氯化钠在生活中的用途有________________
____(写1点)。
真题分点·明趋势
常见的盐(近5年5考)
命题点1
×
作调味品(合理即
可)
3.我国化学家侯德榜发明的侯氏制碱法,开创了世界制碱工业的新纪元。制碱工艺中的关键反应为NaCl+CO2+NH3+H2O ===== NaHCO3↓+NH4Cl。室温(20 ℃)下,某兴趣小组在实验室利用如图装置模拟该反应。
已知:
①20 ℃时,几种盐的溶解度如表:
②氨气极易溶于饱和食盐水,形成的溶液呈碱性。
物质 NaCl NaHCO3 NH4Cl
溶解度/g 36.0 9.6 37.2
(1)为配制饱和食盐水,应向100 g水中至少加入______ g NaCl固体。
(2)仪器a的名称是______,装置D的作用是__________。
(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为_________________________________________。
(4)为使CO2在装置C中能充分吸收,可采取的措施是__________________
____________________________。
36.0
试管
产生氨气
NaHCO3+HCl ===== NaCl +H2O +CO2↑
向装置C中通入NH3
后,再通入CO2(合理即可)
充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。
查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。
(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl的原因是___________________________________________________________________________。
(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是____________
___________________________________________________________________________________。
反应生成的NaHCO3质量较大,且在20 ℃时,NaHCO3溶解度较小(合理
即可)
母液中含有大
量N和少量Na+,加入NaCl,溶液中Cl-浓度增大,使NH4Cl结晶析
出(合理即可)
4.判断如下劳动项目所涉及的化学知识是否正确:
( )
化肥(近5年5考)
命题点2
×
劳动项目 化学知识
给校园中的花草施用草木灰(含K2CO3) K2CO3属于复合肥料
5.(2)经调查发现,长期过量施用一些氮肥是土壤呈酸性的原因之一。请写出一种氮肥的化学式:______________________
__________。
NH4Cl(或NaNO3,合理
即可)
中考一轮复习 教材同步复习
第十单元 常见的酸、碱、盐
课时2 常见的盐
思维导图·构体系
知识精讲·夯基础
真题分点·明趋势
思维导图·构体系
1.盐的概念:指一类组成里含有__________(或__________)和酸根离子的化合物。
知识精讲·夯基础
生活中常见的盐(近5年5考)
知识点1
金属离子
铵根离子
【归纳总结】酸、碱、盐的比较
类别 在水溶液中的特点 举例
酸 阳离子都为______ HCl、H2SO4
碱 阴离子都为________ NaOH、Ca(OH)2
盐 阳离子含有金属离子或铵根离子 Na2CO3、NH4Cl
H+
OH-
2.常见盐的物理性质及用途
名称 (化学式) 氯化钠 (NaCl) 碳酸钠 (Na2CO3) 碳酸氢钠 (NaHCO3) 碳酸钙
(CaCO3)
俗称或 主要 成分 食盐的主要成分 俗称______、苏打 俗称________ 石灰石、大理石的主要成分
溶解性 易溶于水(水溶液呈中性) 易溶于水(水溶液呈____性) 能溶于水(水溶液呈碱性) 不溶于水
纯碱
小苏打
碱
用途 ①配制生理盐水;②选种;③作工业原料;④曾作融雪剂;⑤作调味品,腌渍食物 广泛用于玻璃、造纸、纺织等行业及洗涤剂的生产 ①制作发酵粉;②治疗胃酸过多症 ①石灰石或大理石作建筑材料;②作补钙剂;③在实验室中常用石灰石或大理石制取CO2
【备考补充】侯德榜发明了“联合制碱法”(又称侯氏制碱法),制碱原理为NH3+H2O+CO2+NaClNH4Cl+NaHCO3↓、2NaHCO3 Na2CO3+H2O+CO2↑。
3.盐的化学性质
(1)化学通性(盐四条)
化学性质 举例 化学方程式 现象
与金属反应(可溶性盐+金属→新盐+新金属,置换反应) 硝酸银溶液与铜反应:_____________ ________________________________ 铜表面有银白色固体析出,溶液由____色变为____色
2AgNO3+Cu
===== Cu(NO3)2+2Ag
无
蓝
化学性质 举例 化学方程式 现象
与酸反应(盐+酸→新盐+新酸,复分解反应) 碳酸钠与稀盐酸反应:_____________ _________________________ 有______产生
碳酸氢钠与稀盐酸反应:___________ __________________________________ 2AgNO3+Cu
===== Cu(NO3)2+2Ag
Na2CO3+
2HCl ===== 2NaCl+H2O+CO2↑
气泡
化学性质 举例 化学方程式 现象
与碱反应(可溶性盐+可溶性碱→新碱+新盐,复分解反应) 硫酸铜溶液与氢氧化钙溶液反应: __________________________________________ 有__________产生
CuSO4+Ca(OH)2 ===== Cu(OH)2↓
+CaSO4
蓝色沉淀
化学性质 举例 化学方程式 现象
与盐反应(可溶性盐1+可溶性盐2→新盐1+新盐2,复分解反应) 碳酸钠溶液与氯化钙溶液反应: __________________________________________ 有__________产生
Na2CO3+CaCl2 ===== CaCO3↓+
2NaCl
白色沉淀
(2)化学特性
①碳酸氢钠加热易分解,化学方程式为2NaHCO3 Na2CO3+H2O+CO2↑。
②碳酸钙在高温下能够分解,化学方程式为CaCO3 CaO+CO2↑(用于工业上制取CO2)。
判断下列说法的正误。
1.盐中一定含有金属元素。 ( )
2.纯碱属于碱。 ( )
3.盐溶液的pH都等于7。 ( )
4.氯化钠溶液中存在自由移动的离子,能导电;蔗糖溶液中不存在自由移动的离子,不能导电。 ( )
易错易混
×
×
×
√
5.侯氏制碱法中的“碱”是指小苏打。 ( )
6.用纯碱溶液洗去铁制品表面的铁锈。 ( )
7.碳酸盐与酸反应能放出气体,则与酸反应放出气体的物质一定是碳酸盐。 ( )
×
×
×
1.发生的条件:两种化合物互相交换成分,有______或有______或有____生成。
2.常见复分解反应的类型:①酸+碱;②酸+盐;③酸+金属氧化物;④可溶性碱+可溶性盐;⑤可溶性盐1+可溶性盐2。
复分解反应(近5年3考)
知识点2
沉淀
气体
水
3.应用——物质(离子)共存
(1)物质共存的条件:物质(即所含离子)之间不会反应生成沉淀或气体或水。
(2)常见不能共存的离子对
【巧学巧记】盐的溶解性记忆口诀:钾钠硝铵溶水快,硫酸盐中钡不溶;氯化物中银不溶,碳酸盐溶钾钠铵。
(3)物质共存的隐含条件
①pH<7的溶液或酸性溶液:溶液中一定存在H+。
②pH>7的溶液或碱性溶液:溶液中一定存在OH-。
③无色溶液:溶液中不存在C(显____色)、Fe(显______色)、Fe(显____色)等。
蓝
浅绿
黄
判断下列说法的正误。
1.复分解反应有沉淀或有气体或有水生成,则有沉淀或有气体或有水生成的反应一定是复分解反应。 ( )
2.MgCl2、NaCl、KCl可在能使无色酚酞溶液变红的溶液中共存。
( )
易错易混
×
×
1.常见化肥的化学成分及主要作用
化肥(近5年5考)
知识点3
分类 化学成分 主要作用
____肥 尿素[CO(NH2)2]、氯化铵(NH4Cl)、硝酸钠(NaNO3)等 可以促进____________________,使叶色浓绿,提高植物蛋白质含量
氮
植物茎、叶生长茂盛
分类 化学成分 主要作用
____肥 磷酸钙[Ca3(PO4)2]等 可以促进作物生长,还可以增强作物的____________能力
____肥 硫酸钾(K2SO4)、氯化钾(KCl)等 可以保证各种代谢过程顺利进行、促进植物生长、增强_______
___________能力
复合肥 磷酸二氢铵(NH4H2PO4)、硝酸钾(KNO3)等 能同时均匀地供给作物几种养分
磷
抗寒、抗旱
钾
抗病虫
害和抗倒伏
【巧学巧记】化肥的作用:钾抗倒伏磷抗旱(寒),叶色发黄要用氮。
2.施用化肥和农药的利与弊
(1)利:提高农作物产量,解决了部分地区粮食短缺的问题。
(2)弊:不合理的施用化肥会造成土壤退化,以及土壤、水和大气环境的污染。
判断下列说法的正误。
1.复合肥是指含有N、P、K三种营养元素的化肥。 ( )
2.目前,施用化肥和农药是提高农作物产量的重要手段,不能禁止施用,应合理施用。 ( )
易错易混
×
√
1.判断说法是否正确:向某固体中加入稀盐酸,有气体产生,则该固体一定是Na2CO3。 ( )
2.(4)氯化钠在生活中的用途有________________
____(写1点)。
真题分点·明趋势
常见的盐(近5年5考)
命题点1
×
作调味品(合理即
可)
3.我国化学家侯德榜发明的侯氏制碱法,开创了世界制碱工业的新纪元。制碱工艺中的关键反应为NaCl+CO2+NH3+H2O ===== NaHCO3↓+NH4Cl。室温(20 ℃)下,某兴趣小组在实验室利用如图装置模拟该反应。
已知:
①20 ℃时,几种盐的溶解度如表:
②氨气极易溶于饱和食盐水,形成的溶液呈碱性。
物质 NaCl NaHCO3 NH4Cl
溶解度/g 36.0 9.6 37.2
(1)为配制饱和食盐水,应向100 g水中至少加入______ g NaCl固体。
(2)仪器a的名称是______,装置D的作用是__________。
(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为_________________________________________。
(4)为使CO2在装置C中能充分吸收,可采取的措施是__________________
____________________________。
36.0
试管
产生氨气
NaHCO3+HCl ===== NaCl +H2O +CO2↑
向装置C中通入NH3
后,再通入CO2(合理即可)
充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。
查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。
(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl的原因是___________________________________________________________________________。
(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是____________
___________________________________________________________________________________。
反应生成的NaHCO3质量较大,且在20 ℃时,NaHCO3溶解度较小(合理
即可)
母液中含有大
量N和少量Na+,加入NaCl,溶液中Cl-浓度增大,使NH4Cl结晶析
出(合理即可)
4.判断如下劳动项目所涉及的化学知识是否正确:
( )
化肥(近5年5考)
命题点2
×
劳动项目 化学知识
给校园中的花草施用草木灰(含K2CO3) K2CO3属于复合肥料
5.(2)经调查发现,长期过量施用一些氮肥是土壤呈酸性的原因之一。请写出一种氮肥的化学式:______________________
__________。
NH4Cl(或NaNO3,合理
即可)
同课章节目录
