人教版高中化学选修4 2.1 化学反应速率(课件) (共17张PPT)
文档属性
| 名称 | 人教版高中化学选修4 2.1 化学反应速率(课件) (共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 168.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-08 00:00:00 | ||
图片预览





文档简介
课件17张PPT。第二章 化学反应速率和化学平衡第一节 化学反应速率化学反应速率这一物理量是如何定义的?
怎样写表达式?
常用的单位是什么?
计算中应注意什么?
单位时间内反应物浓度的减少或生成物浓度的增加表达式:v=△C/△t单位:mol/(L.min)或mol/(L.s)
1.化学反应速率是指单位时间内物质的量浓度的变化,而不是指物质的量或物质质量的变化。
2.反应速率不取负值,通常所指的反应速率是一段时间内的平均速率,而不是某一时刻的瞬时速率。
3.在同一反应中,选用不同的物质表示速率,其数值不一样,故应标明是哪种物质 表示的化学反应速率,但这些数值表示的意义是一样的,均表示该反应的快慢。
4.各物质表示的反应速率之比等于各物质的化学计量数之比。
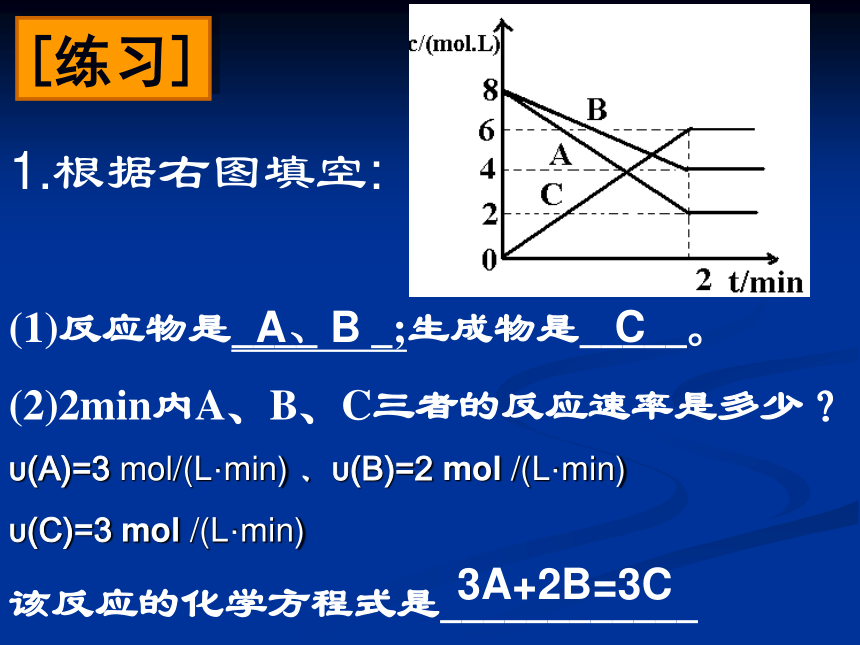
1.根据右图填空:(1)反应物是____ _;生成物是_____。
(2)2min内A、B、C三者的反应速率是多少?
υ(A)=3 mol/(L·min) 、υ(B)=2 mol /(L·min)
υ(C)=3 mol /(L·min)
该反应的化学方程式是____________[练习]A、BC3A+2B=3C2.在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(mol·L-1·s-1)表示,
且υ(A)、υ(B)、υ(C)之间有如下所示的关系: υ(B)=3υ(A) 3υ(C)=2υ(B)
则此反应可表示为( )
(A)2A+3B=2C (B)A+3B=2C
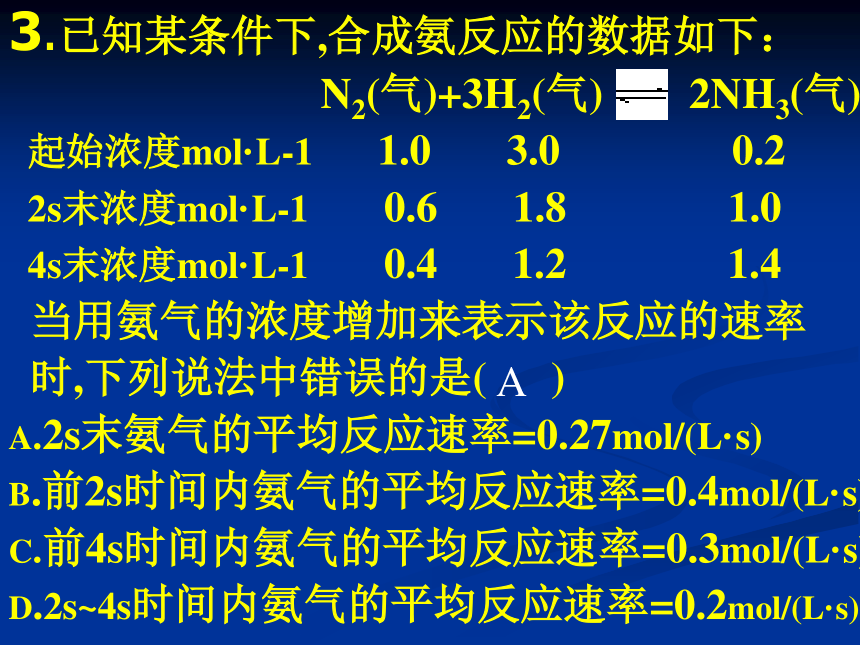
(C)3A+B=2C (D)A+B=C答案:B3.已知某条件下,合成氨反应的数据如下:
N2(气)+3H2(气) 2NH3(气)
起始浓度mol·L-1 1.0 3.0 0.2
2s末浓度mol·L-1 0.6 1.8 1.0
4s末浓度mol·L-1 0.4 1.2 1.4
当用氨气的浓度增加来表示该反应的速率
时,下列说法中错误的是( )
A.2s末氨气的平均反应速率=0.27mol/(L·s)
B.前2s时间内氨气的平均反应速率=0.4mol/(L·s)
C.前4s时间内氨气的平均反应速率=0.3mol/(L·s)
D.2s~4s时间内氨气的平均反应速率=0.2mol/(L·s)A4.反应4NH3+5O2 = 4NO+6H2O,在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率υ(x)(表示反应物的消耗速率或生成物的生成速率)为( )
(A)υ(O2)=0.01 mol·L-1·s-1
(B)υ(NO)=0.008 mol·L-1·s-1
(C)υ(H2O)=0.003 mol·L-1·s-1
(D)υ(NH3)=0.002 mol·L-1·s-1 答案: CD5.在四个不同的容器中,在不同的条件下进行合成氨反应。根据在相同时间内测定的结果判断,生成氨的速率最快的是( )
(A)υ(H2)=0.1 mol·L-1·min-1
(B)υ(N2)=0.2 mol·L-1·min-1
(C)υ(NH3)=0.15 mol·L-1·min-1
(D)υ(H2)=0.3 mol·L-1·min-1
答案: B比较一个反应的反应速率的快慢,必须找同一参照物答案:A6.在一个容积为2L的密闭容器中,发生如下反应:
3X(g)+Y(g)=2Z(g)
若最初加入的X、Y和Z都是1mol,反应中X的平均反应速率为0.12 mol·L-1·s-1。若要产物Z为1.8mol,反应所需的时间为( )
(A)5s (B)10s (C)15s (D)20s
思考??实验步骤:
1、连接实验装置
2、检查装置的气密性
3、先向锥形瓶中加入锌粒
然后再向分液漏斗中加入稀硫酸
4、使稀硫酸滴入锥形瓶与锌粒反应
5、观察收集10mLH2所用的时间
(实验2一1)实验分析∶用量气法测定该实验的速率时需注意什么问题?
怎样才能使反应速率的测定更加准确?
1)装置的气密性要好
2)倒入稀硫酸时速率要快
3)锌粒大小(表面积)基本相同
4)计时要迅速、准确分析探讨实验中需要注意的问题1.在该实验中难以控制的变量是什么?
锌粒大小(表面积)
2.根据你的掌握知识量气装置还有哪些?测量氢气体积方法有:当体系的温度恢复到室温后,要调节量筒的高度,使量筒内外的液面相平要上下移动量筒,使量筒内的液面与广口瓶中的液面相平要上下移动右边的玻璃管,使左右两管中的液面相平。思考:在室温和大气压强下,用右上图
示的装置进行实验,测得某一反应产生的
气体体积。
请回答下列问题:
(1)若反应刚结束时,观察到的实验现
象如右下图所示,这时不能立即取出导气
管,理由是 。
(2)本实验中测量气体体积时应注意到
的事项有 。参考答案
(1)因为装置内气体的温度没有恢复到室温,气体压强还不等于大气压强。
(2)待装置内气体的温度恢复到室温后,调节量筒使其内外液面持平。本实验还可以如何测定锌和稀硫酸反应的速率
1、测量溶液中的H+的浓度的变化
2、测量溶液中的Zn2+的浓度变化
3、测量1分钟收集到的H2的体积
4、测量反应体系的热量变化
… … … … … 学与问:19.广东2009年高考(12分)
某实验小组利用如下装置(部分固定装置略)
制备氧化钙(Ca3N2),并探究其实验式。
(1)按图连接好实验装置。检查装置的气密性,
方法是 。
(2)反应过程中末端导管必须插入试管A的水中,
目的是 。【答案】
(1)关闭活塞K,将玻璃导管A插入盛有水的试管中,微热反应管,试管A中有气泡冒出,停止加热。冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好。
(2)防止反应过程中空气进入反应管;便于观察N2的流速
怎样写表达式?
常用的单位是什么?
计算中应注意什么?
单位时间内反应物浓度的减少或生成物浓度的增加表达式:v=△C/△t单位:mol/(L.min)或mol/(L.s)
1.化学反应速率是指单位时间内物质的量浓度的变化,而不是指物质的量或物质质量的变化。
2.反应速率不取负值,通常所指的反应速率是一段时间内的平均速率,而不是某一时刻的瞬时速率。
3.在同一反应中,选用不同的物质表示速率,其数值不一样,故应标明是哪种物质 表示的化学反应速率,但这些数值表示的意义是一样的,均表示该反应的快慢。
4.各物质表示的反应速率之比等于各物质的化学计量数之比。
1.根据右图填空:(1)反应物是____ _;生成物是_____。
(2)2min内A、B、C三者的反应速率是多少?
υ(A)=3 mol/(L·min) 、υ(B)=2 mol /(L·min)
υ(C)=3 mol /(L·min)
该反应的化学方程式是____________[练习]A、BC3A+2B=3C2.在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(mol·L-1·s-1)表示,
且υ(A)、υ(B)、υ(C)之间有如下所示的关系: υ(B)=3υ(A) 3υ(C)=2υ(B)
则此反应可表示为( )
(A)2A+3B=2C (B)A+3B=2C
(C)3A+B=2C (D)A+B=C答案:B3.已知某条件下,合成氨反应的数据如下:
N2(气)+3H2(气) 2NH3(气)
起始浓度mol·L-1 1.0 3.0 0.2
2s末浓度mol·L-1 0.6 1.8 1.0
4s末浓度mol·L-1 0.4 1.2 1.4
当用氨气的浓度增加来表示该反应的速率
时,下列说法中错误的是( )
A.2s末氨气的平均反应速率=0.27mol/(L·s)
B.前2s时间内氨气的平均反应速率=0.4mol/(L·s)
C.前4s时间内氨气的平均反应速率=0.3mol/(L·s)
D.2s~4s时间内氨气的平均反应速率=0.2mol/(L·s)A4.反应4NH3+5O2 = 4NO+6H2O,在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率υ(x)(表示反应物的消耗速率或生成物的生成速率)为( )
(A)υ(O2)=0.01 mol·L-1·s-1
(B)υ(NO)=0.008 mol·L-1·s-1
(C)υ(H2O)=0.003 mol·L-1·s-1
(D)υ(NH3)=0.002 mol·L-1·s-1 答案: CD5.在四个不同的容器中,在不同的条件下进行合成氨反应。根据在相同时间内测定的结果判断,生成氨的速率最快的是( )
(A)υ(H2)=0.1 mol·L-1·min-1
(B)υ(N2)=0.2 mol·L-1·min-1
(C)υ(NH3)=0.15 mol·L-1·min-1
(D)υ(H2)=0.3 mol·L-1·min-1
答案: B比较一个反应的反应速率的快慢,必须找同一参照物答案:A6.在一个容积为2L的密闭容器中,发生如下反应:
3X(g)+Y(g)=2Z(g)
若最初加入的X、Y和Z都是1mol,反应中X的平均反应速率为0.12 mol·L-1·s-1。若要产物Z为1.8mol,反应所需的时间为( )
(A)5s (B)10s (C)15s (D)20s
思考??实验步骤:
1、连接实验装置
2、检查装置的气密性
3、先向锥形瓶中加入锌粒
然后再向分液漏斗中加入稀硫酸
4、使稀硫酸滴入锥形瓶与锌粒反应
5、观察收集10mLH2所用的时间
(实验2一1)实验分析∶用量气法测定该实验的速率时需注意什么问题?
怎样才能使反应速率的测定更加准确?
1)装置的气密性要好
2)倒入稀硫酸时速率要快
3)锌粒大小(表面积)基本相同
4)计时要迅速、准确分析探讨实验中需要注意的问题1.在该实验中难以控制的变量是什么?
锌粒大小(表面积)
2.根据你的掌握知识量气装置还有哪些?测量氢气体积方法有:当体系的温度恢复到室温后,要调节量筒的高度,使量筒内外的液面相平要上下移动量筒,使量筒内的液面与广口瓶中的液面相平要上下移动右边的玻璃管,使左右两管中的液面相平。思考:在室温和大气压强下,用右上图
示的装置进行实验,测得某一反应产生的
气体体积。
请回答下列问题:
(1)若反应刚结束时,观察到的实验现
象如右下图所示,这时不能立即取出导气
管,理由是 。
(2)本实验中测量气体体积时应注意到
的事项有 。参考答案
(1)因为装置内气体的温度没有恢复到室温,气体压强还不等于大气压强。
(2)待装置内气体的温度恢复到室温后,调节量筒使其内外液面持平。本实验还可以如何测定锌和稀硫酸反应的速率
1、测量溶液中的H+的浓度的变化
2、测量溶液中的Zn2+的浓度变化
3、测量1分钟收集到的H2的体积
4、测量反应体系的热量变化
… … … … … 学与问:19.广东2009年高考(12分)
某实验小组利用如下装置(部分固定装置略)
制备氧化钙(Ca3N2),并探究其实验式。
(1)按图连接好实验装置。检查装置的气密性,
方法是 。
(2)反应过程中末端导管必须插入试管A的水中,
目的是 。【答案】
(1)关闭活塞K,将玻璃导管A插入盛有水的试管中,微热反应管,试管A中有气泡冒出,停止加热。冷却后若末端导管中水柱上升且高度保持不变,则说明装置气密性良好。
(2)防止反应过程中空气进入反应管;便于观察N2的流速
