人教版(2019)必修一 1.1.2 物质的转化 学案(含答案)
文档属性
| 名称 | 人教版(2019)必修一 1.1.2 物质的转化 学案(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 376.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-18 00:00:00 | ||
图片预览


文档简介
课题2:物质的转化 班级 姓名______ ___
一、学习目标
1.理解单质、氧化物、酸、碱、盐等物质之间的相互转化关系。
2.初步了解通过化学反应实现物质相互转化的重要意义。
二、重点知识梳理
(一)酸、碱、盐的性质
1.酸的通性(以盐酸为例,写出相关反应的化学方程式)
酸的通性 实例 反应类型 生成物
与碱反应 HCl+NaOH=== 盐和水
与活泼金属单质反应 2HCl+Fe=== 盐和氢气
与碱性氧化物反应 2HCl+CaO=== 盐和水
与某些盐反应 2HCl+CaCO3=== 盐和酸
2.碱的通性(以NaOH为例,写出相关反应的化学方程式)
碱的通性 实例 反应类型 生成物
与酸反应 NaOH+HCl=== 盐和水
与酸性氧化物反应 2NaOH+CO2=== 盐和水
与某些盐反应 2NaOH+MgCl2=== 碱和盐
3.盐的通性(以Na2CO3为例,写出相关反应的化学方程式)
盐的通性 实例 反应类型 生成物
与酸反应 Na2CO3+2HCl=== 盐和酸
与碱反应 Na2CO3+Ba(OH)2=== 盐和碱
与某些盐反应 Na2CO3+CaCl2=== 盐和盐
不同的酸、碱、盐具有相似的化学性质,从微观角度看,酸溶液中都有_ __,碱溶液中都有__ __,碳酸盐溶液中都有__ _等。
(二)物质的转化
1、写出下列物质之间转化的化学方程式,体会由金属单质、非金属单质到盐的转化关系
CaCaOCa(OH)2CaSO4 CCO2H2CO3CaCO3
①______________________、②______________________、③_____________________
④______________________、⑤______________________、⑥_____________________
如何利用CaCO3获得Ca(OH)2?
___________________________________________________________________
例1、根据上面的转化过程,写出非金属单质S到对应盐Na2SO3的转化过程。
例2、以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )
CCO2H2CO3CaCO3CO2
A.化合、置换、分解、复分解 B.置换、复分解、化合、分解
C.置换、化合、分解、复分解 D.置换、化合、复分解、分解
2、在工业生产中要制取某种物质,需要考虑:
____________,_____________,______________,_______________
三、课堂反馈
1.判断正误(正确的打“√”,错误的打“×”)。
(1)在化学变化过程中,元素、原子和分子的种类均不发生变化。( )
(2)HCl、H2SO4、HNO3溶液中都含有H+,因此具有相似的化学性质。( )
(3)酸和金属反应均能产生氢气,均可用于实验室制取氢气。( )
(4)酸与碱、酸与金属、金属与盐之间可以发生置换反应。( )
(5)利用碱性氧化物与水反应、盐与碱反应均可以制取碱。( )
2.盐是一类常见的物质,下列物质通过一定反应可直接形成盐的是( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A.①②③ B.①④⑥ C.②⑤⑥ D.全部
3.给如图中①~⑤选择适当的物质,使有连线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、
铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉。下列说法正确的是( )
A.单质①为铜
B.氧化物④为CO2
C.①与②反应为置换反应
D.③与④反应为复分解反应
4.现有碳、二氧化碳、氧化铁、石灰水、稀硫酸和纯碱溶液等6种物质。
①除稀硫酸外,试分别将其他物质的化学式填入如图相应的5个圆圈内,使每个圆圈内的物质都能与 相邻物质发生反应。
②用化学方程式将它们与相邻物质间发生的反应表示出来:
_____________________________________________________、
_____________________________________________________、
_____________________________________________________、
_____________________________________________________、
_____________________________________________________、
_____________________________________________________。
四、课后限时练习
1.有CuO、Fe、H2、Ba(OH)2溶液、K2CO3溶液、NaOH溶液、稀硫酸七种物质,在常温下物质两两间能发生反应最多有( )
A.4个 B.5个 C.6个 D.7个
2.下列关于化学反应类型的叙述中,正确的是( )
A.凡是生成盐和水的反应都是中和反应 B.复分解反应一定没有单质参加
C.生成一种单质和一种化合物的反应一定是置换反应 D.分解反应的生成物一定有单质
3.火箭常用联氨(N2H4)作燃料,反应的化学方程式为:N2H4+ 2NO2X+2H2O,则X的化学式为( )
A.N2 B.NO2 C.NH3 D.NO
4.A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如图所示,其中所含的相同元素是( )
A.铜 B.碳 C.铁 D.钙
5.在一定条件下,跟酸、碱、盐都能反应的物质是( )
A.CaO B.Na2CO3 C.CaCO3 D.CO2
6.下列关于氧化物的叙述正确的是( )
A.酸性氧化物均可以和碱发生反应 B.酸性氧化物在常温下均为气态
C.金属氧化物都是碱性氧化物 D.不能与酸反应的氧化物一定能与碱反应
7.下列化合物中,属于碱性氧化物且能与水反应的是( )
A.FeO B.CaO C.Al2O3 D.CuO
8.下列变化,只有加入酸才能一步实现的是( )
A.Zn→ZnSO4 B.CaCO3→CO2 C.MgO→MgCl2 D.BaCl2→BaSO4
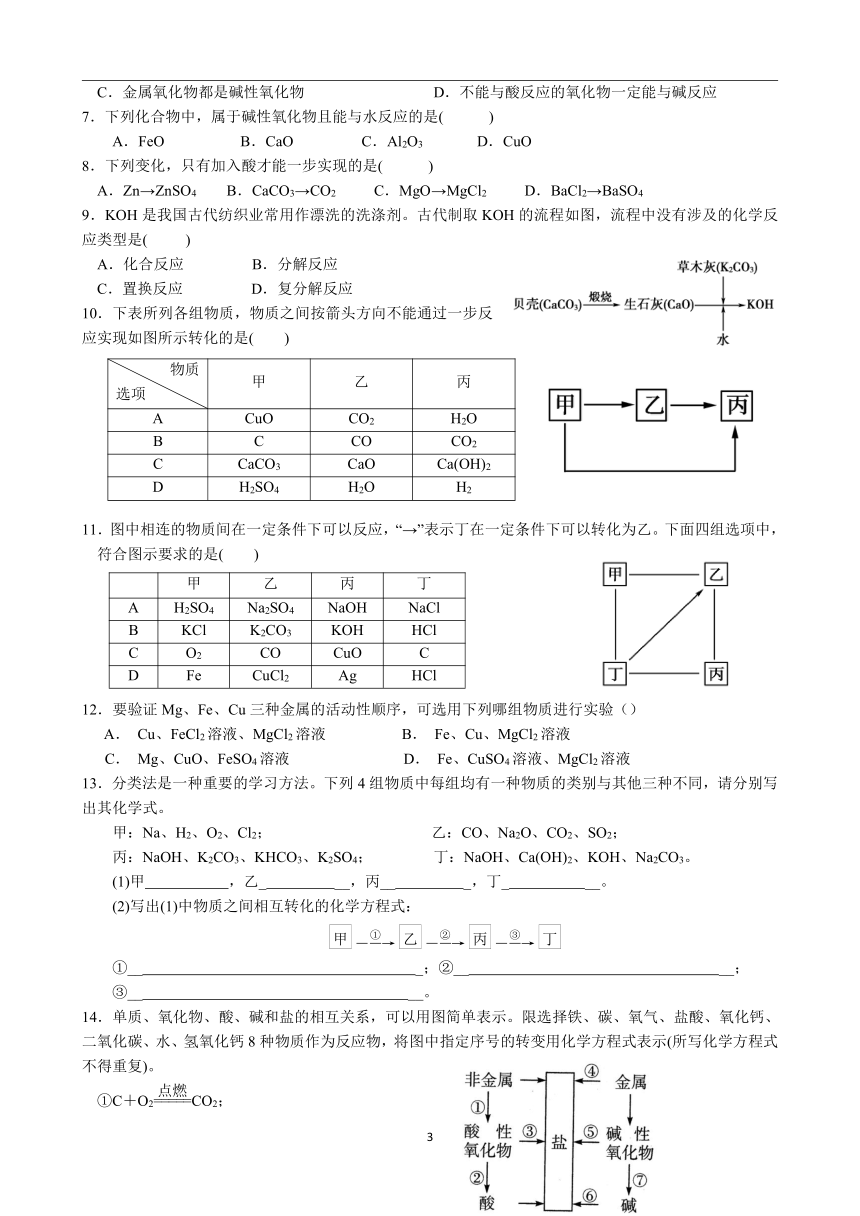
9.KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如图,流程中没有涉及的化学反应类型是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
10.下表所列各组物质,物质之间按箭头方向不能通过一步反应实现如图所示转化的是( )
物质 选项 甲 乙 丙
A CuO CO2 H2O
B C CO CO2
C CaCO3 CaO Ca(OH)2
D H2SO4 H2O H2
11.图中相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙。下面四组选项中,
符合图示要求的是( )
甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B KCl K2CO3 KOH HCl
C O2 CO CuO C
D Fe CuCl2 Ag HCl
12.要验证Mg、Fe、Cu三种金属的活动性顺序,可选用下列哪组物质进行实验()
A. Cu、FeCl2溶液、MgCl2溶液 B. Fe、Cu、MgCl2溶液
C. Mg、CuO、FeSO4溶液 D. Fe、CuSO4溶液、MgCl2溶液
13.分类法是一种重要的学习方法。下列4组物质中每组均有一种物质的类别与其他三种不同,请分别写出其化学式。
甲:Na、H2、O2、Cl2; 乙:CO、Na2O、CO2、SO2;
丙:NaOH、K2CO3、KHCO3、K2SO4; 丁:NaOH、Ca(OH)2、KOH、Na2CO3。
(1)甲 ,乙_ __,丙__ _,丁_ __。
(2)写出(1)中物质之间相互转化的化学方程式:
①__ _;②__ __;
③__ __。
14.单质、氧化物、酸、碱和盐的相互关系,可以用图简单表示。限选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转变用化学方程式表示(所写化学方程式不得重复)。
①C+O2CO2;
②________________________________;
③________________________________;
④________________________________;
⑤________________________________;
⑥________________________________;
⑦________________________________。
★15.已知:H3PO2+NaOH(过量)===NaH2PO2+H2O。据此回答下列问题。
(1)H3PO2中磷元素的化合价是 价。该反应属于四种基本反应类型中的_ (填“化合”“分解”“置换”或“复分解”)反应。
(2)H3PO2属于 (填“一”“二”或“三”)元酸。NaH2PO2属于 (填“正盐”或“酸式盐”)。
★16. “探险队员”——盐酸不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫(用图中物质前的序号和“→”连接起来表示所走的路线):
__ _。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有_ _个,其中能“吃掉”盐酸的盐是__ _ _(填化学式,下同),能“吃掉”盐酸的氧化物有_ 和__ __。
(3)在不能与盐酸反应的物质中,属于氧化物的是_ _(填物质序号,下同),属于单质的是_ _。
(4)如果将盐酸换成氧气,它能沿着盐酸走出的路线走出这个迷宫吗?为什么?_
_ 。
预习:课题3 电解质的电离
电解质和非电解质
常见电解质如:
常见非电解质如:
常见强电解质如:
常见弱电解质如:
电离
电离方程式的书写:
H2SO4:
Ba(OH)2:
CaCl2:
课题2:物质的转化答案
1.酸的通性(以盐酸为例,写出相关反应的化学方程式)
酸的通性 实例 生成物
与碱反应 HCl+NaOH===NaCl+H2O 盐和水
与活泼金属 单质反应 2HCl+Fe===FeCl2+H2↑ 盐和 氢气
与碱性氧 化物反应 2HCl+CaO===CaCl2+H2O 盐和水
与某些 盐反应 2HCl+CaCO3===CaCl2+CO2↑+H2O 盐和酸
2.碱的通性(以NaOH为例,写出相关反应的化学方程式)
碱的通性 实例 生成物
与酸反应 NaOH+HCl===NaCl+H2O 盐和水
与酸性氧 化物反应 2NaOH+CO2===Na2CO3+H2O 盐和水
与某些 盐反应 2NaOH+MgCl2===Mg(OH)2↓+2NaCl 碱和盐
3.盐的通性(以Na2CO3为例,写出相关反应的化学方程式)
盐的通性 实例 生成物
与酸反应 Na2CO3+2HCl===2NaCl+CO2↑+H2O 盐和酸
与碱反应 Na2CO3+Ba(OH)2===BaCO3↓+2NaOH 盐和碱
与某些 盐反应 Na2CO3+CaCl2===2NaCl+CaCO3↓ 盐和盐
不同的酸、碱、盐具有相似的化学性质,从微观角度看,酸溶液中都有__H+__,碱溶液中都有__OH-__,碳酸盐溶液中都有__CO__等。
(二)物质的转化
1 ①__2Ca+O2===2CaO__;②__CaO+H2O===Ca(OH)2__;
③ Ca(OH)2+H2SO4===CaSO4↓+2H2O [或 Ca(OH)2+SO3===CaSO4↓+H2O] ;
④__C+O2CO2__;⑤__CO2+H2O===H2CO3__;
⑥__Ca(OH)2+H2CO3===CaCO3↓+2H2O(或CaO+H2CO3===CaCO3↓+H2O)__。
【检测反馈答案】
1. × √ × × √ 2.D 3.C
4.①
②H2SO4+Na2CO3===Na2SO4+CO2↑+H2O
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
Ca(OH)2+CO2===CaCO3↓+H2O
CO2+C2CO
2Fe2O3+3C4Fe+3CO2↑
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O(其他答案合理也可)
【课后限时练习答案】
1-5C B A D B 6-10 A B C C C 11-12 C D
13.(1) 甲__Na__,乙__Na2O__,丙__NaOH__,丁_ Na2 CO3__。
(2)①__4Na+O2===2Na2O__; ②__Na2O+H2O===2NaOH__;③_2_NaOH+CO2===Na2 CO3+H2O__。
14.②CO2+H2O===H2CO3 ③CO2+Ca(OH)2===CaCO3↓+H2O
④Fe+2HCl===FeCl2+H2↑ ⑤CaO+2HCl===CaCl2+H2O
⑥Ca(OH)2+2HCl===CaCl2+2H2O ⑦CaO+H2O===Ca(OH)2
15. (1)+1价 复分解 (2) 一元酸 正盐。
16. (1) __③→⑥→⑩→⑦→ → __。
(2) __2__个, __Na2CO3__ __Fe2O3__和__MgO__。
(3) __③⑩_, __⑦ __。
(4) __不能,因为氧气遇到CO、Cu、Ag会被“吃掉”__。
(
6
)
一、学习目标
1.理解单质、氧化物、酸、碱、盐等物质之间的相互转化关系。
2.初步了解通过化学反应实现物质相互转化的重要意义。
二、重点知识梳理
(一)酸、碱、盐的性质
1.酸的通性(以盐酸为例,写出相关反应的化学方程式)
酸的通性 实例 反应类型 生成物
与碱反应 HCl+NaOH=== 盐和水
与活泼金属单质反应 2HCl+Fe=== 盐和氢气
与碱性氧化物反应 2HCl+CaO=== 盐和水
与某些盐反应 2HCl+CaCO3=== 盐和酸
2.碱的通性(以NaOH为例,写出相关反应的化学方程式)
碱的通性 实例 反应类型 生成物
与酸反应 NaOH+HCl=== 盐和水
与酸性氧化物反应 2NaOH+CO2=== 盐和水
与某些盐反应 2NaOH+MgCl2=== 碱和盐
3.盐的通性(以Na2CO3为例,写出相关反应的化学方程式)
盐的通性 实例 反应类型 生成物
与酸反应 Na2CO3+2HCl=== 盐和酸
与碱反应 Na2CO3+Ba(OH)2=== 盐和碱
与某些盐反应 Na2CO3+CaCl2=== 盐和盐
不同的酸、碱、盐具有相似的化学性质,从微观角度看,酸溶液中都有_ __,碱溶液中都有__ __,碳酸盐溶液中都有__ _等。
(二)物质的转化
1、写出下列物质之间转化的化学方程式,体会由金属单质、非金属单质到盐的转化关系
CaCaOCa(OH)2CaSO4 CCO2H2CO3CaCO3
①______________________、②______________________、③_____________________
④______________________、⑤______________________、⑥_____________________
如何利用CaCO3获得Ca(OH)2?
___________________________________________________________________
例1、根据上面的转化过程,写出非金属单质S到对应盐Na2SO3的转化过程。
例2、以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )
CCO2H2CO3CaCO3CO2
A.化合、置换、分解、复分解 B.置换、复分解、化合、分解
C.置换、化合、分解、复分解 D.置换、化合、复分解、分解
2、在工业生产中要制取某种物质,需要考虑:
____________,_____________,______________,_______________
三、课堂反馈
1.判断正误(正确的打“√”,错误的打“×”)。
(1)在化学变化过程中,元素、原子和分子的种类均不发生变化。( )
(2)HCl、H2SO4、HNO3溶液中都含有H+,因此具有相似的化学性质。( )
(3)酸和金属反应均能产生氢气,均可用于实验室制取氢气。( )
(4)酸与碱、酸与金属、金属与盐之间可以发生置换反应。( )
(5)利用碱性氧化物与水反应、盐与碱反应均可以制取碱。( )
2.盐是一类常见的物质,下列物质通过一定反应可直接形成盐的是( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A.①②③ B.①④⑥ C.②⑤⑥ D.全部
3.给如图中①~⑤选择适当的物质,使有连线的两物质能发生反应。供选择的试剂有稀硫酸、二氧化碳、
铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉。下列说法正确的是( )
A.单质①为铜
B.氧化物④为CO2
C.①与②反应为置换反应
D.③与④反应为复分解反应
4.现有碳、二氧化碳、氧化铁、石灰水、稀硫酸和纯碱溶液等6种物质。
①除稀硫酸外,试分别将其他物质的化学式填入如图相应的5个圆圈内,使每个圆圈内的物质都能与 相邻物质发生反应。
②用化学方程式将它们与相邻物质间发生的反应表示出来:
_____________________________________________________、
_____________________________________________________、
_____________________________________________________、
_____________________________________________________、
_____________________________________________________、
_____________________________________________________。
四、课后限时练习
1.有CuO、Fe、H2、Ba(OH)2溶液、K2CO3溶液、NaOH溶液、稀硫酸七种物质,在常温下物质两两间能发生反应最多有( )
A.4个 B.5个 C.6个 D.7个
2.下列关于化学反应类型的叙述中,正确的是( )
A.凡是生成盐和水的反应都是中和反应 B.复分解反应一定没有单质参加
C.生成一种单质和一种化合物的反应一定是置换反应 D.分解反应的生成物一定有单质
3.火箭常用联氨(N2H4)作燃料,反应的化学方程式为:N2H4+ 2NO2X+2H2O,则X的化学式为( )
A.N2 B.NO2 C.NH3 D.NO
4.A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如图所示,其中所含的相同元素是( )
A.铜 B.碳 C.铁 D.钙
5.在一定条件下,跟酸、碱、盐都能反应的物质是( )
A.CaO B.Na2CO3 C.CaCO3 D.CO2
6.下列关于氧化物的叙述正确的是( )
A.酸性氧化物均可以和碱发生反应 B.酸性氧化物在常温下均为气态
C.金属氧化物都是碱性氧化物 D.不能与酸反应的氧化物一定能与碱反应
7.下列化合物中,属于碱性氧化物且能与水反应的是( )
A.FeO B.CaO C.Al2O3 D.CuO
8.下列变化,只有加入酸才能一步实现的是( )
A.Zn→ZnSO4 B.CaCO3→CO2 C.MgO→MgCl2 D.BaCl2→BaSO4
9.KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如图,流程中没有涉及的化学反应类型是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
10.下表所列各组物质,物质之间按箭头方向不能通过一步反应实现如图所示转化的是( )
物质 选项 甲 乙 丙
A CuO CO2 H2O
B C CO CO2
C CaCO3 CaO Ca(OH)2
D H2SO4 H2O H2
11.图中相连的物质间在一定条件下可以反应,“→”表示丁在一定条件下可以转化为乙。下面四组选项中,
符合图示要求的是( )
甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B KCl K2CO3 KOH HCl
C O2 CO CuO C
D Fe CuCl2 Ag HCl
12.要验证Mg、Fe、Cu三种金属的活动性顺序,可选用下列哪组物质进行实验()
A. Cu、FeCl2溶液、MgCl2溶液 B. Fe、Cu、MgCl2溶液
C. Mg、CuO、FeSO4溶液 D. Fe、CuSO4溶液、MgCl2溶液
13.分类法是一种重要的学习方法。下列4组物质中每组均有一种物质的类别与其他三种不同,请分别写出其化学式。
甲:Na、H2、O2、Cl2; 乙:CO、Na2O、CO2、SO2;
丙:NaOH、K2CO3、KHCO3、K2SO4; 丁:NaOH、Ca(OH)2、KOH、Na2CO3。
(1)甲 ,乙_ __,丙__ _,丁_ __。
(2)写出(1)中物质之间相互转化的化学方程式:
①__ _;②__ __;
③__ __。
14.单质、氧化物、酸、碱和盐的相互关系,可以用图简单表示。限选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转变用化学方程式表示(所写化学方程式不得重复)。
①C+O2CO2;
②________________________________;
③________________________________;
④________________________________;
⑤________________________________;
⑥________________________________;
⑦________________________________。
★15.已知:H3PO2+NaOH(过量)===NaH2PO2+H2O。据此回答下列问题。
(1)H3PO2中磷元素的化合价是 价。该反应属于四种基本反应类型中的_ (填“化合”“分解”“置换”或“复分解”)反应。
(2)H3PO2属于 (填“一”“二”或“三”)元酸。NaH2PO2属于 (填“正盐”或“酸式盐”)。
★16. “探险队员”——盐酸不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助它走出迷宫(用图中物质前的序号和“→”连接起来表示所走的路线):
__ _。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有_ _个,其中能“吃掉”盐酸的盐是__ _ _(填化学式,下同),能“吃掉”盐酸的氧化物有_ 和__ __。
(3)在不能与盐酸反应的物质中,属于氧化物的是_ _(填物质序号,下同),属于单质的是_ _。
(4)如果将盐酸换成氧气,它能沿着盐酸走出的路线走出这个迷宫吗?为什么?_
_ 。
预习:课题3 电解质的电离
电解质和非电解质
常见电解质如:
常见非电解质如:
常见强电解质如:
常见弱电解质如:
电离
电离方程式的书写:
H2SO4:
Ba(OH)2:
CaCl2:
课题2:物质的转化答案
1.酸的通性(以盐酸为例,写出相关反应的化学方程式)
酸的通性 实例 生成物
与碱反应 HCl+NaOH===NaCl+H2O 盐和水
与活泼金属 单质反应 2HCl+Fe===FeCl2+H2↑ 盐和 氢气
与碱性氧 化物反应 2HCl+CaO===CaCl2+H2O 盐和水
与某些 盐反应 2HCl+CaCO3===CaCl2+CO2↑+H2O 盐和酸
2.碱的通性(以NaOH为例,写出相关反应的化学方程式)
碱的通性 实例 生成物
与酸反应 NaOH+HCl===NaCl+H2O 盐和水
与酸性氧 化物反应 2NaOH+CO2===Na2CO3+H2O 盐和水
与某些 盐反应 2NaOH+MgCl2===Mg(OH)2↓+2NaCl 碱和盐
3.盐的通性(以Na2CO3为例,写出相关反应的化学方程式)
盐的通性 实例 生成物
与酸反应 Na2CO3+2HCl===2NaCl+CO2↑+H2O 盐和酸
与碱反应 Na2CO3+Ba(OH)2===BaCO3↓+2NaOH 盐和碱
与某些 盐反应 Na2CO3+CaCl2===2NaCl+CaCO3↓ 盐和盐
不同的酸、碱、盐具有相似的化学性质,从微观角度看,酸溶液中都有__H+__,碱溶液中都有__OH-__,碳酸盐溶液中都有__CO__等。
(二)物质的转化
1 ①__2Ca+O2===2CaO__;②__CaO+H2O===Ca(OH)2__;
③ Ca(OH)2+H2SO4===CaSO4↓+2H2O [或 Ca(OH)2+SO3===CaSO4↓+H2O] ;
④__C+O2CO2__;⑤__CO2+H2O===H2CO3__;
⑥__Ca(OH)2+H2CO3===CaCO3↓+2H2O(或CaO+H2CO3===CaCO3↓+H2O)__。
【检测反馈答案】
1. × √ × × √ 2.D 3.C
4.①
②H2SO4+Na2CO3===Na2SO4+CO2↑+H2O
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
Ca(OH)2+CO2===CaCO3↓+H2O
CO2+C2CO
2Fe2O3+3C4Fe+3CO2↑
Fe2O3+3H2SO4===Fe2(SO4)3+3H2O(其他答案合理也可)
【课后限时练习答案】
1-5C B A D B 6-10 A B C C C 11-12 C D
13.(1) 甲__Na__,乙__Na2O__,丙__NaOH__,丁_ Na2 CO3__。
(2)①__4Na+O2===2Na2O__; ②__Na2O+H2O===2NaOH__;③_2_NaOH+CO2===Na2 CO3+H2O__。
14.②CO2+H2O===H2CO3 ③CO2+Ca(OH)2===CaCO3↓+H2O
④Fe+2HCl===FeCl2+H2↑ ⑤CaO+2HCl===CaCl2+H2O
⑥Ca(OH)2+2HCl===CaCl2+2H2O ⑦CaO+H2O===Ca(OH)2
15. (1)+1价 复分解 (2) 一元酸 正盐。
16. (1) __③→⑥→⑩→⑦→ → __。
(2) __2__个, __Na2CO3__ __Fe2O3__和__MgO__。
(3) __③⑩_, __⑦ __。
(4) __不能,因为氧气遇到CO、Cu、Ag会被“吃掉”__。
(
6
)
