人教版高中化学必修2 2.1《化学能与热能》 (共22张PPT)
文档属性
| 名称 | 人教版高中化学必修2 2.1《化学能与热能》 (共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 541.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-09 00:00:00 | ||
图片预览






文档简介
课件22张PPT。高中化学系列教学资源之课件学科:化学;
教材:新人教版必修2
整理:德安一中化学备课组
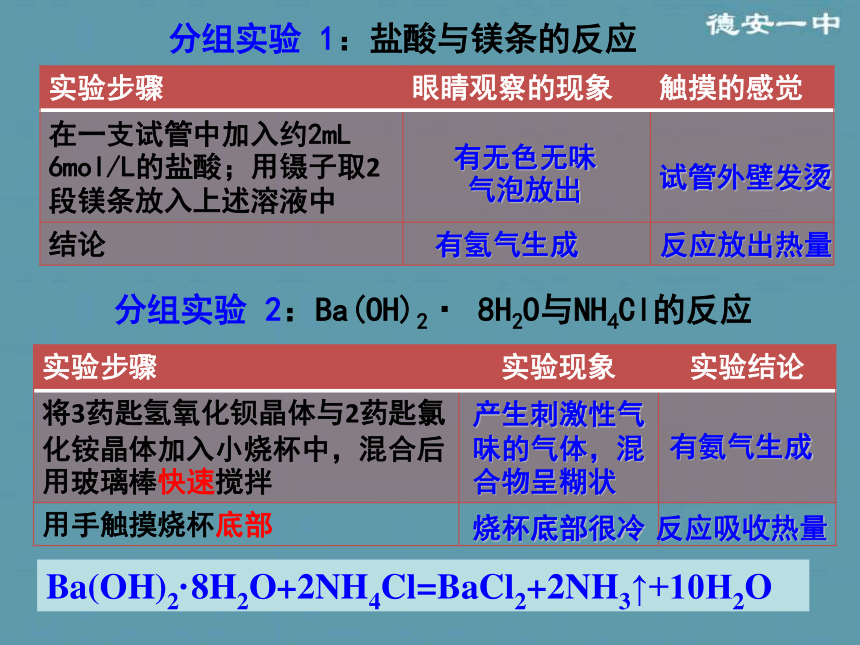
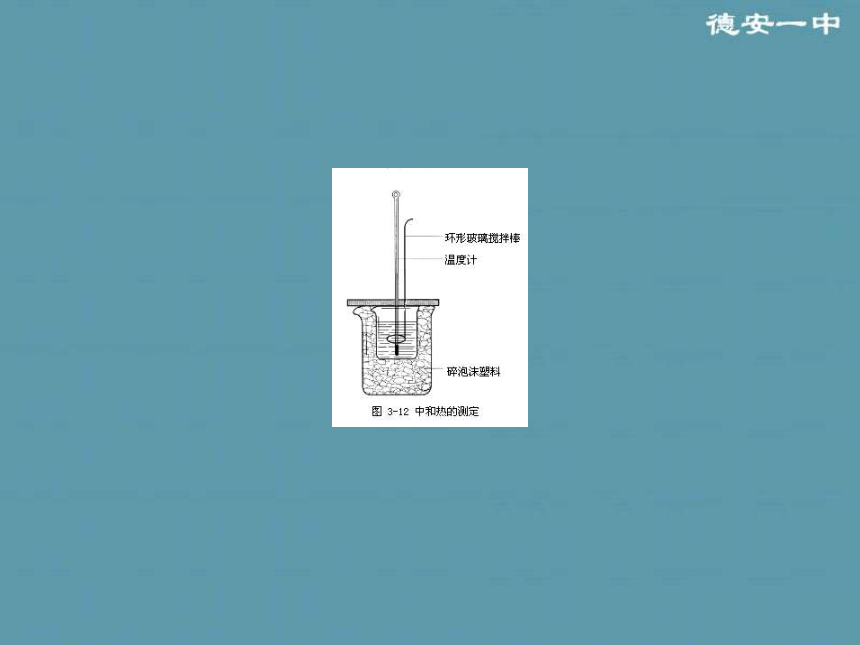
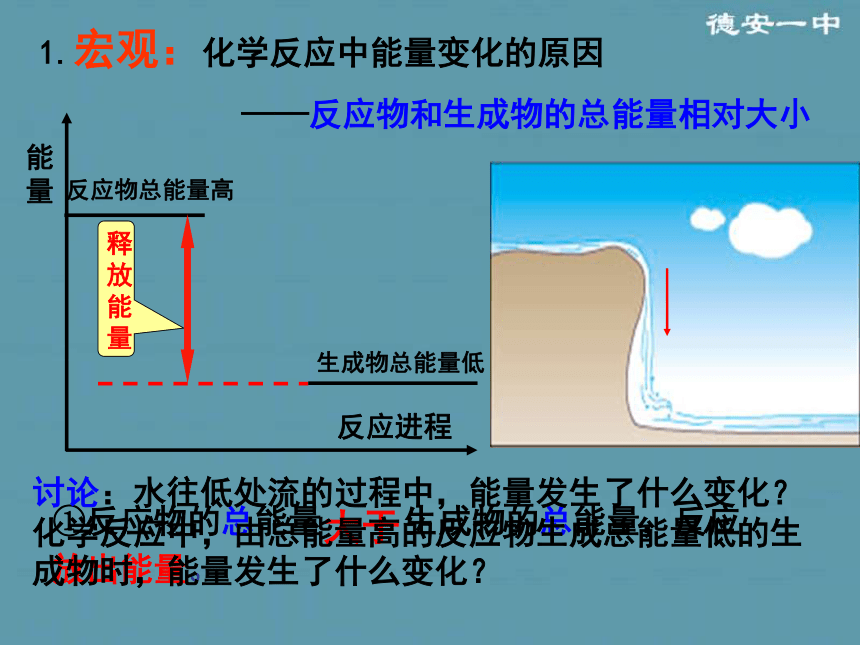
QQ:22095876江西省德安县第一中学科研处第二章 化学反应与能量第一节 化学能与热能在生活中你都见过哪些形式的能量转换?思考?哪些属于化学能与其他形式能量的转换?(比一比看谁说的方法多)用什么方法可以把一壶冷水变为开水?讨论:哪些方法是通过化学反应实现的?通过以上讨论你对化学反应有何新的认识?分组实验 1:盐酸与镁条的反应 分组实验 2:Ba(OH)2· 8H2O与NH4Cl的反应 Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O有无色无味气泡放出 试管外壁发烫产生刺激性气味的气体,混合物呈糊状烧杯底部很冷反应吸收热量反应放出热量有氢气生成有氨气生成思考与交流测量中和反应热应该注意哪些问题?1、保温隔热的效果一定要好。2、温度计要读准,水银球要全浸在溶液中,且要稳定一段时间再读。3、实验操作时动作要快,以尽量减少热量的散失。4、多次测量取平均值 同样是化学反应,为什么有的放热,有的吸热?思考?①反应物的总能量 生成物的总能量,反应放出能量。1.宏观:化学反应中能量变化的原因
——反应物和生成物的总能量相对大小大于讨论:水往低处流的过程中,能量发生了什么变化?化学反应中,由总能量高的反应物生成总能量低的生成物时,能量发生了什么变化?能量反应进程②反应物总能量 生成物总能量,反应吸收能量。小于小结:宏观:化学反应中能量的变化------总能量守恒(能量守恒定律)1.E(反应物)> E(生成物)反应放热
2.E(生成物) > E(反应物)反应吸热
断裂和形成化学键与吸收和释放能量有什么关系呢?断裂反应物中的化学键吸收能量, 形成生成物中的化学键释放能量思
考2、微观:化学反应中能量变化的主要原因
——化学键的断裂和形成大于①断开化学键吸收的总能量 形成化学键释放出的总能量,反应放出能量。②断开化学键吸收的总能量 形成化学键释放出的总能量,反应吸收能量。小于思考:从能量的角度考虑,你对化学反应有新的认识吗? 1、化学反应的过程,可以看成是能量的
“贮存”或“释放”的过程。2.化学反应实质:化学反应的特点是有新物质生成。
“新”是指物质组成、物质结构、物质所具有的能量与原反应物不同。
3.化学反应中能量守恒。
(1)宏观:化学反应中,化学反应中能量变化主要取决于反应物的总能量和生成物的总能量的相对大小。
(2)微观:化学键的断裂和形成是化学反应中能量变化的主要原因。小结断键吸收总能量 <成键放出总能量断键吸收总能量 > 成键放出总能量反应物的总能量 >生成物的总能量反应物的总能量 <生成物的总能量2、化学反应中能量变化遵循能量守恒定律1、化学反应中能量变化原因常见的放热反应和吸热反应放热反应物质与氧气的反应
燃料的燃烧
中和反应
金属与酸
活泼金属与水的反应
生石灰和水反应
大部分化合反应 吸热反应C+CO2
C+H2O
H2+CuO
Ba(OH)2·8H2O+NH4Cl
Fe+H2O(g)
Na2CO3·10H2O+NH4NO3
大部分分解反应1、已知反应A+B=C+D为放热反应,对该反应的下列说法中正确的是( )
A、A的能量一定高于C
B、B的能量一定高于D
C、A和B的总能量一定高于C和D的总能量
D、该反应为放热反应,故不必加热就一定能发生典型例题:c2、氢气在氧气中燃烧产生蓝色火焰,
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是 ( )
A、2Q1 + Q2 > 4Q3
B、2Q1 + Q2 < 4Q3
C、Q1 + Q2 < Q3
D、Q1 + Q2 = Q3B3、下列物质加入水中显著放热的是( )
A、固体氢氧化钠 B、生石灰
C、无水乙醇 D、固体硝酸铵A、B4、某个确定的化学反应在发生过程中需要吸收能量,提供的能量主要起的作用是( )
A、形成生成物的化学键
B、形成反应物中的化学键
C、破坏反应物中的化学键
D、破坏生成物中的化学键C课外练习:
1、判断下列的说法是否正确 :
(1)加热的反应一定是吸热反应
(2)吸热反应一定是需要加热反应
(3)一个反应是吸热或放热与反应条件没有直接联系,与反应物与生成物的总能量的相对大小有关;
(4)化学反应中的能量变化都表现为热能变化。
(5)物质发生化学反应都伴随着能量变化
(6)伴有能量变化的物质变化都是化学反应2、如右图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.
(1)实验中观察到的现象是 ;
(2)产生上述现象的原因是 ;
(3)写出有关反应的离子方程式;
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”、“小于”、“等于”)镁片和盐酸的总能量.
教材:新人教版必修2
整理:德安一中化学备课组
QQ:22095876江西省德安县第一中学科研处第二章 化学反应与能量第一节 化学能与热能在生活中你都见过哪些形式的能量转换?思考?哪些属于化学能与其他形式能量的转换?(比一比看谁说的方法多)用什么方法可以把一壶冷水变为开水?讨论:哪些方法是通过化学反应实现的?通过以上讨论你对化学反应有何新的认识?分组实验 1:盐酸与镁条的反应 分组实验 2:Ba(OH)2· 8H2O与NH4Cl的反应 Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O有无色无味气泡放出 试管外壁发烫产生刺激性气味的气体,混合物呈糊状烧杯底部很冷反应吸收热量反应放出热量有氢气生成有氨气生成思考与交流测量中和反应热应该注意哪些问题?1、保温隔热的效果一定要好。2、温度计要读准,水银球要全浸在溶液中,且要稳定一段时间再读。3、实验操作时动作要快,以尽量减少热量的散失。4、多次测量取平均值 同样是化学反应,为什么有的放热,有的吸热?思考?①反应物的总能量 生成物的总能量,反应放出能量。1.宏观:化学反应中能量变化的原因
——反应物和生成物的总能量相对大小大于讨论:水往低处流的过程中,能量发生了什么变化?化学反应中,由总能量高的反应物生成总能量低的生成物时,能量发生了什么变化?能量反应进程②反应物总能量 生成物总能量,反应吸收能量。小于小结:宏观:化学反应中能量的变化------总能量守恒(能量守恒定律)1.E(反应物)> E(生成物)反应放热
2.E(生成物) > E(反应物)反应吸热
断裂和形成化学键与吸收和释放能量有什么关系呢?断裂反应物中的化学键吸收能量, 形成生成物中的化学键释放能量思
考2、微观:化学反应中能量变化的主要原因
——化学键的断裂和形成大于①断开化学键吸收的总能量 形成化学键释放出的总能量,反应放出能量。②断开化学键吸收的总能量 形成化学键释放出的总能量,反应吸收能量。小于思考:从能量的角度考虑,你对化学反应有新的认识吗? 1、化学反应的过程,可以看成是能量的
“贮存”或“释放”的过程。2.化学反应实质:化学反应的特点是有新物质生成。
“新”是指物质组成、物质结构、物质所具有的能量与原反应物不同。
3.化学反应中能量守恒。
(1)宏观:化学反应中,化学反应中能量变化主要取决于反应物的总能量和生成物的总能量的相对大小。
(2)微观:化学键的断裂和形成是化学反应中能量变化的主要原因。小结断键吸收总能量 <成键放出总能量断键吸收总能量 > 成键放出总能量反应物的总能量 >生成物的总能量反应物的总能量 <生成物的总能量2、化学反应中能量变化遵循能量守恒定律1、化学反应中能量变化原因常见的放热反应和吸热反应放热反应物质与氧气的反应
燃料的燃烧
中和反应
金属与酸
活泼金属与水的反应
生石灰和水反应
大部分化合反应 吸热反应C+CO2
C+H2O
H2+CuO
Ba(OH)2·8H2O+NH4Cl
Fe+H2O(g)
Na2CO3·10H2O+NH4NO3
大部分分解反应1、已知反应A+B=C+D为放热反应,对该反应的下列说法中正确的是( )
A、A的能量一定高于C
B、B的能量一定高于D
C、A和B的总能量一定高于C和D的总能量
D、该反应为放热反应,故不必加热就一定能发生典型例题:c2、氢气在氧气中燃烧产生蓝色火焰,
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是 ( )
A、2Q1 + Q2 > 4Q3
B、2Q1 + Q2 < 4Q3
C、Q1 + Q2 < Q3
D、Q1 + Q2 = Q3B3、下列物质加入水中显著放热的是( )
A、固体氢氧化钠 B、生石灰
C、无水乙醇 D、固体硝酸铵A、B4、某个确定的化学反应在发生过程中需要吸收能量,提供的能量主要起的作用是( )
A、形成生成物的化学键
B、形成反应物中的化学键
C、破坏反应物中的化学键
D、破坏生成物中的化学键C课外练习:
1、判断下列的说法是否正确 :
(1)加热的反应一定是吸热反应
(2)吸热反应一定是需要加热反应
(3)一个反应是吸热或放热与反应条件没有直接联系,与反应物与生成物的总能量的相对大小有关;
(4)化学反应中的能量变化都表现为热能变化。
(5)物质发生化学反应都伴随着能量变化
(6)伴有能量变化的物质变化都是化学反应2、如右图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.
(1)实验中观察到的现象是 ;
(2)产生上述现象的原因是 ;
(3)写出有关反应的离子方程式;
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”、“小于”、“等于”)镁片和盐酸的总能量.
