2025年广东省大湾区初中学业水平质量监测卷化学试卷一(含答案)
文档属性
| 名称 | 2025年广东省大湾区初中学业水平质量监测卷化学试卷一(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 7.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-18 22:13:33 | ||
图片预览



文档简介
2025年广东省大湾区初中学业水平质量监测卷化学试卷一
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.广东文化底蕴深厚,越看“粤”精彩。下列物品主要由金属材料制成的是
A.西周铜盉(信宜) B.潮汕嵌瓷(潮州)
C.木制龙舟(顺德) D.粤剧戏服(广州)
2.广东省有着浓厚的岭南文化气息,具有众多非物质文化遗产。下列说法正确的是
A.绘画的墨汁属天然有机色素 B.工夫茶的茶水,属于纯净物
C.剪纸的运剪过程属物理变化 D.木雕的雕刻过程属化学变化
3.强调实验安全非常重要,下列图标与做“粗盐中难溶性杂质的去除”实验无关的是
A.明火 B.护目镜 C.洗手 D.锐器
4.铌元素广泛用于航空航天、超导材料等领域,它在元素周期表中的信息如图所示,下列说法错误的是
A.铌的原子序数为41 B.一个铌原子的质量为92.91g
C.铌的单质有导电性 D.铌的元素符号为Nb
5.参加下乡学农研学活动,可以掌握多种生活技能。做饭时的做法与对应的原理不符合的是
选项 做法 原理
A 用木柴生火 木柴是可燃物
B 用废纸引燃木柴 使温度达到木柴的着火点
C 将木柴架空摆放 有利于空气流通
D 对灶膛扇风 降温,防止煮焦米饭
A.A B.B C.C D.D
6.分类是一种科学方法,可使学习更高效。下列物质的分类合理的是
A.酸:HCl、CH4 B.氧化物:Na2O、H2O
C.碱:Cu2(OH)2CO3、Fe(OH)3 D.盐:Al2O3、AlCl3
7.我国现代科学家为化学学科发展作出了不懈的努力,下列叙述错误的是
A.张青莲院士为元素名称的中文命名作出了卓越贡献
B.闵恩泽院士为我国炼油催化剂制造技术奠定了基础
C.屠呦呦研究员为世界治疗疟疾作出了巨大贡献
D.徐光宪院士为我国稀土工业发展作出了卓越贡献
8.化学用语是学习化学的重要工具,下列含氮物质中氮元素的化合价显+3价的是
A.NH3 B.N2 C.HNO2 D.NO2
9.氢化钛(TiH2)作为储氢材料备受关注。其可用钛粉(Ti)和H2在一种纳米催化剂的作用下,控制一定的温度和压强反应得到,反应的微观示意图如图所示。下列说法正确的是
A.该反应共生成两种物质
B.反应的化学方程式为
C.参加反应的物质的质量比为2:3
D.反应前后纳米催化剂的化学性质不变
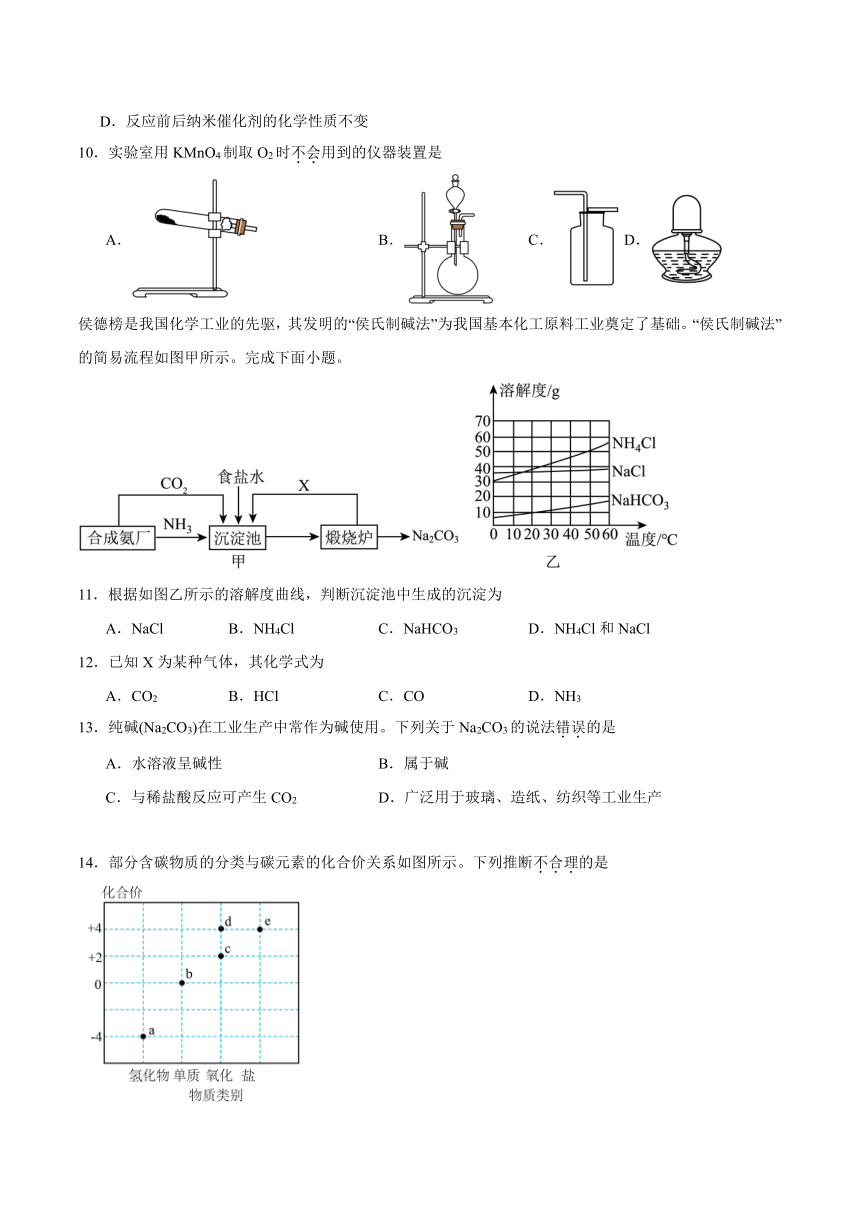
10.实验室用KMnO4制取O2时不会用到的仪器装置是
A. B. C. D.
侯德榜是我国化学工业的先驱,其发明的“侯氏制碱法”为我国基本化工原料工业奠定了基础。“侯氏制碱法”的简易流程如图甲所示。完成下面小题。
11.根据如图乙所示的溶解度曲线,判断沉淀池中生成的沉淀为
A.NaCl B.NH4Cl C.NaHCO3 D.NH4Cl和NaCl
12.已知X为某种气体,其化学式为
A.CO2 B.HCl C.CO D.NH3
13.纯碱(Na2CO3)在工业生产中常作为碱使用。下列关于Na2CO3的说法错误的是
A.水溶液呈碱性 B.属于碱
C.与稀盐酸反应可产生CO2 D.广泛用于玻璃、造纸、纺织等工业生产
14.部分含碳物质的分类与碳元素的化合价关系如图所示。下列推断不合理的是
A.a是可燃冰的主要成分
B.b可能是天然存在的最硬的物质
C.实验室中可用e制备d
D.c和d不可以相互转化
15.下列鉴别或除杂操作正确的是
选项 实验目的 操作
A 除去CO2中混有的HCl 通过足量NaOH溶液
B 除去CuO中的Cu 加入过量稀盐酸,过滤
C 鉴别BaCl2溶液与CaCl2溶液 加入适量Na2CO3溶液
D 鉴别NaOH固体与NH4NO3固体 分别加水溶解,用温度计测量温度变化
A.A B.B C.C D.D
二、填空与简答
16.《天工开物》蕴含着丰富的化学知识与方法。其中关于银的冶炼过程如图所示。
(1)铅、银属于 (填“金属”或“非金属”)单质。
(2)“淘洗”时可用水除去矿砂中的一些杂质,其原理是利用了 。
(3)补充完整“熔矿”时氧气与Ag2S反应的化学方程式: 。
(4)“熔矿”“结银”操作如图乙所示,所需热量由木炭燃烧提供,木炭充分燃烧反应的化学方程式为 。
(5)为使图乙中木炭燃烧更充分,可采取的措施是 (写一条)。
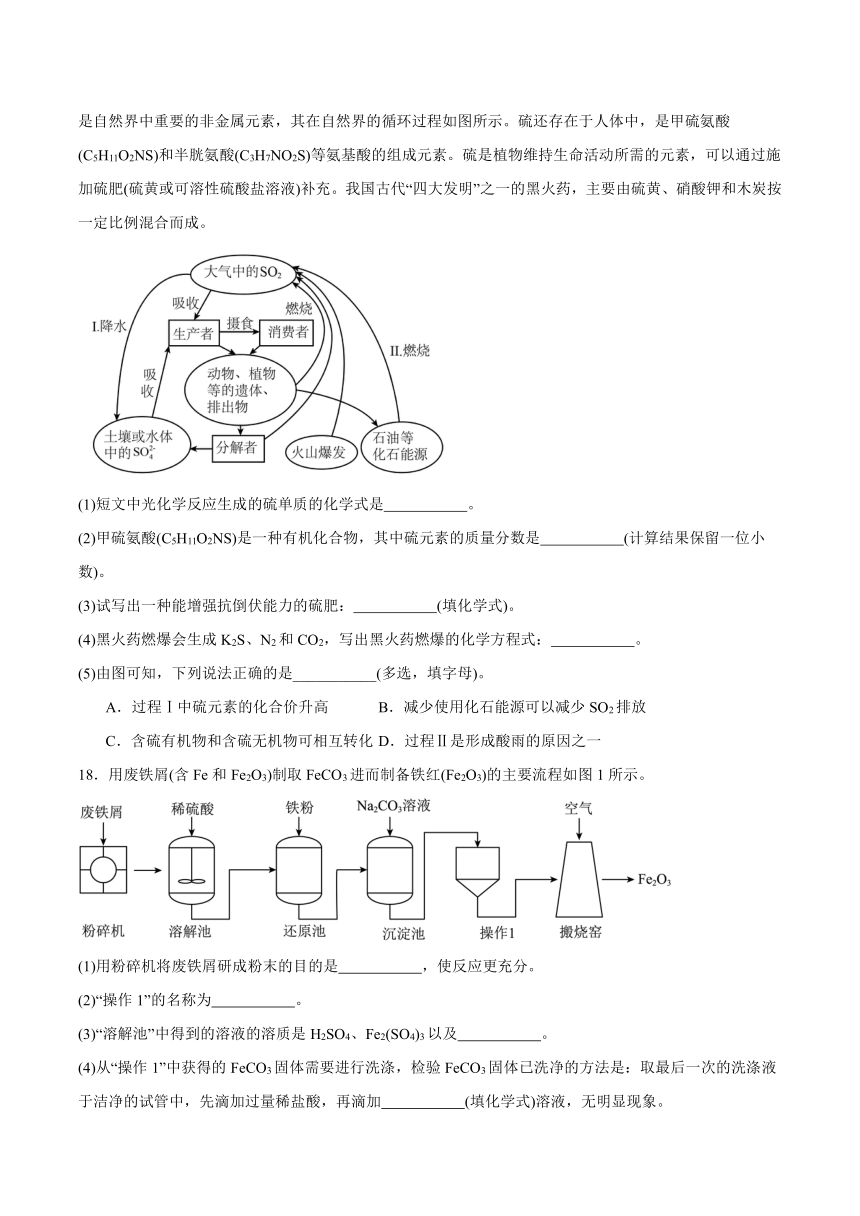
17.硫元素以硫化物、硫酸盐、有机硫和单质硫等形式广泛存在于自然界。硫在某些系外行星的大气层中以H2S和SO2的形式存在,这些物质经过光化学反应,产生了S8和H2SO4;硫在地壳中的含量为0.048%,是自然界中重要的非金属元素,其在自然界的循环过程如图所示。硫还存在于人体中,是甲硫氨酸(C5H11O2NS)和半胱氨酸(C3H7NO2S)等氨基酸的组成元素。硫是植物维持生命活动所需的元素,可以通过施加硫肥(硫黄或可溶性硫酸盐溶液)补充。我国古代“四大发明”之一的黑火药,主要由硫黄、硝酸钾和木炭按一定比例混合而成。
(1)短文中光化学反应生成的硫单质的化学式是 。
(2)甲硫氨酸(C5H11O2NS)是一种有机化合物,其中硫元素的质量分数是 (计算结果保留一位小数)。
(3)试写出一种能增强抗倒伏能力的硫肥: (填化学式)。
(4)黑火药燃爆会生成K2S、N2和CO2,写出黑火药燃爆的化学方程式: 。
(5)由图可知,下列说法正确的是___________(多选,填字母)。
A.过程Ⅰ中硫元素的化合价升高 B.减少使用化石能源可以减少SO2排放
C.含硫有机物和含硫无机物可相互转化 D.过程Ⅱ是形成酸雨的原因之一
18.用废铁屑(含Fe和Fe2O3)制取FeCO3进而制备铁红(Fe2O3)的主要流程如图1所示。
(1)用粉碎机将废铁屑研成粉末的目的是 ,使反应更充分。
(2)“操作1”的名称为 。
(3)“溶解池”中得到的溶液的溶质是H2SO4、Fe2(SO4)3以及 。
(4)从“操作1”中获得的FeCO3固体需要进行洗涤,检验FeCO3固体已洗净的方法是:取最后一次的洗涤液于洁净的试管中,先滴加过量稀盐酸,再滴加 (填化学式)溶液,无明显现象。
(5)“煅烧窑”中发生反应的化学方程式为 。
(6)研究团队模拟炼铁的过程,对一定质量的:Fe2O3进行加热,通过精密仪器测定反应过程中固体质量随温度变化的曲线,结果如图所示。
【查阅资料】用CO还原Fe2O3炼铁的过程大致分为以下三个阶段。
阶段1:
阶段2:
阶段3:
i.温度控制在300~500℃时,固体质量没有发生变化,原因是 。
ii.图中H点对应的固体成分是 。
iii.图中M点对应a的值为 。
三、实验题
19.在化学实验操作中,小明和小红分别抽取了Ⅰ、Ⅱ组试题进行实验。
Ⅰ组:O2和CO2的制取与性质探究
(1)实验室中装置A、B都可以用来制取氧气和二氧化碳,其中仪器a的名称是 ,实验室制取二氧化碳的反应的化学方程式为 ,装置C中凹陷的软质塑料瓶的优点与装置 (填“A”或“B”)相似。
(2)小明提出用装置C可以验证可燃物燃烧的条件,进行如下实验:
i.捏住乙处瓶身(如图所示)一段时间后,点燃丁处酒精灯,观察到丙处硫不燃烧。
ii.继续实验:放开乙处瓶身,捏住甲处瓶身一段时间,观察到丙处的现象是 。
通过对比实验i、ii,可以得出结论:物质燃烧需要 。并且能够得出CO2的化学性质之一是 。
(3)戊中氢氧化钠溶液的作用是 。
Ⅱ组:制作简易供氧器
小红制作了如图所示的简易供氧器,她选用的试剂是过碳酸钠和二氧化锰。过碳酸钠易溶于水,在水中分解产生Na2CO3和H2O2.
(4)检验生成的气体是氧气的方法: 。
(5)右瓶中水的作用是 。(写一点)
四、科学探究题
20.老师要求同学们设计实验鉴别稀盐酸、碳酸钠溶液和澄清石灰水三种无色溶液。两组同学分别设计实验如下:
(1)第1组:用紫色石蕊溶液鉴别三种溶液,其设计的理由是 。老师认为这个方案不严谨,原因是 。
(2)第2组:分别用三支试管将三种溶液(编号分别为a、b、c)两两进行混合,观察到的现象如下表所示。
溶液 a b c
a — 有沉淀产生 有气体产生
b 有沉淀产生 — 无明显现象
c 有气体产生 无明显现象 —
由实验现象可推断溶液b是 。溶液a与溶液c反应的化学方程式是 。
【实验拓展】将第2组实验剩余的稀盐酸和澄清石灰水进行混合,等充分反应后对所得溶液中溶质的成分进行探究。
【作出猜想】猜想一:只有CaCl2;猜想二:有CaCl2和HCl;猜想三:有CaCl2和Ca(OH)2;猜想四:有CaCl2、HCl和Ca(OH)2。
老师认为猜想四不合理,理由是 。
【实验探究】为证明其余猜想是否正确,同学们进行了如下实验:
实验序号 操作 现象 结论
Ⅰ 取少量反应后的溶液于试管中,加入CuCl2溶液 无明显现象 猜想 不成立
Ⅱ 取少量反应后的溶液于另一支试管中,加入硝酸银溶液 有 产生 猜想一成立
【交流评价】同学们反思后发现实验Ⅱ所得结论不严谨,其理由是 。
【反思拓展】在分析化学反应后所得物质的成分时,除考虑生成物外,还需考虑 。
五、综合应用题
21.我国有着储量丰富的低品铝土矿资源,科研人员通过采用焙烧—碱浸预脱硅工艺,获得高铝硅比铝精矿,实现“贫矿变富矿”,并有效地提高了氧化铝的溶出率。其工艺流程如图所示。
(1)流程中的“碱浸脱硅”是使用烧碱溶液浸泡“铝土矿焙砂”,以除去矿砂中的SiO2,其反应同CO2与烧碱反应相似。请写出“碱浸脱硅”反应的化学方程式: 。
(2)现有一种铝土矿样品,氧化铝的含量为40%,其中有95%的氧化铝能转化成高纯度氧化铝,然后通过电解制得金属铝,理论上100t该铝土矿可制得金属铝 t(写出计算过程,计算结果保留一位小数,工业制铝反应的化学方程式:)。
(3)某种铝土矿采用上述工艺可获得铝精矿。其预脱硅效果受焙烧温度等因素影响。其中焙烧温度对脱硅率的影响如图所示,根据曲线图判断,最佳焙烧温度是 。
《2025年广东省大湾区初中学业水平质量监测卷化学试卷一》参考答案
1.A
2.C
3.D
4.B
5.D
6.B
7.A
8.C
9.D
10.B
11.C 12.A 13.B
14.D
15.D
16.(1)金属
(2)物质的溶解性不同(合理即可)
(3)2Ag2O
(4)
(5)适当向炉膛鼓风(合理即可)
17.(1)S8
(2)21.5%
(3)K2SO4(答案合理即可)
(4)
(5)ABCD
18.(1)增大反应物之间的接触面积,使反应更快更充分
(2)过滤
(3)硫酸亚铁/FeSO4
(4)BaCl2(合理即可)
(5)
(6) 没有达到反应温度 四氧化三铁/Fe3O4 18.0/18
19.(1) 长颈漏斗 A
(2) 发出明亮的蓝紫色火焰 与氧气接触 不燃烧、不支持燃烧
(3)吸收SO2,防止污染空气
(4)将带火星的木条放在导管口,木条复燃,说明是氧气
(5)湿润氧气,且可通过产生气泡的速率观测生成氧气的速率
20.(1) 酸性、碱性溶液能使紫色石蕊溶液变色 碳酸钠溶液与澄清石灰水均能使紫色石蕊溶液变蓝色
(2) 澄清石灰水 Ca(OH)2与HCl不能共存 三 白色沉淀 氯化钙、盐酸均能与硝酸银反应生成氯化银白色沉淀,故加入硝酸银溶液,产生白色沉淀,不能说明猜想一成立 反应物是否过量
21.(1)
(2)解:设可制得金属铝的质量为x。
x=20.1t
答:可制得20.1t的金属铝
(3)1050℃
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.广东文化底蕴深厚,越看“粤”精彩。下列物品主要由金属材料制成的是
A.西周铜盉(信宜) B.潮汕嵌瓷(潮州)
C.木制龙舟(顺德) D.粤剧戏服(广州)
2.广东省有着浓厚的岭南文化气息,具有众多非物质文化遗产。下列说法正确的是
A.绘画的墨汁属天然有机色素 B.工夫茶的茶水,属于纯净物
C.剪纸的运剪过程属物理变化 D.木雕的雕刻过程属化学变化
3.强调实验安全非常重要,下列图标与做“粗盐中难溶性杂质的去除”实验无关的是
A.明火 B.护目镜 C.洗手 D.锐器
4.铌元素广泛用于航空航天、超导材料等领域,它在元素周期表中的信息如图所示,下列说法错误的是
A.铌的原子序数为41 B.一个铌原子的质量为92.91g
C.铌的单质有导电性 D.铌的元素符号为Nb
5.参加下乡学农研学活动,可以掌握多种生活技能。做饭时的做法与对应的原理不符合的是
选项 做法 原理
A 用木柴生火 木柴是可燃物
B 用废纸引燃木柴 使温度达到木柴的着火点
C 将木柴架空摆放 有利于空气流通
D 对灶膛扇风 降温,防止煮焦米饭
A.A B.B C.C D.D
6.分类是一种科学方法,可使学习更高效。下列物质的分类合理的是
A.酸:HCl、CH4 B.氧化物:Na2O、H2O
C.碱:Cu2(OH)2CO3、Fe(OH)3 D.盐:Al2O3、AlCl3
7.我国现代科学家为化学学科发展作出了不懈的努力,下列叙述错误的是
A.张青莲院士为元素名称的中文命名作出了卓越贡献
B.闵恩泽院士为我国炼油催化剂制造技术奠定了基础
C.屠呦呦研究员为世界治疗疟疾作出了巨大贡献
D.徐光宪院士为我国稀土工业发展作出了卓越贡献
8.化学用语是学习化学的重要工具,下列含氮物质中氮元素的化合价显+3价的是
A.NH3 B.N2 C.HNO2 D.NO2
9.氢化钛(TiH2)作为储氢材料备受关注。其可用钛粉(Ti)和H2在一种纳米催化剂的作用下,控制一定的温度和压强反应得到,反应的微观示意图如图所示。下列说法正确的是
A.该反应共生成两种物质
B.反应的化学方程式为
C.参加反应的物质的质量比为2:3
D.反应前后纳米催化剂的化学性质不变
10.实验室用KMnO4制取O2时不会用到的仪器装置是
A. B. C. D.
侯德榜是我国化学工业的先驱,其发明的“侯氏制碱法”为我国基本化工原料工业奠定了基础。“侯氏制碱法”的简易流程如图甲所示。完成下面小题。
11.根据如图乙所示的溶解度曲线,判断沉淀池中生成的沉淀为
A.NaCl B.NH4Cl C.NaHCO3 D.NH4Cl和NaCl
12.已知X为某种气体,其化学式为
A.CO2 B.HCl C.CO D.NH3
13.纯碱(Na2CO3)在工业生产中常作为碱使用。下列关于Na2CO3的说法错误的是
A.水溶液呈碱性 B.属于碱
C.与稀盐酸反应可产生CO2 D.广泛用于玻璃、造纸、纺织等工业生产
14.部分含碳物质的分类与碳元素的化合价关系如图所示。下列推断不合理的是
A.a是可燃冰的主要成分
B.b可能是天然存在的最硬的物质
C.实验室中可用e制备d
D.c和d不可以相互转化
15.下列鉴别或除杂操作正确的是
选项 实验目的 操作
A 除去CO2中混有的HCl 通过足量NaOH溶液
B 除去CuO中的Cu 加入过量稀盐酸,过滤
C 鉴别BaCl2溶液与CaCl2溶液 加入适量Na2CO3溶液
D 鉴别NaOH固体与NH4NO3固体 分别加水溶解,用温度计测量温度变化
A.A B.B C.C D.D
二、填空与简答
16.《天工开物》蕴含着丰富的化学知识与方法。其中关于银的冶炼过程如图所示。
(1)铅、银属于 (填“金属”或“非金属”)单质。
(2)“淘洗”时可用水除去矿砂中的一些杂质,其原理是利用了 。
(3)补充完整“熔矿”时氧气与Ag2S反应的化学方程式: 。
(4)“熔矿”“结银”操作如图乙所示,所需热量由木炭燃烧提供,木炭充分燃烧反应的化学方程式为 。
(5)为使图乙中木炭燃烧更充分,可采取的措施是 (写一条)。
17.硫元素以硫化物、硫酸盐、有机硫和单质硫等形式广泛存在于自然界。硫在某些系外行星的大气层中以H2S和SO2的形式存在,这些物质经过光化学反应,产生了S8和H2SO4;硫在地壳中的含量为0.048%,是自然界中重要的非金属元素,其在自然界的循环过程如图所示。硫还存在于人体中,是甲硫氨酸(C5H11O2NS)和半胱氨酸(C3H7NO2S)等氨基酸的组成元素。硫是植物维持生命活动所需的元素,可以通过施加硫肥(硫黄或可溶性硫酸盐溶液)补充。我国古代“四大发明”之一的黑火药,主要由硫黄、硝酸钾和木炭按一定比例混合而成。
(1)短文中光化学反应生成的硫单质的化学式是 。
(2)甲硫氨酸(C5H11O2NS)是一种有机化合物,其中硫元素的质量分数是 (计算结果保留一位小数)。
(3)试写出一种能增强抗倒伏能力的硫肥: (填化学式)。
(4)黑火药燃爆会生成K2S、N2和CO2,写出黑火药燃爆的化学方程式: 。
(5)由图可知,下列说法正确的是___________(多选,填字母)。
A.过程Ⅰ中硫元素的化合价升高 B.减少使用化石能源可以减少SO2排放
C.含硫有机物和含硫无机物可相互转化 D.过程Ⅱ是形成酸雨的原因之一
18.用废铁屑(含Fe和Fe2O3)制取FeCO3进而制备铁红(Fe2O3)的主要流程如图1所示。
(1)用粉碎机将废铁屑研成粉末的目的是 ,使反应更充分。
(2)“操作1”的名称为 。
(3)“溶解池”中得到的溶液的溶质是H2SO4、Fe2(SO4)3以及 。
(4)从“操作1”中获得的FeCO3固体需要进行洗涤,检验FeCO3固体已洗净的方法是:取最后一次的洗涤液于洁净的试管中,先滴加过量稀盐酸,再滴加 (填化学式)溶液,无明显现象。
(5)“煅烧窑”中发生反应的化学方程式为 。
(6)研究团队模拟炼铁的过程,对一定质量的:Fe2O3进行加热,通过精密仪器测定反应过程中固体质量随温度变化的曲线,结果如图所示。
【查阅资料】用CO还原Fe2O3炼铁的过程大致分为以下三个阶段。
阶段1:
阶段2:
阶段3:
i.温度控制在300~500℃时,固体质量没有发生变化,原因是 。
ii.图中H点对应的固体成分是 。
iii.图中M点对应a的值为 。
三、实验题
19.在化学实验操作中,小明和小红分别抽取了Ⅰ、Ⅱ组试题进行实验。
Ⅰ组:O2和CO2的制取与性质探究
(1)实验室中装置A、B都可以用来制取氧气和二氧化碳,其中仪器a的名称是 ,实验室制取二氧化碳的反应的化学方程式为 ,装置C中凹陷的软质塑料瓶的优点与装置 (填“A”或“B”)相似。
(2)小明提出用装置C可以验证可燃物燃烧的条件,进行如下实验:
i.捏住乙处瓶身(如图所示)一段时间后,点燃丁处酒精灯,观察到丙处硫不燃烧。
ii.继续实验:放开乙处瓶身,捏住甲处瓶身一段时间,观察到丙处的现象是 。
通过对比实验i、ii,可以得出结论:物质燃烧需要 。并且能够得出CO2的化学性质之一是 。
(3)戊中氢氧化钠溶液的作用是 。
Ⅱ组:制作简易供氧器
小红制作了如图所示的简易供氧器,她选用的试剂是过碳酸钠和二氧化锰。过碳酸钠易溶于水,在水中分解产生Na2CO3和H2O2.
(4)检验生成的气体是氧气的方法: 。
(5)右瓶中水的作用是 。(写一点)
四、科学探究题
20.老师要求同学们设计实验鉴别稀盐酸、碳酸钠溶液和澄清石灰水三种无色溶液。两组同学分别设计实验如下:
(1)第1组:用紫色石蕊溶液鉴别三种溶液,其设计的理由是 。老师认为这个方案不严谨,原因是 。
(2)第2组:分别用三支试管将三种溶液(编号分别为a、b、c)两两进行混合,观察到的现象如下表所示。
溶液 a b c
a — 有沉淀产生 有气体产生
b 有沉淀产生 — 无明显现象
c 有气体产生 无明显现象 —
由实验现象可推断溶液b是 。溶液a与溶液c反应的化学方程式是 。
【实验拓展】将第2组实验剩余的稀盐酸和澄清石灰水进行混合,等充分反应后对所得溶液中溶质的成分进行探究。
【作出猜想】猜想一:只有CaCl2;猜想二:有CaCl2和HCl;猜想三:有CaCl2和Ca(OH)2;猜想四:有CaCl2、HCl和Ca(OH)2。
老师认为猜想四不合理,理由是 。
【实验探究】为证明其余猜想是否正确,同学们进行了如下实验:
实验序号 操作 现象 结论
Ⅰ 取少量反应后的溶液于试管中,加入CuCl2溶液 无明显现象 猜想 不成立
Ⅱ 取少量反应后的溶液于另一支试管中,加入硝酸银溶液 有 产生 猜想一成立
【交流评价】同学们反思后发现实验Ⅱ所得结论不严谨,其理由是 。
【反思拓展】在分析化学反应后所得物质的成分时,除考虑生成物外,还需考虑 。
五、综合应用题
21.我国有着储量丰富的低品铝土矿资源,科研人员通过采用焙烧—碱浸预脱硅工艺,获得高铝硅比铝精矿,实现“贫矿变富矿”,并有效地提高了氧化铝的溶出率。其工艺流程如图所示。
(1)流程中的“碱浸脱硅”是使用烧碱溶液浸泡“铝土矿焙砂”,以除去矿砂中的SiO2,其反应同CO2与烧碱反应相似。请写出“碱浸脱硅”反应的化学方程式: 。
(2)现有一种铝土矿样品,氧化铝的含量为40%,其中有95%的氧化铝能转化成高纯度氧化铝,然后通过电解制得金属铝,理论上100t该铝土矿可制得金属铝 t(写出计算过程,计算结果保留一位小数,工业制铝反应的化学方程式:)。
(3)某种铝土矿采用上述工艺可获得铝精矿。其预脱硅效果受焙烧温度等因素影响。其中焙烧温度对脱硅率的影响如图所示,根据曲线图判断,最佳焙烧温度是 。
《2025年广东省大湾区初中学业水平质量监测卷化学试卷一》参考答案
1.A
2.C
3.D
4.B
5.D
6.B
7.A
8.C
9.D
10.B
11.C 12.A 13.B
14.D
15.D
16.(1)金属
(2)物质的溶解性不同(合理即可)
(3)2Ag2O
(4)
(5)适当向炉膛鼓风(合理即可)
17.(1)S8
(2)21.5%
(3)K2SO4(答案合理即可)
(4)
(5)ABCD
18.(1)增大反应物之间的接触面积,使反应更快更充分
(2)过滤
(3)硫酸亚铁/FeSO4
(4)BaCl2(合理即可)
(5)
(6) 没有达到反应温度 四氧化三铁/Fe3O4 18.0/18
19.(1) 长颈漏斗 A
(2) 发出明亮的蓝紫色火焰 与氧气接触 不燃烧、不支持燃烧
(3)吸收SO2,防止污染空气
(4)将带火星的木条放在导管口,木条复燃,说明是氧气
(5)湿润氧气,且可通过产生气泡的速率观测生成氧气的速率
20.(1) 酸性、碱性溶液能使紫色石蕊溶液变色 碳酸钠溶液与澄清石灰水均能使紫色石蕊溶液变蓝色
(2) 澄清石灰水 Ca(OH)2与HCl不能共存 三 白色沉淀 氯化钙、盐酸均能与硝酸银反应生成氯化银白色沉淀,故加入硝酸银溶液,产生白色沉淀,不能说明猜想一成立 反应物是否过量
21.(1)
(2)解:设可制得金属铝的质量为x。
x=20.1t
答:可制得20.1t的金属铝
(3)1050℃
同课章节目录
