人教版(2019)选择性必修二 第一章 物质结构与性质 解读课件(49张)
文档属性
| 名称 | 人教版(2019)选择性必修二 第一章 物质结构与性质 解读课件(49张) |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-20 00:00:00 | ||
图片预览











文档简介
(共49张PPT)
第一章《原子结构与性质》
解 读
1
课标要求
2
教学内容分析
3
教学建议
目 录
一、课标要求
延时符
1.内容要求
1.1 原子核外电子的运动状态
了解有关核外电子运动模型的历史发展过程,认识核外电子的运动特点。知道电子运动的能量状态具有量子化的特征(能量不连续),电子可以处于不同的能级,在一定条件下会发生激发与跃迁。知道电子的运动状态(空间分布及能量)可通过原子轨道和电子云模型来描述。
1.2 核外电子排布规律
知道原子核外电子的能级高低顺序,了解原子核外电子排布的构造原理,认识基态原子中核外电子的排布遵循能量最低原理、泡利不相容原理和洪特规则等。知道1~36号元素基态原子核外电子的排布。
1.3 核外电子排布与元素周期律(表)
认识元素的原子半径、第一电离能、电负性等元素性质的周期性变化,知道原子核外电子排布呈现周期性变化是导致元素性质周期性变化的原因。知道元素周期表中分区、周期和族的元素原子核外电子排布特征,了解元素周期律(表)的应用价值。
一、课标要求
延时符
2.学业要求
能说明微观粒子的运动状态与宏观物体运动特点的差异。
能结合能量最低原理、泡利不相容原理、洪特规则书写1~36号元素基态原子的核外电子排布式和轨道表示式,并说明含义。
能说出元素电离能、电负性的含义,能描述主族元素第一电离能、电负性变化的一般规律,能从电子排布的角度对这一规律进行解释。能说明电负性大小与原子在化合物中吸引电子能力的关系,能利用电负性判断元素的金属性与非金属性的强弱,推测化学键的极性。
能从原子价电子数目和价电子排布的角度解释元素周期表的分区、周期和族的划分。能举例元素周期律(表)的应用。
能说明构建思维模型在人类认识原子结构过程中的重要作用,能论证证据与模型建立及其发展之间的关系。能简要说明原子核外电子运动规律的理论探究对研究元素性质及其变化规律的意义。
一、课标要求
延时符
3.《指导意见》学习目标
1.通过原子光谱,认识核外电子运动的量子化特征,了解能层、能级、基态与激发态等概念。借助电子云认识原子轨道,发展对微观结构的想象能力。能运用原子轨道研究核外电子排布,掌握核外电子排布的构造原理及表征,建立宏观性质与微观结构的有机联系。
2.知道N、Cr、Cu等原子的核外电子排布是原子光谱实验测定的结果,归纳出泡利原理、洪特规则与能量最低原理等经验规则,能熟练书写1~36号元素基态原子的核外电子排布式。能用构造原理对元素的部分性质,如原子半径、电离能等进行解释与比较,能根据原子结构预测元素在特定条件下可能具有的性质和发生的变化,养成“结构决定性质,性质反映结构”的观念。
3.以同主族、同周期元素的性质变化为认知依据,归纳出元素周期律和对角线规则,知道化学变化遵循一定的规律,能用元素周期律预测物质的性质。在使用经验规则分析和解决问题的过程中,认知经验规则的局限性,知道需要从内因与外因、量变与质变等多角度分析物质的化学变化,构建科学的“变化观念”。
一、课标要求
延时符
3.《指导意见》学习目标
4.基于原子结构模型演变过程,认识到证据的重要性。知道能量最低原理、洪特规则、泡利原理等是基于原子光谱的推理结果,理解科学家根据宏观现象推理出微观结构的思维过程,培育证据意识。能够以实验数据为证据,归纳主族元素第一电离能、电负性的变化规律,认识观点、结论和证据间的逻辑关系,发展证据推理能力。对部分不符合经验规律的例外,能够从原子角度给出合理解释。借助实验、数据、推理的思维过程发展“证据推理和模型认知”素养。
5.能以电子云模型为基础建构原子轨道模型(s、p能级)。能根据元素周期表建构“位”“构”“性”系统思维模型。能利用模型解释和预测性质变化,在事实与理论模型之间建立有机联系和合理匹配,具备构建解决复杂问题的思维框架的能力。
6.知道对性质的预测必须经实验的证实或证伪,养成注重实证、严谨求实的“科学态度”。发现与对角线规则等经验规律不一致的实验事实时,能够尊重事实,养成独立思考、敢于质疑的精神。借助结构理论的演变,了解科学家的思维过程、领悟科学方法,培养探索未知、勇于创新的科学精神,认同“物质结构的探索是无止境的”。能对生活中的“量子科技产品”作出正确评价,自觉抵制伪科学,强化“社会责任”。从中国古代哲学家对原子的思考、徐光宪的n+0.7l规则等,认识我国科学家对物质结构的发展的重大贡献,培育民族自豪感与认同感。
一、课标要求
延时符
4.《指导意见》评价目标
1.通过对原子光谱谱图的交流与讨论,诊断和发展学生从定性角度认识电子运动的量子化特征;通过对原子结构模型演变的交流与讨论,诊断并发展学生对“人类对物质结构的认识是不断发展的”的认识。
2.通过对1~36号元素基态原子的核外电子排布式、价层电子式和轨道式等的书写,诊断和发展学生对能级的定性认识水平,发展学生对能量最低原理、泡利原理和洪特规则的系统认识水平,从学科价值视角认识“电子运动规律的理论探索”对研究元素性质的重要意义。
3.通过建立原子结构与元素周期系的有机联系,诊断并发展学生从原子构造视角认识元素周期表的结构(族、周期、分区)的水平;结合实验数据,学习电离能、电负性及其变化规律,诊断并发展学生从定性定量、宏微结合等视角对物质及其变化规律的认识水平,发展逻辑推理能力;通过列举化学事实,诊断并发展学生从学科和社会价值视角认识元素周期律(表)在生产与科学研究中的应用。
4.借助具体案例认识建构模型对推动结构理论发展的重要作用,在推断论证中认识模型的局限性,诊断和发展学生建立、改进和优化模型的水平,诊断和发展学生根据问题的复杂性匹配思维模型的水平,知道对物质结构的研究有助于发现具有预期性质的新物质,赞赏原子结构及其理论发展对化学学科新发现的推动与贡献。
二、教学内容分析
延时符
1.新人教版与旧苏教版教材内容变化比较
新增内容
1.能级
2.概率密度
3.电子云轮廓图绘制
4.原子光谱
5.元素周期系
6.元素周期表中区的划分
7.原子半径的影响因素
8.对角线规则
删除内容
1.人类对原子结构的认识(发展史)
2.洪特规则的特例
①内容增减
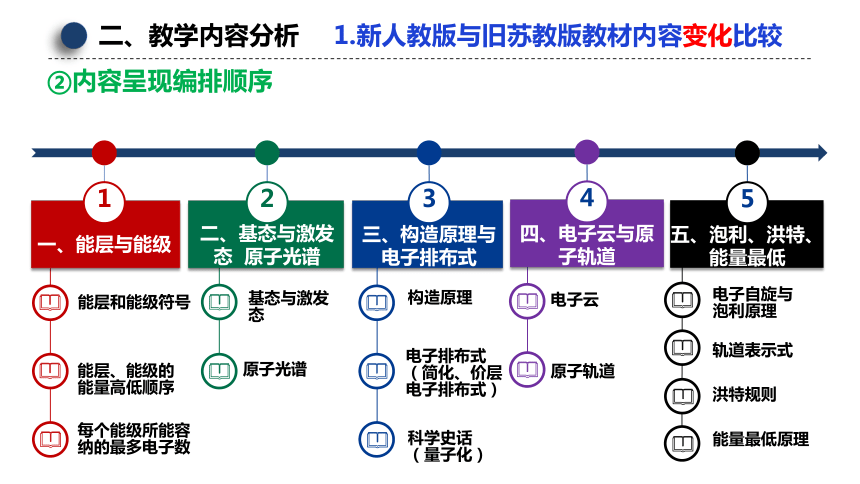
一、能层与能级
1
能层和能级符号
能层、能级的能量高低顺序
每个能级所能容纳的最多电子数
二、基态与激发态 原子光谱
2
三、构造原理与电子排布式
3
基态与激发态
原子光谱
二、教学内容分析
1.新人教版与旧苏教版教材内容变化比较
②内容呈现编排顺序
四、电子云与原子轨道
4
五、泡利、洪特、能量最低
5
构造原理
电子排布式(简化、价层电子排布式)
科学史话(量子化)
电子云
原子轨道
电子自旋与泡利原理
轨道表示式
洪特规则
能量最低原理
一、原子结构与元素周期表
1
元素周期律、元素周期系和元素周期表
构造原理与元素周期表(周期、族、区)
二、元素周期律
2
原子半径
电离能
电负性
二、教学内容分析
1.新人教版与旧苏教版教材内容变化比较
对角线规则
新教材从“构造原理”得出的电子排布出发,探讨元素周期表的特点
②内容呈现编排顺序
二、教学内容分析
2.基本知识框架
原子结构与性质
原子结构
元素的性质
元素周期系
元素周期表
元素周期律
原子半径
电离能
电负性
电子云和原子轨道
电子排布
运动状态
能层、能级
基态、激发态、原子光谱
构造原理
泡利原理
洪特规则
能量最低原理
核外电子排布
决 定
应用
3.课时分配
节 内容 课时建议
第一节 原子结构 一、能层与能级 二、基态与激发态 原子光谱 三、构造原理与电子排布式 四、电子云与原子轨道 五、泡利原理、洪特规则、能量最低原理 4
第二节 原子结构与元素的性质 一、原子结构与元素周期表 二、元素周期律 3
整理与提升 2
合计 9
(原子半径、电离能、电负性)
二、教学内容分析
1课时
1课时
2课时
1课时
2课时
2课时
4.考试内容
二、教学内容分析
(2012 浙江)(1)可正确表示原子轨道的是: ① 。
A.2s B.2d C.3pz D.3f
(2)写出基态镓(Ga)原子的电子排布式: ② 。
(5)用“>” “< ” “=” 填空:
第一电离能的大小:Mg ⑧ Al;
(2013 浙江)请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是 ① (填写元素符号)。
(2)基态锗(Ge)原子的电子排布式是 ② 。
电离能 I1 I2 I3 I4 ……
In/kJ.mol-1 578 1817 2745 11578 ……
4.考试内容
二、教学内容分析
(2014 浙江)(1)31Ga基态原子的核外电子排布式是 ① 。
某种半导体材料由Ga和As两种元素组成,该半导体材料的化学式是 ② ,
(2015 浙江)(1)Cu2+的电子排布式是 ① ;
(5)下列有关性质的比较,正确的是 ⑤ ;
A.第一电离能:O>N
4.考试内容
二、教学内容分析
(2021.6全国甲卷)(1)Si的价电子层的电子排布式为________;
(2021.6全国乙卷)(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
考试不难,但知识抽象理解难;
上课不难,但核心素养培育难。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
【文章1(王后雄)】人教版选择性必修二第一章《原子结构与性质》中的内容具有以下特点:(1)抽象内容多;(2)立体知识多;(3)概念多。本章引进了很多新颖的、抽象程度很高的概念和原理,如光谱、原子轨道等,旨在让学生在已有基础上进一步理解原子结构,认识结构与性质之间的关系,因此对学生学习和应用化学基本理论的要求比其他模块相对都要高,因此在讲解时要力求通俗易懂、深入浅出。
【文章2(郑长龙)】《物质结构与性质》模块的特点是知识深奥、理论性强、比较抽象,因此,对相当一部分学生来说难度很大,对教师来说也是一种挑战。《物质结构与性质》模块中有些知识点在知识体系中属于大学教材中的内容,十分抽象难懂,超出了一般学生的思维能力,因此,教师在教学过程中会遇到各种各样的困难与挑战。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
《学科指导意见》教学中要注意控制教学内容的深广度,避免加重学生的学习负担。
抽象
如,在已知核外电子按照能量不同可以分成不同能层(电子层),从而引出能级的概念,介绍了能级的填充顺序,但并没有详细介绍或解释能级交错现象,教学中要注意点到为止。但有时为了促进学生对原子构造原理的理解,教学中可以根据学生的实际情况适度拓展教学内容。
易懂
拓展
简单化
选择
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
【案例1.电子云】
旧苏教版
小黑点的疏密表示该区域内出现机会的大小
三、教学建议
新苏教版
小点的疏密表示该区域内出现机会的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
新鲁科版
小点的疏密程度表示单位体积内出现概率的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
新人教版
小点的疏密程度表示概率密度的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
小点的疏密表示该区域内出现机会的大小
小点的疏密程度表示单位体积内出现概率的大小
小点的疏密程度表示概率密度的大小
小点的疏密表示概率的大小
小点的疏密表示机会的大小
小点的疏密表示概率密度的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
概率与概率密度?
新鲁科版教参38页
新人教版教参28页
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
电子云模型是为了说明电子在原子核外的运动状态
原子轨道
原子结构(原子核外电子排布)
共价键成键分析
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
【案例2.原子光谱】
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
电子跃迁
原子光谱
电子排布
鉴定元素
基态与激发态
发射光谱与吸收光谱
能层、能级的量子化
应用
产生
证据推理
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
【物理选修3-5】
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
原子光谱
抽象
易懂
拓展
简单化
选择
电子排布
简单化
选择
量子化与计算
电子跃迁就像上下楼梯,电子从基态到激发态就像爬楼梯,脚只能踩在台阶上,不能踩在台阶的中间;所以电子跃迁所吸收或释放的能量是量子化的,不是连续的。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
电子跃迁的能量量子化
三、教学建议
【陈光巨教授】
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
要注意形象化教学,降低对抽象知识的理解难度。本章知识较为抽象,不能依据中学化学实验进行佐证,在教学中可借助实物模型、图片、视频、计算机软件模拟等多种直观手段,降低教学内容的抽象性,帮助学生思考和理解。例如,在教学中要充分发挥教科书中的电子云轮廓图、原子半径示意图等图片的功能,让教学内容通俗易懂。教学中还要深入思考如何在保证所授知识的科学性和严谨性的前提下,把深奥的原子结构理论用形象易懂的语言进行表达,以提高学生对抽象知识的接受与理解。
《学科指导意见》2.教学方法
2.借助模型、实验、视频,降低学习难度。
三、教学建议
《学科指导意见》2.教学方法
教学中要关注物质结构研究的过程、思路和方法的介绍,让学生掌握知识的同时发展核心素养。如利用原子光谱及其发展历程等化学史素材创设教学情境,帮助学生认识知识从何而来,基于哪些证据,经过怎样的逻辑推理,如何建立理论模型与完善,实现“化学史给人以智慧”的教学效果。在教学中要思考如何增强教学的探究性,如对构造原理,可按照“实验情境(原子光谱)→发现问题→科学假说→科学推论(建立科学理论)”的过程进行教学:根据氢原子光谱实验(氢原子的不连续的线状光谱),发现卢瑟福原子模型不能解释的问题,提出电子运动的量子化特征,引入“原子轨道”假设,归纳得出电子排布规律的“构造原理”。
2.借助模型、实验、视频,降低学习难度。
三、教学建议
2.借助模型、实验、视频,降低学习难度。
能层与能级
能层是楼层,能级是楼梯的阶梯。
三、教学建议
2.借助模型、实验、视频,降低学习难度。
【杭二中朱文博】
问题1:水为什么不停留在某个台阶上?
问题2:水为什么不停留在某两个台阶之间?
问题3:同一个台阶上的水面高度呈现什么特征
能量最低原理
洪特规则
量子化
问题4:与核外电子排布的规律有何相同之处?
问题5:生活中还有哪些现象与核外电子排布规律相似?
三、教学建议
2.借助模型、实验、视频,降低学习难度。
三、教学建议
【北师大附中王澜老师】
钠灯
棱镜分光镜
2.借助模型、实验、视频,降低学习难度。
三、教学建议
核外电子运动模型的发展史
核外电子模型的建构与完善
【案例3.基于证据推理与模型认知的教学设计】
证据推理
原子光谱
【内容要求】了解有关核外电子运动模型的历史发展过程,认识核外电子的运动特点。
【学业要求】能说明构建思维模型在人类认识原子结构过程中的重要作用,能论证证据与模型建立及其发展之间的关系。
?
2.借助模型、实验、视频,降低学习难度。
三、教学建议
【案例3.基于证据推理与模型认知的教学设计】
4.核外电子分层排布模型的演变
道尔顿模型
汤姆生模型
卢瑟福模型
玻尔模型
量子力学模型
1.核外电子分层排布
2.离核较远的区域运动的电子能量高
3.电子一般总是先从内层排起
2.借助模型、实验、视频,降低学习难度。
三、教学建议
【案例3.基于证据推理与模型认知的教学设计】
4.核外电子分层排布模型的演变
1.核外电子分层排布
2.离核较远的区域运动的电子能量高
3.电子一般总是先从内层排起
1.能层与能级
2.能量的量子化
3.构造原理
4.量子力学模型(电子云与原子轨道)
化学必修第一册
物质结构与性质
证据
光谱
2.借助模型、实验、视频,降低学习难度。
三、教学建议
构造原理
不同能层的能量不同
相同能层的不同能级的能量不同
电子自旋
核外电子运动模型发展史
模型建构与完善
【案例3.基于证据推理与模型认知的教学设计】
证据推理
原子光谱
E(K)E(ns)2.借助模型、实验、视频,降低学习难度。
第一章《原子结构与性质》
解 读
1
课标要求
2
教学内容分析
3
教学建议
目 录
一、课标要求
延时符
1.内容要求
1.1 原子核外电子的运动状态
了解有关核外电子运动模型的历史发展过程,认识核外电子的运动特点。知道电子运动的能量状态具有量子化的特征(能量不连续),电子可以处于不同的能级,在一定条件下会发生激发与跃迁。知道电子的运动状态(空间分布及能量)可通过原子轨道和电子云模型来描述。
1.2 核外电子排布规律
知道原子核外电子的能级高低顺序,了解原子核外电子排布的构造原理,认识基态原子中核外电子的排布遵循能量最低原理、泡利不相容原理和洪特规则等。知道1~36号元素基态原子核外电子的排布。
1.3 核外电子排布与元素周期律(表)
认识元素的原子半径、第一电离能、电负性等元素性质的周期性变化,知道原子核外电子排布呈现周期性变化是导致元素性质周期性变化的原因。知道元素周期表中分区、周期和族的元素原子核外电子排布特征,了解元素周期律(表)的应用价值。
一、课标要求
延时符
2.学业要求
能说明微观粒子的运动状态与宏观物体运动特点的差异。
能结合能量最低原理、泡利不相容原理、洪特规则书写1~36号元素基态原子的核外电子排布式和轨道表示式,并说明含义。
能说出元素电离能、电负性的含义,能描述主族元素第一电离能、电负性变化的一般规律,能从电子排布的角度对这一规律进行解释。能说明电负性大小与原子在化合物中吸引电子能力的关系,能利用电负性判断元素的金属性与非金属性的强弱,推测化学键的极性。
能从原子价电子数目和价电子排布的角度解释元素周期表的分区、周期和族的划分。能举例元素周期律(表)的应用。
能说明构建思维模型在人类认识原子结构过程中的重要作用,能论证证据与模型建立及其发展之间的关系。能简要说明原子核外电子运动规律的理论探究对研究元素性质及其变化规律的意义。
一、课标要求
延时符
3.《指导意见》学习目标
1.通过原子光谱,认识核外电子运动的量子化特征,了解能层、能级、基态与激发态等概念。借助电子云认识原子轨道,发展对微观结构的想象能力。能运用原子轨道研究核外电子排布,掌握核外电子排布的构造原理及表征,建立宏观性质与微观结构的有机联系。
2.知道N、Cr、Cu等原子的核外电子排布是原子光谱实验测定的结果,归纳出泡利原理、洪特规则与能量最低原理等经验规则,能熟练书写1~36号元素基态原子的核外电子排布式。能用构造原理对元素的部分性质,如原子半径、电离能等进行解释与比较,能根据原子结构预测元素在特定条件下可能具有的性质和发生的变化,养成“结构决定性质,性质反映结构”的观念。
3.以同主族、同周期元素的性质变化为认知依据,归纳出元素周期律和对角线规则,知道化学变化遵循一定的规律,能用元素周期律预测物质的性质。在使用经验规则分析和解决问题的过程中,认知经验规则的局限性,知道需要从内因与外因、量变与质变等多角度分析物质的化学变化,构建科学的“变化观念”。
一、课标要求
延时符
3.《指导意见》学习目标
4.基于原子结构模型演变过程,认识到证据的重要性。知道能量最低原理、洪特规则、泡利原理等是基于原子光谱的推理结果,理解科学家根据宏观现象推理出微观结构的思维过程,培育证据意识。能够以实验数据为证据,归纳主族元素第一电离能、电负性的变化规律,认识观点、结论和证据间的逻辑关系,发展证据推理能力。对部分不符合经验规律的例外,能够从原子角度给出合理解释。借助实验、数据、推理的思维过程发展“证据推理和模型认知”素养。
5.能以电子云模型为基础建构原子轨道模型(s、p能级)。能根据元素周期表建构“位”“构”“性”系统思维模型。能利用模型解释和预测性质变化,在事实与理论模型之间建立有机联系和合理匹配,具备构建解决复杂问题的思维框架的能力。
6.知道对性质的预测必须经实验的证实或证伪,养成注重实证、严谨求实的“科学态度”。发现与对角线规则等经验规律不一致的实验事实时,能够尊重事实,养成独立思考、敢于质疑的精神。借助结构理论的演变,了解科学家的思维过程、领悟科学方法,培养探索未知、勇于创新的科学精神,认同“物质结构的探索是无止境的”。能对生活中的“量子科技产品”作出正确评价,自觉抵制伪科学,强化“社会责任”。从中国古代哲学家对原子的思考、徐光宪的n+0.7l规则等,认识我国科学家对物质结构的发展的重大贡献,培育民族自豪感与认同感。
一、课标要求
延时符
4.《指导意见》评价目标
1.通过对原子光谱谱图的交流与讨论,诊断和发展学生从定性角度认识电子运动的量子化特征;通过对原子结构模型演变的交流与讨论,诊断并发展学生对“人类对物质结构的认识是不断发展的”的认识。
2.通过对1~36号元素基态原子的核外电子排布式、价层电子式和轨道式等的书写,诊断和发展学生对能级的定性认识水平,发展学生对能量最低原理、泡利原理和洪特规则的系统认识水平,从学科价值视角认识“电子运动规律的理论探索”对研究元素性质的重要意义。
3.通过建立原子结构与元素周期系的有机联系,诊断并发展学生从原子构造视角认识元素周期表的结构(族、周期、分区)的水平;结合实验数据,学习电离能、电负性及其变化规律,诊断并发展学生从定性定量、宏微结合等视角对物质及其变化规律的认识水平,发展逻辑推理能力;通过列举化学事实,诊断并发展学生从学科和社会价值视角认识元素周期律(表)在生产与科学研究中的应用。
4.借助具体案例认识建构模型对推动结构理论发展的重要作用,在推断论证中认识模型的局限性,诊断和发展学生建立、改进和优化模型的水平,诊断和发展学生根据问题的复杂性匹配思维模型的水平,知道对物质结构的研究有助于发现具有预期性质的新物质,赞赏原子结构及其理论发展对化学学科新发现的推动与贡献。
二、教学内容分析
延时符
1.新人教版与旧苏教版教材内容变化比较
新增内容
1.能级
2.概率密度
3.电子云轮廓图绘制
4.原子光谱
5.元素周期系
6.元素周期表中区的划分
7.原子半径的影响因素
8.对角线规则
删除内容
1.人类对原子结构的认识(发展史)
2.洪特规则的特例
①内容增减
一、能层与能级
1
能层和能级符号
能层、能级的能量高低顺序
每个能级所能容纳的最多电子数
二、基态与激发态 原子光谱
2
三、构造原理与电子排布式
3
基态与激发态
原子光谱
二、教学内容分析
1.新人教版与旧苏教版教材内容变化比较
②内容呈现编排顺序
四、电子云与原子轨道
4
五、泡利、洪特、能量最低
5
构造原理
电子排布式(简化、价层电子排布式)
科学史话(量子化)
电子云
原子轨道
电子自旋与泡利原理
轨道表示式
洪特规则
能量最低原理
一、原子结构与元素周期表
1
元素周期律、元素周期系和元素周期表
构造原理与元素周期表(周期、族、区)
二、元素周期律
2
原子半径
电离能
电负性
二、教学内容分析
1.新人教版与旧苏教版教材内容变化比较
对角线规则
新教材从“构造原理”得出的电子排布出发,探讨元素周期表的特点
②内容呈现编排顺序
二、教学内容分析
2.基本知识框架
原子结构与性质
原子结构
元素的性质
元素周期系
元素周期表
元素周期律
原子半径
电离能
电负性
电子云和原子轨道
电子排布
运动状态
能层、能级
基态、激发态、原子光谱
构造原理
泡利原理
洪特规则
能量最低原理
核外电子排布
决 定
应用
3.课时分配
节 内容 课时建议
第一节 原子结构 一、能层与能级 二、基态与激发态 原子光谱 三、构造原理与电子排布式 四、电子云与原子轨道 五、泡利原理、洪特规则、能量最低原理 4
第二节 原子结构与元素的性质 一、原子结构与元素周期表 二、元素周期律 3
整理与提升 2
合计 9
(原子半径、电离能、电负性)
二、教学内容分析
1课时
1课时
2课时
1课时
2课时
2课时
4.考试内容
二、教学内容分析
(2012 浙江)(1)可正确表示原子轨道的是: ① 。
A.2s B.2d C.3pz D.3f
(2)写出基态镓(Ga)原子的电子排布式: ② 。
(5)用“>” “< ” “=” 填空:
第一电离能的大小:Mg ⑧ Al;
(2013 浙江)请回答下列问题:
(1)N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:
则该元素是 ① (填写元素符号)。
(2)基态锗(Ge)原子的电子排布式是 ② 。
电离能 I1 I2 I3 I4 ……
In/kJ.mol-1 578 1817 2745 11578 ……
4.考试内容
二、教学内容分析
(2014 浙江)(1)31Ga基态原子的核外电子排布式是 ① 。
某种半导体材料由Ga和As两种元素组成,该半导体材料的化学式是 ② ,
(2015 浙江)(1)Cu2+的电子排布式是 ① ;
(5)下列有关性质的比较,正确的是 ⑤ ;
A.第一电离能:O>N
4.考试内容
二、教学内容分析
(2021.6全国甲卷)(1)Si的价电子层的电子排布式为________;
(2021.6全国乙卷)(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
考试不难,但知识抽象理解难;
上课不难,但核心素养培育难。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
【文章1(王后雄)】人教版选择性必修二第一章《原子结构与性质》中的内容具有以下特点:(1)抽象内容多;(2)立体知识多;(3)概念多。本章引进了很多新颖的、抽象程度很高的概念和原理,如光谱、原子轨道等,旨在让学生在已有基础上进一步理解原子结构,认识结构与性质之间的关系,因此对学生学习和应用化学基本理论的要求比其他模块相对都要高,因此在讲解时要力求通俗易懂、深入浅出。
【文章2(郑长龙)】《物质结构与性质》模块的特点是知识深奥、理论性强、比较抽象,因此,对相当一部分学生来说难度很大,对教师来说也是一种挑战。《物质结构与性质》模块中有些知识点在知识体系中属于大学教材中的内容,十分抽象难懂,超出了一般学生的思维能力,因此,教师在教学过程中会遇到各种各样的困难与挑战。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
《学科指导意见》教学中要注意控制教学内容的深广度,避免加重学生的学习负担。
抽象
如,在已知核外电子按照能量不同可以分成不同能层(电子层),从而引出能级的概念,介绍了能级的填充顺序,但并没有详细介绍或解释能级交错现象,教学中要注意点到为止。但有时为了促进学生对原子构造原理的理解,教学中可以根据学生的实际情况适度拓展教学内容。
易懂
拓展
简单化
选择
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
【案例1.电子云】
旧苏教版
小黑点的疏密表示该区域内出现机会的大小
三、教学建议
新苏教版
小点的疏密表示该区域内出现机会的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
新鲁科版
小点的疏密程度表示单位体积内出现概率的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
新人教版
小点的疏密程度表示概率密度的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
小点的疏密表示该区域内出现机会的大小
小点的疏密程度表示单位体积内出现概率的大小
小点的疏密程度表示概率密度的大小
小点的疏密表示概率的大小
小点的疏密表示机会的大小
小点的疏密表示概率密度的大小
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
概率与概率密度?
新鲁科版教参38页
新人教版教参28页
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
电子云模型是为了说明电子在原子核外的运动状态
原子轨道
原子结构(原子核外电子排布)
共价键成键分析
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
【案例2.原子光谱】
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
电子跃迁
原子光谱
电子排布
鉴定元素
基态与激发态
发射光谱与吸收光谱
能层、能级的量子化
应用
产生
证据推理
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
【物理选修3-5】
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
原子光谱
抽象
易懂
拓展
简单化
选择
电子排布
简单化
选择
量子化与计算
电子跃迁就像上下楼梯,电子从基态到激发态就像爬楼梯,脚只能踩在台阶上,不能踩在台阶的中间;所以电子跃迁所吸收或释放的能量是量子化的,不是连续的。
三、教学建议
1.加强专业知识的学习,提高对知识的把握。
电子跃迁的能量量子化
三、教学建议
【陈光巨教授】
1.加强专业知识的学习,提高对知识的把握。
三、教学建议
要注意形象化教学,降低对抽象知识的理解难度。本章知识较为抽象,不能依据中学化学实验进行佐证,在教学中可借助实物模型、图片、视频、计算机软件模拟等多种直观手段,降低教学内容的抽象性,帮助学生思考和理解。例如,在教学中要充分发挥教科书中的电子云轮廓图、原子半径示意图等图片的功能,让教学内容通俗易懂。教学中还要深入思考如何在保证所授知识的科学性和严谨性的前提下,把深奥的原子结构理论用形象易懂的语言进行表达,以提高学生对抽象知识的接受与理解。
《学科指导意见》2.教学方法
2.借助模型、实验、视频,降低学习难度。
三、教学建议
《学科指导意见》2.教学方法
教学中要关注物质结构研究的过程、思路和方法的介绍,让学生掌握知识的同时发展核心素养。如利用原子光谱及其发展历程等化学史素材创设教学情境,帮助学生认识知识从何而来,基于哪些证据,经过怎样的逻辑推理,如何建立理论模型与完善,实现“化学史给人以智慧”的教学效果。在教学中要思考如何增强教学的探究性,如对构造原理,可按照“实验情境(原子光谱)→发现问题→科学假说→科学推论(建立科学理论)”的过程进行教学:根据氢原子光谱实验(氢原子的不连续的线状光谱),发现卢瑟福原子模型不能解释的问题,提出电子运动的量子化特征,引入“原子轨道”假设,归纳得出电子排布规律的“构造原理”。
2.借助模型、实验、视频,降低学习难度。
三、教学建议
2.借助模型、实验、视频,降低学习难度。
能层与能级
能层是楼层,能级是楼梯的阶梯。
三、教学建议
2.借助模型、实验、视频,降低学习难度。
【杭二中朱文博】
问题1:水为什么不停留在某个台阶上?
问题2:水为什么不停留在某两个台阶之间?
问题3:同一个台阶上的水面高度呈现什么特征
能量最低原理
洪特规则
量子化
问题4:与核外电子排布的规律有何相同之处?
问题5:生活中还有哪些现象与核外电子排布规律相似?
三、教学建议
2.借助模型、实验、视频,降低学习难度。
三、教学建议
【北师大附中王澜老师】
钠灯
棱镜分光镜
2.借助模型、实验、视频,降低学习难度。
三、教学建议
核外电子运动模型的发展史
核外电子模型的建构与完善
【案例3.基于证据推理与模型认知的教学设计】
证据推理
原子光谱
【内容要求】了解有关核外电子运动模型的历史发展过程,认识核外电子的运动特点。
【学业要求】能说明构建思维模型在人类认识原子结构过程中的重要作用,能论证证据与模型建立及其发展之间的关系。
?
2.借助模型、实验、视频,降低学习难度。
三、教学建议
【案例3.基于证据推理与模型认知的教学设计】
4.核外电子分层排布模型的演变
道尔顿模型
汤姆生模型
卢瑟福模型
玻尔模型
量子力学模型
1.核外电子分层排布
2.离核较远的区域运动的电子能量高
3.电子一般总是先从内层排起
2.借助模型、实验、视频,降低学习难度。
三、教学建议
【案例3.基于证据推理与模型认知的教学设计】
4.核外电子分层排布模型的演变
1.核外电子分层排布
2.离核较远的区域运动的电子能量高
3.电子一般总是先从内层排起
1.能层与能级
2.能量的量子化
3.构造原理
4.量子力学模型(电子云与原子轨道)
化学必修第一册
物质结构与性质
证据
光谱
2.借助模型、实验、视频,降低学习难度。
三、教学建议
构造原理
不同能层的能量不同
相同能层的不同能级的能量不同
电子自旋
核外电子运动模型发展史
模型建构与完善
【案例3.基于证据推理与模型认知的教学设计】
证据推理
原子光谱
E(K)
