人教版初中化学九上课件6.3二氧化碳和一氧化碳(1)(共20张PPT)
文档属性
| 名称 | 人教版初中化学九上课件6.3二氧化碳和一氧化碳(1)(共20张PPT) |
|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-12 00:00:00 | ||
图片预览





文档简介
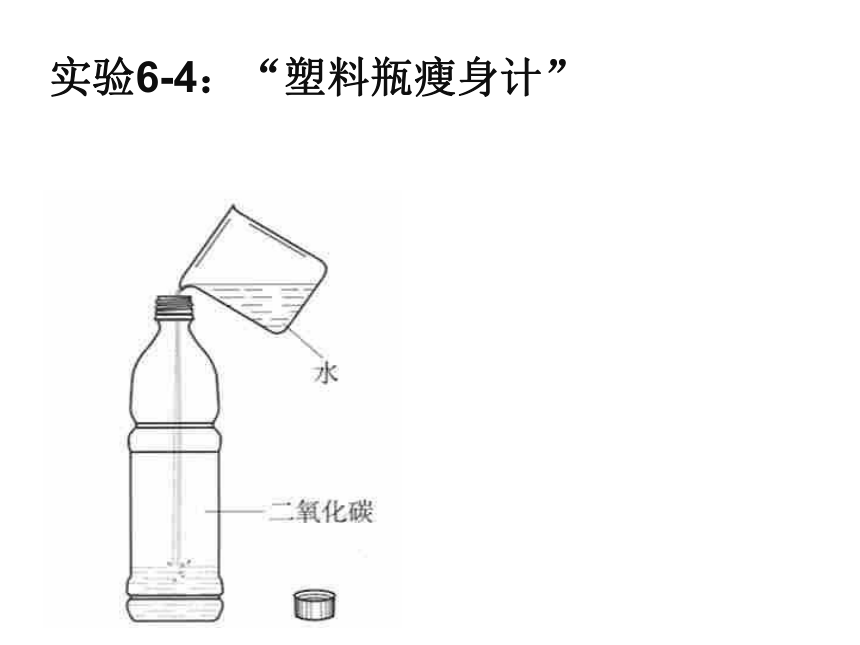
课件20张PPT。课题3二氧化碳和一氧化碳(1)CO2学习目标:1、探究并掌握二氧化碳的物理性质和化学性质
2、了解二氧化碳在生活和生产中的运用
3、了解温室效应及防范措施二氧化碳熄灭蜡烛的实验二氧化碳不能燃烧,通常
也不能支持燃烧二氧化碳的密度比空气大二氧化碳的性质
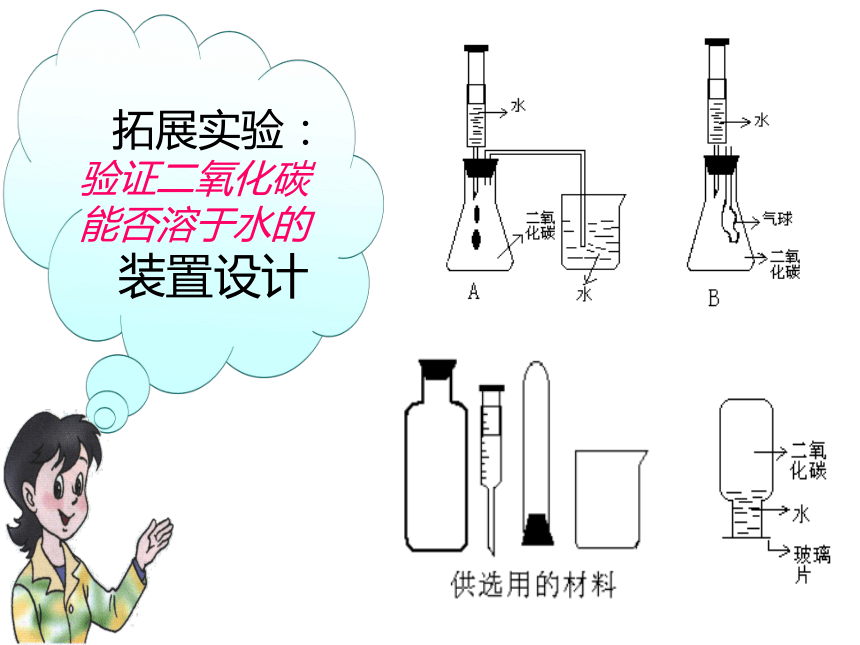
实验6-3实验6-4:“塑料瓶瘦身计” 拓展实验:
验证二氧化碳
能否溶于水的
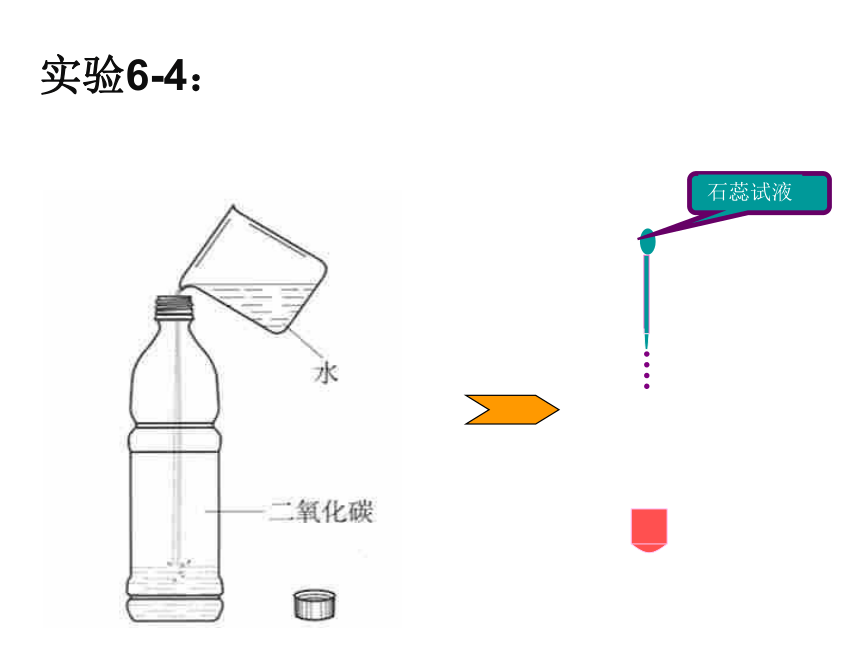
装置设计实验6-4: 活动三:
探究二氧化碳
气体是否与水
反应石蕊的自述:
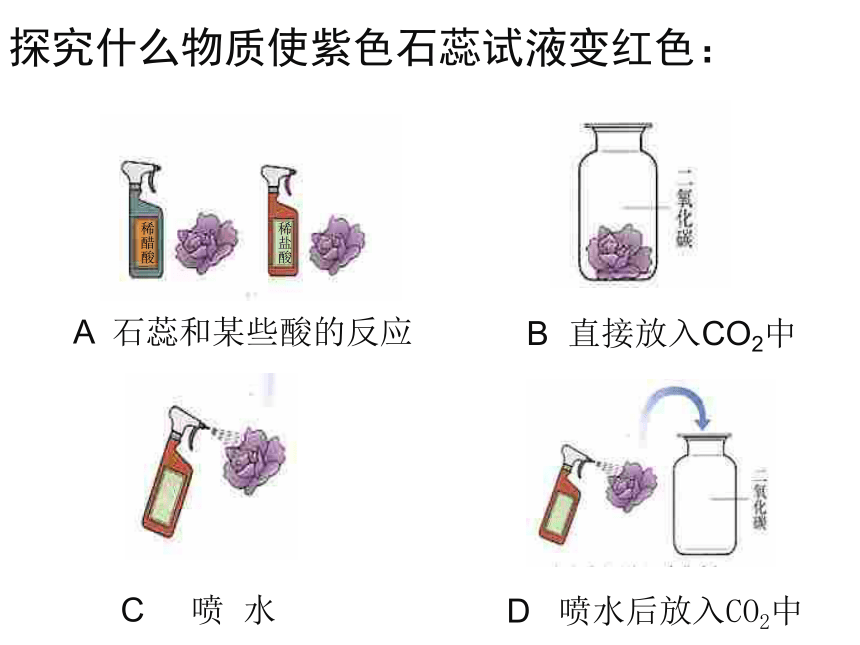
我叫石蕊,是一种色素, 能够检验溶液的酸碱性,当我遇到酸性溶液变红色,遇到碱性溶液变蓝色。A 石蕊和某些酸的反应B 直接放入CO2中C 喷 水D 喷水后放入CO2中探究什么物质使紫色石蕊试液变红色:二氧化碳与水反应原理:CO2+H2O === H2CO3H2CO3 === CO2↑ +H2O 现象:通入二氧化碳时,紫色石蕊试液变红色。 碳酸不稳定,加热易分解。当加热上述变红色的溶液,
二氧化碳气体逸出,红色又变成紫色。4、与石灰水反应:现象:澄清的石灰水变浑浊。
原理:CO2 + Ca(OH)2 = CaCO3 ↓+ H2O
碳酸钙
此反应原理是用来检验
或鉴定二氧化碳气体。无
色气
态无
味溶
于
水不能
支持
燃烧与水
反应
生成
碳酸生成
碳酸
钙和
水总 结 与 回 顾:二氧化碳的用途:1、灭火;灭火的原因是:二氧化碳既不能燃,也不支持燃,
且密度比空气大,所以,二氧化碳
能覆盖在可燃物的表面,使可燃物
隔绝氧气而熄灭。2、干冰作致冷剂;3、植物光合作用作气肥;4、工业原料.纯碱汽水尿素人工降雨灭火工业原料致冷剂气体肥料二氧化碳的用途人、动植物的呼吸,
煤等燃料的燃烧光合作用二氧化碳的循环利用二氧化碳对生活环境的影响:温 室 效 应小结:学完本课,你有什么收获?
2、了解二氧化碳在生活和生产中的运用
3、了解温室效应及防范措施二氧化碳熄灭蜡烛的实验二氧化碳不能燃烧,通常
也不能支持燃烧二氧化碳的密度比空气大二氧化碳的性质
实验6-3实验6-4:“塑料瓶瘦身计” 拓展实验:
验证二氧化碳
能否溶于水的
装置设计实验6-4: 活动三:
探究二氧化碳
气体是否与水
反应石蕊的自述:
我叫石蕊,是一种色素, 能够检验溶液的酸碱性,当我遇到酸性溶液变红色,遇到碱性溶液变蓝色。A 石蕊和某些酸的反应B 直接放入CO2中C 喷 水D 喷水后放入CO2中探究什么物质使紫色石蕊试液变红色:二氧化碳与水反应原理:CO2+H2O === H2CO3H2CO3 === CO2↑ +H2O 现象:通入二氧化碳时,紫色石蕊试液变红色。 碳酸不稳定,加热易分解。当加热上述变红色的溶液,
二氧化碳气体逸出,红色又变成紫色。4、与石灰水反应:现象:澄清的石灰水变浑浊。
原理:CO2 + Ca(OH)2 = CaCO3 ↓+ H2O
碳酸钙
此反应原理是用来检验
或鉴定二氧化碳气体。无
色气
态无
味溶
于
水不能
支持
燃烧与水
反应
生成
碳酸生成
碳酸
钙和
水总 结 与 回 顾:二氧化碳的用途:1、灭火;灭火的原因是:二氧化碳既不能燃,也不支持燃,
且密度比空气大,所以,二氧化碳
能覆盖在可燃物的表面,使可燃物
隔绝氧气而熄灭。2、干冰作致冷剂;3、植物光合作用作气肥;4、工业原料.纯碱汽水尿素人工降雨灭火工业原料致冷剂气体肥料二氧化碳的用途人、动植物的呼吸,
煤等燃料的燃烧光合作用二氧化碳的循环利用二氧化碳对生活环境的影响:温 室 效 应小结:学完本课,你有什么收获?
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
