人教版初中化学九年级:5.3利用化学方程式的简单计算 (共18张PPT)
文档属性
| 名称 | 人教版初中化学九年级:5.3利用化学方程式的简单计算 (共18张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 90.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-14 00:00:00 | ||
图片预览




文档简介
课件18张PPT。第五单元课题3利用化学方程式的简单计算学习目标1、在理解化学方程式涵义的基础上,掌
握有关反应物、生成物质量的计算。
2、通过有关化学方程式计算,掌握化学
方程式计算的书写格式,同时培养、
提高思维能力和解题能力。学习重点1、掌握已知一种反应物(或生成物)的 质量,求生成物(或反应物)的质量。
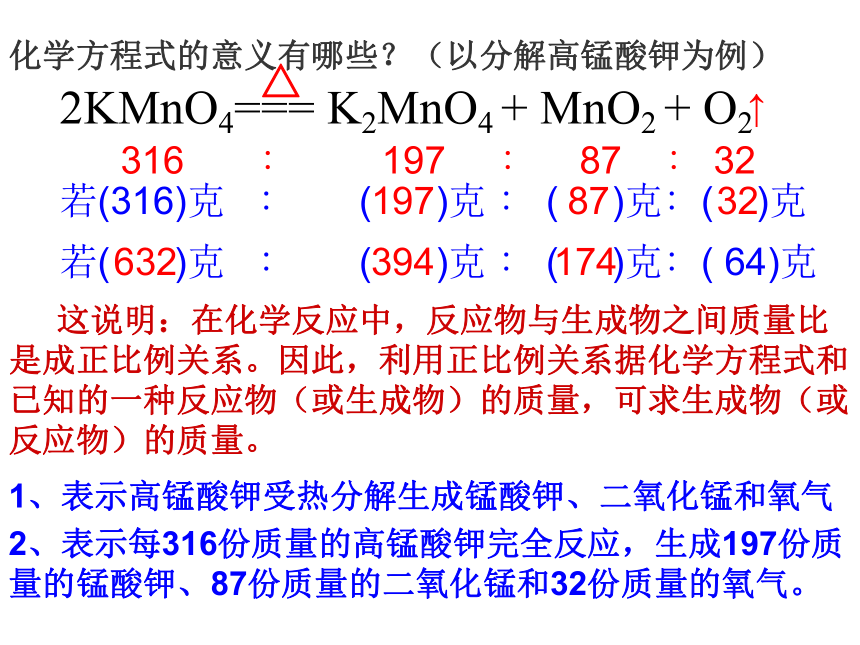
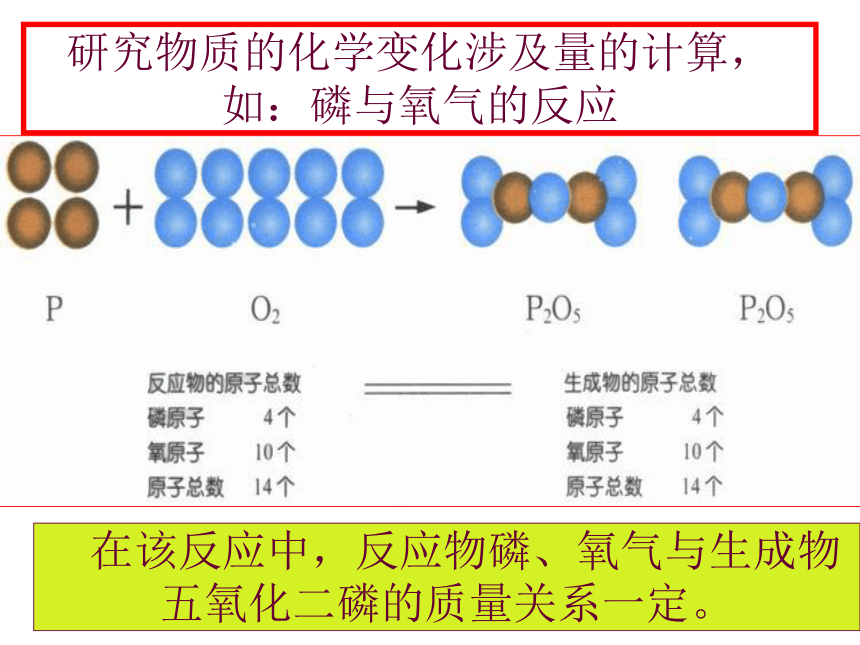
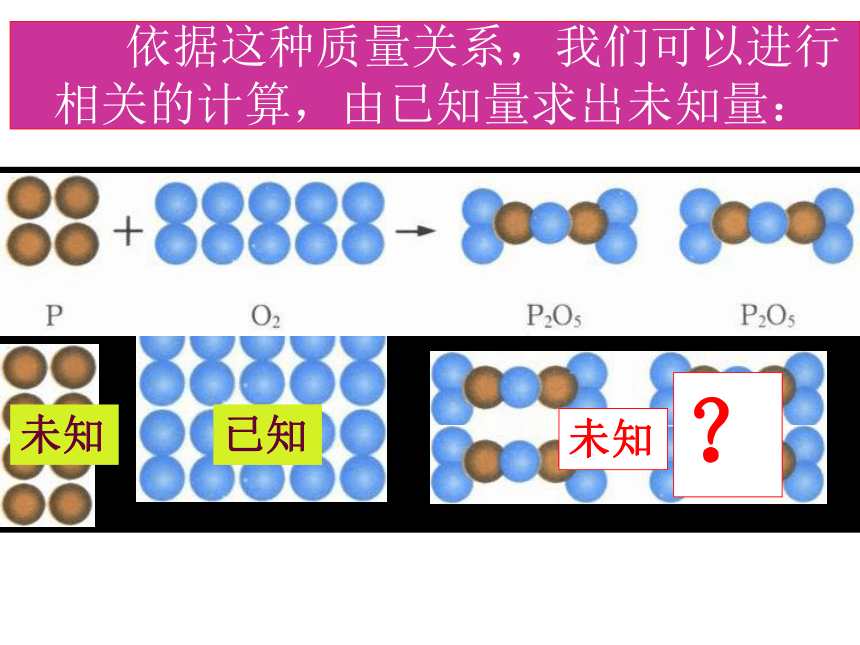
2、根据化学方程式计算的书写格式规范化。化学方程式的意义有哪些?(以分解高锰酸钾为例)1、表示高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气2、表示每316份质量的高锰酸钾完全反应,生成197份质量的锰酸钾、87份质量的二氧化锰和32份质量的氧气。316 ∶ 197 ∶ 87 ∶ 32若(316)克 ∶ ( )克 ∶ ( )克∶( )克1978732若( )克 ∶ ( )克 ∶ ( )克∶( 64)克632394174 这说明:在化学反应中,反应物与生成物之间质量比是成正比例关系。因此,利用正比例关系据化学方程式和已知的一种反应物(或生成物)的质量,可求生成物(或反应物)的质量。研究物质的化学变化涉及量的计算, 如:磷与氧气的反应 在该反应中,反应物磷、氧气与生成物五氧化二磷的质量关系一定。 依据这种质量关系,我们可以进行相关的计算,由已知量求出未知量:?已知未知未知? 在化学反应中,反应物与生成物之间的质量比是成正比例关系。因此,利用正比例关系根据化学方程式中已知的一种反应(或生成物)的质量,可出求生成物反应物)。 说明例题:3克镁在氧气中充分燃烧,可以生成多少克氧化镁?解:设可生成氧化镁的质量为X(1)设未知数 …......….设2 Mg + O 2 ==2Mg O点燃48 80
3克 X (2)写出化学方程式….方 (3) 写出有关物质的式量、
已知量和未知量 .....关48------ = ------803克X(4) 列比例式,求解.…..比X = -------- 80×3克48 = 5 克答:3克镁在氧气中充分燃烧可生成氧化镁 5 克。…….算 (5) 简明地写出答案...答根据化学方程式计算的三个要领和三个关键三个要领:
(1)步骤要完整(设、写、算、标、列、解、答)
(2)格式要规范
(3)得数要准确(保留两位小数)三个关键:
(1)准确书写化学方程式
(2)准确计算相对分子质量
(3)代入量均指纯净物的质量(单位要代入计算过程)15.5克红磷在氧气中充分燃烧,可生成五氧化二磷多少克?(找出下列所解答案中的错误)31 142
15.5 XX= 71××××未配平计算结果错误且无单位×P + O 2 P 2 O 5点燃解:设可生成X克五氧化二磷相对分子质量计算错误没有简明的写出答案×××格式不正确练习2(1) 加热分解12.25克氯酸钾,可得到多少克的氧气?同时生成氯化钾多少克?
(2) 制取4.8克氧气,需要氯酸钾多少克?(1)解:设:可得到氧气的质量为X,生成氯化钾的质量为Y2KClO3======MnO2△2KCl+3O2↑2459612.25克X245-------96=12.25克-------XX =96×5.8克--------------245= 2.3克答:解5.8克氯酸钾可得到氧气 2.3克.………...……….方……….……设}……...………….关…………… 比……………算………………………..答149
Y245 12.25克------- = ----------149 YY = ---------------
245149×12.25克= 7.45克 可生成氯化钾7.45克.(2) 解:设:需要氯酸钾的质量为X。2KClO3======MnO22KCl+3O224596△↑4.8克X245X4.8克96=--------------X = --------------4.8克×24596= 12.25克答:需要氯酸钾12.25克.讨论 课堂小节:
根据化学方程式进行计算的步骤(1)设未知数 ....…设(2)写出化学方程式 …...方(3)写出有关物质的式量、已知量和
未知量 ..............关(4)列比例式,求解 …...….….比(5) 简明地写出答案 ….…...答………………….….算简化格式:答:加热分解 6g高锰酸钾,可以得到0.6g氧气。设:加热分解 6g高锰酸钾,可以得到氧气的质量为x[解]练习3.加热分解6克高锰酸钾,可得到多少克的氧气?2.加热490g氯酸钾,则最多能生成多少氧气?3、将纯净的氯酸钾和二氧化锰的混合物6g放在试管中,加热不再产生气体 为止,剩余固体的质量 为4.04g问
(1)反应中制得了多少克氧气?
(2)原混合物中有多少克氯酸钾?
(3)加热后剩余固体中含有哪些物质各是多少克?1.96g5gKCl:3.04g MnO2:1g192g4.有一种含有水的过氧化氢样品10g,在二氧化锰的催化作用下,完全分解得到3.2g氧气,试求过氧化氢样品中过氧化氢的质量分数?5.在反应4A+3B==2C中,若2.7gA完全反应生成 5.1 g的C.已知B的相对分子质量为32,则C的相对分子质量为( )
A、34 B、68 C、102 D、204C68% 1. 含杂质15%的石灰石200克,应含有碳酸钙的质量的计算过程是________。
2. 高炉炼铁的主要反应是:
Fe2O3 +3CO 2Fe + 3CO2
计算20吨含氧化铁80%的铁矿石,可以炼出多少吨铁??
挑战题:小结: 根据化学方程式计算要求:
化学方程式要配平
需将纯量代方程
关系式对关系量
计算单位不能忘
关系量间成比例
解设比答要牢记
握有关反应物、生成物质量的计算。
2、通过有关化学方程式计算,掌握化学
方程式计算的书写格式,同时培养、
提高思维能力和解题能力。学习重点1、掌握已知一种反应物(或生成物)的 质量,求生成物(或反应物)的质量。
2、根据化学方程式计算的书写格式规范化。化学方程式的意义有哪些?(以分解高锰酸钾为例)1、表示高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气2、表示每316份质量的高锰酸钾完全反应,生成197份质量的锰酸钾、87份质量的二氧化锰和32份质量的氧气。316 ∶ 197 ∶ 87 ∶ 32若(316)克 ∶ ( )克 ∶ ( )克∶( )克1978732若( )克 ∶ ( )克 ∶ ( )克∶( 64)克632394174 这说明:在化学反应中,反应物与生成物之间质量比是成正比例关系。因此,利用正比例关系据化学方程式和已知的一种反应物(或生成物)的质量,可求生成物(或反应物)的质量。研究物质的化学变化涉及量的计算, 如:磷与氧气的反应 在该反应中,反应物磷、氧气与生成物五氧化二磷的质量关系一定。 依据这种质量关系,我们可以进行相关的计算,由已知量求出未知量:?已知未知未知? 在化学反应中,反应物与生成物之间的质量比是成正比例关系。因此,利用正比例关系根据化学方程式中已知的一种反应(或生成物)的质量,可出求生成物反应物)。 说明例题:3克镁在氧气中充分燃烧,可以生成多少克氧化镁?解:设可生成氧化镁的质量为X(1)设未知数 …......….设2 Mg + O 2 ==2Mg O点燃48 80
3克 X (2)写出化学方程式….方 (3) 写出有关物质的式量、
已知量和未知量 .....关48------ = ------803克X(4) 列比例式,求解.…..比X = -------- 80×3克48 = 5 克答:3克镁在氧气中充分燃烧可生成氧化镁 5 克。…….算 (5) 简明地写出答案...答根据化学方程式计算的三个要领和三个关键三个要领:
(1)步骤要完整(设、写、算、标、列、解、答)
(2)格式要规范
(3)得数要准确(保留两位小数)三个关键:
(1)准确书写化学方程式
(2)准确计算相对分子质量
(3)代入量均指纯净物的质量(单位要代入计算过程)15.5克红磷在氧气中充分燃烧,可生成五氧化二磷多少克?(找出下列所解答案中的错误)31 142
15.5 XX= 71××××未配平计算结果错误且无单位×P + O 2 P 2 O 5点燃解:设可生成X克五氧化二磷相对分子质量计算错误没有简明的写出答案×××格式不正确练习2(1) 加热分解12.25克氯酸钾,可得到多少克的氧气?同时生成氯化钾多少克?
(2) 制取4.8克氧气,需要氯酸钾多少克?(1)解:设:可得到氧气的质量为X,生成氯化钾的质量为Y2KClO3======MnO2△2KCl+3O2↑2459612.25克X245-------96=12.25克-------XX =96×5.8克--------------245= 2.3克答:解5.8克氯酸钾可得到氧气 2.3克.………...……….方……….……设}……...………….关…………… 比……………算………………………..答149
Y245 12.25克------- = ----------149 YY = ---------------
245149×12.25克= 7.45克 可生成氯化钾7.45克.(2) 解:设:需要氯酸钾的质量为X。2KClO3======MnO22KCl+3O224596△↑4.8克X245X4.8克96=--------------X = --------------4.8克×24596= 12.25克答:需要氯酸钾12.25克.讨论 课堂小节:
根据化学方程式进行计算的步骤(1)设未知数 ....…设(2)写出化学方程式 …...方(3)写出有关物质的式量、已知量和
未知量 ..............关(4)列比例式,求解 …...….….比(5) 简明地写出答案 ….…...答………………….….算简化格式:答:加热分解 6g高锰酸钾,可以得到0.6g氧气。设:加热分解 6g高锰酸钾,可以得到氧气的质量为x[解]练习3.加热分解6克高锰酸钾,可得到多少克的氧气?2.加热490g氯酸钾,则最多能生成多少氧气?3、将纯净的氯酸钾和二氧化锰的混合物6g放在试管中,加热不再产生气体 为止,剩余固体的质量 为4.04g问
(1)反应中制得了多少克氧气?
(2)原混合物中有多少克氯酸钾?
(3)加热后剩余固体中含有哪些物质各是多少克?1.96g5gKCl:3.04g MnO2:1g192g4.有一种含有水的过氧化氢样品10g,在二氧化锰的催化作用下,完全分解得到3.2g氧气,试求过氧化氢样品中过氧化氢的质量分数?5.在反应4A+3B==2C中,若2.7gA完全反应生成 5.1 g的C.已知B的相对分子质量为32,则C的相对分子质量为( )
A、34 B、68 C、102 D、204C68% 1. 含杂质15%的石灰石200克,应含有碳酸钙的质量的计算过程是________。
2. 高炉炼铁的主要反应是:
Fe2O3 +3CO 2Fe + 3CO2
计算20吨含氧化铁80%的铁矿石,可以炼出多少吨铁??
挑战题:小结: 根据化学方程式计算要求:
化学方程式要配平
需将纯量代方程
关系式对关系量
计算单位不能忘
关系量间成比例
解设比答要牢记
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
