人教版高中化学必修一 4.2《富集在海水中的元素---氯》课件(共55张PPT)
文档属性
| 名称 | 人教版高中化学必修一 4.2《富集在海水中的元素---氯》课件(共55张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-15 00:00:00 | ||
图片预览











文档简介
课件55张PPT。 富集在海水中的元素-氯第一课时图片欣赏浩瀚的大海 美丽的大海图片欣赏浩瀚的大海 美丽的大海图片欣赏浩瀚的大海 美丽的大海1000g海水的化学组成示意图食 盐:NaCl我们生活中的亲密朋友—氯消毒剂:NaClO Ca(ClO)2
清洁剂:HCl
问题 二 为什么氯气罐投入放大量烧碱的水中? 问题一 氯气泄漏时为什么用水枪稀释?问题一
氯气泄漏时为什么用水枪稀释?
大胆猜想是气体溶解?
还是发生化学反应?氯气与水反应探究探究一 氯气发生溶解少量发生溶解,氯水中有氯气氯气与水反应探究HCl(Cl- 、 H+)如果发生化学反应,根据元素守恒可能会产生哪些产物?探究二 氯气与水发生化学反应讨论
验证该物质的存在需要哪些试剂?1、Cl-的检验方法:
AgNO3 和稀HNO3溶液
2、H+的检验方法:
药品:Na2CO3,活泼金属
试纸:PH试纸
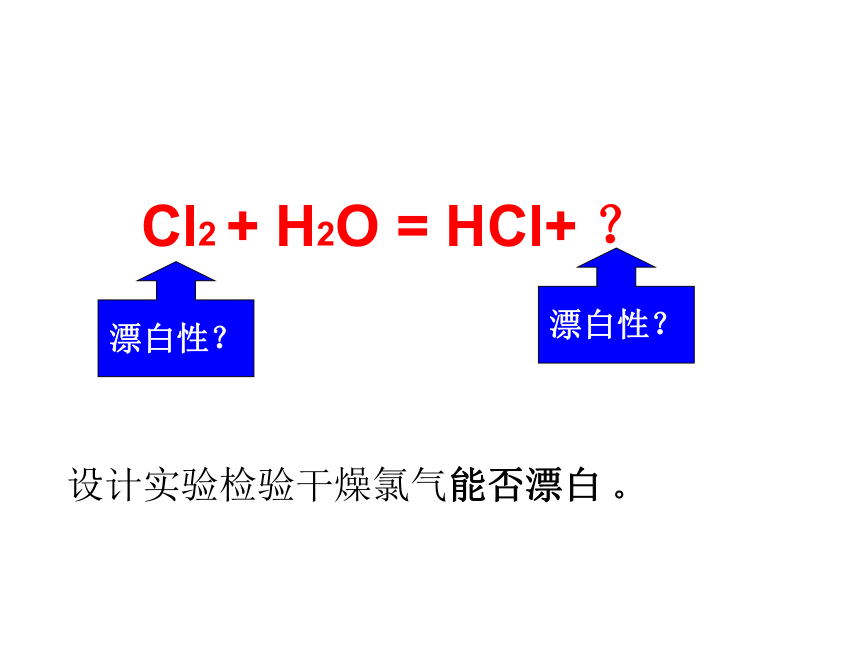
指示剂:紫色石蕊溶液验证新制氯水中的微粒Cl2 + H2O = HCl+ ?漂白性?漂白性?设计实验检验干燥氯气能否漂白 。活泼的黄绿色气体——氯气物理性质通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。Cl2 + H2O = HCl +HClO0-1+1(二)氯气(Cl2)的化学性质1、氯气与水的反应:次氯酸既是氧化剂又是还原剂(1)一元弱酸,H2CO3 >HClO(2) HClO具有强氧化性, 能杀菌消毒。能使某些染料和有机色素 褪色,可用作棉、纸张等的漂白剂。HClO的性质和用途:活泼的黄绿色气体——氯气物理性质通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。化学性质1、氯气与水反应Cl2 + H2O == HCl + HClOl氯水的保存?(3)不稳定,光照易分解次氯酸光照分解实验.练习:将新制得的氯水加入到下列溶液中,看到的现象为?起作用的微粒是什么:
1、加到石蕊溶液中 .
2、加到Na2CO3溶中 。
3、加到AgNO3溶液中 。
4、加到FeCl2溶液中 。
离子方程式为 。
5、加到KI-淀粉溶液中 。
先变红后褪色有气泡产生有白色沉淀生成溶液成浅绿色变棕黄色溶液变为蓝色2Fe2++Cl2=2Fe3++2Cl-南昌儿童游泳集体氯气中毒 中新网南昌6月6日消息:南昌发生一起儿童游泳集体氯气中毒事件,11名症状较重的儿童被立刻送往医院抢救。
原因是馆内一工作人员操作失误,在泳池内还有队员的情 况下,将净 化水质用的氯气管道 打开消毒,当即导致靠近管道附近的多名小选手出现呕吐、头晕、四肢无力等氯气中毒症状。用氯气消毒自来水有一定的负面影响。如今,人们已开始研究并试用新的自来水消毒剂,如:二氧化氯(ClO2)、臭氧(O3)、活性炭等。
来自生活中的疑问? 活泼的黄绿色气体——氯气物理性质通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。化学性质1、氯气与水反应HClO的性质:①弱酸性②漂白性②不稳定性新制氯水中的微粒:分子:H2O、Cl2、HClO离子:H+ 、Cl-、ClO-、2、氯气可与其他物质反应Cl2 + H2O == HCl + HClO人们在用自来水养鱼时,常常将
自来水在阳光下暴晒1-2天,你
知道这是为什么吗?原因:除去自来水中溶有的少
量Cl2。问题二
为什么氯气罐投放了放大量烧碱的水中?
想一想(二) 、氯气与碱溶液的反应2Ca(OH)2+2Cl2==CaCl2+Ca(ClO)2+2H2O用途:既可做漂白棉、麻、纸张的漂白剂,
又可做游泳池及环境的消毒剂用NaOH溶液吸收氯气2NaOH+Cl2= NaCl+NaClO+H2O漂白液漂白粉、漂粉精有效成分:NaClO有效成分:Ca(ClO)2疾控人员在玉树州体育场受灾群众安置点开展防疫消毒。 漂白粉的漂白(杀菌消毒)原理:酸性:H2CO3 > HClO链接生活1998年,我国长江流域和松花江流域发生了百年
不遇的特大洪灾,灾区人们饮用水必须用漂白粉
等消毒后才能饮用,但瓶装漂白粉久置空气中会
呈稀粥状而失效。试分析其原因,并写出相应的
化学方程式。Ca(ClO)2+ CO2 + H2O== + CaCO3↓2HClO
次氯酸盐比次氯酸稳定更有利于贮存和运输问题 为 什么不用次氯酸漂白而用次氯酸盐?密封放在阴暗通风干燥的地方追问 如何保存漂白粉?1、下列物质能使红墨水褪色的是
A、活性炭 B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液AD(1)与铁反应现象:剧烈燃烧,生成棕黄色的烟。2Fe + 3Cl2 == 2FeCl3点燃 Cl2化学性质:3.与金属反应1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应现象:剧烈燃烧,生成棕黄色的烟。点燃 Cl2化学性质:3.与金属反应1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(2)与铜反应Cu + Cl2 == CuCl2现象:剧烈燃烧,生成棕黄色的烟。点燃 Cl2化学性质:3.与金属反应1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应(3)与钠反应2Na + Cl2 == 2NaCl Cl2化学性质:1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应4.与非金属反应(1)与氢气反应4.与非金属反应苍白色火焰
瓶口有白雾(1)与氢气反应 Cl2化学性质:1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应4.与非金属反应(1)与氢气反应(2)与磷反应4.与非金属反应(2)与磷反应2P + 3 Cl2 == 2PCl3点燃2P + 5 Cl2 == 2PCl5点燃现象:白色烟雾思考与交流通过观察,你发现这些反应的现象有什么共同之处吗?你对燃烧的条件和本质有新的认识吗?燃烧不一定有氧气参加;
所有发光发热的剧烈的化学反应都称为燃烧;
燃烧的本质是氧化还原反应。1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应4.与非金属反应(1)与氢气反应(2)与磷反应三、氯气的用途★ 杀菌、消毒★ 重要的化工原料:制漂白粉、
农药、氯仿等二. 氯气的实验室制取:
已知:软锰矿(MnO2)与浓盐酸(HCl)反应产生黄绿色气体Cl2。你能根据已学过的氧化还原反应和相关的知识完成这个反应吗?思考、交流、探究:MnO2 + HCl(浓) = Cl2 ↑ + ?+?仪器组装顺序:自下而上、从左到右收集装置:尾气处理装置:发生装置:固、液加热向上排气法(或排饱和食盐水法)碱液(NaOH)吸收四、氯气的实验室制法***★ 根据反应原理选择反应装置净化装置:洗气瓶:饱和食盐水(HCl)、浓硫酸(H2O)能否用澄清石灰水代替NaOH?为什么?如何检验氯气已收集满?
多余氯气能否直接排放到空气中?应如何处理?MnO2浓HCl饱和食盐水(除HCl)浓硫酸
(除H2O)注意导气管的进出方式(长进短出)
为什么?氯气的检验练习:某学生设计如下实验装置用于制备纯净的氯气。 (1)装置中有六处错误,请指出。 1、烧瓶下面缺石棉网 2、铁圈下面缺酒精灯 3、原料使用了稀盐酸 4、不应使用长颈漏斗 5、盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了 6、洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞
物
理
性
质①色:黄绿色 ②味:有刺激性气味 ③态: 气体 ④密度:密度比空气大 ⑤ 易液化(液化后形成液氯)(一)氯气的物理性质用手轻轻地在瓶口扇动,
使极少量的氯气飘进鼻孔怎样闻氯气气味?溶解性:能溶于水(1:2),形成氯水⑥第二课时氯气和水混合
1、氯水呈什么颜色?水中溶解了氯气分子(Cl2) 2、为什么氯水显黄
绿色 ?提出问题——氯水的成分氯水自来水形成猜想 化学变化:与水反应
存在微粒:
Cl-、 H+Cl2、H2O实验二:氢离子的检验
将氯水加入紫色石蕊试剂中,振荡紫色石蕊试剂先变红,后褪色先变红说明氯水中含有H+后褪色说明在氯水中存在着具有漂白性的物质
物
理
性
质①色:黄绿色 ②味:有刺激性气味 ③态: 气体 ④密度:密度比空气大 ⑤ 易液化(液化后形成液氯)(一)氯气的物理性质用手轻轻地在瓶口扇动,
使极少量的氯气飘进鼻孔怎样闻氯气气味?溶解性:能溶于水(1:2),形成氯水⑥实验三:漂白性物质的探究氯气漂白性HClO (次氯酸 )不褪色布条颜
色褪去氯气和水生成的物质具有漂白性干燥氯气不起漂白作用 三、氯气的用途阅读课文P85, 联系氯气的性质归纳氯的用途阅读与思考归纳氯气的物理性质氯气是一种黄绿色、有刺激性气味、有毒、密度比空气大、易液化、能溶于水的气体。用手轻轻地在瓶口扇动,
使极少量的氯气飘进鼻孔氯气溶于水可能有Cl-可能有H+取少量氯水,滴加AgNO3溶液取少量氯水,滴加紫色石蕊溶液白色沉淀变红后褪色有Cl-生成有H+生成实验探究设计实验证明,氯水中滴加紫色石蕊溶液变红后褪色,褪色的原因是因为氯气吗,还是因为盐酸呢?
一、阅读82页,思考问题。
1、氯元素在自然界中以_________存在。
如何从微观角度解释?
2、氯气由________发现的,由__________
确认的。此反应是实验室制取氯气的主
要方法之一,药品是______________,
反应原理为
__________________________________。一、实验室制取氯气原理化合态舍勒戴维软锰矿和浓盐酸小知识: 次氯酸是一种弱酸,在水中微弱电离得到H+和ClO-。
它能使某些染料和有机色素褪色,能杀死水里的病菌而用于消毒和杀菌(用于自来水),属于永久性漂白。 小结1、经过实验探究,我们知道新制氯水的成分:H2O、 Cl2、Cl-、H+和HClO(次氯酸)、ClO-。 2、具有漂白作用的是:HClO3、写出相关的化学方程式:Cl2 + H2O = HCl + HClO(一) 、 与水反应新制氯水中有哪些分子和离子:(弱酸)H2O、Cl2、HCl、HClO新制氯水的组成Cl2+H2O=HCl+HClO从氧化还原角度分析反应。次氯酸次氯酸的性质1 次氯酸是一元弱酸,其酸性比碳酸还弱。
2 强氧化性,能杀死水里的病菌,具有杀菌消毒作用(常用于自来水杀菌消毒),能使某些染料和有机色素 褪色,可用作棉、纸张等的漂白剂。
次氯酸不稳定,且见光分解放出氧气。
对氯气泄漏事件发生后的思考如果你在事故现场,你应怎样自救。氯气有毒:逆风撤离,转移到高处,在没有防毒面具的情况下,可用湿毛巾捂住眼睛和呼吸道,顶风撤离到上风和侧风方向。活泼的黄绿色气体——氯气化学性质1、氯气与水反应HClO的性质:①弱酸性②漂白性②不稳定性新制氯水中的微粒:分子:H2O、Cl2、HClO离子:H+ 、Cl-、ClO-、2、氯气可与碱反应Cl2 + H2O == HCl + HClO2NaOH+Cl2==NaCl+
NaClO+H2O2Ca(OH)2+2Cl2==CaCl2
+Ca(ClO)2+2H2OCa(ClO)2 + CO2 + H2O==
CaCO3↓ + 2HClO漂白原理问题探究消防员用水处理泄漏空气中的氯气,氯气是否与水发生了反应? 从氯原子的结构预测氯气还能与
哪些物质反应? 设计验证氯气氧化性
的实验方法.课后探究
清洁剂:HCl
问题 二 为什么氯气罐投入放大量烧碱的水中? 问题一 氯气泄漏时为什么用水枪稀释?问题一
氯气泄漏时为什么用水枪稀释?
大胆猜想是气体溶解?
还是发生化学反应?氯气与水反应探究探究一 氯气发生溶解少量发生溶解,氯水中有氯气氯气与水反应探究HCl(Cl- 、 H+)如果发生化学反应,根据元素守恒可能会产生哪些产物?探究二 氯气与水发生化学反应讨论
验证该物质的存在需要哪些试剂?1、Cl-的检验方法:
AgNO3 和稀HNO3溶液
2、H+的检验方法:
药品:Na2CO3,活泼金属
试纸:PH试纸
指示剂:紫色石蕊溶液验证新制氯水中的微粒Cl2 + H2O = HCl+ ?漂白性?漂白性?设计实验检验干燥氯气能否漂白 。活泼的黄绿色气体——氯气物理性质通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。Cl2 + H2O = HCl +HClO0-1+1(二)氯气(Cl2)的化学性质1、氯气与水的反应:次氯酸既是氧化剂又是还原剂(1)一元弱酸,H2CO3 >HClO(2) HClO具有强氧化性, 能杀菌消毒。能使某些染料和有机色素 褪色,可用作棉、纸张等的漂白剂。HClO的性质和用途:活泼的黄绿色气体——氯气物理性质通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。化学性质1、氯气与水反应Cl2 + H2O == HCl + HClOl氯水的保存?(3)不稳定,光照易分解次氯酸光照分解实验.练习:将新制得的氯水加入到下列溶液中,看到的现象为?起作用的微粒是什么:
1、加到石蕊溶液中 .
2、加到Na2CO3溶中 。
3、加到AgNO3溶液中 。
4、加到FeCl2溶液中 。
离子方程式为 。
5、加到KI-淀粉溶液中 。
先变红后褪色有气泡产生有白色沉淀生成溶液成浅绿色变棕黄色溶液变为蓝色2Fe2++Cl2=2Fe3++2Cl-南昌儿童游泳集体氯气中毒 中新网南昌6月6日消息:南昌发生一起儿童游泳集体氯气中毒事件,11名症状较重的儿童被立刻送往医院抢救。
原因是馆内一工作人员操作失误,在泳池内还有队员的情 况下,将净 化水质用的氯气管道 打开消毒,当即导致靠近管道附近的多名小选手出现呕吐、头晕、四肢无力等氯气中毒症状。用氯气消毒自来水有一定的负面影响。如今,人们已开始研究并试用新的自来水消毒剂,如:二氧化氯(ClO2)、臭氧(O3)、活性炭等。
来自生活中的疑问? 活泼的黄绿色气体——氯气物理性质通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。化学性质1、氯气与水反应HClO的性质:①弱酸性②漂白性②不稳定性新制氯水中的微粒:分子:H2O、Cl2、HClO离子:H+ 、Cl-、ClO-、2、氯气可与其他物质反应Cl2 + H2O == HCl + HClO人们在用自来水养鱼时,常常将
自来水在阳光下暴晒1-2天,你
知道这是为什么吗?原因:除去自来水中溶有的少
量Cl2。问题二
为什么氯气罐投放了放大量烧碱的水中?
想一想(二) 、氯气与碱溶液的反应2Ca(OH)2+2Cl2==CaCl2+Ca(ClO)2+2H2O用途:既可做漂白棉、麻、纸张的漂白剂,
又可做游泳池及环境的消毒剂用NaOH溶液吸收氯气2NaOH+Cl2= NaCl+NaClO+H2O漂白液漂白粉、漂粉精有效成分:NaClO有效成分:Ca(ClO)2疾控人员在玉树州体育场受灾群众安置点开展防疫消毒。 漂白粉的漂白(杀菌消毒)原理:酸性:H2CO3 > HClO链接生活1998年,我国长江流域和松花江流域发生了百年
不遇的特大洪灾,灾区人们饮用水必须用漂白粉
等消毒后才能饮用,但瓶装漂白粉久置空气中会
呈稀粥状而失效。试分析其原因,并写出相应的
化学方程式。Ca(ClO)2+ CO2 + H2O== + CaCO3↓2HClO
次氯酸盐比次氯酸稳定更有利于贮存和运输问题 为 什么不用次氯酸漂白而用次氯酸盐?密封放在阴暗通风干燥的地方追问 如何保存漂白粉?1、下列物质能使红墨水褪色的是
A、活性炭 B、二氧化碳
C、NaCl溶液 D、酸化的NaClO溶液AD(1)与铁反应现象:剧烈燃烧,生成棕黄色的烟。2Fe + 3Cl2 == 2FeCl3点燃 Cl2化学性质:3.与金属反应1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应现象:剧烈燃烧,生成棕黄色的烟。点燃 Cl2化学性质:3.与金属反应1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(2)与铜反应Cu + Cl2 == CuCl2现象:剧烈燃烧,生成棕黄色的烟。点燃 Cl2化学性质:3.与金属反应1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应(3)与钠反应2Na + Cl2 == 2NaCl Cl2化学性质:1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应4.与非金属反应(1)与氢气反应4.与非金属反应苍白色火焰
瓶口有白雾(1)与氢气反应 Cl2化学性质:1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应4.与非金属反应(1)与氢气反应(2)与磷反应4.与非金属反应(2)与磷反应2P + 3 Cl2 == 2PCl3点燃2P + 5 Cl2 == 2PCl5点燃现象:白色烟雾思考与交流通过观察,你发现这些反应的现象有什么共同之处吗?你对燃烧的条件和本质有新的认识吗?燃烧不一定有氧气参加;
所有发光发热的剧烈的化学反应都称为燃烧;
燃烧的本质是氧化还原反应。1、氯气与水反应Cl2 + H2O == HCl + HClO化学性质2.与碱的反应2NaOH+Cl2= NaCl+NaClO+H2O3.与金属反应(1)与铁反应(2)与铜反应(3)与钠反应4.与非金属反应(1)与氢气反应(2)与磷反应三、氯气的用途★ 杀菌、消毒★ 重要的化工原料:制漂白粉、
农药、氯仿等二. 氯气的实验室制取:
已知:软锰矿(MnO2)与浓盐酸(HCl)反应产生黄绿色气体Cl2。你能根据已学过的氧化还原反应和相关的知识完成这个反应吗?思考、交流、探究:MnO2 + HCl(浓) = Cl2 ↑ + ?+?仪器组装顺序:自下而上、从左到右收集装置:尾气处理装置:发生装置:固、液加热向上排气法(或排饱和食盐水法)碱液(NaOH)吸收四、氯气的实验室制法***★ 根据反应原理选择反应装置净化装置:洗气瓶:饱和食盐水(HCl)、浓硫酸(H2O)能否用澄清石灰水代替NaOH?为什么?如何检验氯气已收集满?
多余氯气能否直接排放到空气中?应如何处理?MnO2浓HCl饱和食盐水(除HCl)浓硫酸
(除H2O)注意导气管的进出方式(长进短出)
为什么?氯气的检验练习:某学生设计如下实验装置用于制备纯净的氯气。 (1)装置中有六处错误,请指出。 1、烧瓶下面缺石棉网 2、铁圈下面缺酒精灯 3、原料使用了稀盐酸 4、不应使用长颈漏斗 5、盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了 6、洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞
物
理
性
质①色:黄绿色 ②味:有刺激性气味 ③态: 气体 ④密度:密度比空气大 ⑤ 易液化(液化后形成液氯)(一)氯气的物理性质用手轻轻地在瓶口扇动,
使极少量的氯气飘进鼻孔怎样闻氯气气味?溶解性:能溶于水(1:2),形成氯水⑥第二课时氯气和水混合
1、氯水呈什么颜色?水中溶解了氯气分子(Cl2) 2、为什么氯水显黄
绿色 ?提出问题——氯水的成分氯水自来水形成猜想 化学变化:与水反应
存在微粒:
Cl-、 H+Cl2、H2O实验二:氢离子的检验
将氯水加入紫色石蕊试剂中,振荡紫色石蕊试剂先变红,后褪色先变红说明氯水中含有H+后褪色说明在氯水中存在着具有漂白性的物质
物
理
性
质①色:黄绿色 ②味:有刺激性气味 ③态: 气体 ④密度:密度比空气大 ⑤ 易液化(液化后形成液氯)(一)氯气的物理性质用手轻轻地在瓶口扇动,
使极少量的氯气飘进鼻孔怎样闻氯气气味?溶解性:能溶于水(1:2),形成氯水⑥实验三:漂白性物质的探究氯气漂白性HClO (次氯酸 )不褪色布条颜
色褪去氯气和水生成的物质具有漂白性干燥氯气不起漂白作用 三、氯气的用途阅读课文P85, 联系氯气的性质归纳氯的用途阅读与思考归纳氯气的物理性质氯气是一种黄绿色、有刺激性气味、有毒、密度比空气大、易液化、能溶于水的气体。用手轻轻地在瓶口扇动,
使极少量的氯气飘进鼻孔氯气溶于水可能有Cl-可能有H+取少量氯水,滴加AgNO3溶液取少量氯水,滴加紫色石蕊溶液白色沉淀变红后褪色有Cl-生成有H+生成实验探究设计实验证明,氯水中滴加紫色石蕊溶液变红后褪色,褪色的原因是因为氯气吗,还是因为盐酸呢?
一、阅读82页,思考问题。
1、氯元素在自然界中以_________存在。
如何从微观角度解释?
2、氯气由________发现的,由__________
确认的。此反应是实验室制取氯气的主
要方法之一,药品是______________,
反应原理为
__________________________________。一、实验室制取氯气原理化合态舍勒戴维软锰矿和浓盐酸小知识: 次氯酸是一种弱酸,在水中微弱电离得到H+和ClO-。
它能使某些染料和有机色素褪色,能杀死水里的病菌而用于消毒和杀菌(用于自来水),属于永久性漂白。 小结1、经过实验探究,我们知道新制氯水的成分:H2O、 Cl2、Cl-、H+和HClO(次氯酸)、ClO-。 2、具有漂白作用的是:HClO3、写出相关的化学方程式:Cl2 + H2O = HCl + HClO(一) 、 与水反应新制氯水中有哪些分子和离子:(弱酸)H2O、Cl2、HCl、HClO新制氯水的组成Cl2+H2O=HCl+HClO从氧化还原角度分析反应。次氯酸次氯酸的性质1 次氯酸是一元弱酸,其酸性比碳酸还弱。
2 强氧化性,能杀死水里的病菌,具有杀菌消毒作用(常用于自来水杀菌消毒),能使某些染料和有机色素 褪色,可用作棉、纸张等的漂白剂。
次氯酸不稳定,且见光分解放出氧气。
对氯气泄漏事件发生后的思考如果你在事故现场,你应怎样自救。氯气有毒:逆风撤离,转移到高处,在没有防毒面具的情况下,可用湿毛巾捂住眼睛和呼吸道,顶风撤离到上风和侧风方向。活泼的黄绿色气体——氯气化学性质1、氯气与水反应HClO的性质:①弱酸性②漂白性②不稳定性新制氯水中的微粒:分子:H2O、Cl2、HClO离子:H+ 、Cl-、ClO-、2、氯气可与碱反应Cl2 + H2O == HCl + HClO2NaOH+Cl2==NaCl+
NaClO+H2O2Ca(OH)2+2Cl2==CaCl2
+Ca(ClO)2+2H2OCa(ClO)2 + CO2 + H2O==
CaCO3↓ + 2HClO漂白原理问题探究消防员用水处理泄漏空气中的氯气,氯气是否与水发生了反应? 从氯原子的结构预测氯气还能与
哪些物质反应? 设计验证氯气氧化性
的实验方法.课后探究
