人教版高中化学必修一4.4 《氨 硝酸 硫酸》课件(共40张PPT)
文档属性
| 名称 | 人教版高中化学必修一4.4 《氨 硝酸 硫酸》课件(共40张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 870.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-15 00:00:00 | ||
图片预览






文档简介
课件40张PPT。第四章 非金属及其化合物第四节
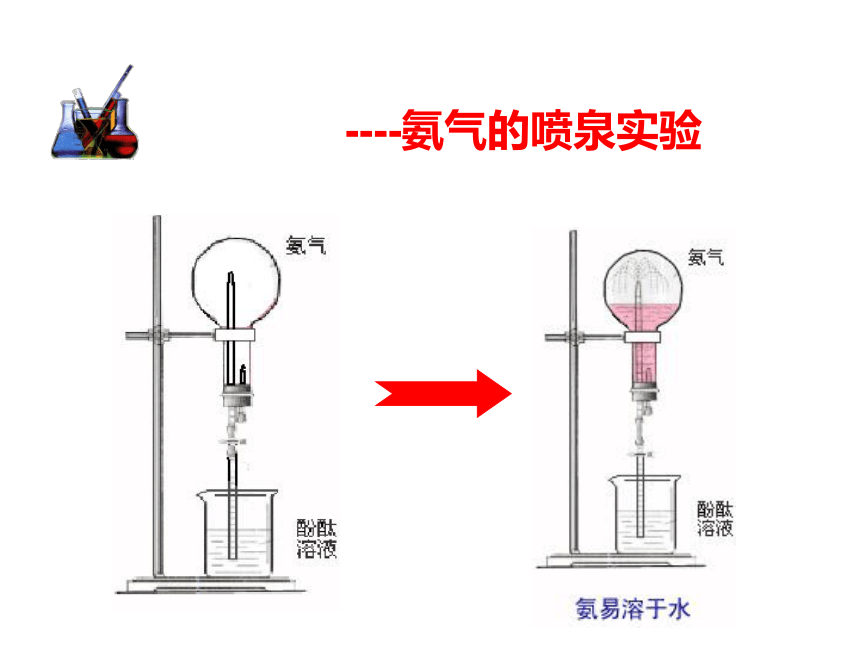
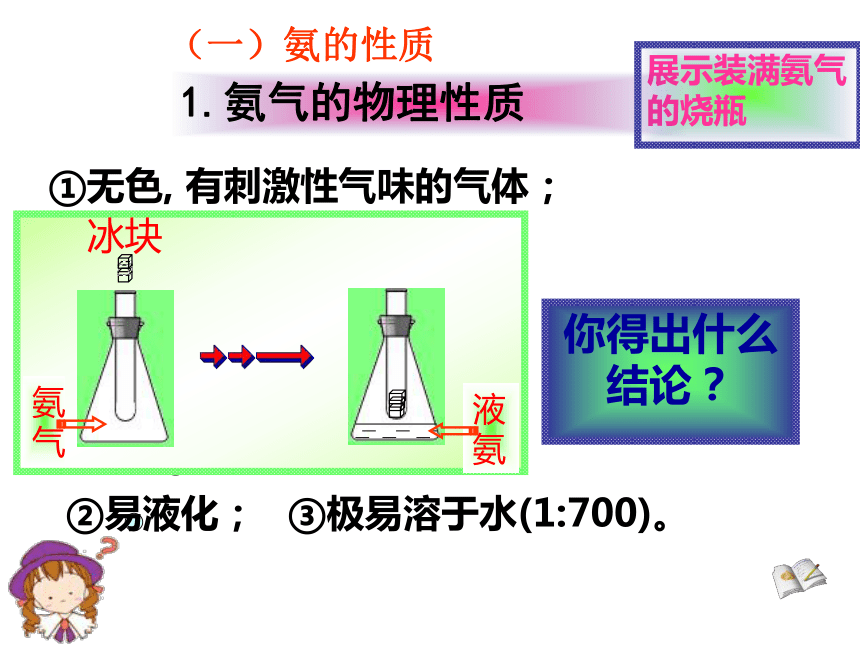
《氨 硝酸 硫酸》 ----氨气的喷泉实验展示装满氨气的烧瓶①无色, 有刺激性气味的气体;你得出什么结论?②易液化;冰块氨气液氨1.氨气的物理性质③极易溶于水(1:700)。(一)氨的性质2、氨的化学性质(1)氨跟水反应——显弱碱性①NH3极易溶于水。(1 :700),
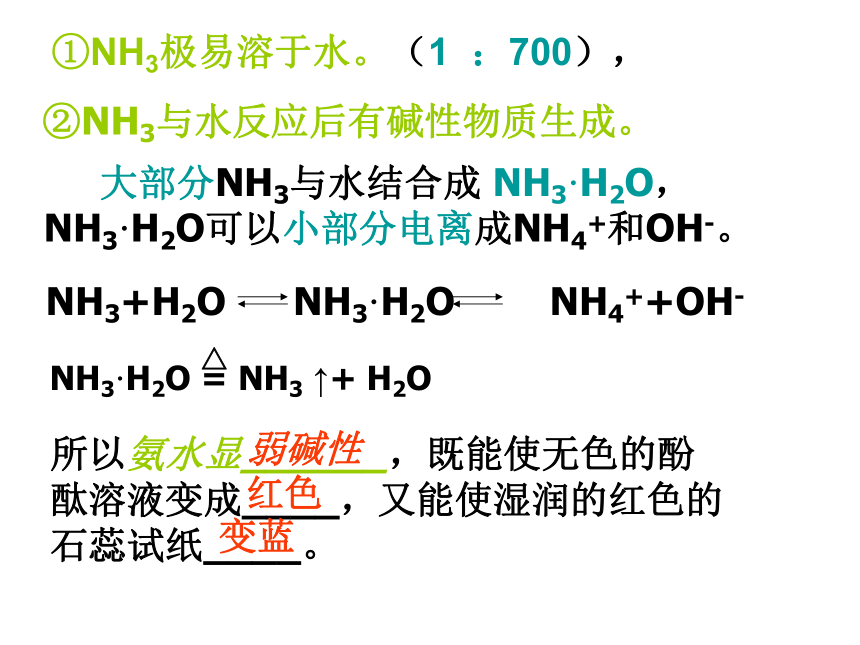
所以氨水显______,既能使无色的酚酞溶液变成____,又能使湿润的红色的石蕊试纸____。
②NH3与水反应后有碱性物质生成。 大部分NH3与水结合成 NH3·H2O,
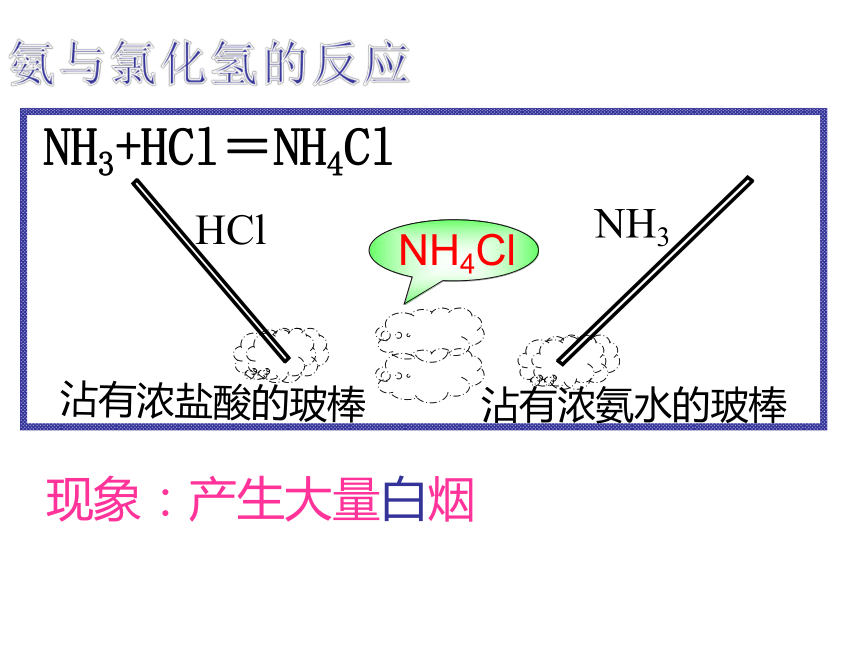
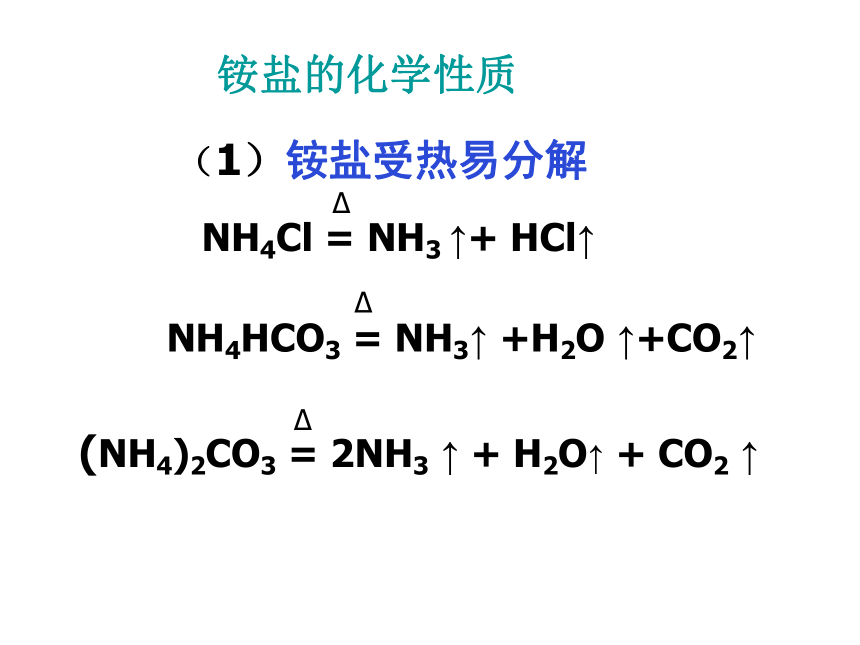
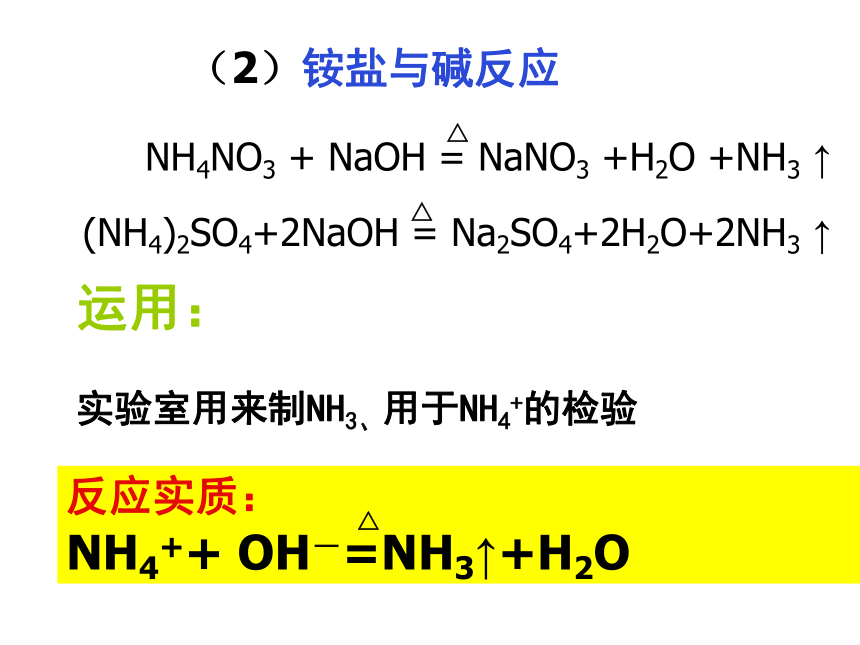
NH3·H2O可以小部分电离成NH4+和OH-。红色变蓝弱碱性(2)氨跟酸的反应 写出上述反应的离子方程式氨与氯化氢的反应沾有浓盐酸的玻棒沾有浓氨水的玻棒HClNH3现象:产生大量白烟NH3+HCl=NH4Cl不能 1.在反应中为什么会产生白烟? 挥发出的氨气和氯化氢气体在空中反应生成氯化铵固体小颗粒。 2.硫酸或磷酸与氨气反应能否产生白烟? 铵盐物理性质:铵盐都是晶体铵盐都易溶于水铵盐的形成:NH3 + H+=NH4+铵盐都不稳定,受热易分解铵盐的化学性质(1)铵盐受热易分解(2)铵盐与碱反应NH4NO3 + NaOH = NaNO3 +H2O +NH3 ↑(NH4)2SO4+2NaOH = Na2SO4+2H2O+2NH3 ↑运用:
实验室用来制NH3、用于NH4+的检验反应实质:
NH4++ OH-=NH3↑+H2O△△△铵盐的用途大量的铵盐用于生产氮肥硝酸铵用于制炸药、氯化铵常用作
印染和制干电池的原料,也可以用于
金属的焊接,以除去金属表面的氧化物薄膜。氮 肥氯化铵的妙用——防火布 将一块普通的棉布浸在氯化铵的饱和溶液中,片刻之后,取出晾干就成防火布了。将这块经过化学处理的布用火柴点,不但点不着,而且还冒出白色的烟雾。 科学视野 原来,经过这种化学处理的棉布(防火布)的表面附满了氯化铵的晶体颗粒,氯化铵这种物质,它有个怪脾气,就是特别怕热,一遇热就会发生化学变化,分解出两种不能燃烧的气体,一种是氨气,另一种是氯化氢气体。 这两种气体把棉布与空气隔绝起来,棉布在没有氧气的条件下当然就不能燃烧了。当这两种气体保护棉布不被火烧的同时,它们又在空气中相遇,重新化合而成氯化铵小晶体,这些小晶体分布在空气中,就象白烟一样。实际上,氯化铵这种化学物质是很好的防火能手,戏院里的舞台布景、舰艇上的木料等,都经常用氯化铵处理,以求达到防火的目的。(二)NH3的实验室制法原理:加热铵盐与碱的固体混合物
如:将固体NH4Cl与Ca(OH)2混合加热,即得到NH3讨论:
NH3如何收集?
如何检验NH3已经收满?剩余的NH3如何处理?
若要制备干燥的NH3 ,可用什么作干燥剂?
NH3的实验室制法(1)原料:NH4Cl Ca(OH)2 (2)原理:
2NH4Cl+Ca(OH)2==2NH3↑+2H2O+CaCl2
(3)制取装置:
固固加热装置棉花的作用:防止空气对流△(4)收集装置: 向下排空气法
(5)检验: a:使湿润的酚酞试纸变红
b:遇浓盐酸产生大量的白烟
(6)尾气处理:用水吸收NH3要得到干燥的氨气,常用试剂有哪些?
①CaO、碱石灰等碱性干燥剂
②无水CaCl2不能用来干燥NH3(形成CaCl2.8NH3)除了利用上述方法之外,实验室有无其他简单可行的方法来制得氨气?浓氨水方法二:加热浓氨水制氨气←浓氨水←固体CaO思考:有什么现象?为什么有此现象?方法三1、吸收水分,减少溶剂。
2、增加OH-的浓度。
3、放出热量,升高温度。使指示剂变色:与碱发生中和反应:与碱性氧化物反应:与盐反应:稀硫酸与硝酸使紫色石蕊试液变红H+ + OH - = H2O2 H+ + CuO = Cu2+ + H2O 2 H+ + CO3 2- = H2O + CO2与活泼金属反应二、硫酸和硝酸的氧化性思考与交流 1、硫酸、硝酸、盐酸都是酸,它们在组成上用什么特点? 它们都是酸,在水溶液中电离出H+,硫酸、硝酸是含氧酸,盐酸是无氧酸;硫酸是二元酸,硝酸和盐酸是一元酸2、这些特点与酸的通性有什么关系?用电离方程式表示。 在水溶液中都电离出氢离子HA=H++A—1、 硫酸的性质【思考】稀硫酸和浓硫酸的性质有何不同?
浓H2SO4的物理性质
A.色态:无色、粘稠的油状液体
B.沸点:约338℃——难挥发酸(高沸点酸)
C.密度:1.84g/cm3——高密度酸
D.溶解性:跟水任意比互溶,溶解放出大量热。
两高:沸点、密度高
两大:溶解度、溶解放热量大你对浓硫酸知多少?(1)浓硫酸在稀释时应注意什么问题?应将浓硫酸沿烧杯壁向水中慢慢注入,并用玻璃棒不断搅拌。(2)实验室制HCl气体是用以下反应制备,你能说明反应进行的理由吗?注:高沸点酸制低沸点酸,难挥发性酸制易挥发性酸
浓硫酸的特性:1) 吸水性:能吸收水份可干燥与它不反应的气体思考:1.能用浓硫酸干燥H2S、NH3气体吗?2.将硫酸铜晶体投入浓硫酸中,有何现象?2)、脱水性浓硫酸与木屑、棉花、纸屑反应浓硫酸与蔗糖反应浓硫酸能按水的组成比脱去有机物中的氢和氧元素a.浓硫酸沾到衣服上应如何处理?
b.浓硫酸沾到皮肤上应如何处理?浓硫酸的吸水性与脱水性有何区别?实验:将浓硫酸慢慢加入蔗糖中,并用玻
璃棒搅拌
现象: 蔗糖变黑,体积膨胀,变成疏松多孔的海绵状,并放出有刺激性气味的气体原因:C12H22O11 浓硫酸能将蔗糖中的H和O按原子个数比2:1脱去形成水,使蔗糖生成炭问题探究1、写出蔗糖遇浓硫酸发生的化学方程式: C12H22O11 =12C+11H2O2、蔗糖分子中含有水,浓硫酸将水吸去使它生成炭而变黑,这种说法对吗?试分析。不对,因为蔗糖分子中没有水练习并讨论:3)与铜反应:强氧化性分析上述反应中电子转移的方向和数目,指出氧化剂和还原剂,并分析浓硫酸在上述反应中体现的性质。失去2e-得到2e-氧化剂:H2SO4 还原剂:Cu 加热时,浓硫酸能与大多数金属反应(Au、Pt除外) ,一般没有氢气生成,通常生成SO2气体。铜与浓硫酸的反应
现象:有气体产生,此气体使品红溶液褪色或紫色的石蕊试液变红反应后溶液倒入少量的水中,溶液呈蓝色反应原理:Cu+2H2SO4 (浓)== CuSO4+SO2↑+2H2O△浓硫酸与碳的反应:C+2H2SO(浓)== CO2↑+2SO2 ↑+2H2O△4)与非金属反应思考并讨论:请设计实验方案,验证碳和浓硫酸反应的产物加热时,浓硫酸也能与某些非金属反应(S、C等)仪器连接如下说明:应首先用无水硫酸铜验证水,然后用品红验证二氧化硫,再用高锰酸钾氧化多余的二氧化硫,接着再次验证二氧化硫是否全部被氧化,最后才验证二氧化碳。验证碳和浓硫酸反应的产物如何检验浓硫酸与碳反应生成的各种产物? 无水硫酸铜、品红、酸性高锰酸钾或溴水、品红、澄清的石灰水注意:硫酸分子中的硫元素的化合价为
价,处于硫元素所有化合价中的 价态,在氧化还原反应中化合价只能 ,表现 ,浓硫酸被还原一般得到的产物为 。+6最高降低氧化性SO2 常温下,浓硫酸可用铁槽车或铝槽车运输,这是因为常温下,浓硫酸可使铁或铝的表面生成一层致密的氧化膜,阻止了内部金属与浓硫酸进一步反应,这种现象叫做——钝化。硫酸车槽 【思考】浓硫酸具有强氧化性,稀硫酸是否有氧化性?如果有,其氧化性与浓硫酸的氧化性有何不同?
浓硫酸与稀硫酸比较:
稀H2SO4:由H+和SO42-构成——弱氧化性(由H+体现)——可与活泼金属反应生成H2
浓H2SO4:由H2SO4分子构成——强氧化性(由 S 体现)— 加热时可与大多数金属和某些非金属反应,通常生成SO22.硫酸的用途: 三、硝酸的性质:1.物理性质:无色,易挥发、有刺激性气味的液体,能以任意比溶于水,含HNO3 98%的硝酸—发烟硝酸
2.化学性质:(1)酸性(2)氧化性① 与金属反应(除Au和 Pt外)Cu + 4HNO3(浓) = Cu(NO3)2 + 2NO2 +2H2O3Cu + 8HNO3(稀) = 3 Cu(NO3)2 + 2NO +4H2O注意:Fe 和Al遇到冷的浓硝酸被钝化,被氧化成一层致密的氧化膜,与浓硫酸一样。氧化性:浓硝酸>稀硝酸(3)不稳定性②与非金属反应 C +4HNO3 (浓)=2H2O +4NO2 +CO2结论:硝酸跟非金属反应,生成NO2、 H2O和相应的含氧酸③硝酸还能氧化FeO、 Fe(NO3)2(Fe2+)、 HBr(Br-)、 HI(I-) 、H2S (S2-)、 SO2等具有还原性的化合物发生氧化还原反应,因此,不能用硝酸与有关的盐反应制取HI、 SO2、 H2S、 HBr等气体小结:硝酸与金属反应时,主要是HNO3中+5价的氮得到电子,被还原成较低价氮的物质,稀硝酸的还原产物一般是NO,浓硝酸的还原产物一般是NO2,而不像盐酸与金属反应那样生成H2。3、硝酸的用途:制化肥、农药、炸药、染料、盐等
《氨 硝酸 硫酸》 ----氨气的喷泉实验展示装满氨气的烧瓶①无色, 有刺激性气味的气体;你得出什么结论?②易液化;冰块氨气液氨1.氨气的物理性质③极易溶于水(1:700)。(一)氨的性质2、氨的化学性质(1)氨跟水反应——显弱碱性①NH3极易溶于水。(1 :700),
所以氨水显______,既能使无色的酚酞溶液变成____,又能使湿润的红色的石蕊试纸____。
②NH3与水反应后有碱性物质生成。 大部分NH3与水结合成 NH3·H2O,
NH3·H2O可以小部分电离成NH4+和OH-。红色变蓝弱碱性(2)氨跟酸的反应 写出上述反应的离子方程式氨与氯化氢的反应沾有浓盐酸的玻棒沾有浓氨水的玻棒HClNH3现象:产生大量白烟NH3+HCl=NH4Cl不能 1.在反应中为什么会产生白烟? 挥发出的氨气和氯化氢气体在空中反应生成氯化铵固体小颗粒。 2.硫酸或磷酸与氨气反应能否产生白烟? 铵盐物理性质:铵盐都是晶体铵盐都易溶于水铵盐的形成:NH3 + H+=NH4+铵盐都不稳定,受热易分解铵盐的化学性质(1)铵盐受热易分解(2)铵盐与碱反应NH4NO3 + NaOH = NaNO3 +H2O +NH3 ↑(NH4)2SO4+2NaOH = Na2SO4+2H2O+2NH3 ↑运用:
实验室用来制NH3、用于NH4+的检验反应实质:
NH4++ OH-=NH3↑+H2O△△△铵盐的用途大量的铵盐用于生产氮肥硝酸铵用于制炸药、氯化铵常用作
印染和制干电池的原料,也可以用于
金属的焊接,以除去金属表面的氧化物薄膜。氮 肥氯化铵的妙用——防火布 将一块普通的棉布浸在氯化铵的饱和溶液中,片刻之后,取出晾干就成防火布了。将这块经过化学处理的布用火柴点,不但点不着,而且还冒出白色的烟雾。 科学视野 原来,经过这种化学处理的棉布(防火布)的表面附满了氯化铵的晶体颗粒,氯化铵这种物质,它有个怪脾气,就是特别怕热,一遇热就会发生化学变化,分解出两种不能燃烧的气体,一种是氨气,另一种是氯化氢气体。 这两种气体把棉布与空气隔绝起来,棉布在没有氧气的条件下当然就不能燃烧了。当这两种气体保护棉布不被火烧的同时,它们又在空气中相遇,重新化合而成氯化铵小晶体,这些小晶体分布在空气中,就象白烟一样。实际上,氯化铵这种化学物质是很好的防火能手,戏院里的舞台布景、舰艇上的木料等,都经常用氯化铵处理,以求达到防火的目的。(二)NH3的实验室制法原理:加热铵盐与碱的固体混合物
如:将固体NH4Cl与Ca(OH)2混合加热,即得到NH3讨论:
NH3如何收集?
如何检验NH3已经收满?剩余的NH3如何处理?
若要制备干燥的NH3 ,可用什么作干燥剂?
NH3的实验室制法(1)原料:NH4Cl Ca(OH)2 (2)原理:
2NH4Cl+Ca(OH)2==2NH3↑+2H2O+CaCl2
(3)制取装置:
固固加热装置棉花的作用:防止空气对流△(4)收集装置: 向下排空气法
(5)检验: a:使湿润的酚酞试纸变红
b:遇浓盐酸产生大量的白烟
(6)尾气处理:用水吸收NH3要得到干燥的氨气,常用试剂有哪些?
①CaO、碱石灰等碱性干燥剂
②无水CaCl2不能用来干燥NH3(形成CaCl2.8NH3)除了利用上述方法之外,实验室有无其他简单可行的方法来制得氨气?浓氨水方法二:加热浓氨水制氨气←浓氨水←固体CaO思考:有什么现象?为什么有此现象?方法三1、吸收水分,减少溶剂。
2、增加OH-的浓度。
3、放出热量,升高温度。使指示剂变色:与碱发生中和反应:与碱性氧化物反应:与盐反应:稀硫酸与硝酸使紫色石蕊试液变红H+ + OH - = H2O2 H+ + CuO = Cu2+ + H2O 2 H+ + CO3 2- = H2O + CO2与活泼金属反应二、硫酸和硝酸的氧化性思考与交流 1、硫酸、硝酸、盐酸都是酸,它们在组成上用什么特点? 它们都是酸,在水溶液中电离出H+,硫酸、硝酸是含氧酸,盐酸是无氧酸;硫酸是二元酸,硝酸和盐酸是一元酸2、这些特点与酸的通性有什么关系?用电离方程式表示。 在水溶液中都电离出氢离子HA=H++A—1、 硫酸的性质【思考】稀硫酸和浓硫酸的性质有何不同?
浓H2SO4的物理性质
A.色态:无色、粘稠的油状液体
B.沸点:约338℃——难挥发酸(高沸点酸)
C.密度:1.84g/cm3——高密度酸
D.溶解性:跟水任意比互溶,溶解放出大量热。
两高:沸点、密度高
两大:溶解度、溶解放热量大你对浓硫酸知多少?(1)浓硫酸在稀释时应注意什么问题?应将浓硫酸沿烧杯壁向水中慢慢注入,并用玻璃棒不断搅拌。(2)实验室制HCl气体是用以下反应制备,你能说明反应进行的理由吗?注:高沸点酸制低沸点酸,难挥发性酸制易挥发性酸
浓硫酸的特性:1) 吸水性:能吸收水份可干燥与它不反应的气体思考:1.能用浓硫酸干燥H2S、NH3气体吗?2.将硫酸铜晶体投入浓硫酸中,有何现象?2)、脱水性浓硫酸与木屑、棉花、纸屑反应浓硫酸与蔗糖反应浓硫酸能按水的组成比脱去有机物中的氢和氧元素a.浓硫酸沾到衣服上应如何处理?
b.浓硫酸沾到皮肤上应如何处理?浓硫酸的吸水性与脱水性有何区别?实验:将浓硫酸慢慢加入蔗糖中,并用玻
璃棒搅拌
现象: 蔗糖变黑,体积膨胀,变成疏松多孔的海绵状,并放出有刺激性气味的气体原因:C12H22O11 浓硫酸能将蔗糖中的H和O按原子个数比2:1脱去形成水,使蔗糖生成炭问题探究1、写出蔗糖遇浓硫酸发生的化学方程式: C12H22O11 =12C+11H2O2、蔗糖分子中含有水,浓硫酸将水吸去使它生成炭而变黑,这种说法对吗?试分析。不对,因为蔗糖分子中没有水练习并讨论:3)与铜反应:强氧化性分析上述反应中电子转移的方向和数目,指出氧化剂和还原剂,并分析浓硫酸在上述反应中体现的性质。失去2e-得到2e-氧化剂:H2SO4 还原剂:Cu 加热时,浓硫酸能与大多数金属反应(Au、Pt除外) ,一般没有氢气生成,通常生成SO2气体。铜与浓硫酸的反应
现象:有气体产生,此气体使品红溶液褪色或紫色的石蕊试液变红反应后溶液倒入少量的水中,溶液呈蓝色反应原理:Cu+2H2SO4 (浓)== CuSO4+SO2↑+2H2O△浓硫酸与碳的反应:C+2H2SO(浓)== CO2↑+2SO2 ↑+2H2O△4)与非金属反应思考并讨论:请设计实验方案,验证碳和浓硫酸反应的产物加热时,浓硫酸也能与某些非金属反应(S、C等)仪器连接如下说明:应首先用无水硫酸铜验证水,然后用品红验证二氧化硫,再用高锰酸钾氧化多余的二氧化硫,接着再次验证二氧化硫是否全部被氧化,最后才验证二氧化碳。验证碳和浓硫酸反应的产物如何检验浓硫酸与碳反应生成的各种产物? 无水硫酸铜、品红、酸性高锰酸钾或溴水、品红、澄清的石灰水注意:硫酸分子中的硫元素的化合价为
价,处于硫元素所有化合价中的 价态,在氧化还原反应中化合价只能 ,表现 ,浓硫酸被还原一般得到的产物为 。+6最高降低氧化性SO2 常温下,浓硫酸可用铁槽车或铝槽车运输,这是因为常温下,浓硫酸可使铁或铝的表面生成一层致密的氧化膜,阻止了内部金属与浓硫酸进一步反应,这种现象叫做——钝化。硫酸车槽 【思考】浓硫酸具有强氧化性,稀硫酸是否有氧化性?如果有,其氧化性与浓硫酸的氧化性有何不同?
浓硫酸与稀硫酸比较:
稀H2SO4:由H+和SO42-构成——弱氧化性(由H+体现)——可与活泼金属反应生成H2
浓H2SO4:由H2SO4分子构成——强氧化性(由 S 体现)— 加热时可与大多数金属和某些非金属反应,通常生成SO22.硫酸的用途: 三、硝酸的性质:1.物理性质:无色,易挥发、有刺激性气味的液体,能以任意比溶于水,含HNO3 98%的硝酸—发烟硝酸
2.化学性质:(1)酸性(2)氧化性① 与金属反应(除Au和 Pt外)Cu + 4HNO3(浓) = Cu(NO3)2 + 2NO2 +2H2O3Cu + 8HNO3(稀) = 3 Cu(NO3)2 + 2NO +4H2O注意:Fe 和Al遇到冷的浓硝酸被钝化,被氧化成一层致密的氧化膜,与浓硫酸一样。氧化性:浓硝酸>稀硝酸(3)不稳定性②与非金属反应 C +4HNO3 (浓)=2H2O +4NO2 +CO2结论:硝酸跟非金属反应,生成NO2、 H2O和相应的含氧酸③硝酸还能氧化FeO、 Fe(NO3)2(Fe2+)、 HBr(Br-)、 HI(I-) 、H2S (S2-)、 SO2等具有还原性的化合物发生氧化还原反应,因此,不能用硝酸与有关的盐反应制取HI、 SO2、 H2S、 HBr等气体小结:硝酸与金属反应时,主要是HNO3中+5价的氮得到电子,被还原成较低价氮的物质,稀硝酸的还原产物一般是NO,浓硝酸的还原产物一般是NO2,而不像盐酸与金属反应那样生成H2。3、硝酸的用途:制化肥、农药、炸药、染料、盐等
