人教版高中化学必修一课件3.1 《金属的化学性质》课件(共24张PPT)
文档属性
| 名称 | 人教版高中化学必修一课件3.1 《金属的化学性质》课件(共24张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-15 23:06:22 | ||
图片预览







文档简介
(共24张PPT)
第三章
金属及其化合物
第一节
金属的化学性质
就让我们一起走进神奇的金属世界……
第一课时
活动一:金属分布特征
含量特征
§地壳中元素含量较多是O、Si、Al、Fe。其中含量最多的金属元素是铝。
存在形式特征
§除金、铂等少数极不活泼
金属以游离态存在外,大多数金属元素在自然界中以化合态存在。
活动二:金属有哪些物理共性?
金属的物理共性:
不透明,有金属光泽、易导电、易导热、有延展性等。
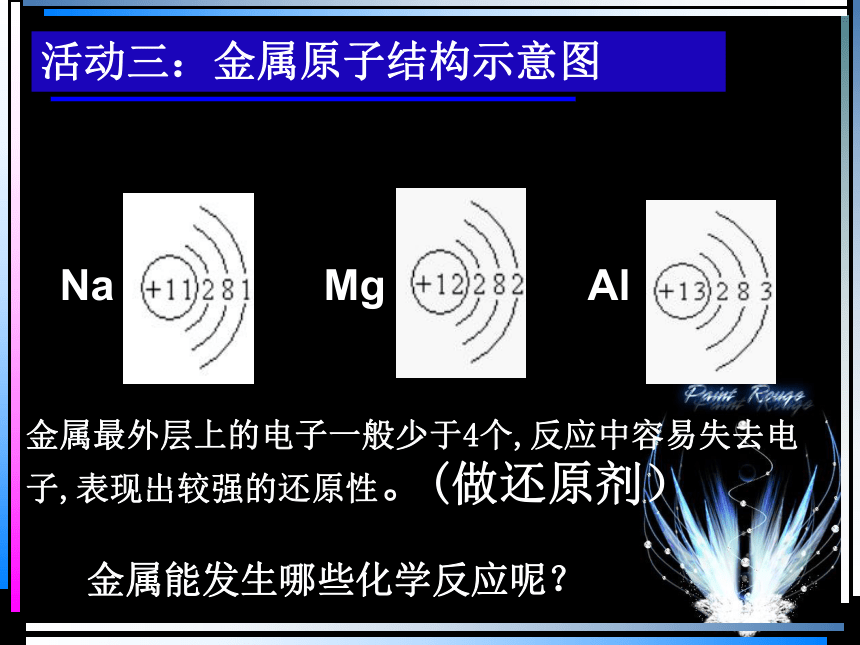
活动三:金属原子结构示意图
金属最外层上的电子一般少于4个,反应中容易失去电子,表现出较强的还原性。(做还原剂)
金属能发生哪些化学反应呢?
金属共同的化学性质:
①金属能与酸反应
②与盐溶液发生反应
③与非金属单质的反应
(是不是所有的金属都能与酸反应)
2Mg+O2=2MgO
2Al+3CuSO4=Al2(SO4)3+3Cu
Cu+2AgNO3=Cu(NO3)2+2Ag
一、金属的化学性质
(一).金属与非金属的反应(氧气)
常温
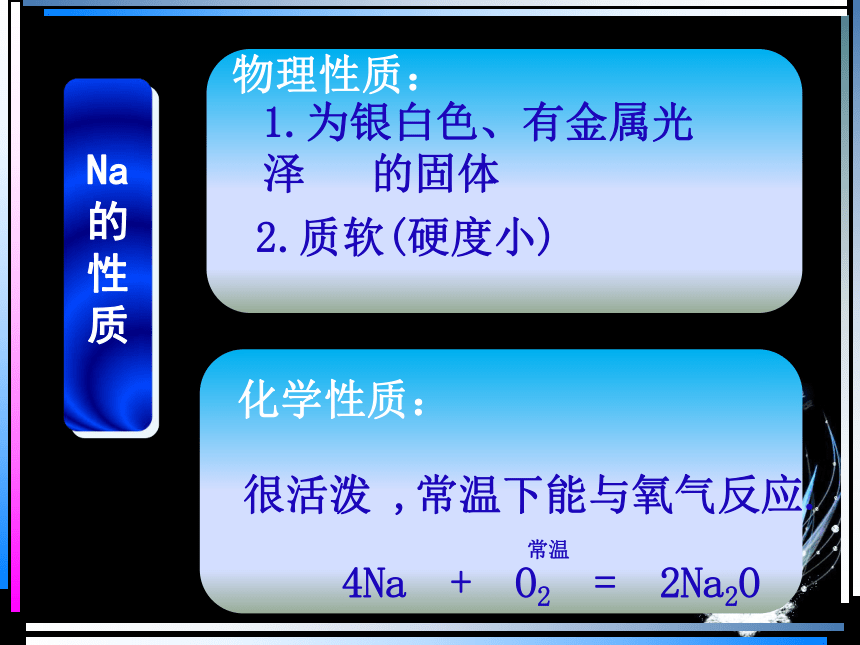
1.为银白色、有金属光泽
的固体
2.质软(硬度小)
很活泼
,常温下能与氧气反应.
4Na
+
O2
=
2Na2O
常温
现象:可观察到钠先熔化后燃烧,燃烧时火焰呈黄色,生成淡黄色的固体。
能隔绝空气。
钠的保存
常温
白色固体
淡黄色固体
加热
-2
-1
比较Na2O和Na2O2
Na2O
Na2O2
色
态
氧元素的价态
生成条件
现
象:铝箔熔化,表面失去光泽,熔化的铝并不滴落,好象有一层膜兜着
是不是所有的氧化膜都能起保护作用呢?
思考
金属与非金属反应
金属除了能和氧气反应外,金属还能被氯气Cl2、S等氧化性的物质所氧化,生成相应的氯化物或硫化物。
试着相信自己写写化学方程式看!
二、金属与酸和水的反应
1、钠与水的反应
钠浮在水面上,熔成小球,迅速游动,嘶嘶作响,溶液变红
现象:
2Na+2H2O=2NaOH+H2↑
反应方程式:
1、钠与水的反应
现象分析
现象
原因
浮
密度比水小
熔
钠和水反应放热,使钠熔成闪亮的小球
游
钠和水反应生成气体,推动钠游动
响
钠和水反应放出热量使水局部蒸发为气体
红
钠和水反应生成了碱
2、铁和水反应
铁不能和冷水、热水反应但能和水蒸气反应
从水蒸气的产生,水蒸气与铁粉反应,
反应产物的检验设计装置。
点燃肥皂泡可听到爆鸣声
现象:
反应方程式:
1.下列关于钠的叙述中,不正确的是(
)
A.钠燃烧时发出黄色的火焰
B.钠燃烧时生成氧化钠
C.钠有很强的还原性
D.钠原子的最外层只有一个电子
B
2.下列关于铝的叙述中,不正确的是(
)
A.铝是地壳中含量最多的金属元素
B.在常温下,铝不能与氧气反应
C.铝是一种比较活泼的金属
D.在化学反应中,铝容易失去电子,是还原剂
B
3.下列物质放置在空气中,因发生氧化还原反应而变质的是( )
A、Na
B、NaCl
C、NaOH
D、Na2O
A
4.取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是( )
①金属先熔化②在空气中燃烧火焰呈黄色③燃烧时火星四射④燃烧后生成淡黄色固体⑤燃烧后生成白色固体
A、①②③
B、①②④
C、①②⑤
D、①③⑤
B
5. 下列说法中,错误的是
( )
A.钠在空气中燃烧时,先熔化,再燃烧,最后所得产物为Na2O2
B.镁因在空气中形成一薄层致密的氧化膜保护了里面的镁,故镁不需要像钠似的特殊保护
C.铝制品在生活中非常普遍,是因为铝不活泼
D.铁因在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属,故铁制品往往需要涂保护层
C
第三章
金属及其化合物
第一节
金属的化学性质
就让我们一起走进神奇的金属世界……
第一课时
活动一:金属分布特征
含量特征
§地壳中元素含量较多是O、Si、Al、Fe。其中含量最多的金属元素是铝。
存在形式特征
§除金、铂等少数极不活泼
金属以游离态存在外,大多数金属元素在自然界中以化合态存在。
活动二:金属有哪些物理共性?
金属的物理共性:
不透明,有金属光泽、易导电、易导热、有延展性等。
活动三:金属原子结构示意图
金属最外层上的电子一般少于4个,反应中容易失去电子,表现出较强的还原性。(做还原剂)
金属能发生哪些化学反应呢?
金属共同的化学性质:
①金属能与酸反应
②与盐溶液发生反应
③与非金属单质的反应
(是不是所有的金属都能与酸反应)
2Mg+O2=2MgO
2Al+3CuSO4=Al2(SO4)3+3Cu
Cu+2AgNO3=Cu(NO3)2+2Ag
一、金属的化学性质
(一).金属与非金属的反应(氧气)
常温
1.为银白色、有金属光泽
的固体
2.质软(硬度小)
很活泼
,常温下能与氧气反应.
4Na
+
O2
=
2Na2O
常温
现象:可观察到钠先熔化后燃烧,燃烧时火焰呈黄色,生成淡黄色的固体。
能隔绝空气。
钠的保存
常温
白色固体
淡黄色固体
加热
-2
-1
比较Na2O和Na2O2
Na2O
Na2O2
色
态
氧元素的价态
生成条件
现
象:铝箔熔化,表面失去光泽,熔化的铝并不滴落,好象有一层膜兜着
是不是所有的氧化膜都能起保护作用呢?
思考
金属与非金属反应
金属除了能和氧气反应外,金属还能被氯气Cl2、S等氧化性的物质所氧化,生成相应的氯化物或硫化物。
试着相信自己写写化学方程式看!
二、金属与酸和水的反应
1、钠与水的反应
钠浮在水面上,熔成小球,迅速游动,嘶嘶作响,溶液变红
现象:
2Na+2H2O=2NaOH+H2↑
反应方程式:
1、钠与水的反应
现象分析
现象
原因
浮
密度比水小
熔
钠和水反应放热,使钠熔成闪亮的小球
游
钠和水反应生成气体,推动钠游动
响
钠和水反应放出热量使水局部蒸发为气体
红
钠和水反应生成了碱
2、铁和水反应
铁不能和冷水、热水反应但能和水蒸气反应
从水蒸气的产生,水蒸气与铁粉反应,
反应产物的检验设计装置。
点燃肥皂泡可听到爆鸣声
现象:
反应方程式:
1.下列关于钠的叙述中,不正确的是(
)
A.钠燃烧时发出黄色的火焰
B.钠燃烧时生成氧化钠
C.钠有很强的还原性
D.钠原子的最外层只有一个电子
B
2.下列关于铝的叙述中,不正确的是(
)
A.铝是地壳中含量最多的金属元素
B.在常温下,铝不能与氧气反应
C.铝是一种比较活泼的金属
D.在化学反应中,铝容易失去电子,是还原剂
B
3.下列物质放置在空气中,因发生氧化还原反应而变质的是( )
A、Na
B、NaCl
C、NaOH
D、Na2O
A
4.取一小块钠放在玻璃燃烧匙里加热,下列实验现象正确的是( )
①金属先熔化②在空气中燃烧火焰呈黄色③燃烧时火星四射④燃烧后生成淡黄色固体⑤燃烧后生成白色固体
A、①②③
B、①②④
C、①②⑤
D、①③⑤
B
5. 下列说法中,错误的是
( )
A.钠在空气中燃烧时,先熔化,再燃烧,最后所得产物为Na2O2
B.镁因在空气中形成一薄层致密的氧化膜保护了里面的镁,故镁不需要像钠似的特殊保护
C.铝制品在生活中非常普遍,是因为铝不活泼
D.铁因在潮湿的空气中生成的氧化物疏松多孔,不能保护内层金属,故铁制品往往需要涂保护层
C
