5.1 化学反应中的质量守恒 教学课件(共22张PPT)初中化学鲁教版五四制(2024)八年级全一册
文档属性
| 名称 | 5.1 化学反应中的质量守恒 教学课件(共22张PPT)初中化学鲁教版五四制(2024)八年级全一册 |  | |
| 格式 | pptx | ||
| 文件大小 | 37.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-29 22:20:26 | ||
图片预览








文档简介
(共22张PPT)
5.1 化学反应中的质量守恒
核心素养目标
1.化学观念:
建立 "化学反应前后物质总质量守恒" 的基本观念,理解质量守恒定律的宏观表现与微观本质。
通过实验探究,认识化学反应中物质的变化遵循质量守恒定律,形成 "定量研究是化学科学重要方法" 的认知逻辑。
2.科学思维:
基于实验数据(如红磷燃烧后剩余固体质量与消耗氧气质量之和等于初始总质量),通过归纳推理得出质量守恒定律,建立 "宏观现象→微观解释→符号表达" 的思维链。
通过微观模型解释质量守恒的本质,突破 "原子重组导致质量不变" 的抽象认知。
3.科学态度与责任:
结合生活实例,认识质量守恒定律在解释自然现象中的应用价值,树立 "化学规律普遍存在" 的科学观念。
学习重难点
学习重点
1.质量守恒定律的实验验证。
2.质量守恒定律的微观解释。
3.质量守恒定律的应用。
学习难点
1.实验设计的逻辑推理。
2.微观解释的抽象性。
3.化学史与实验的融合。
课前导入
我们已经知道,化学反应的结果是反应物转化为生成物。那么,在化学反应过程中,反应物和生成物的质量是如何变化的呢
金属生锈,质量如何变化
蜡烛燃烧生成二氧化碳与水,质量如何变化
化学反应中物质的质量关系
PART 01
1.推测过氧化氢分解过程中物质的质量关系
过氧化氢在催化剂作用下分解生成水和氧气。分解的过氧化氢的质量与生成的水和氧气的质量具有怎样的关系呢
(1)过氧化氢分解了,分子变了,质量当然也就变了!
(2)质量怎么会变呢 在化学反应中,分子虽然变了,但是原子没有改变,质量应该不变!
这两种说法你认为哪一种是对的呢?
1.推测过氧化氢分解过程中物质的质量关系
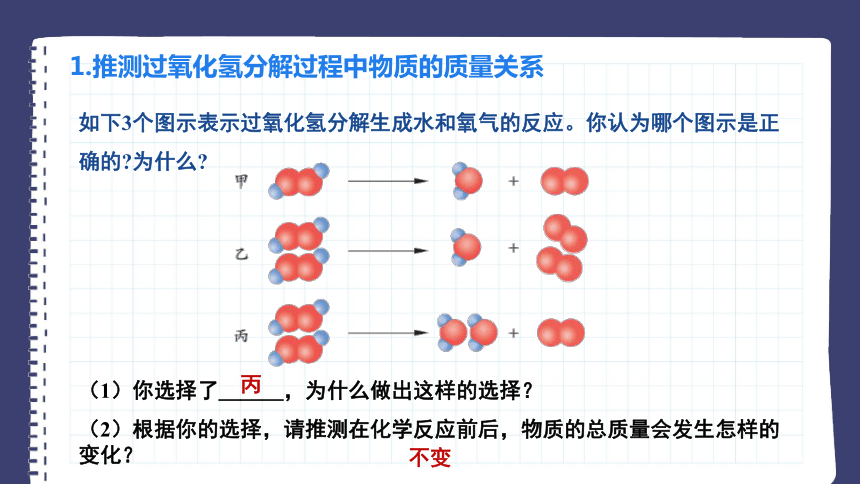
如下3个图示表示过氧化氢分解生成水和氧气的反应。你认为哪个图示是正确的 为什么
(1)你选择了___,为什么做出这样的选择?
(2)根据你的选择,请推测在化学反应前后,物质的总质量会发生怎样的变化?
丙
不变
2.探究化学反应前后物质的质量有无变化
在上述活动中,可能你对物质在化学反应前后质量是否改变已经作出了推测。那么,如何设计实验来检验这一推测是否正确
需要考虑的有:容易发生的反应、如何测定反应前后质量、需要哪些仪器、药品
【实验用品】
托盘天平(或电子秤)、烧杯、试管、胶头滴管、锥形瓶、酒精灯、单孔橡皮塞、玻璃导管、试管夹、玻璃棒、塑料袋(或气球)、细线、细沙、放大镜、火柴。
盐酸、大理石、硫酸铜溶液、氢氧化钠溶液、白磷等。
2.探究化学反应前后物质的质量有无变化
【实验方案】
确定一个化学反应作为研究对象
下列反应可供你选择,当然也可以选择其他你熟悉的反应。
(1)氢氧化钠(NaOH)溶液和硫酸铜(CuSO )溶液反应,生成硫酸钠(Na SO )和氢氧化铜[Cu(OH) ]。
(2)盐酸和大理石(主要成分是CaCO )反应,生成二氧化碳、水和氯化钙(CaCl )。
(3)白磷在空气中燃烧生成五氧化二磷(P O )。
2.探究化学反应前后物质的质量有无变化
氢氧化钠溶液与硫酸铜溶液反应
实验现象:
(1)锥形瓶中出现蓝色沉淀;(2)天平保持平衡
实验结论:
(1)二者反应的文字表达式为
硫酸铜 + 氢氧化钠
硫酸钠 + 氢氧化铜
CuSO4
NaOH
Cu(OH)2
Na2SO4
反应前后质量总和不变
2.探究化学反应前后物质的质量有无变化
盐酸与碳酸钙反应
反应前后质量总和不变
实验现象:
(1)石灰石不断溶解,表面有气泡产生;
(2)天平保持平衡
实验结论:
(1)二者反应的文字表达式为
碳酸钙 + 盐酸
氯化钙 + 水 + 二氧化碳
CaCO3
HCl
CO2
CaCl2
H2O
2.探究化学反应前后物质的质量有无变化
2.探究化学反应前后物质的质量有无变化
白磷燃烧
反应前后质量总和不变
实验现象:
(1)白磷燃烧,瓶内充满大量白烟,气球先鼓起后变瘪;
(2)反应前后,天平保持平衡
实验结论:
(1)二者反应的文字表达式为
白磷 + 氧气
五氧化二磷
点燃
P4
O2
P2O5
白磷有毒,取用时不要沾到皮肤和衣物上;白磷易燃烧,产生大量白烟,要严格控制实验用量。
质量守恒定律
PART 02
1.质量守恒定律
无数实验证明,参加化学反应的各物质的质量总和等于反应后生成的各物
质的质量总和,这个规律叫做质量守恒定律。
对质量守恒定律的理解 适用范围 适用于所有的化学反应,不适用于物理变化
研究的量 是质量的守恒,不包括体积等其他方面的守恒
研究对象 “参加化学反应”的物质,即实际反应掉的那一部分物质,没有参加反应的物质不计算在内
各物质 是指所有参加反应的反应物和生成物,包括固态、液态、气态的所有的物质。
总质量 指物质的总质量守恒,而非某一种或几种物质的质量守恒。
2.质量守恒定律的原因
化学反应的过程就是参加反应的各物质(反应物)的原子重新组合而生成其他物质(生成物)的过程。在化学反应前后,原子的种类没有改变,原
子的数目没有增减,原子的质量没有变化。所以,反应生成的各物质的质量总和必然等于参加反应的各物质的质量总和。
宏观 化学反应前后元素的种类、质量没有改变
微观 化学反应前后原子的种类和数目不变,原子的质量也不变
3.质量守恒定律的发现
质量守恒定律的发现经历了漫长、曲折的过程。
1673 年,英国化学家波义耳将金属汞放在密闭容器里煅烧,然后
打开容器盖进行称量,发现固体物质的质量增加了。
1756 年,俄国化学家罗蒙诺索夫把金属锡放在密闭容器里煅烧,
生成白色的氧化锡,进行称量发现容器里的物质的总质量在煅烧
前后并没有发生变化。经过反复实验,都得到相同结果。但这一
重大发现并没有引起科学界的重视。
1777 年,法国化学家拉瓦锡借鉴波义耳和罗蒙诺索夫的实验,在密闭容器里进行多种金属和非金属的煅烧实验,研究反应中各物质的质量关系,得到以下结论:在化学反应中,物质的总质量在反应前后保持不变。
在密闭容器里
煅烧金属汞
随堂测试
1.下列现象能用质量守恒定律解释的是( )
A.蔗糖溶于水后总质量不变
B.水杯内饮用水敞口放置质量减少
C.小树苗长成参天大树
D.10mL水和10mL酒精混合后体积小于20mL
C
随堂测试
2.在化学反应前后,肯定不会变化的是( )
①原子数目,②分子数目, ③物质的状态,④物质的质量总和, ⑤物质种类,⑥物质的体积, ⑦元素种类,
A.①④⑦
B.①③④
C.①④⑥
D.②④⑦
A
随堂测试
3.将等容积、等质量(含瓶塞、导管、燃烧匙及瓶内少量液体)的两个集气瓶置于天平的左右两盘,并调至平衡,然后同时迅速放入点燃的等质量的白磷和木炭(白磷和木炭均足量),使两者充分燃烧后冷却至室温,并且瓶中的所有物质均充分完全反应后打开止水夹,此时的天平指针( )
A.向左偏 B.向右偏
C.先向左偏后向右偏 D.仍处于标尺中央
D
随堂测试
4.质量守恒定律揭示了化学反应中反应物和生成物之间的关系,下列关于质量守恒定律说法错误的是( )
A.木炭在空气中燃烧成灰,固体质量减少了,这违背了质量守恒定律
B.在化学反应前后,反应物和生成物中原子的种类和数目都不变
C.在化学反应前后,反应物和生成物中元素的种类和质量都不变
D.在化学反应前后,反应物和生成物中分子的种类一定改变,数目可能改变
A
谢谢观看
5.1 化学反应中的质量守恒
核心素养目标
1.化学观念:
建立 "化学反应前后物质总质量守恒" 的基本观念,理解质量守恒定律的宏观表现与微观本质。
通过实验探究,认识化学反应中物质的变化遵循质量守恒定律,形成 "定量研究是化学科学重要方法" 的认知逻辑。
2.科学思维:
基于实验数据(如红磷燃烧后剩余固体质量与消耗氧气质量之和等于初始总质量),通过归纳推理得出质量守恒定律,建立 "宏观现象→微观解释→符号表达" 的思维链。
通过微观模型解释质量守恒的本质,突破 "原子重组导致质量不变" 的抽象认知。
3.科学态度与责任:
结合生活实例,认识质量守恒定律在解释自然现象中的应用价值,树立 "化学规律普遍存在" 的科学观念。
学习重难点
学习重点
1.质量守恒定律的实验验证。
2.质量守恒定律的微观解释。
3.质量守恒定律的应用。
学习难点
1.实验设计的逻辑推理。
2.微观解释的抽象性。
3.化学史与实验的融合。
课前导入
我们已经知道,化学反应的结果是反应物转化为生成物。那么,在化学反应过程中,反应物和生成物的质量是如何变化的呢
金属生锈,质量如何变化
蜡烛燃烧生成二氧化碳与水,质量如何变化
化学反应中物质的质量关系
PART 01
1.推测过氧化氢分解过程中物质的质量关系
过氧化氢在催化剂作用下分解生成水和氧气。分解的过氧化氢的质量与生成的水和氧气的质量具有怎样的关系呢
(1)过氧化氢分解了,分子变了,质量当然也就变了!
(2)质量怎么会变呢 在化学反应中,分子虽然变了,但是原子没有改变,质量应该不变!
这两种说法你认为哪一种是对的呢?
1.推测过氧化氢分解过程中物质的质量关系
如下3个图示表示过氧化氢分解生成水和氧气的反应。你认为哪个图示是正确的 为什么
(1)你选择了___,为什么做出这样的选择?
(2)根据你的选择,请推测在化学反应前后,物质的总质量会发生怎样的变化?
丙
不变
2.探究化学反应前后物质的质量有无变化
在上述活动中,可能你对物质在化学反应前后质量是否改变已经作出了推测。那么,如何设计实验来检验这一推测是否正确
需要考虑的有:容易发生的反应、如何测定反应前后质量、需要哪些仪器、药品
【实验用品】
托盘天平(或电子秤)、烧杯、试管、胶头滴管、锥形瓶、酒精灯、单孔橡皮塞、玻璃导管、试管夹、玻璃棒、塑料袋(或气球)、细线、细沙、放大镜、火柴。
盐酸、大理石、硫酸铜溶液、氢氧化钠溶液、白磷等。
2.探究化学反应前后物质的质量有无变化
【实验方案】
确定一个化学反应作为研究对象
下列反应可供你选择,当然也可以选择其他你熟悉的反应。
(1)氢氧化钠(NaOH)溶液和硫酸铜(CuSO )溶液反应,生成硫酸钠(Na SO )和氢氧化铜[Cu(OH) ]。
(2)盐酸和大理石(主要成分是CaCO )反应,生成二氧化碳、水和氯化钙(CaCl )。
(3)白磷在空气中燃烧生成五氧化二磷(P O )。
2.探究化学反应前后物质的质量有无变化
氢氧化钠溶液与硫酸铜溶液反应
实验现象:
(1)锥形瓶中出现蓝色沉淀;(2)天平保持平衡
实验结论:
(1)二者反应的文字表达式为
硫酸铜 + 氢氧化钠
硫酸钠 + 氢氧化铜
CuSO4
NaOH
Cu(OH)2
Na2SO4
反应前后质量总和不变
2.探究化学反应前后物质的质量有无变化
盐酸与碳酸钙反应
反应前后质量总和不变
实验现象:
(1)石灰石不断溶解,表面有气泡产生;
(2)天平保持平衡
实验结论:
(1)二者反应的文字表达式为
碳酸钙 + 盐酸
氯化钙 + 水 + 二氧化碳
CaCO3
HCl
CO2
CaCl2
H2O
2.探究化学反应前后物质的质量有无变化
2.探究化学反应前后物质的质量有无变化
白磷燃烧
反应前后质量总和不变
实验现象:
(1)白磷燃烧,瓶内充满大量白烟,气球先鼓起后变瘪;
(2)反应前后,天平保持平衡
实验结论:
(1)二者反应的文字表达式为
白磷 + 氧气
五氧化二磷
点燃
P4
O2
P2O5
白磷有毒,取用时不要沾到皮肤和衣物上;白磷易燃烧,产生大量白烟,要严格控制实验用量。
质量守恒定律
PART 02
1.质量守恒定律
无数实验证明,参加化学反应的各物质的质量总和等于反应后生成的各物
质的质量总和,这个规律叫做质量守恒定律。
对质量守恒定律的理解 适用范围 适用于所有的化学反应,不适用于物理变化
研究的量 是质量的守恒,不包括体积等其他方面的守恒
研究对象 “参加化学反应”的物质,即实际反应掉的那一部分物质,没有参加反应的物质不计算在内
各物质 是指所有参加反应的反应物和生成物,包括固态、液态、气态的所有的物质。
总质量 指物质的总质量守恒,而非某一种或几种物质的质量守恒。
2.质量守恒定律的原因
化学反应的过程就是参加反应的各物质(反应物)的原子重新组合而生成其他物质(生成物)的过程。在化学反应前后,原子的种类没有改变,原
子的数目没有增减,原子的质量没有变化。所以,反应生成的各物质的质量总和必然等于参加反应的各物质的质量总和。
宏观 化学反应前后元素的种类、质量没有改变
微观 化学反应前后原子的种类和数目不变,原子的质量也不变
3.质量守恒定律的发现
质量守恒定律的发现经历了漫长、曲折的过程。
1673 年,英国化学家波义耳将金属汞放在密闭容器里煅烧,然后
打开容器盖进行称量,发现固体物质的质量增加了。
1756 年,俄国化学家罗蒙诺索夫把金属锡放在密闭容器里煅烧,
生成白色的氧化锡,进行称量发现容器里的物质的总质量在煅烧
前后并没有发生变化。经过反复实验,都得到相同结果。但这一
重大发现并没有引起科学界的重视。
1777 年,法国化学家拉瓦锡借鉴波义耳和罗蒙诺索夫的实验,在密闭容器里进行多种金属和非金属的煅烧实验,研究反应中各物质的质量关系,得到以下结论:在化学反应中,物质的总质量在反应前后保持不变。
在密闭容器里
煅烧金属汞
随堂测试
1.下列现象能用质量守恒定律解释的是( )
A.蔗糖溶于水后总质量不变
B.水杯内饮用水敞口放置质量减少
C.小树苗长成参天大树
D.10mL水和10mL酒精混合后体积小于20mL
C
随堂测试
2.在化学反应前后,肯定不会变化的是( )
①原子数目,②分子数目, ③物质的状态,④物质的质量总和, ⑤物质种类,⑥物质的体积, ⑦元素种类,
A.①④⑦
B.①③④
C.①④⑥
D.②④⑦
A
随堂测试
3.将等容积、等质量(含瓶塞、导管、燃烧匙及瓶内少量液体)的两个集气瓶置于天平的左右两盘,并调至平衡,然后同时迅速放入点燃的等质量的白磷和木炭(白磷和木炭均足量),使两者充分燃烧后冷却至室温,并且瓶中的所有物质均充分完全反应后打开止水夹,此时的天平指针( )
A.向左偏 B.向右偏
C.先向左偏后向右偏 D.仍处于标尺中央
D
随堂测试
4.质量守恒定律揭示了化学反应中反应物和生成物之间的关系,下列关于质量守恒定律说法错误的是( )
A.木炭在空气中燃烧成灰,固体质量减少了,这违背了质量守恒定律
B.在化学反应前后,反应物和生成物中原子的种类和数目都不变
C.在化学反应前后,反应物和生成物中元素的种类和质量都不变
D.在化学反应前后,反应物和生成物中分子的种类一定改变,数目可能改变
A
谢谢观看
同课章节目录
