人教版高中化学必修第二册第五章化工生产中的重要非金属元素微专题二喷泉实验原理及应用课件(共17张PPT)
文档属性
| 名称 | 人教版高中化学必修第二册第五章化工生产中的重要非金属元素微专题二喷泉实验原理及应用课件(共17张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 986.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-04 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
微专题二 喷泉实验原理及应用
专题 精讲
1. NH3的喷泉实验
实验装置 操作及现象 结论
①打开弹簧夹并挤压胶头滴管;
②烧杯中的溶液由玻璃管进入烧瓶,形成红色喷泉 氨极易溶于水,水溶液呈 碱性
2. 喷泉实验应注意的问题
(1)盛气装置要预先进行气密性检查,只有气密性良好才能使用。
(2)圆底烧瓶在充入氨气前应是干燥的,否则会浪费氨气。
(3)圆底烧瓶内要充满氨气,氨气过少往往不能形成喷泉。
(4)玻璃导管插入滴加酚酞溶液的水中的部分不能太短,以防导管过早地与水脱离 而导致喷泉停喷。
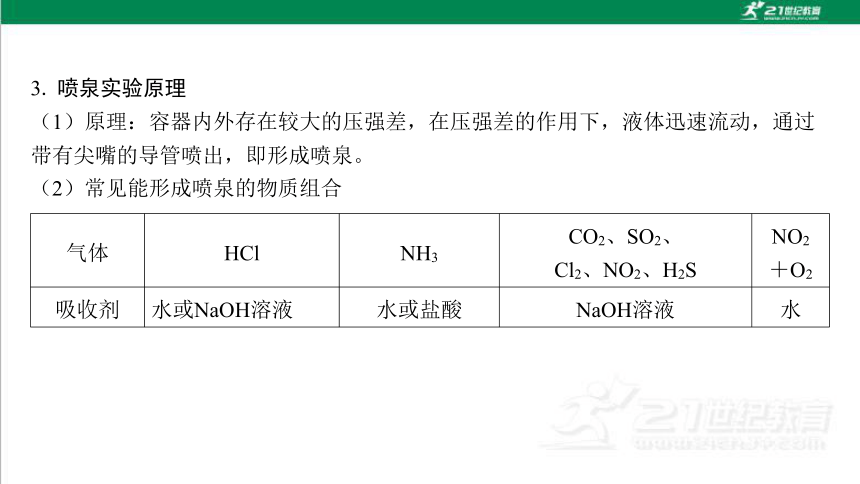
3. 喷泉实验原理
(1)原理:容器内外存在较大的压强差,在压强差的作用下,液体迅速流动,通过 带有尖嘴的导管喷出,即形成喷泉。
(2)常见能形成喷泉的物质组合
气体 HCl NH3 CO2、SO2、
Cl2、NO2、H2S NO2
+O2
吸收剂 水或NaOH溶液 水或盐酸 NaOH溶液 水
4. 使容器内外产生较大压强差的两种方法
(1)减小内压法:如图1所示。
图1
容器内气体与水或其他液体接触 气体溶解或发生化学反应
容器内压强减小 外部液体迅速进入形成喷泉
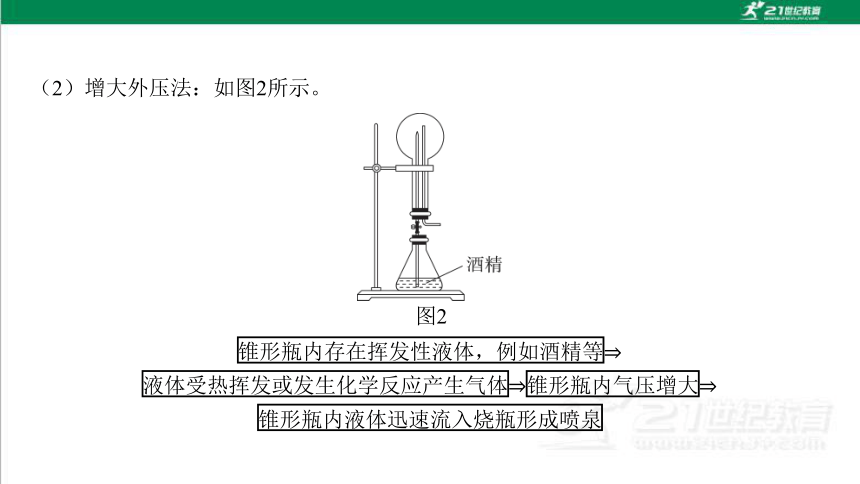
(2)增大外压法:如图2所示。
图2
锥形瓶内存在挥发性液体,例如酒精等
液体受热挥发或发生化学反应产生气体 锥形瓶内气压增大
锥形瓶内液体迅速流入烧瓶形成喷泉
5. 喷泉实验的有关计算
专题 训练
A. Cl2(饱和食盐水) 无色喷泉
B. NH3(H2O含石蕊) 蓝色喷泉
C. HCl(H2O含石蕊) 红色喷泉
D. CO2(NaOH溶液) 无色喷泉
解析:氯气在饱和食盐水中溶解度很小,不会形成压强差,不会产生喷泉,A项与实 验事实不相符;氨气极易溶于水,可形成喷泉,又因氨水溶液显碱性,石蕊遇碱变 蓝,所以形成蓝色喷泉,B项与实验事实相符;HCl极易溶于水,可形成喷泉,又因 盐酸显酸性,石蕊遇酸变红,C项与实验事实相符;CO2与NaOH反应,形成压强差而 产生喷泉,Na2CO3溶液无色,所以喷泉颜色为无色,D项与实验事实相符。
A
2. 喷泉是一种常见的自然现象,其产生的原因是存在压强差。
打开
止水夹,挤压胶头滴管
NH3溶于少量水中,使圆底烧瓶内压强
减小,烧杯内的水进入圆底烧瓶,形成喷泉
打开止水夹,用热毛巾捂住圆
底烧瓶至有气泡从水中冒出,移去热毛巾
解析:(1)图1引发喷泉,只需打开止水夹,挤压胶头滴管即可,图2则需先打开止 水夹,再用热毛巾捂住圆底烧瓶,发现有气泡冒出后,移去热毛巾即可。
A. Cu与稀盐酸
B. NaHCO3溶液与NaOH溶液
C. CaCO3与稀硫酸
D. NH4HCO3与稀盐酸
解析:(2)能在锥形瓶内反应产生气体,使锥形瓶内压强大于圆底烧瓶内压强方 可,NH4HCO3与盐酸反应生成CO2,故应选NH4HCO3和稀盐酸,其他要么不反应, 要么反应不生成气体或产生气体很少。
D
解析:(3)图1、2是上部压强减小导致喷泉,图3是下部压强增大导致喷泉,人造喷 泉及火山爆发均与图3原理相似。
减小
增大
3
图Ⅰ
D
A. SO2和H2O
B. CO2和NaOH溶液
C. NH3和H2O
D. NO和H2O
解析:(1)气体极易溶于水或气体与溶液易发生化学反应可形成图Ⅰ中喷泉,A、C 利用气体的溶解性形成喷泉,B中发生化学反应形成喷泉,而D中NO不溶于水,不能 形成喷泉。
(2)某学生积极思考喷泉原理的应用,设计了如图Ⅱ所示的装置。
图Ⅱ
HCl气体
进入盛有NH3的集气瓶,产生大量的白烟
两烧瓶同时产生喷泉
解析:(2)①如果关闭活塞c,打开活塞a、b,再挤压胶头滴管,盛氨气的烧瓶内气 压减小,HCl气体进入盛有NH3的烧瓶,HCl与氨气结合生成氯化铵,产生大量的白 烟。②在①操作的基础上,打开活塞c,烧瓶内气体减少,外压大于内压,形成喷 泉,则现象为两烧瓶同时产生喷泉。
归纳总结
气体压强在实验中的应用
(1)
(2)喷泉实验
易溶于水的HCl、NH3等溶解,烧瓶内压强减小,烧杯中水被大气压入烧瓶。
(3)测量气体体积
反应管中产生气体使压强增大,将水(或其他液体)压入右侧漏斗中,反应完全 后冷却至室温,调节液面,读数测量产生的气体体积。
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
微专题二 喷泉实验原理及应用
专题 精讲
1. NH3的喷泉实验
实验装置 操作及现象 结论
①打开弹簧夹并挤压胶头滴管;
②烧杯中的溶液由玻璃管进入烧瓶,形成红色喷泉 氨极易溶于水,水溶液呈 碱性
2. 喷泉实验应注意的问题
(1)盛气装置要预先进行气密性检查,只有气密性良好才能使用。
(2)圆底烧瓶在充入氨气前应是干燥的,否则会浪费氨气。
(3)圆底烧瓶内要充满氨气,氨气过少往往不能形成喷泉。
(4)玻璃导管插入滴加酚酞溶液的水中的部分不能太短,以防导管过早地与水脱离 而导致喷泉停喷。
3. 喷泉实验原理
(1)原理:容器内外存在较大的压强差,在压强差的作用下,液体迅速流动,通过 带有尖嘴的导管喷出,即形成喷泉。
(2)常见能形成喷泉的物质组合
气体 HCl NH3 CO2、SO2、
Cl2、NO2、H2S NO2
+O2
吸收剂 水或NaOH溶液 水或盐酸 NaOH溶液 水
4. 使容器内外产生较大压强差的两种方法
(1)减小内压法:如图1所示。
图1
容器内气体与水或其他液体接触 气体溶解或发生化学反应
容器内压强减小 外部液体迅速进入形成喷泉
(2)增大外压法:如图2所示。
图2
锥形瓶内存在挥发性液体,例如酒精等
液体受热挥发或发生化学反应产生气体 锥形瓶内气压增大
锥形瓶内液体迅速流入烧瓶形成喷泉
5. 喷泉实验的有关计算
专题 训练
A. Cl2(饱和食盐水) 无色喷泉
B. NH3(H2O含石蕊) 蓝色喷泉
C. HCl(H2O含石蕊) 红色喷泉
D. CO2(NaOH溶液) 无色喷泉
解析:氯气在饱和食盐水中溶解度很小,不会形成压强差,不会产生喷泉,A项与实 验事实不相符;氨气极易溶于水,可形成喷泉,又因氨水溶液显碱性,石蕊遇碱变 蓝,所以形成蓝色喷泉,B项与实验事实相符;HCl极易溶于水,可形成喷泉,又因 盐酸显酸性,石蕊遇酸变红,C项与实验事实相符;CO2与NaOH反应,形成压强差而 产生喷泉,Na2CO3溶液无色,所以喷泉颜色为无色,D项与实验事实相符。
A
2. 喷泉是一种常见的自然现象,其产生的原因是存在压强差。
打开
止水夹,挤压胶头滴管
NH3溶于少量水中,使圆底烧瓶内压强
减小,烧杯内的水进入圆底烧瓶,形成喷泉
打开止水夹,用热毛巾捂住圆
底烧瓶至有气泡从水中冒出,移去热毛巾
解析:(1)图1引发喷泉,只需打开止水夹,挤压胶头滴管即可,图2则需先打开止 水夹,再用热毛巾捂住圆底烧瓶,发现有气泡冒出后,移去热毛巾即可。
A. Cu与稀盐酸
B. NaHCO3溶液与NaOH溶液
C. CaCO3与稀硫酸
D. NH4HCO3与稀盐酸
解析:(2)能在锥形瓶内反应产生气体,使锥形瓶内压强大于圆底烧瓶内压强方 可,NH4HCO3与盐酸反应生成CO2,故应选NH4HCO3和稀盐酸,其他要么不反应, 要么反应不生成气体或产生气体很少。
D
解析:(3)图1、2是上部压强减小导致喷泉,图3是下部压强增大导致喷泉,人造喷 泉及火山爆发均与图3原理相似。
减小
增大
3
图Ⅰ
D
A. SO2和H2O
B. CO2和NaOH溶液
C. NH3和H2O
D. NO和H2O
解析:(1)气体极易溶于水或气体与溶液易发生化学反应可形成图Ⅰ中喷泉,A、C 利用气体的溶解性形成喷泉,B中发生化学反应形成喷泉,而D中NO不溶于水,不能 形成喷泉。
(2)某学生积极思考喷泉原理的应用,设计了如图Ⅱ所示的装置。
图Ⅱ
HCl气体
进入盛有NH3的集气瓶,产生大量的白烟
两烧瓶同时产生喷泉
解析:(2)①如果关闭活塞c,打开活塞a、b,再挤压胶头滴管,盛氨气的烧瓶内气 压减小,HCl气体进入盛有NH3的烧瓶,HCl与氨气结合生成氯化铵,产生大量的白 烟。②在①操作的基础上,打开活塞c,烧瓶内气体减少,外压大于内压,形成喷 泉,则现象为两烧瓶同时产生喷泉。
归纳总结
气体压强在实验中的应用
(1)
(2)喷泉实验
易溶于水的HCl、NH3等溶解,烧瓶内压强减小,烧杯中水被大气压入烧瓶。
(3)测量气体体积
反应管中产生气体使压强增大,将水(或其他液体)压入右侧漏斗中,反应完全 后冷却至室温,调节液面,读数测量产生的气体体积。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
