人教版高中化学必修第二册第五章化工生产中的重要非金属元素微专题三硝酸与金属反应的相关计算课件(共15张PPT)
文档属性
| 名称 | 人教版高中化学必修第二册第五章化工生产中的重要非金属元素微专题三硝酸与金属反应的相关计算课件(共15张PPT) |  | |
| 格式 | ppt | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-04 09:57:05 | ||
图片预览






文档简介
(共15张PPT)
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
微专题三 硝酸与金属反应的相关计算
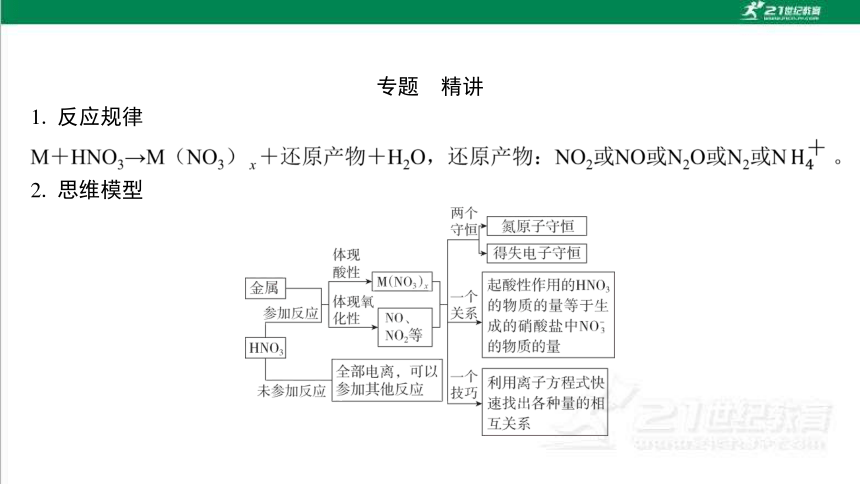
专题 精讲
1. 反应规律
2. 思维模型
[特别提醒] (1)起氧化作用的HNO3转化成了气体(NO、NO2),可根据气体的 物质的量求出。
(2)起酸性作用的HNO3转化成了硝酸盐,可以根据金属阳离子的物质的量求出。
(3)没有参加反应的HNO3,可根据溶液中H+的物质的量求出。
3. 计算方法
(1)得失电子守恒:金属失电子的物质的量=n(NO2)+3n(NO)。
(2)氮原子守恒:n(HNO3)消耗=xn[M(NO3)x]+n(NO2)+n(NO)。
(4)离子方程式计算法:金属与硫酸、硝酸的混合酸反应时,
专题 训练
A. 该合金中n(Cu)∶n(Mg)=2∶1
B. 该浓硝酸中HNO3的物质的量浓度是13.0 mol·L-1
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL
B
A. 1.2 mol B. 1.1 mol
C. 0.9 mol D. 0.8 mol
B
A. (m+2.28) g B. (m+2.04) g
C. (m+3.32) g D. (m+4.34) g
B
A. 0.15 mol·L-1 B. 0.225 mol·L-1
C. 0.35 mol·L-1 D. 0.45 mol·L-1
B
A. 原混合酸中H2SO4物质的量为0.4 mol
C. 混合酸中HNO3物质的量浓度为2 mol·L-1
D. 第二份溶液中最终溶质为FeSO4
A
6. 将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生标准状况下的一氧 化氮和二氧化氮混合气体共11.2 L。请回答下列问题:
5.824
解析:(3)通入氧气的目的是将0.26 mol NO和0.24 mol NO2全部转化为HNO3。根 据得失电子守恒:4n(O2)=3n(NO)+n(NO2)=3×0.26 mol+0.24 mol= 1.02 mol,则n(O2)=0.255 mol。
0.255
第五章 化工生产中的重要非金属元素
第二节 氮及其化合物
微专题三 硝酸与金属反应的相关计算
专题 精讲
1. 反应规律
2. 思维模型
[特别提醒] (1)起氧化作用的HNO3转化成了气体(NO、NO2),可根据气体的 物质的量求出。
(2)起酸性作用的HNO3转化成了硝酸盐,可以根据金属阳离子的物质的量求出。
(3)没有参加反应的HNO3,可根据溶液中H+的物质的量求出。
3. 计算方法
(1)得失电子守恒:金属失电子的物质的量=n(NO2)+3n(NO)。
(2)氮原子守恒:n(HNO3)消耗=xn[M(NO3)x]+n(NO2)+n(NO)。
(4)离子方程式计算法:金属与硫酸、硝酸的混合酸反应时,
专题 训练
A. 该合金中n(Cu)∶n(Mg)=2∶1
B. 该浓硝酸中HNO3的物质的量浓度是13.0 mol·L-1
C. NO2和N2O4的混合气体中,NO2的体积分数是80%
D. 得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL
B
A. 1.2 mol B. 1.1 mol
C. 0.9 mol D. 0.8 mol
B
A. (m+2.28) g B. (m+2.04) g
C. (m+3.32) g D. (m+4.34) g
B
A. 0.15 mol·L-1 B. 0.225 mol·L-1
C. 0.35 mol·L-1 D. 0.45 mol·L-1
B
A. 原混合酸中H2SO4物质的量为0.4 mol
C. 混合酸中HNO3物质的量浓度为2 mol·L-1
D. 第二份溶液中最终溶质为FeSO4
A
6. 将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生标准状况下的一氧 化氮和二氧化氮混合气体共11.2 L。请回答下列问题:
5.824
解析:(3)通入氧气的目的是将0.26 mol NO和0.24 mol NO2全部转化为HNO3。根 据得失电子守恒:4n(O2)=3n(NO)+n(NO2)=3×0.26 mol+0.24 mol= 1.02 mol,则n(O2)=0.255 mol。
0.255
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
