南宁市第三中学2025届高三下学期5月第二次适应性考试化学试卷(图片版,含答案)
文档属性
| 名称 | 南宁市第三中学2025届高三下学期5月第二次适应性考试化学试卷(图片版,含答案) |  | |
| 格式 | |||
| 文件大小 | 3.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-03 21:45:46 | ||
图片预览


文档简介
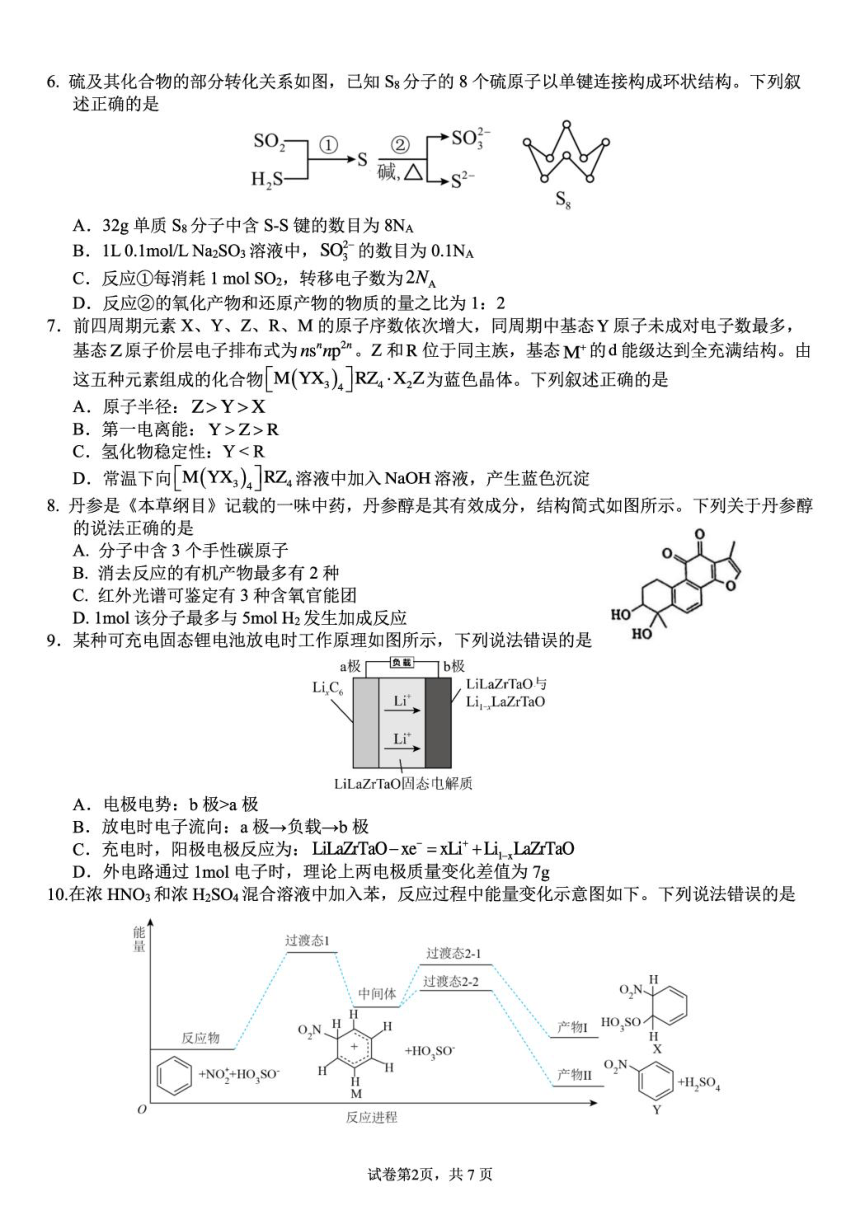
南宁三中2025届毕业班五月第二次适应性测试
化学试卷
可能用到的相对原子质量:Li-7S32
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题
目要求。
1.化学与生活息息相关,下列有关叙述正确的是
A.由苯乙烯和丁二烯合成的SBS橡胶属于天然有机高分子化合物
B.春晚“宇树”机器人的核心芯片材料主要为二氧化硅
C.神舟十九号飞船返回舱表层材料玻璃纤维属于无机非金属材料
D.比亚迪新能源汽车“刀片”锂离子电池属于燃料电池
2.C0会与人体血红蛋白中的F(I⑩形成配位键,使其丧失运输氧的能力。
下列有关说法错误的是
A.基态Fe2+的价电子排布式为3d
B.1602和1803互为同位素
C.基态C原子2p轨道的电子云轮廓图为
D.人体血红蛋白中的F(四形成配位键时,CO分子提供孤电子对
3.下列实验装置和操作能达到实验目的的是
P,0
NH.
苯、溴混合液
C02
Zn
饱和
铁粉
AgNO
食盐水
冷水
溶液
溶液
甲
丙
A,用装置甲制备NHCO3时,先通入NH3再通入CO,
B.用装置乙制备溴苯并验证该反应为取代反应
C.用装置丙在铁上镀锌
D.用装置丁蒸发MgCL2溶液制无水MgCl2
4.下列对一些实验事实的理论解释,错误的是
选项
实验事实
理论解释
A
键角:NH3>NF3
氟的电负性大于氢,N-F的成键电子对更偏向氟,
氮周围电子云密度较小,斥力较小,键角较小
B
酸性:CECOOH>CCl,COOH
氟的电负性大于氯,导致CF3COOH的羧基中的羟
基的极性更大,更易电离出H
O
沸点:
OH
OH
前者形成分子间氢键,后者形成分子内氢键
HO
OH
D
用杯酚分离C6o和C0
超分子具有自组装特征
A.A
B.B
C.C
D.D
5.下列离子方程式书写正确的是
A.向澄清石灰水中滴加少量草酸溶液:Ca2++2OH+H,C,0,=CaC,04↓+2H,O
B.铅酸蓄电池充电时的阳极反应:Pb2++2H,0-2e=PbO2↓+4H
C.将S02通入酸性KMnO4溶液中:3S02+2MnO,+4H=3SO}+2n2+2H,O
D.甲醛与足量银氨溶液反应:HCHO+2AgNH)2OH_水浴m热→2Ag+3NH↑+HCO0+NH4+H2O
试卷第1页,共7页
6.硫及其化合物的部分转化关系如图,己知S8分子的8个硫原子以单键连接构成环状结构。下列叙
述正确的是
S02
①
②
S
H,S-
碱,△→S2
A.32g单质S8分子中含S-S键的数目为8NA
B.1L0.1mol/LNa2SO3溶液中,SO的数目为0.1Na
C.反应①海消耗1molS02,转移电子数为2N
D.反应②的氧化产物和还原产物的物质的量之比为1:2
7.前四周期元素X、Y、Z、R、M的原子序数依次增大,同周期中基态Y原子未成对电子数最多,
基态Z原子价层电子排布式为s"m2”。Z和R位于同主族,基态M的d能级达到全充满结构。由
这五种元素组成的化合物M(YX)4]RZ·X,Z为蓝色晶体。下列叙述正确的是
A.原子半径:Z>Y>X
B.第一电离能:Y>Z>R
C.氢化物稳定性:YD.常温下向M(YX)4RZ4溶液中加入NaOH溶液,产生蓝色沉淀
8.丹参是《本草纲目》记载的一味中药,丹参醇是其有效成分,结构简式如图所示。下列关于丹参醇
的说法正确的是
A.分子中含3个手性碳原子
B.消去反应的有机产物最多有2种
C.红外光谱可鉴定有3种含氧官能团
D.lmol该分子最多与5molH2发生加成反应
HO
9.某种可充电固态锂电池放电时工作原理如图所示,下列说法错误的是
HO
a极负超 b极
Li.Co
LiLaZrTaO.与
Li
LiLaZrTaO
Li
LiLaZrTaO固态电解质
A.电极电势:b极>a极
B.放电时电子流向:a极→负载→b极
C.充电时,阳极电极反应为:LiLaZrTaO-xe=xLi计+LiLaZrTaO
D.外电路通过1ol电子时,理论上两电极质量变化差值为7g
10.在浓HNO3和浓H2SO4混合溶液中加入苯,反应过程中能量变化示意图如下。下列说法错误的是
量
过渡态1
过渡态21
过渡态2-2
中间体
O,N.
H
产物H0,S0个
反应物
O,N、H
+HO,SO
+NO;+HO SO
H
O.N
产物Ⅱ
+H,S04
M
反应进程
试卷第2页,共7页
化学试卷
可能用到的相对原子质量:Li-7S32
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题
目要求。
1.化学与生活息息相关,下列有关叙述正确的是
A.由苯乙烯和丁二烯合成的SBS橡胶属于天然有机高分子化合物
B.春晚“宇树”机器人的核心芯片材料主要为二氧化硅
C.神舟十九号飞船返回舱表层材料玻璃纤维属于无机非金属材料
D.比亚迪新能源汽车“刀片”锂离子电池属于燃料电池
2.C0会与人体血红蛋白中的F(I⑩形成配位键,使其丧失运输氧的能力。
下列有关说法错误的是
A.基态Fe2+的价电子排布式为3d
B.1602和1803互为同位素
C.基态C原子2p轨道的电子云轮廓图为
D.人体血红蛋白中的F(四形成配位键时,CO分子提供孤电子对
3.下列实验装置和操作能达到实验目的的是
P,0
NH.
苯、溴混合液
C02
Zn
饱和
铁粉
AgNO
食盐水
冷水
溶液
溶液
甲
丙
A,用装置甲制备NHCO3时,先通入NH3再通入CO,
B.用装置乙制备溴苯并验证该反应为取代反应
C.用装置丙在铁上镀锌
D.用装置丁蒸发MgCL2溶液制无水MgCl2
4.下列对一些实验事实的理论解释,错误的是
选项
实验事实
理论解释
A
键角:NH3>NF3
氟的电负性大于氢,N-F的成键电子对更偏向氟,
氮周围电子云密度较小,斥力较小,键角较小
B
酸性:CECOOH>CCl,COOH
氟的电负性大于氯,导致CF3COOH的羧基中的羟
基的极性更大,更易电离出H
O
沸点:
OH
OH
前者形成分子间氢键,后者形成分子内氢键
HO
OH
D
用杯酚分离C6o和C0
超分子具有自组装特征
A.A
B.B
C.C
D.D
5.下列离子方程式书写正确的是
A.向澄清石灰水中滴加少量草酸溶液:Ca2++2OH+H,C,0,=CaC,04↓+2H,O
B.铅酸蓄电池充电时的阳极反应:Pb2++2H,0-2e=PbO2↓+4H
C.将S02通入酸性KMnO4溶液中:3S02+2MnO,+4H=3SO}+2n2+2H,O
D.甲醛与足量银氨溶液反应:HCHO+2AgNH)2OH_水浴m热→2Ag+3NH↑+HCO0+NH4+H2O
试卷第1页,共7页
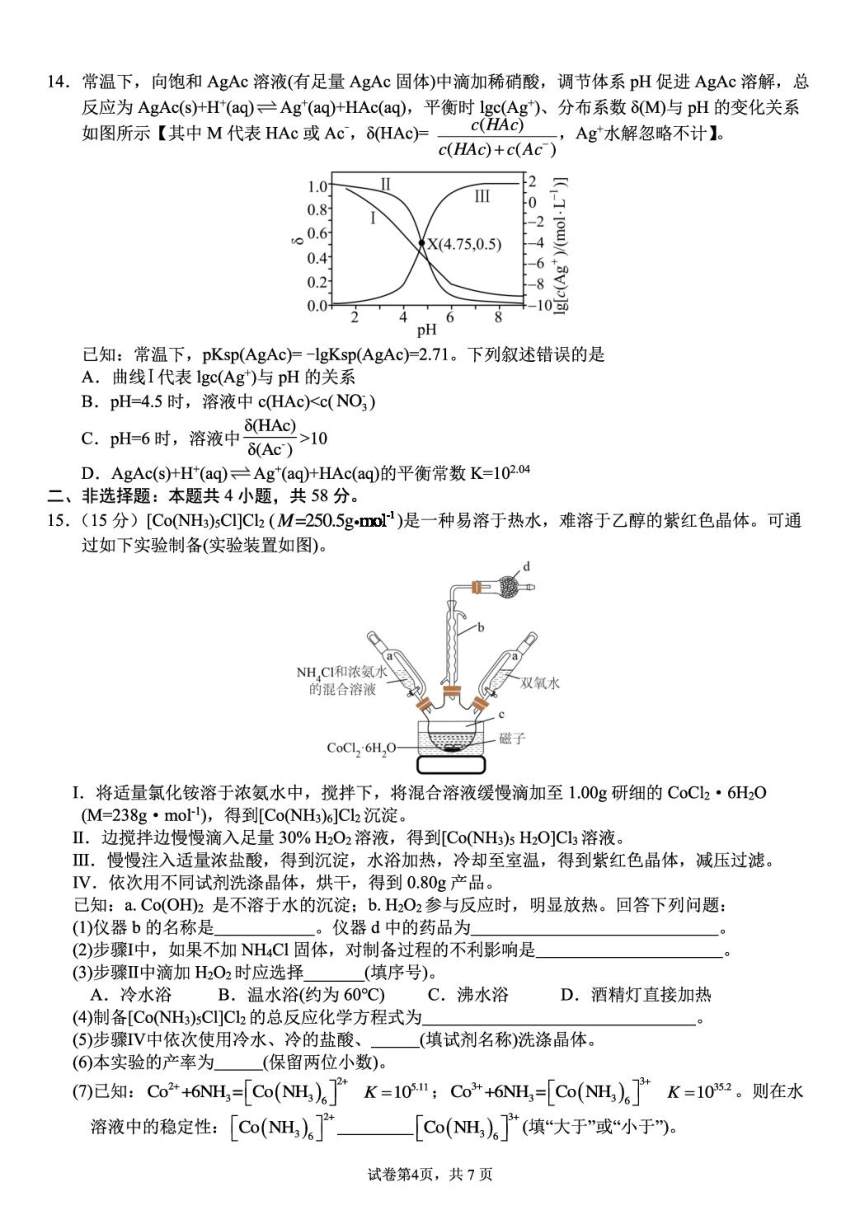
6.硫及其化合物的部分转化关系如图,己知S8分子的8个硫原子以单键连接构成环状结构。下列叙
述正确的是
S02
①
②
S
H,S-
碱,△→S2
A.32g单质S8分子中含S-S键的数目为8NA
B.1L0.1mol/LNa2SO3溶液中,SO的数目为0.1Na
C.反应①海消耗1molS02,转移电子数为2N
D.反应②的氧化产物和还原产物的物质的量之比为1:2
7.前四周期元素X、Y、Z、R、M的原子序数依次增大,同周期中基态Y原子未成对电子数最多,
基态Z原子价层电子排布式为s"m2”。Z和R位于同主族,基态M的d能级达到全充满结构。由
这五种元素组成的化合物M(YX)4]RZ·X,Z为蓝色晶体。下列叙述正确的是
A.原子半径:Z>Y>X
B.第一电离能:Y>Z>R
C.氢化物稳定性:Y
8.丹参是《本草纲目》记载的一味中药,丹参醇是其有效成分,结构简式如图所示。下列关于丹参醇
的说法正确的是
A.分子中含3个手性碳原子
B.消去反应的有机产物最多有2种
C.红外光谱可鉴定有3种含氧官能团
D.lmol该分子最多与5molH2发生加成反应
HO
9.某种可充电固态锂电池放电时工作原理如图所示,下列说法错误的是
HO
a极负超 b极
Li.Co
LiLaZrTaO.与
Li
LiLaZrTaO
Li
LiLaZrTaO固态电解质
A.电极电势:b极>a极
B.放电时电子流向:a极→负载→b极
C.充电时,阳极电极反应为:LiLaZrTaO-xe=xLi计+LiLaZrTaO
D.外电路通过1ol电子时,理论上两电极质量变化差值为7g
10.在浓HNO3和浓H2SO4混合溶液中加入苯,反应过程中能量变化示意图如下。下列说法错误的是
量
过渡态1
过渡态21
过渡态2-2
中间体
O,N.
H
产物H0,S0个
反应物
O,N、H
+HO,SO
+NO;+HO SO
H
O.N
产物Ⅱ
+H,S04
M
反应进程
试卷第2页,共7页
同课章节目录
