人教版高中化学课件必修二 2.1《化学能与热能》PPT课件(共47张PPT)
文档属性
| 名称 | 人教版高中化学课件必修二 2.1《化学能与热能》PPT课件(共47张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-20 00:00:00 | ||
图片预览











文档简介
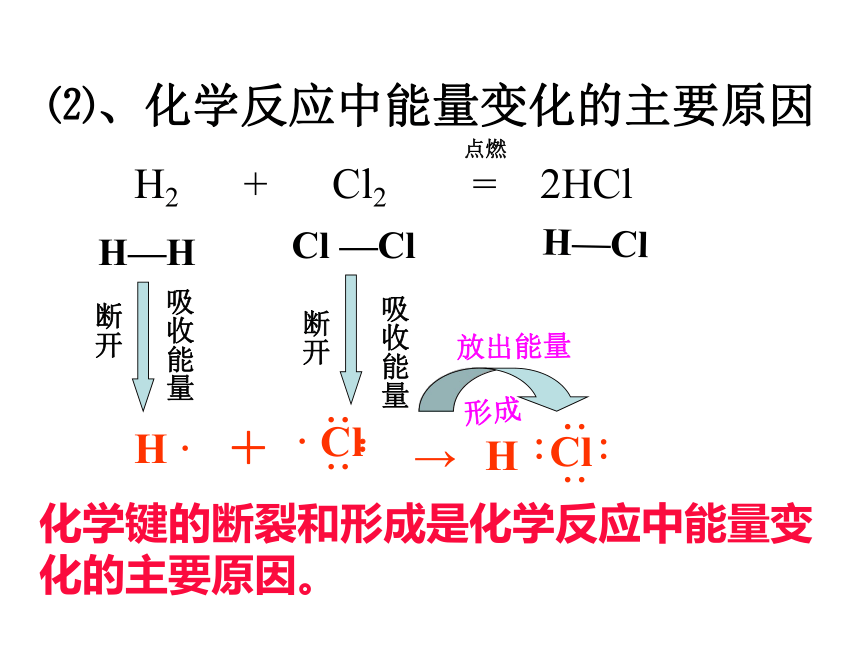
课件47张PPT。化学能与热能能源与人类 能源是人类赖以生存和发展的物质基础,我们每时每刻、分分秒秒都离不开它。迄今为止,人类所能利用的能源主要是化学能、电能、以及核能等等。但是,由于人类大量开发和浪费资源,造成了资源的不合理利用从而引发了不可回避的能源危机。16.6%2.1%5.1%76.2%我国化石燃料和水电能源消耗构成图你知道吗? 煤、石油、天然气的主要化学成分是烃类等有机物(煤中含有大量的碳),它们燃烧时放出热能。你一定想知道,这种能量从何而来?它与化学物质和化学反应有什么关系?石灰石(主要成分是碳酸钙)要经过高温煅烧才能变成生石灰,高温提供的热能在石灰石的分解反应中起到什么作用?一、化学键与化学反应中能量变化的关系思考:不同的燃料其组成不同,燃烧后放出的热量也不相等。为什么不同的燃料燃烧时放出的热量会不同?燃料在燃烧反应中产生的热能来自哪里?1、化学反应中能量的变化⑴、化学反应的本质是什么?以氢气在氯气中燃烧为例,用化学键的观点分析反应的本质过程。H2 + Cl2 = 2HClH—H Cl —ClH—Cl断开断开点燃 一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。形成⑵、化学反应中能量变化的主要原因H2 + Cl2 = 2HClH—H Cl —ClH—Cl吸收能量断开断开吸收能量形成放出能量点燃化学键的断裂和形成是化学反应中能量变化的主要原因。⑶. 从化学键的观点来分析能量的变化所以:一个化学反应是否为放热还是吸热取决于什么呢?取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小想一想:
在化学反应中,随着物质的变化,既有反应物中化学键的断裂,又有生成物中化学键的形成,化学能也随之而改变。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢? 实验测得,在25℃,101KPa条件下,将1molH2(H-H)变为2molH原子需吸收436kJ能量,而2molH原子变成1molH2(H-H)放出436kJ能量,这个能量就是H-H的键能。某些化学键的键能某些键的键能(kJ/mol)对于某个确定的化学反应,如何判断它是放出能量还是吸收能量呢?键能越大含该键的分子越稳定化学键越牢固在反应H2 + Cl2 =2HCl中,已知
H-H 键能为436kJ/mol,Cl-Cl键能为247
kJ/mol,H-Cl键能为431kJ/mol,判断该反应是 反应
放热课堂练习一则(1)化学键断裂时需要吸收能量。吸收总能量为:436kJ+247kJ=683 kJ,
(2)化学键形成时需要释放能量。释放总能量为:431kJ+431kJ=862 kJ,
(3)反应中放出的热量的计算:
862kJ—683kJ=179kJ小结: 一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。看图讨论:分析化学反应:反应物的总能量 > 生成物的总能量化学反应放出能量看图讨论: 将水由低处抽向高处需提供能量
(电能转换为机械能,再转换为势能)分析化学反应:反应物的总能量 < 生成物的总能量化学反应吸收能量反应物的总能量高生成物的总能量低生成物的总能量高反应物的总能量低放热反应吸热反应反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量 化学反应的过程,可以看成是能量的“贮存”或“释放”的过程小结:规律:(1)如果反应物所具有的总能量高于生成物所具有的总能量,那么在发生化学反应时,就有部分能量以热的形式释放出来;
(2)如果反应物所具有的总能量低于生成物所具有的总能量,那么在发生化学反应时,反应物就需要吸收能量,才能转化为生成物。小结:能量公式化E(反应物)=E(生成物)-△H(能量守恒定律)E(生成物)-E(反应物)=△H△H>0为吸热反应△H<0为放热反应二、化学能与热能的相互转化1、两条基本的自然定律(1)质量守恒定律:(2)能量守恒定律:一种能量可以转化为另一种能量,
总能量保持不变。
2、吸热反应和放热反应根据能量变化情况角度分:(1)化学上把有热量放出的化学反应叫做放热反应(2)化学上把吸收热量的化学反应叫做吸热反应(1)放热反应(2)吸热反应小结:规律:练习:1、在化学反应中,断裂化学键需要_______,形成化学键要_________。化学反应是吸热反应还是放热反应决定于_____________________ 吸收能量放出能量反应物的总能量与生成物的总能量的相对大小2、两位同学讨论放热和吸热反应。甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们的说法正确吗?为什么?三、化学能的应用1、利用热量进行生活、生产和科研。
2、利用热能使很多化学反应得以发生。如:小结:实验2-11.铝与盐酸反应的化学方程式: ????????????????????????。
2.在反应过程中你将能看到什么现象?
3.用眼睛不能直接观察到反应中的热量变化,你将采取哪些简单易行的办法来了解反应中的热量变化?
4.要明显的感知或测量反应中的热量变化,你在实验中应注意哪些问题?思考与讨论:实验记录:有气泡冒出,溶液的温度明显升高。铝与盐酸反应的过程放出热量。反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量【课堂小结】问题探究整个反应过程(放出/吸收) kJ热量 13681852放出4842、氢气在氧气中燃烧产生蓝色火焰,在反应中,
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是( )
A. 2Q1 + Q2 > 4Q3 B. 2Q1 + Q2 < 4Q3
C. Q1 + Q2 < Q3 D. Q1 + Q2 = Q3B化学反应热能煤、石油、天然气的燃烧(产生)CaCO3经过高温煅烧分解成CaO(动力)热能对化学反应的支持作用,利用热能来完成常温下很难发生的化学反应。获取能量探索与总结常见的放热反应和吸热反应
放热反应燃料的燃烧(与O2的反应)
中 和 反 应
活泼金属与水或酸的反应
大部分化合反应(生石灰和水)
物质的缓慢氧化吸热反应C+CO2
H2+CuO
C+H2O
Ba(OH)2.8H2O+NH4Cl
CaCO3高温分解
大部分分解反应
多数铵盐溶于水反应过程中的能量变化1、人类文明与能源开发、利用的关系人类文明史引出燃料充分燃烧化石 燃料 合理 利用新技术的开发化学反应中的能量变化能源的利用反映着人类进步2. 常见的能源主要有以下十种:太阳能、化石能源、水能、 风能、潮汐能、地热能、生物质能、核能以 及氢能。1、下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了反应
结果是放热还是吸热
D.吸热反应在一定条件下才能发生反应CD 2、判断:
(1)加热的反应一定是吸热反应。
(2)一个反应是吸热或放热与反应条件
没有直接联系,与反应物与生成物
的总能量的相对大小有关。
(3)化学反应中的能量变化都表现为热
能变化。科学视野1、社会发展与能源利用2、人类利用能源的三个阶段柴草时期化石能源时期多能源结构时期生物体中的能量转化人体内发生的氧化还原反应与体外的燃烧
本质相同,都是放热反应。只是二者条件
不同,且前者更加合理有效。实验2-2有刺激性气味气体产生;玻璃片上的水结成冰,玻璃片与烧杯底被冰粘在了一起;用手触摸杯壁下部,有凉的感觉。Ba(OH)2·8H2O与NH4Cl反应的过程吸收热量。化学反应方程式:
Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑
+10H2O玻璃棒的作用:搅拌,使混合物充分接触反应物成糊状的原因:结冰粘结结论:该反应是吸热反应思考:酸与碱的中和反应是吸热反应还是放热反应?实验2-3 酸碱反应的本质就是H+ + OH- = H2O 。
可得出推论:酸碱中和反应都是放热反应。
反应中H+和OH-离子的量相等 ,生成水的量相等,放出的热量也相等 .中和反应后溶液的温度比反应前盐酸和氢氧化钠溶液的温度高。盐酸和氢氧化钠溶液的反应过程中放出热量,使溶液混合物的温度升高。分析: 中和热的概念:
酸与碱发生中和反应生成1molH2O时所释放的热量称为中和热。
思考与交流:注:(1)中和反应都放出热量
(2)稀溶液中,强酸与强碱的中和
热为定值:57.3KJ/mol思考与交流:
在设计实验装置和操作时应该注意哪些问题?(1)用隔热装置,尽量减少热量散失;(2)酸碱的量要准确:n=C×Va、浓度要越精确越好
b、量体积的容器越精确越好,最好用移液管(3)温度计越精确越好(4)注意控制反应时间(5)多做几次,取平均值 在设计实验装置和操作时应从两个方面考虑,一是注重“量”的问题,如① 反应物的浓度和体积取定值;② 测量反应前后的温度值;③ 做平行实验取平均值。二是尽量减小实验误差,如① 用经过标定的盐酸和氢氧化钠溶液;② 量液器最好使用移液管;③ 搅拌使反应充分进行;④ 及时散热,使混合液温度均衡;⑤ 温度计的精确度高,最好使用精度为0.1 ℃或更高的温度计;⑥ 盐酸跟氢氧化钠溶液混合后液面上方的空间尽可能小;⑦ 使用绝缘装置,避免热量散发到反应体系之外;⑧ 温度计要读准确。1L1mol/L的硫酸溶液与2L2mol/L的NaOH溶液完全反应,放出114.6KJ的热量,有人由此得出强酸与强碱反应的中和热为114.6KJ/mol。这种结论是否正确,为什么?
形成新键放出的总能量的相对大小想一想:
在化学反应中,随着物质的变化,既有反应物中化学键的断裂,又有生成物中化学键的形成,化学能也随之而改变。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢? 实验测得,在25℃,101KPa条件下,将1molH2(H-H)变为2molH原子需吸收436kJ能量,而2molH原子变成1molH2(H-H)放出436kJ能量,这个能量就是H-H的键能。某些化学键的键能某些键的键能(kJ/mol)对于某个确定的化学反应,如何判断它是放出能量还是吸收能量呢?键能越大含该键的分子越稳定化学键越牢固在反应H2 + Cl2 =2HCl中,已知
H-H 键能为436kJ/mol,Cl-Cl键能为247
kJ/mol,H-Cl键能为431kJ/mol,判断该反应是 反应
放热课堂练习一则(1)化学键断裂时需要吸收能量。吸收总能量为:436kJ+247kJ=683 kJ,
(2)化学键形成时需要释放能量。释放总能量为:431kJ+431kJ=862 kJ,
(3)反应中放出的热量的计算:
862kJ—683kJ=179kJ小结: 一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。看图讨论:分析化学反应:反应物的总能量 > 生成物的总能量化学反应放出能量看图讨论: 将水由低处抽向高处需提供能量
(电能转换为机械能,再转换为势能)分析化学反应:反应物的总能量 < 生成物的总能量化学反应吸收能量反应物的总能量高生成物的总能量低生成物的总能量高反应物的总能量低放热反应吸热反应反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量 化学反应的过程,可以看成是能量的“贮存”或“释放”的过程小结:规律:(1)如果反应物所具有的总能量高于生成物所具有的总能量,那么在发生化学反应时,就有部分能量以热的形式释放出来;
(2)如果反应物所具有的总能量低于生成物所具有的总能量,那么在发生化学反应时,反应物就需要吸收能量,才能转化为生成物。小结:能量公式化E(反应物)=E(生成物)-△H(能量守恒定律)E(生成物)-E(反应物)=△H△H>0为吸热反应△H<0为放热反应二、化学能与热能的相互转化1、两条基本的自然定律(1)质量守恒定律:(2)能量守恒定律:一种能量可以转化为另一种能量,
总能量保持不变。
2、吸热反应和放热反应根据能量变化情况角度分:(1)化学上把有热量放出的化学反应叫做放热反应(2)化学上把吸收热量的化学反应叫做吸热反应(1)放热反应(2)吸热反应小结:规律:练习:1、在化学反应中,断裂化学键需要_______,形成化学键要_________。化学反应是吸热反应还是放热反应决定于_____________________ 吸收能量放出能量反应物的总能量与生成物的总能量的相对大小2、两位同学讨论放热和吸热反应。甲说加热后才能发生的化学反应是吸热反应,乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们的说法正确吗?为什么?三、化学能的应用1、利用热量进行生活、生产和科研。
2、利用热能使很多化学反应得以发生。如:小结:实验2-11.铝与盐酸反应的化学方程式: ????????????????????????。
2.在反应过程中你将能看到什么现象?
3.用眼睛不能直接观察到反应中的热量变化,你将采取哪些简单易行的办法来了解反应中的热量变化?
4.要明显的感知或测量反应中的热量变化,你在实验中应注意哪些问题?思考与讨论:实验记录:有气泡冒出,溶液的温度明显升高。铝与盐酸反应的过程放出热量。反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量【课堂小结】问题探究整个反应过程(放出/吸收) kJ热量 13681852放出4842、氢气在氧气中燃烧产生蓝色火焰,在反应中,
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是( )
A. 2Q1 + Q2 > 4Q3 B. 2Q1 + Q2 < 4Q3
C. Q1 + Q2 < Q3 D. Q1 + Q2 = Q3B化学反应热能煤、石油、天然气的燃烧(产生)CaCO3经过高温煅烧分解成CaO(动力)热能对化学反应的支持作用,利用热能来完成常温下很难发生的化学反应。获取能量探索与总结常见的放热反应和吸热反应
放热反应燃料的燃烧(与O2的反应)
中 和 反 应
活泼金属与水或酸的反应
大部分化合反应(生石灰和水)
物质的缓慢氧化吸热反应C+CO2
H2+CuO
C+H2O
Ba(OH)2.8H2O+NH4Cl
CaCO3高温分解
大部分分解反应
多数铵盐溶于水反应过程中的能量变化1、人类文明与能源开发、利用的关系人类文明史引出燃料充分燃烧化石 燃料 合理 利用新技术的开发化学反应中的能量变化能源的利用反映着人类进步2. 常见的能源主要有以下十种:太阳能、化石能源、水能、 风能、潮汐能、地热能、生物质能、核能以 及氢能。1、下列说法正确的是( )
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了反应
结果是放热还是吸热
D.吸热反应在一定条件下才能发生反应CD 2、判断:
(1)加热的反应一定是吸热反应。
(2)一个反应是吸热或放热与反应条件
没有直接联系,与反应物与生成物
的总能量的相对大小有关。
(3)化学反应中的能量变化都表现为热
能变化。科学视野1、社会发展与能源利用2、人类利用能源的三个阶段柴草时期化石能源时期多能源结构时期生物体中的能量转化人体内发生的氧化还原反应与体外的燃烧
本质相同,都是放热反应。只是二者条件
不同,且前者更加合理有效。实验2-2有刺激性气味气体产生;玻璃片上的水结成冰,玻璃片与烧杯底被冰粘在了一起;用手触摸杯壁下部,有凉的感觉。Ba(OH)2·8H2O与NH4Cl反应的过程吸收热量。化学反应方程式:
Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑
+10H2O玻璃棒的作用:搅拌,使混合物充分接触反应物成糊状的原因:结冰粘结结论:该反应是吸热反应思考:酸与碱的中和反应是吸热反应还是放热反应?实验2-3 酸碱反应的本质就是H+ + OH- = H2O 。
可得出推论:酸碱中和反应都是放热反应。
反应中H+和OH-离子的量相等 ,生成水的量相等,放出的热量也相等 .中和反应后溶液的温度比反应前盐酸和氢氧化钠溶液的温度高。盐酸和氢氧化钠溶液的反应过程中放出热量,使溶液混合物的温度升高。分析: 中和热的概念:
酸与碱发生中和反应生成1molH2O时所释放的热量称为中和热。
思考与交流:注:(1)中和反应都放出热量
(2)稀溶液中,强酸与强碱的中和
热为定值:57.3KJ/mol思考与交流:
在设计实验装置和操作时应该注意哪些问题?(1)用隔热装置,尽量减少热量散失;(2)酸碱的量要准确:n=C×Va、浓度要越精确越好
b、量体积的容器越精确越好,最好用移液管(3)温度计越精确越好(4)注意控制反应时间(5)多做几次,取平均值 在设计实验装置和操作时应从两个方面考虑,一是注重“量”的问题,如① 反应物的浓度和体积取定值;② 测量反应前后的温度值;③ 做平行实验取平均值。二是尽量减小实验误差,如① 用经过标定的盐酸和氢氧化钠溶液;② 量液器最好使用移液管;③ 搅拌使反应充分进行;④ 及时散热,使混合液温度均衡;⑤ 温度计的精确度高,最好使用精度为0.1 ℃或更高的温度计;⑥ 盐酸跟氢氧化钠溶液混合后液面上方的空间尽可能小;⑦ 使用绝缘装置,避免热量散发到反应体系之外;⑧ 温度计要读准确。1L1mol/L的硫酸溶液与2L2mol/L的NaOH溶液完全反应,放出114.6KJ的热量,有人由此得出强酸与强碱反应的中和热为114.6KJ/mol。这种结论是否正确,为什么?
