四川省绵阳市三台县2024-2025学年高二下学期期中考试化学试卷(PDF版,含答案)
文档属性
| 名称 | 四川省绵阳市三台县2024-2025学年高二下学期期中考试化学试卷(PDF版,含答案) |

|
|
| 格式 | |||
| 文件大小 | 530.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-09 00:00:00 | ||
图片预览



文档简介
三台县 2024 年春高二半期教学质量调研测试
化学试题
本试卷分为试题卷和答题卷两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)组成,共 6页;答题
卷共 2页。满分 100分,考试时间 75分钟。
第Ⅰ卷(选择题,共 42 分)
可能用到的相对原于质量:H-1 C-12 O-16 Si-28 Ga-70 As-75
注意事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、考号准确填写在答题卡上。
2.每小题选出答案后,用铅笔把答题卷上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后再选涂其
它答案,不能答在试题卷上。
一、选择题(本题共 14小题,每小题 3 分,共 42 分。每小题只有一个选项符合题意)
1.下列表示不正确的是
A.甲烷的空间填充模型: B.乙烯的球棍模型:
C.乙炔的结构简式:CHCH D.戊烷的分子式:C5H12
2.有六种物质:①甲烷 ②苯 ③聚乙烯 ④SO2 ⑤2-丁炔 ⑥环己烯,既能使酸性高锰酸钾溶
液褪色,又能使溴水因反应而褪色的是
A.②④⑤ B.③④⑤ C.③⑤⑥ D.④⑤⑥
3.某气态烃 0.5mol能与 1mol HCl完全加成,加成后产物分子上的氢原子可又被 3mol Cl2取代,
则此气态烃可能是
A. CH3-CH3 B. CH2=C(CH3)2 C. CH≡CH D. CH≡C-CH3
4.下列关于物质性质的比较错误的是
A.沸点:H2O>H2S>H2Se B.熔点: NaF>NaCl>NaBr>NaI
C.硬度:金刚石>碳化硅>晶体硅 D.沸点:正戊烷>异戊烷>新戊烷
5.设 NA为阿伏伽德罗常数的值,下列有关说法正确的是
A.14g乙烯和环丙烷的混合物中含 C-H键的数目为 2NA
B.标准状况下,2.24L苯的分子数为 0.1NA
C.12 g石墨中含有的 C-C键的数目为 2 NA
D.60 g SiO2中含 Si-O键的数目为 2 NA
6.下列有关同分异构体数目(不考虑立体异构)的判断正确的是
A CH. 3 的一溴代物有 4种 B.分子式为 C3H6Cl2的有机物共有 5种
C.C8H10含苯环的同分异构体有 3种 D.C5H10属于烯烃共有 5种
高二化学(第 1 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
7.向盛有硫酸锌水溶液的试管中加入氨水,首先形成沉淀,继续滴加氨水, 沉淀溶解得到无色
透明的溶液。下列说法正确的是
A.最后所得溶液中不存在沉淀,所以反应前后 c (Zn2+)不变
B.沉淀溶解是因为生成了无色的配离子[Zn(NH3)4]2+
C.用硝酸锌溶液代替硫酸锌溶液进行实验,不能观察到同样的现象
D.在[Zn(NH3)4]2+配离子中 Zn2+提供孤对电子,NH3提供空轨道
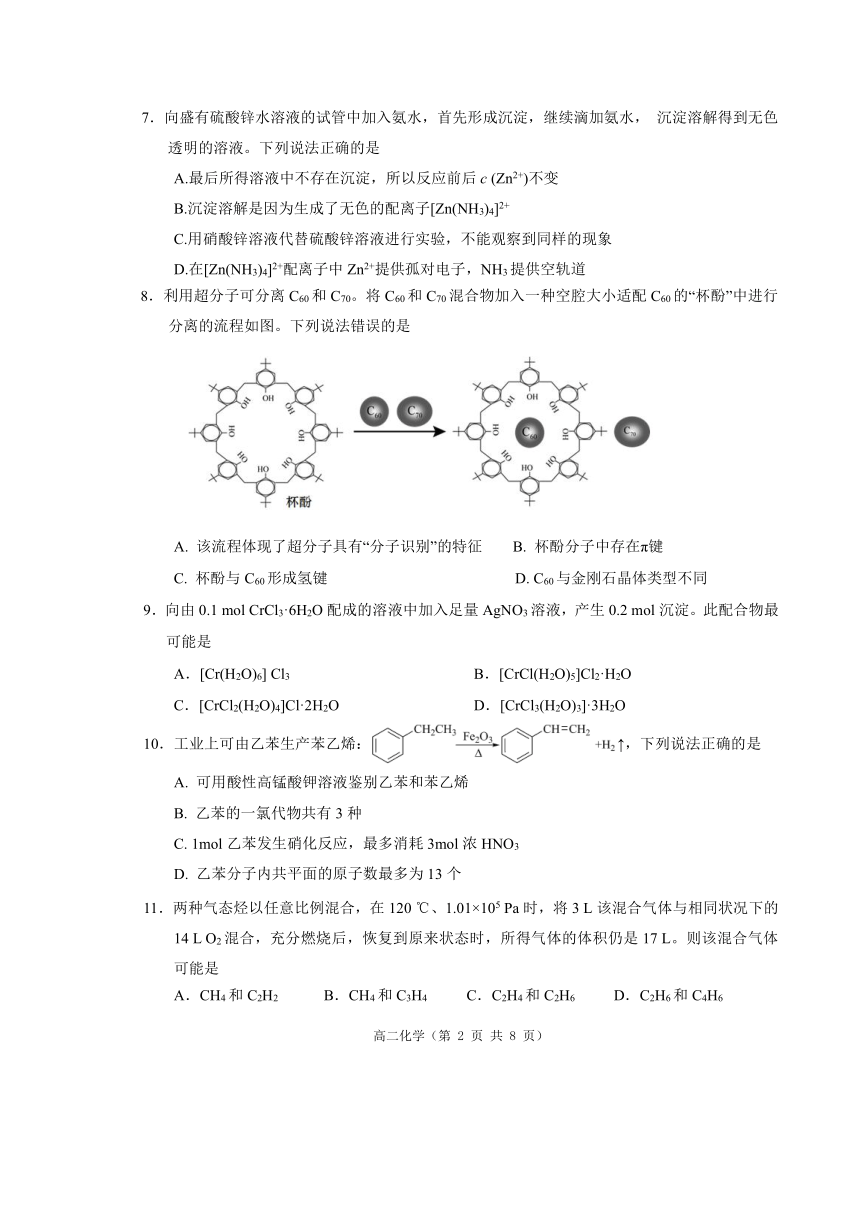
8.利用超分子可分离 C60和 C70。将 C60和 C70混合物加入一种空腔大小适配 C60的“杯酚”中进行
分离的流程如图。下列说法错误的是
A. 该流程体现了超分子具有“分子识别”的特征 B. 杯酚分子中存在π键
C. 杯酚与 C60形成氢键 D. C60与金刚石晶体类型不同
9.向由 0.1 mol CrCl3·6H2O配成的溶液中加入足量 AgNO3溶液,产生 0.2 mol沉淀。此配合物最
可能是
A.[Cr(H2O)6] Cl3 B.[CrCl(H2O)5]Cl2·H2O
C.[CrCl2(H2O)4]Cl·2H2O D.[CrCl3(H2O)3]·3H2O
10.工业上可由乙苯生产苯乙烯: ↑,下列说法正确的是
A. 可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯
B. 乙苯的一氯代物共有 3种
C. 1mol乙苯发生硝化反应,最多消耗 3mol浓 HNO3
D. 乙苯分子内共平面的原子数最多为 13个
11.两种气态烃以任意比例混合,在 120℃、1.01×105 Pa时,将 3 L该混合气体与相同状况下的
14 L O2混合,充分燃烧后,恢复到原来状态时,所得气体的体积仍是 17 L。则该混合气体
可能是
A.CH4和 C2H2 B.CH4和 C3H4 C.C2H4和 C2H6 D.C2H6和 C4H6
高二化学(第 2 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
12.下列实验方案不能达到实验目的是
序号 实验目的 实验方案
验证乙炔能被酸性高锰酸 将电石与饱和食盐水反应生成的气体通入酸性高锰
A
钾溶液氧化 酸钾溶液,观察溶液是否褪色
先加入过量 NaOH 溶液后蒸出乙醇,再加入过量
B 分离乙醇和乙酸
H2SO4后蒸出乙酸
证明溴乙烷发生消去反应 向试管中加入适量的溴乙烷和 NaOH的乙醇溶液,
C
有乙烯生成 加热,将反应产生的气体通入溴的四氯化碳溶液
检验卤代烃中卤原子的种 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液滴
D
类 加硝酸酸化后滴加硝酸银溶液
13.某有机化合物 X经元素分析测定,各元素的质量分数是:碳 70.6%、氢 5.9%、氧 23.5%,X
的核磁共振氢谱有 4个峰且面积之比为 3∶2∶2∶1,X分子中只含一个苯环且苯环上只有一
个取代基,其质谱图、核磁共振氢谱与红外光谱如图。关于 X的下列叙述错误的是
A.X的相对分子质量为 136
B.X的分子式为 C8H8O2
C.X分子中所有的原子可能在同一个平面上
D COOCH.符合题中 X分子结构的有机物的结构简式可能为 3
14.有一种蓝色晶体可表示为[MxFey(CN)6],经 X-射线研究发现,它的结构特征是 Fe3+和 Fe2+互
相占据立方体互不相邻的顶点,而 CN-位于立方体的棱上。其晶体中阴离子的最小结构单元
如图所示。下列说法不正确的是
A. 该晶体属于离子晶体
B. 该晶体的化学式为MFe2(CN)6
C. 该晶体中M呈+2价
D. -晶体中与每个 Fe3+距离最近且等距离的 CN 为 6个
高二化学(第 3 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
第Ⅱ卷(非选择题,共 58 分)
注意事项: 用钢笔或圆珠笔(蓝或黑色)将答案写在答题卷上。
二、填空题(本题包括 4个小题,共 58分)
15.(18分) I.现有下列有机化合物,请按要求回答下列问题。
A.CH3CH=CHCH3 B. C. D.CH≡CH
E. F. G . H .
(1)用系统命名法命名,C: ,
F: 。
(2)上述有机物中互为同系物的是 (填字母)。
(3)上述有机物中互为同分异构体的是 (填字母)。
(4)写出 A的顺式结构的结构简式 。
(5)写出实验室制备 D的化学方程式 。
(6)写出 H与液溴反应的化学方程式 。
II.某烷烃的结构简式为。
(7)若该烷烃是由烯烃和 1 mol H2加成得到的,则原烯烃可能有 种结构。(不
包括立体异构)
(8)戊二醇与该烷烃的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成
该差异的原因是 。
16.(12分)已知:CH3 CH CH2 HBr CH3 CHBr CH3 (主要产物),1mol某芳香烃 A相
对分子质量为 104。该烃 A在不同条件下能发生如下图所示的一系列变化。
高二化学(第 4 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
(1)A的分子式: 。
(2)上述反应中,①是 反应,②是 反应。(填反应类型)
(3)写出 C、E物质的结构简式:
C ,E 。
(4)写出有关反应的化学方程式:
① ;
⑥ 。
17.(11分)青蒿素为无色针状晶体,熔点为 156~157℃,易溶于丙酮、氯仿和苯,在水中几乎
不溶。
Ⅰ.实验室用乙醚提取青蒿素的工艺流程如图所示。
(1)在操作 i前要对青蒿进行粉碎,其目的是 。
(2)操作 ii的名称是 。
(3)操作 iii涉及重结晶,则操作 iii的步骤为加热溶解、 、过滤、
洗涤、干燥。
Ⅱ.已知青蒿素是一种烃的含氧衍生物,某同学为确定其化学式,进行如图实验:
氧气
实验步骤:
高二化学(第 5 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
①按图所示连接装置,检查装置的气密性;②称量装置 E、F 中仪器及试剂的质量;③取
14.10g青蒿素放入硬质玻璃管 C中,点燃装置 C、D处的酒精灯;④实验结束后冷却至室温,称
量装置 E、F中仪器及试剂的质量。
(4)装置 E、F应装入的试剂分别为 、 。
(5)实验测得数据如表:
装置 实验前 实验后
E 24.00g 33.90g
F 100.00g 133.00g
通过质谱仪测得青蒿素的相对分子质量为 282,结合上述数据,得出青蒿素的分子式
为 。
(6)某同学认为使用上述方法会产生较大实验误差,你的优化方案是 。
18.(17分)常见的电池有碳、氢、氧等元素组成的燃料电池,还有 GaAs太阳能电池及铜铟镓
硒薄膜太阳能电池等。
(1)已知 GaCl3晶体熔点为 77.9℃,沸点为 201.3℃,则 GaCl3晶体类型为 。
(2)在配合物[Cu(NH3)4]SO4·H2O中 是中心离子, 是配位
原子, [Cu(NH3)4]2+的结构式为 。1mol 该物质中含σ键数目
为 。该物质中含有的化学键类型为 (填选项)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
(3)写出氢氧化铜溶于氨水的离子方程式 。
(4)砷化镓晶胞结构如图。
①砷化镓晶胞中 Ga原子的数目为 。
②晶体中与 Ga最近且等距离的 As数目为 。
③已知晶体的棱长为 a pm,则 GaAs晶体的密度为 g·cm-3。(用 NA表示阿伏加德
罗常数的值)
高二化学(第 6 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
三台县 2024 年春高二半期教学质量调研测试
参考答案 化学
一、单选题(每题 3分,本题共 14小题,共 42分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
选项 C D D A A D B C B C B A C C
二、填空题(除标注外,每空 2分,共 58分)
15.(18分)
(1) 2-甲基-2-丁烯 2,2,4-三甲基戊烷 (2) A和 C ;B和 F (3)CE
(4)
(5)CaC2+2H2O Ca(OH)2+CH≡CH↑
(6) (7)5
(8)戊二醇分子间存在氢键,但 2,3-二甲基戊烷分子间不存在氢键
16.(12分)
(1)C8H8 (2)①加成(1分) ②消去 (1分)
(3)
(4)①
②
17.(11分)
(1)增大青蒿与乙醚的接触面积,提高青蒿素的浸出率 (2)蒸馏(1分)
(3)趁热过滤、冷却结晶 (4)无水氯化钙(或五氧化二磷等)(1分) 碱石灰(1分)
(5)C15H22O5 (6)在装置 F右侧增防止空气中二氧化碳、水蒸气进入 F的装置(合理均
可)
18.(17分)
(1)分子晶体(1分)
(2)Cu2+(1分) N(1分) 22 NA BCD
高二化学(第 7 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
(3) 或
58 304 4 4 --0--×- 10( )① ② ③ a3N--------A
高二化学(第 8 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
化学试题
本试卷分为试题卷和答题卷两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)组成,共 6页;答题
卷共 2页。满分 100分,考试时间 75分钟。
第Ⅰ卷(选择题,共 42 分)
可能用到的相对原于质量:H-1 C-12 O-16 Si-28 Ga-70 As-75
注意事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、考号准确填写在答题卡上。
2.每小题选出答案后,用铅笔把答题卷上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后再选涂其
它答案,不能答在试题卷上。
一、选择题(本题共 14小题,每小题 3 分,共 42 分。每小题只有一个选项符合题意)
1.下列表示不正确的是
A.甲烷的空间填充模型: B.乙烯的球棍模型:
C.乙炔的结构简式:CHCH D.戊烷的分子式:C5H12
2.有六种物质:①甲烷 ②苯 ③聚乙烯 ④SO2 ⑤2-丁炔 ⑥环己烯,既能使酸性高锰酸钾溶
液褪色,又能使溴水因反应而褪色的是
A.②④⑤ B.③④⑤ C.③⑤⑥ D.④⑤⑥
3.某气态烃 0.5mol能与 1mol HCl完全加成,加成后产物分子上的氢原子可又被 3mol Cl2取代,
则此气态烃可能是
A. CH3-CH3 B. CH2=C(CH3)2 C. CH≡CH D. CH≡C-CH3
4.下列关于物质性质的比较错误的是
A.沸点:H2O>H2S>H2Se B.熔点: NaF>NaCl>NaBr>NaI
C.硬度:金刚石>碳化硅>晶体硅 D.沸点:正戊烷>异戊烷>新戊烷
5.设 NA为阿伏伽德罗常数的值,下列有关说法正确的是
A.14g乙烯和环丙烷的混合物中含 C-H键的数目为 2NA
B.标准状况下,2.24L苯的分子数为 0.1NA
C.12 g石墨中含有的 C-C键的数目为 2 NA
D.60 g SiO2中含 Si-O键的数目为 2 NA
6.下列有关同分异构体数目(不考虑立体异构)的判断正确的是
A CH. 3 的一溴代物有 4种 B.分子式为 C3H6Cl2的有机物共有 5种
C.C8H10含苯环的同分异构体有 3种 D.C5H10属于烯烃共有 5种
高二化学(第 1 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
7.向盛有硫酸锌水溶液的试管中加入氨水,首先形成沉淀,继续滴加氨水, 沉淀溶解得到无色
透明的溶液。下列说法正确的是
A.最后所得溶液中不存在沉淀,所以反应前后 c (Zn2+)不变
B.沉淀溶解是因为生成了无色的配离子[Zn(NH3)4]2+
C.用硝酸锌溶液代替硫酸锌溶液进行实验,不能观察到同样的现象
D.在[Zn(NH3)4]2+配离子中 Zn2+提供孤对电子,NH3提供空轨道
8.利用超分子可分离 C60和 C70。将 C60和 C70混合物加入一种空腔大小适配 C60的“杯酚”中进行
分离的流程如图。下列说法错误的是
A. 该流程体现了超分子具有“分子识别”的特征 B. 杯酚分子中存在π键
C. 杯酚与 C60形成氢键 D. C60与金刚石晶体类型不同
9.向由 0.1 mol CrCl3·6H2O配成的溶液中加入足量 AgNO3溶液,产生 0.2 mol沉淀。此配合物最
可能是
A.[Cr(H2O)6] Cl3 B.[CrCl(H2O)5]Cl2·H2O
C.[CrCl2(H2O)4]Cl·2H2O D.[CrCl3(H2O)3]·3H2O
10.工业上可由乙苯生产苯乙烯: ↑,下列说法正确的是
A. 可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯
B. 乙苯的一氯代物共有 3种
C. 1mol乙苯发生硝化反应,最多消耗 3mol浓 HNO3
D. 乙苯分子内共平面的原子数最多为 13个
11.两种气态烃以任意比例混合,在 120℃、1.01×105 Pa时,将 3 L该混合气体与相同状况下的
14 L O2混合,充分燃烧后,恢复到原来状态时,所得气体的体积仍是 17 L。则该混合气体
可能是
A.CH4和 C2H2 B.CH4和 C3H4 C.C2H4和 C2H6 D.C2H6和 C4H6
高二化学(第 2 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
12.下列实验方案不能达到实验目的是
序号 实验目的 实验方案
验证乙炔能被酸性高锰酸 将电石与饱和食盐水反应生成的气体通入酸性高锰
A
钾溶液氧化 酸钾溶液,观察溶液是否褪色
先加入过量 NaOH 溶液后蒸出乙醇,再加入过量
B 分离乙醇和乙酸
H2SO4后蒸出乙酸
证明溴乙烷发生消去反应 向试管中加入适量的溴乙烷和 NaOH的乙醇溶液,
C
有乙烯生成 加热,将反应产生的气体通入溴的四氯化碳溶液
检验卤代烃中卤原子的种 将溴乙烷与氢氧化钠溶液共热,取冷却后反应液滴
D
类 加硝酸酸化后滴加硝酸银溶液
13.某有机化合物 X经元素分析测定,各元素的质量分数是:碳 70.6%、氢 5.9%、氧 23.5%,X
的核磁共振氢谱有 4个峰且面积之比为 3∶2∶2∶1,X分子中只含一个苯环且苯环上只有一
个取代基,其质谱图、核磁共振氢谱与红外光谱如图。关于 X的下列叙述错误的是
A.X的相对分子质量为 136
B.X的分子式为 C8H8O2
C.X分子中所有的原子可能在同一个平面上
D COOCH.符合题中 X分子结构的有机物的结构简式可能为 3
14.有一种蓝色晶体可表示为[MxFey(CN)6],经 X-射线研究发现,它的结构特征是 Fe3+和 Fe2+互
相占据立方体互不相邻的顶点,而 CN-位于立方体的棱上。其晶体中阴离子的最小结构单元
如图所示。下列说法不正确的是
A. 该晶体属于离子晶体
B. 该晶体的化学式为MFe2(CN)6
C. 该晶体中M呈+2价
D. -晶体中与每个 Fe3+距离最近且等距离的 CN 为 6个
高二化学(第 3 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
第Ⅱ卷(非选择题,共 58 分)
注意事项: 用钢笔或圆珠笔(蓝或黑色)将答案写在答题卷上。
二、填空题(本题包括 4个小题,共 58分)
15.(18分) I.现有下列有机化合物,请按要求回答下列问题。
A.CH3CH=CHCH3 B. C. D.CH≡CH
E. F. G . H .
(1)用系统命名法命名,C: ,
F: 。
(2)上述有机物中互为同系物的是 (填字母)。
(3)上述有机物中互为同分异构体的是 (填字母)。
(4)写出 A的顺式结构的结构简式 。
(5)写出实验室制备 D的化学方程式 。
(6)写出 H与液溴反应的化学方程式 。
II.某烷烃的结构简式为。
(7)若该烷烃是由烯烃和 1 mol H2加成得到的,则原烯烃可能有 种结构。(不
包括立体异构)
(8)戊二醇与该烷烃的相对分子质量和范德华力均相近,但是二者的沸点相差很大,造成
该差异的原因是 。
16.(12分)已知:CH3 CH CH2 HBr CH3 CHBr CH3 (主要产物),1mol某芳香烃 A相
对分子质量为 104。该烃 A在不同条件下能发生如下图所示的一系列变化。
高二化学(第 4 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
(1)A的分子式: 。
(2)上述反应中,①是 反应,②是 反应。(填反应类型)
(3)写出 C、E物质的结构简式:
C ,E 。
(4)写出有关反应的化学方程式:
① ;
⑥ 。
17.(11分)青蒿素为无色针状晶体,熔点为 156~157℃,易溶于丙酮、氯仿和苯,在水中几乎
不溶。
Ⅰ.实验室用乙醚提取青蒿素的工艺流程如图所示。
(1)在操作 i前要对青蒿进行粉碎,其目的是 。
(2)操作 ii的名称是 。
(3)操作 iii涉及重结晶,则操作 iii的步骤为加热溶解、 、过滤、
洗涤、干燥。
Ⅱ.已知青蒿素是一种烃的含氧衍生物,某同学为确定其化学式,进行如图实验:
氧气
实验步骤:
高二化学(第 5 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
①按图所示连接装置,检查装置的气密性;②称量装置 E、F 中仪器及试剂的质量;③取
14.10g青蒿素放入硬质玻璃管 C中,点燃装置 C、D处的酒精灯;④实验结束后冷却至室温,称
量装置 E、F中仪器及试剂的质量。
(4)装置 E、F应装入的试剂分别为 、 。
(5)实验测得数据如表:
装置 实验前 实验后
E 24.00g 33.90g
F 100.00g 133.00g
通过质谱仪测得青蒿素的相对分子质量为 282,结合上述数据,得出青蒿素的分子式
为 。
(6)某同学认为使用上述方法会产生较大实验误差,你的优化方案是 。
18.(17分)常见的电池有碳、氢、氧等元素组成的燃料电池,还有 GaAs太阳能电池及铜铟镓
硒薄膜太阳能电池等。
(1)已知 GaCl3晶体熔点为 77.9℃,沸点为 201.3℃,则 GaCl3晶体类型为 。
(2)在配合物[Cu(NH3)4]SO4·H2O中 是中心离子, 是配位
原子, [Cu(NH3)4]2+的结构式为 。1mol 该物质中含σ键数目
为 。该物质中含有的化学键类型为 (填选项)。
A.金属键 B.离子键 C.共价键 D.配位键 E.氢键
(3)写出氢氧化铜溶于氨水的离子方程式 。
(4)砷化镓晶胞结构如图。
①砷化镓晶胞中 Ga原子的数目为 。
②晶体中与 Ga最近且等距离的 As数目为 。
③已知晶体的棱长为 a pm,则 GaAs晶体的密度为 g·cm-3。(用 NA表示阿伏加德
罗常数的值)
高二化学(第 6 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
三台县 2024 年春高二半期教学质量调研测试
参考答案 化学
一、单选题(每题 3分,本题共 14小题,共 42分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
选项 C D D A A D B C B C B A C C
二、填空题(除标注外,每空 2分,共 58分)
15.(18分)
(1) 2-甲基-2-丁烯 2,2,4-三甲基戊烷 (2) A和 C ;B和 F (3)CE
(4)
(5)CaC2+2H2O Ca(OH)2+CH≡CH↑
(6) (7)5
(8)戊二醇分子间存在氢键,但 2,3-二甲基戊烷分子间不存在氢键
16.(12分)
(1)C8H8 (2)①加成(1分) ②消去 (1分)
(3)
(4)①
②
17.(11分)
(1)增大青蒿与乙醚的接触面积,提高青蒿素的浸出率 (2)蒸馏(1分)
(3)趁热过滤、冷却结晶 (4)无水氯化钙(或五氧化二磷等)(1分) 碱石灰(1分)
(5)C15H22O5 (6)在装置 F右侧增防止空气中二氧化碳、水蒸气进入 F的装置(合理均
可)
18.(17分)
(1)分子晶体(1分)
(2)Cu2+(1分) N(1分) 22 NA BCD
高二化学(第 7 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
(3) 或
58 304 4 4 --0--×- 10( )① ② ③ a3N--------A
高二化学(第 8 页 共 8 页)
{#{QQABZYSh4wiwgIZACZ6bAUHkCkqQkJESLYomAQAIKAwKgRFABCA=}#}
同课章节目录
