人教版高中化学课件必修二 2.1 化学能与热能(共77张PPT)
文档属性
| 名称 | 人教版高中化学课件必修二 2.1 化学能与热能(共77张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-20 00:00:00 | ||
图片预览











文档简介
课件77张PPT。新课标人教版化学必修Ⅱ 第二章 第一节 化学能与热能
(第1课时)学习目标知道化学键的断裂和形成是化学反应中能量变化的主要原因。
通过生产、生活中的实例了解化学能与热能的相互转化。
探究化学能转化为热能在生产、生活中的应用。
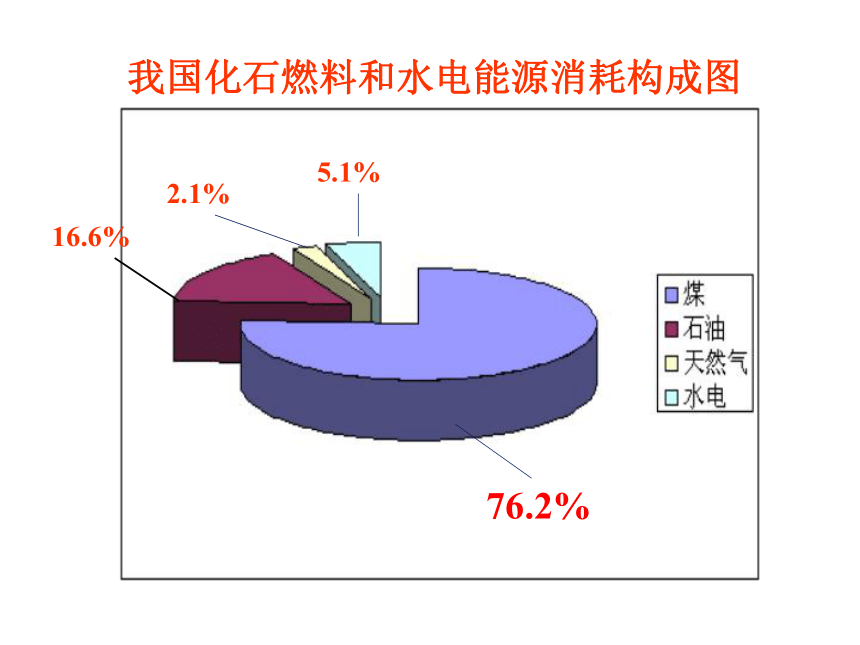
课题引入能源与人类 能源是人类赖以生存和发展的物质基础,我们每时每刻、分分秒秒都离不开它。迄今为止,人类所能利用的能源主要是化学能、电能、以及核能等等。但是,由于人类大量开发和浪费资源,造成了资源的不合理利用从而引发了不可回避的能源危机。我国化石燃料和水电能源消耗构成图16.6%2.1%5.1%76.2%你知道吗? 煤、石油、天然气的主要化学成分是烃类等有机物(煤中含有大量的碳),它们燃烧时放出热能。你一定想知道,这种能量从何而来?它与化学物质和化学反应有什么关系?石灰石(主要成分是碳酸钙)要经过高温煅烧才能变成生石灰,高温提供的热能在石灰石的分解反应中起到什么作用?一飞冲天:“神舟”五号发射实况回放 生活中哪些事实说明了在化学反应中伴随着能量的变化?【思考与交流】物质发生化学反应的同时还伴随着能量的变化,而这种能量变化又通常表现为热能变化。第一节 化学能与热能一、化学键与化学反应中能量变化的关系1、化学反应的本质是?
以氢气在氯气中燃烧为例,用化学键的观点分析反应的本质过程。H2 + Cl2 = 2HClH—H Cl —ClH—Cl断开断开点燃 一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。形成H2 + Cl2 = 2HClH—H Cl —ClH—Cl吸收能量断开断开吸收能量形成放出能量点燃化学键的断裂和形成是化学反应中能量变化的主要原因。【思考与交流】在化学反应中,随着物质的变化,既有反应物中化学键的断裂,又有生成物中化学键的形成,化学能也随之而改变。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢?2、一个化学反应吸收能量还是放出能量的决定因素看图讨论分析化学反应放出能量看图讨论分析化学反应吸收能量规律如果反应物所具有的总能量高于生成物所具有的总能量,那么在发生化学反应时,就有部分能量以热的形式释放出来;
如果反应物所具有的总能量低于生成物所具有的总能量,那么在发生化学反应时,反应物就需要吸收能量,才能转化为生成物。规律【归纳小结】一个化学反应是为放热反应还是吸热反应
取决于:取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小,
即取决于反应物的总能量与生成物的总能量的相对大小。反应物的能量之和
E反生成物的能量之和
E生(1)若E反> E生,(2)若E反< E生,放出能量吸收能量放热反应吸热反应E反 = E生+ E热2摩H2和1摩O2生成2摩H2O的能量变化(H与H键能是436KJ/mol,O与O键能是496KJ/mol,H与O键能是463KJ/mol)举例:拆开1摩H2所需能量是436KJ,拆1摩O2需要能量是496KJ。算一算:在101.3kPa,298K条件下,断开1molAB为A、B时过程的焓变(即能量的变化),称为A-B键的键能。通常,键能愈大,键愈牢固,由该键构成的分子也愈稳定,该分子本身所具有的能量就愈低。放出484KJ的能量反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量【课堂小结】1、当物质发生化学反应时,断开反应物中
的化学键要 ;而形成生成物中
的化学键要 。一个化学反应是
释放能量还是吸收能量取决于
。吸收能量放出能量反应物总能量与生成物总能量的相对大小 课堂练习:2、若反应物的总能量>生成物的总能量,
化学反应 能量。
若反应物的总能量<生成物的总能量,
化学反应 能量。放出吸收3已知反应A+B=C+D为放热反应,对该反应
的下列说法中正确的是( )
A. A的能量一定高于C
B. B的能量一定高于D
C. A和B的总能量一定高于C和D的总能量
D. 该反应为放热反应,故不必加热就一定
能发生C4、在反应H2 + Cl2 =2HCl中,已知H-H
键能为436kJ,Cl-Cl键能为247kJ,
H-Cl键能为431kJ,判断该反应是( )
A. 吸热反应 B. 放热反应
C. 吸收179kJ热量 D.放出179kJ热量BD5、甲烷燃烧要放出热量,水的分解要吸收能量,
试从化学键变化的角度分析其原因?解析: 形成4molH-O键和2molC=O键释放的能量
比断裂4molC-H键和2molO=O键所吸收的能
量高,因此放出热量。
断裂4molH-O键所吸收的能量比形成2mol
H-H键和1molO=O键放出的能量高,因此
要吸收能量。6、氢气在氧气中燃烧产生蓝色火焰,在反应中,
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是( )
A. 2Q1 + Q2 > 4Q3 B. 2Q1 + Q2 < 4Q3
C. Q1 + Q2 < Q3 D. Q1 + Q2 = Q3B7、下列关于能量转换的认识中不正确的
是( )
A. 电解水生成氢气和氧气时,电能转
化为化学能
B. 绿色植物进行光合作用时,太阳能
转化为热能
C. 煤燃烧时,化学能主要转化为热能
D. 白炽灯工作时,电能全部转化为光能BD8、下列说法中正确的是( )
A. 物质发生化学反应都伴随着能量变化
B. 所有物质的内部都“储存”有能量,而
且这些能量都是相等的
C. 在一个确定的化学反应关系中,反应
物的总能量总是高于生成物的总能量
D. 化学反应的过程实质是断开旧化学键
形成新化学键的过程AD9、在相同条件下,下列物质分别与H2
反应,当消耗等物质的量的H2时,放出
热量最多的是( )
A. Cl2 B. Br2
C. I2 D. SA新课标人教版化学必修Ⅱ 第二章 第一节 化学能与热能 (第2课时)复习:1、不同的物质不仅组成______、结构______,所包含的化学能也_______。
2、一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于
___________________________________
_____________时,有部分能量释放出来;__________时,反应物要吸收能量,才
能转化为生成物。
3、 是化学反应中能量变化的主要原因。不同不同不同反应物的总能量与生成物的总能量的相对大小。若E反> E生若E反< E生化学键的断裂和形成二、化学能与热能的相互转化质量守恒定律
能量守恒定律
化学反应中的能量变化,通常主要表现为热量的变化。
热量的变化:吸热和放热
怎样设计实验来了解反应中的
热量变化情况? 下面我们一起通过实验来认识和感受一下化学能与热能的相互转化![实验探究2—1] 铝片与盐酸的反应 在一支试管中加入2-3mL6mol/L的盐酸,再插入用砂纸打磨光的铝条,观察现象,并用温度计测量溶液温度的变化.实验2-11.铝与盐酸反应的化学方程式:?????????????????????????????? 。
2.在反应过程中你将能看到什么现象?
3.用眼睛不能直接观察到反应中的热量变化,你将采取哪些简单易行的办法来了解反应中的热量变化?
4.要明显的感知或测量反应中的热量变化,你在实验中应注意哪些问题?思考与讨论:实验2-1铝与盐酸反应,放出大量气泡,
温度升高该反应是放热
反应[实验2—2探究] :Ba(OH)2·8H2O与NH4Cl的反应2.整个实验中有哪些创新之处?1.整个实验的现象、反应化学方程式和结论?实验2-2现象:1、玻璃片(小木板)会与小烧杯粘结在一起
2、有少许刺激性气味气体产生
3、有水生成结论:该反应是吸热反应实验探究2-3盐酸与氢氧化钠溶液反应,观察反应中溶液温度的变化。实验2-3结论:中和反应是放热反应。实质:H+ + OH- = H2O反应后温度升高室温室温中和热:酸与碱发生中和反应生成1molH2O时
所释放的热量称为中和热【思考与交流】酸与碱发生中和反应生成1molH2O时所释放的热量称为中和热。如果要通过实验来测定盐酸与氢氧化钠反应的中和热,你认为在设计实验装置和操作时应该注意哪些问题?你准备如何设计并进行实验?请与同学讨论、交流。中和热的测定 装置在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如上图所示。该实验也可在保温杯中进行。 在设计实验装置和操作时应从两个方面考虑,一是注重“量”的问题,如① 反应物的浓度和体积取定值;② 测量反应前后的温度值;③ 做平行实验取平均值。二是尽量减小实验误差,如① 用经过标定的盐酸和氢氧化钠溶液;② 量液器最好使用移液管;③ 搅拌使反应充分进行;④ 及时散热,使混合液温度均衡;⑤ 温度计的精确度高,最好使用精度为0.1 ℃或更高的温度计;⑥ 盐酸跟氢氧化钠溶液混合后液面上方的空间尽可能小;⑦ 使用绝缘装置,避免热量散发到反应体系之外;⑧ 温度计要读准确。思考与交流随堂练习 1. 下列说法正确的是 ( )
A. 大多数的化合反应是释放能量的反应
B. 大多数分解反应是吸收能量的反应
C. 释放能量的反应都不需要加热
D. 吸收能量的反应都需要加热AB2. 下列反应既属于氧化还原反应,又属于吸热反应的是 ( )A.铝片与稀盐酸的反应
B.Ba(OH)2·8H2O和NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在氧气中的燃烧反应
C3、 如右图所示,把试管放入盛有25℃时饱 和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列问题:
(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”、“小于”、“等于”)镁片和盐酸的总能量.(1)①镁片上有大量气泡产生;②镁片逐渐溶解;③烧杯中析出晶体.
(2)镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度升高而减小,故析出Ca(OH)2晶体.
(3)Mg+2H+=Mg2++H2? (4)小于常见的放热反应和吸热反应放热反应所有燃烧
中和反应
溶液里的置换
一般的化合反应
特殊的分解吸热反应电离
强碱与铵盐
一般的分解
特殊的化合新课标人教版化学必修Ⅱ 第二章 第一节 化学能与热能 (第3课时)三、化学能的应用利用热量进行生活、生产和科研。
利用热能使很多化学反应得以发生。如:科学视野 生物体中的能量转化人体内发生的氧化还原反应与体外的燃烧本质相同,最终产物一样(都是二氧化碳和水),都是放热反应,所放出的能量也相等。只是二者反应条件不同。【自主学习】启示:生物化学过程在利用“能源”上更为合理、有效。科学视野人类利用能源的三个阶段1、柴草时期:以树枝杂草为主要能源2、化石能源时期:以煤、石油、天然气为主要能源3、多能源结构时期:可再生能源、清洁能源练习:指出下列说法的正误A、生物体内进行的缓慢氧化反应是放热反应。
B、化学键断裂吸收的能量越多,化学键越牢固。
C、植物光合作用吸收太阳能,与化学能无关。
D、柴草的燃烧与化学能无关。
E、人类的文明程度与人均耗能无关。对对不对不对不对1、物质发生化学反应的同时还伴随着能量的变化,而这种能量变化又通常表现为热能变化。2、化学键的断裂和形成是化学反应中能量变化的主要原因。3、化学反应中能量转化遵循能量守衡原则。【本节小结】【归纳小结】一个化学反应是为放热反应还是吸热反应
取决于:取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小,
即取决于反应物的总能量与生成物的总能量的相对大小。常见的放热反应和吸热反应放热反应所有燃烧
中和反应
溶液里的置换
一般的化合反应
特殊的分解吸热反应电离
强碱与铵盐
一般的分解
特殊的化合一、反应热1、定义:在化学反应过程中放出或吸收的热量符号:△H 单位:KJ/mol△H < 0表示放热反应△H > 0表示吸热反应2、计算方法:反应物的总能量减去生成物的总能量所得的数值3、分类:①燃烧热,②中和热3、分类:①燃烧热,②中和热①燃烧热在101KPa时,1mol纯物质完全燃烧生成稳定的化合物时所放出的热量叫做该物质的燃烧热②中和热在稀溶液中,酸跟碱发生中和反应生成1mol水所释放的热量叫中和热。室温下中和热约为57.3KJ/mol中和反应,燃烧反应均为放热反应有关反应热的计算
【例1】25℃、101kPa时,使1.0 g钠与足量的氯气反应,生成氯钠晶体并放出17.87 kJ的热量,求生成1 mol氯化钠的反应热。
【解】Na(g) + ? Cl2(g) ==NaCl(s)
17.87 kJ / 1g × 23 g / mol = 411 kJ / mol
答:生成1 mol NaCl时放出热量411 kJ。有关燃烧热的计算
【例2】乙醇的燃烧热△H= -1366.8 kJ/ mol,在25℃、101kPa时,1 kg 乙醇充分燃烧后放出多少热量?【解】n(C2H5OH)= 1000 g / 46g/mol
=21.74mol
1 kg C2H5OH燃烧后产生的热量:
1366.8 kJ/ mol× 21.74mol=2.971 ×10 4kJ
答: 1 kg C2H5OH燃烧后放出2.971 ×10 4kJ的热量。
二、盖斯定律1840年,瑞士化学家盖斯(G.H.Hess)通过大量实验事实证明,不管化学反应是一步完成或分几步完成,其反应热是相同的。
换句话说,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。这就是盖斯定律。
看下面的图理解盖斯定律某人从山下A到达山顶B,无论是翻山越岭攀登而上,还是坐缆车直奔山顶,其所处的海拔都高了300m
即山的高度与A、B点的海拔有关,而与由A点到达B点的途径无关
这里的A相当于反应体系的始态,B相当于反应体系的终态.山的高度相当于化学反应的反应热用能量守恒定律论证盖斯定律先从始态S变化到到终态L,体系放出热量(△H1<0),然后从L到S,体系吸收热量(△H2>0)。
经过一个循环,体系仍处于S态,因为物质没有发生变化,所以就不能引发能量变化,即△H1+△H2≡0盖斯定律在科学研究中的重要意义有些反应进行得很慢
有些反应不容易直接发生
有些反应的产品不纯(有副反应发生)
这些都给测量反应热造成了困难
利用盖斯定律可以间接地把它们的反应热计算出来C(s)+ ? O2(g)=CO(g)因为C燃烧时不可能完全生成CO,总有一部分CO2生成,因此这个反应的ΔH无法直接测得,请同学们自己根据盖斯定律设计一个方案计算该反应的ΔH。
提示(1) C (s) + O2(g) = CO2(g)
△H1=-393.5 kJ/mol
(2) CO (g) + ?O2(g) = CO2(g)
△H3=-283.0 kJ/mol△H1= △H2+ △H3
△H2 = △H1- △H3
= -393.5 kJ/mol -(-283.0 kJ/mol)
= -110.5 kJ/mol
C (s) + ? O2 (g) = CO2(g)
△H=-110.5 kJ/mol
应用盖斯定律的计算
【例3】已知下列反应的反应热为
⑴ CH3COOH (l) + 2O2(g) == 2CO2(g) + 2H2O(l)
△H1= -870.3 kJ/mol
⑵ C(s) + O2 (g) == CO2(g)
△H2= -393.5 kJ/mol
⑶ H2(g) + ? O2(g) == H2O(l)
△H3= -285.8 kJ/mol
试计算下述反应的反应热:
2C(s) + 2H2 (g) + O2 (g) == CH3COOH (l) 【解】分析各方程式的关系,知
将方程式按2[⑵ + ⑶] - ⑴组合得上述反应方程式
即:△H = 2[△H 2 + △H3] - △H1
△H =2[(-393.5kJ/mol) + (-285.8kJ/mol)]
-(-870.3kJ/mol)
= - 488.3kJ/mol
答:反应2C(s) + 2H2 (g) + O2 (g) == CH3COOH (l)
反应热为- 488.3kJ/mol
1、下列物质加入水中,显著放热的是( )
A、生石灰 B、固体NaOH
C、无水乙醇 D、固体NH4NO3
2、在相同温度下,下列两个反应放出的热量分别一Q1和Q2表示: ( )
2H2(g)+O2(g)=2H2O(g)+Q1
2H2(g)+O2(g)=2H2O(l)+Q2
A、 Q1 > Q2 B、 Q1 < Q2
C、 Q1 = Q2 D、无法计算ABB3、电解质电离要吸收热量,分别用40g氢氧化钠和盐酸、醋酸溶液完全反应,放出的热量
( )
A、相等
B、前者大于后者
C、前者小于后者
D、无法判断B下课
通过生产、生活中的实例了解化学能与热能的相互转化。
探究化学能转化为热能在生产、生活中的应用。
课题引入能源与人类 能源是人类赖以生存和发展的物质基础,我们每时每刻、分分秒秒都离不开它。迄今为止,人类所能利用的能源主要是化学能、电能、以及核能等等。但是,由于人类大量开发和浪费资源,造成了资源的不合理利用从而引发了不可回避的能源危机。我国化石燃料和水电能源消耗构成图16.6%2.1%5.1%76.2%你知道吗? 煤、石油、天然气的主要化学成分是烃类等有机物(煤中含有大量的碳),它们燃烧时放出热能。你一定想知道,这种能量从何而来?它与化学物质和化学反应有什么关系?石灰石(主要成分是碳酸钙)要经过高温煅烧才能变成生石灰,高温提供的热能在石灰石的分解反应中起到什么作用?一飞冲天:“神舟”五号发射实况回放 生活中哪些事实说明了在化学反应中伴随着能量的变化?【思考与交流】物质发生化学反应的同时还伴随着能量的变化,而这种能量变化又通常表现为热能变化。第一节 化学能与热能一、化学键与化学反应中能量变化的关系1、化学反应的本质是?
以氢气在氯气中燃烧为例,用化学键的观点分析反应的本质过程。H2 + Cl2 = 2HClH—H Cl —ClH—Cl断开断开点燃 一个化学反应的的过程,本质上就是旧化学键断裂和新化学键形成的过程。形成H2 + Cl2 = 2HClH—H Cl —ClH—Cl吸收能量断开断开吸收能量形成放出能量点燃化学键的断裂和形成是化学反应中能量变化的主要原因。【思考与交流】在化学反应中,随着物质的变化,既有反应物中化学键的断裂,又有生成物中化学键的形成,化学能也随之而改变。那么,一个化学反应吸收能量还是放出能量是由什么决定的呢?2、一个化学反应吸收能量还是放出能量的决定因素看图讨论分析化学反应放出能量看图讨论分析化学反应吸收能量规律如果反应物所具有的总能量高于生成物所具有的总能量,那么在发生化学反应时,就有部分能量以热的形式释放出来;
如果反应物所具有的总能量低于生成物所具有的总能量,那么在发生化学反应时,反应物就需要吸收能量,才能转化为生成物。规律【归纳小结】一个化学反应是为放热反应还是吸热反应
取决于:取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小,
即取决于反应物的总能量与生成物的总能量的相对大小。反应物的能量之和
E反生成物的能量之和
E生(1)若E反> E生,(2)若E反< E生,放出能量吸收能量放热反应吸热反应E反 = E生+ E热2摩H2和1摩O2生成2摩H2O的能量变化(H与H键能是436KJ/mol,O与O键能是496KJ/mol,H与O键能是463KJ/mol)举例:拆开1摩H2所需能量是436KJ,拆1摩O2需要能量是496KJ。算一算:在101.3kPa,298K条件下,断开1molAB为A、B时过程的焓变(即能量的变化),称为A-B键的键能。通常,键能愈大,键愈牢固,由该键构成的分子也愈稳定,该分子本身所具有的能量就愈低。放出484KJ的能量反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量【课堂小结】1、当物质发生化学反应时,断开反应物中
的化学键要 ;而形成生成物中
的化学键要 。一个化学反应是
释放能量还是吸收能量取决于
。吸收能量放出能量反应物总能量与生成物总能量的相对大小 课堂练习:2、若反应物的总能量>生成物的总能量,
化学反应 能量。
若反应物的总能量<生成物的总能量,
化学反应 能量。放出吸收3已知反应A+B=C+D为放热反应,对该反应
的下列说法中正确的是( )
A. A的能量一定高于C
B. B的能量一定高于D
C. A和B的总能量一定高于C和D的总能量
D. 该反应为放热反应,故不必加热就一定
能发生C4、在反应H2 + Cl2 =2HCl中,已知H-H
键能为436kJ,Cl-Cl键能为247kJ,
H-Cl键能为431kJ,判断该反应是( )
A. 吸热反应 B. 放热反应
C. 吸收179kJ热量 D.放出179kJ热量BD5、甲烷燃烧要放出热量,水的分解要吸收能量,
试从化学键变化的角度分析其原因?解析: 形成4molH-O键和2molC=O键释放的能量
比断裂4molC-H键和2molO=O键所吸收的能
量高,因此放出热量。
断裂4molH-O键所吸收的能量比形成2mol
H-H键和1molO=O键放出的能量高,因此
要吸收能量。6、氢气在氧气中燃烧产生蓝色火焰,在反应中,
破坏1molH-H键消耗的能量为Q1kJ,
破坏1molO = O键消耗的能量为Q2kJ,
形成1molH-O键释放的能量为Q3kJ。
下列关系式中正确的是( )
A. 2Q1 + Q2 > 4Q3 B. 2Q1 + Q2 < 4Q3
C. Q1 + Q2 < Q3 D. Q1 + Q2 = Q3B7、下列关于能量转换的认识中不正确的
是( )
A. 电解水生成氢气和氧气时,电能转
化为化学能
B. 绿色植物进行光合作用时,太阳能
转化为热能
C. 煤燃烧时,化学能主要转化为热能
D. 白炽灯工作时,电能全部转化为光能BD8、下列说法中正确的是( )
A. 物质发生化学反应都伴随着能量变化
B. 所有物质的内部都“储存”有能量,而
且这些能量都是相等的
C. 在一个确定的化学反应关系中,反应
物的总能量总是高于生成物的总能量
D. 化学反应的过程实质是断开旧化学键
形成新化学键的过程AD9、在相同条件下,下列物质分别与H2
反应,当消耗等物质的量的H2时,放出
热量最多的是( )
A. Cl2 B. Br2
C. I2 D. SA新课标人教版化学必修Ⅱ 第二章 第一节 化学能与热能 (第2课时)复习:1、不同的物质不仅组成______、结构______,所包含的化学能也_______。
2、一个确定的化学反应在发生过程中是吸收能量还是放出能量,决定于
___________________________________
_____________时,有部分能量释放出来;__________时,反应物要吸收能量,才
能转化为生成物。
3、 是化学反应中能量变化的主要原因。不同不同不同反应物的总能量与生成物的总能量的相对大小。若E反> E生若E反< E生化学键的断裂和形成二、化学能与热能的相互转化质量守恒定律
能量守恒定律
化学反应中的能量变化,通常主要表现为热量的变化。
热量的变化:吸热和放热
怎样设计实验来了解反应中的
热量变化情况? 下面我们一起通过实验来认识和感受一下化学能与热能的相互转化![实验探究2—1] 铝片与盐酸的反应 在一支试管中加入2-3mL6mol/L的盐酸,再插入用砂纸打磨光的铝条,观察现象,并用温度计测量溶液温度的变化.实验2-11.铝与盐酸反应的化学方程式:?????????????????????????????? 。
2.在反应过程中你将能看到什么现象?
3.用眼睛不能直接观察到反应中的热量变化,你将采取哪些简单易行的办法来了解反应中的热量变化?
4.要明显的感知或测量反应中的热量变化,你在实验中应注意哪些问题?思考与讨论:实验2-1铝与盐酸反应,放出大量气泡,
温度升高该反应是放热
反应[实验2—2探究] :Ba(OH)2·8H2O与NH4Cl的反应2.整个实验中有哪些创新之处?1.整个实验的现象、反应化学方程式和结论?实验2-2现象:1、玻璃片(小木板)会与小烧杯粘结在一起
2、有少许刺激性气味气体产生
3、有水生成结论:该反应是吸热反应实验探究2-3盐酸与氢氧化钠溶液反应,观察反应中溶液温度的变化。实验2-3结论:中和反应是放热反应。实质:H+ + OH- = H2O反应后温度升高室温室温中和热:酸与碱发生中和反应生成1molH2O时
所释放的热量称为中和热【思考与交流】酸与碱发生中和反应生成1molH2O时所释放的热量称为中和热。如果要通过实验来测定盐酸与氢氧化钠反应的中和热,你认为在设计实验装置和操作时应该注意哪些问题?你准备如何设计并进行实验?请与同学讨论、交流。中和热的测定 装置在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如上图所示。该实验也可在保温杯中进行。 在设计实验装置和操作时应从两个方面考虑,一是注重“量”的问题,如① 反应物的浓度和体积取定值;② 测量反应前后的温度值;③ 做平行实验取平均值。二是尽量减小实验误差,如① 用经过标定的盐酸和氢氧化钠溶液;② 量液器最好使用移液管;③ 搅拌使反应充分进行;④ 及时散热,使混合液温度均衡;⑤ 温度计的精确度高,最好使用精度为0.1 ℃或更高的温度计;⑥ 盐酸跟氢氧化钠溶液混合后液面上方的空间尽可能小;⑦ 使用绝缘装置,避免热量散发到反应体系之外;⑧ 温度计要读准确。思考与交流随堂练习 1. 下列说法正确的是 ( )
A. 大多数的化合反应是释放能量的反应
B. 大多数分解反应是吸收能量的反应
C. 释放能量的反应都不需要加热
D. 吸收能量的反应都需要加热AB2. 下列反应既属于氧化还原反应,又属于吸热反应的是 ( )A.铝片与稀盐酸的反应
B.Ba(OH)2·8H2O和NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在氧气中的燃烧反应
C3、 如右图所示,把试管放入盛有25℃时饱 和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.试回答下列问题:
(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”、“小于”、“等于”)镁片和盐酸的总能量.(1)①镁片上有大量气泡产生;②镁片逐渐溶解;③烧杯中析出晶体.
(2)镁与盐酸反应产生氢气,该反应为放热反应,Ca(OH)2在水中的溶解度随温度升高而减小,故析出Ca(OH)2晶体.
(3)Mg+2H+=Mg2++H2? (4)小于常见的放热反应和吸热反应放热反应所有燃烧
中和反应
溶液里的置换
一般的化合反应
特殊的分解吸热反应电离
强碱与铵盐
一般的分解
特殊的化合新课标人教版化学必修Ⅱ 第二章 第一节 化学能与热能 (第3课时)三、化学能的应用利用热量进行生活、生产和科研。
利用热能使很多化学反应得以发生。如:科学视野 生物体中的能量转化人体内发生的氧化还原反应与体外的燃烧本质相同,最终产物一样(都是二氧化碳和水),都是放热反应,所放出的能量也相等。只是二者反应条件不同。【自主学习】启示:生物化学过程在利用“能源”上更为合理、有效。科学视野人类利用能源的三个阶段1、柴草时期:以树枝杂草为主要能源2、化石能源时期:以煤、石油、天然气为主要能源3、多能源结构时期:可再生能源、清洁能源练习:指出下列说法的正误A、生物体内进行的缓慢氧化反应是放热反应。
B、化学键断裂吸收的能量越多,化学键越牢固。
C、植物光合作用吸收太阳能,与化学能无关。
D、柴草的燃烧与化学能无关。
E、人类的文明程度与人均耗能无关。对对不对不对不对1、物质发生化学反应的同时还伴随着能量的变化,而这种能量变化又通常表现为热能变化。2、化学键的断裂和形成是化学反应中能量变化的主要原因。3、化学反应中能量转化遵循能量守衡原则。【本节小结】【归纳小结】一个化学反应是为放热反应还是吸热反应
取决于:取决于所有断键吸收的总能量与所有
形成新键放出的总能量的相对大小,
即取决于反应物的总能量与生成物的总能量的相对大小。常见的放热反应和吸热反应放热反应所有燃烧
中和反应
溶液里的置换
一般的化合反应
特殊的分解吸热反应电离
强碱与铵盐
一般的分解
特殊的化合一、反应热1、定义:在化学反应过程中放出或吸收的热量符号:△H 单位:KJ/mol△H < 0表示放热反应△H > 0表示吸热反应2、计算方法:反应物的总能量减去生成物的总能量所得的数值3、分类:①燃烧热,②中和热3、分类:①燃烧热,②中和热①燃烧热在101KPa时,1mol纯物质完全燃烧生成稳定的化合物时所放出的热量叫做该物质的燃烧热②中和热在稀溶液中,酸跟碱发生中和反应生成1mol水所释放的热量叫中和热。室温下中和热约为57.3KJ/mol中和反应,燃烧反应均为放热反应有关反应热的计算
【例1】25℃、101kPa时,使1.0 g钠与足量的氯气反应,生成氯钠晶体并放出17.87 kJ的热量,求生成1 mol氯化钠的反应热。
【解】Na(g) + ? Cl2(g) ==NaCl(s)
17.87 kJ / 1g × 23 g / mol = 411 kJ / mol
答:生成1 mol NaCl时放出热量411 kJ。有关燃烧热的计算
【例2】乙醇的燃烧热△H= -1366.8 kJ/ mol,在25℃、101kPa时,1 kg 乙醇充分燃烧后放出多少热量?【解】n(C2H5OH)= 1000 g / 46g/mol
=21.74mol
1 kg C2H5OH燃烧后产生的热量:
1366.8 kJ/ mol× 21.74mol=2.971 ×10 4kJ
答: 1 kg C2H5OH燃烧后放出2.971 ×10 4kJ的热量。
二、盖斯定律1840年,瑞士化学家盖斯(G.H.Hess)通过大量实验事实证明,不管化学反应是一步完成或分几步完成,其反应热是相同的。
换句话说,化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。这就是盖斯定律。
看下面的图理解盖斯定律某人从山下A到达山顶B,无论是翻山越岭攀登而上,还是坐缆车直奔山顶,其所处的海拔都高了300m
即山的高度与A、B点的海拔有关,而与由A点到达B点的途径无关
这里的A相当于反应体系的始态,B相当于反应体系的终态.山的高度相当于化学反应的反应热用能量守恒定律论证盖斯定律先从始态S变化到到终态L,体系放出热量(△H1<0),然后从L到S,体系吸收热量(△H2>0)。
经过一个循环,体系仍处于S态,因为物质没有发生变化,所以就不能引发能量变化,即△H1+△H2≡0盖斯定律在科学研究中的重要意义有些反应进行得很慢
有些反应不容易直接发生
有些反应的产品不纯(有副反应发生)
这些都给测量反应热造成了困难
利用盖斯定律可以间接地把它们的反应热计算出来C(s)+ ? O2(g)=CO(g)因为C燃烧时不可能完全生成CO,总有一部分CO2生成,因此这个反应的ΔH无法直接测得,请同学们自己根据盖斯定律设计一个方案计算该反应的ΔH。
提示(1) C (s) + O2(g) = CO2(g)
△H1=-393.5 kJ/mol
(2) CO (g) + ?O2(g) = CO2(g)
△H3=-283.0 kJ/mol△H1= △H2+ △H3
△H2 = △H1- △H3
= -393.5 kJ/mol -(-283.0 kJ/mol)
= -110.5 kJ/mol
C (s) + ? O2 (g) = CO2(g)
△H=-110.5 kJ/mol
应用盖斯定律的计算
【例3】已知下列反应的反应热为
⑴ CH3COOH (l) + 2O2(g) == 2CO2(g) + 2H2O(l)
△H1= -870.3 kJ/mol
⑵ C(s) + O2 (g) == CO2(g)
△H2= -393.5 kJ/mol
⑶ H2(g) + ? O2(g) == H2O(l)
△H3= -285.8 kJ/mol
试计算下述反应的反应热:
2C(s) + 2H2 (g) + O2 (g) == CH3COOH (l) 【解】分析各方程式的关系,知
将方程式按2[⑵ + ⑶] - ⑴组合得上述反应方程式
即:△H = 2[△H 2 + △H3] - △H1
△H =2[(-393.5kJ/mol) + (-285.8kJ/mol)]
-(-870.3kJ/mol)
= - 488.3kJ/mol
答:反应2C(s) + 2H2 (g) + O2 (g) == CH3COOH (l)
反应热为- 488.3kJ/mol
1、下列物质加入水中,显著放热的是( )
A、生石灰 B、固体NaOH
C、无水乙醇 D、固体NH4NO3
2、在相同温度下,下列两个反应放出的热量分别一Q1和Q2表示: ( )
2H2(g)+O2(g)=2H2O(g)+Q1
2H2(g)+O2(g)=2H2O(l)+Q2
A、 Q1 > Q2 B、 Q1 < Q2
C、 Q1 = Q2 D、无法计算ABB3、电解质电离要吸收热量,分别用40g氢氧化钠和盐酸、醋酸溶液完全反应,放出的热量
( )
A、相等
B、前者大于后者
C、前者小于后者
D、无法判断B下课
