2025年辽宁省铁岭市铁岭县莲花一中中考三模化学试题(PDF版、含答案)
文档属性
| 名称 | 2025年辽宁省铁岭市铁岭县莲花一中中考三模化学试题(PDF版、含答案) |

|
|
| 格式 | |||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-09 00:00:00 | ||
图片预览


文档简介
2025 铁岭县莲花一中中考三模
化 学 试 题
(本试卷共 14 道小题 满分 50 分)
考生注意:所有试题必须在答题卡上作答,在本试卷上作答无效。
可能用到的相对原子质量: H—1 C—12 O—16 Cl—35.5 Ca—40
第一部分 选择题 (共 10 分)
(本部分共包括 10 道小题,每小题 1分。下列每小题只有一个最符合题目要求的选项)
1.二十四节气蕴含丰富的文化内涵,反映了我国劳动人民的智慧。下列说法不.正.确.的是 ( )
A.清明,草木萌发,绿色植物通过光合作用能释放氧气
B.小满,农作物的颗粒逐渐饱满,农业上需合理使用农药化肥
C.大暑,炎热天气能加快食物发生化学变化而变质
D.冬至,传统习俗腌制腊肉、制作泡菜可以使用工业食盐
2.为深入打好蓝天、碧水、净土保卫战,持续优化生态环境,下列做法不提倡的是 ( )
A.工业“三废”直接排放 B.防止海洋垃圾污染
C.对垃圾进行分类回收 D.使用可降解塑料
3.安全离不开化学知识。下列实验操作正确的是( )
4.化学用语是化学学科的核心组成部分,是连接化学理论、实验与应用的纽带。下列有关化
学用语中说法正确的是 ()
A.H 表示氢元素显+1 价 B.2Si 表示两个硅元素
C.3NH 表示三个铵根 D.4H SO 表示四个亚硫酸分子
5.白醋是一种多功能的家居用品,下列关于白醋的叙述不.正.确.的是 ( )
A.食用工业级醋酸 B.在烹饪中调味增香
C.代替清洁剂去除水壶中的水垢 D.用来鉴别淀粉和纯碱
6.探究物质的燃烧条件能够实现能源高效率利用、减少污染物排
放、保障设备安全运行,-并推动技术创新。已知白磷着火点是 4
0℃。如图将两小块白磷固定在 U形管底部基座上,分别加入等体
积冷水和热水,白磷均不燃烧。一段时间后,将装置倒置。下列
说法正确的是 ( )
A.冷水的作用是提供热量和隔绝氧气
B.该实验能证明可燃物的燃烧需要与氧气接触
C.倒置后两块白磷均能燃烧产生大量白烟
D.该实验不能证明可燃物燃烧需要温度达到着火点
7.某同学在趣味实验“点水成冰”中用到了醋酸钠溶液。如图
是醋酸钠的溶解度曲线,下列说法正确的是 ( )
A.醋酸钠饱和溶液从 40℃降温到 10℃,有 29.4g 晶体析出
B.40℃时,配制醋酸钠溶液的溶质质量分数不能超过 39.6%
C.醋酸钠的溶解度是 65.5
D.将 60℃时醋酸钠溶液降温至 40℃,溶质质量分数一定减小
8.微粒观是化学学科的核心思想之一,是化学学习的基石。下列关于化学微粒观的认识中,
不正确的是 ( )
A.能直接构成物质的微观粒子有分子、原子和离子
B.化学变化是反应物的原子重新组合转变为生成物的过程
C.化学反应前后原子种类不变、原子数目不变、原子质量不变
D.分子可以再分,原子不能再分
9.在实验室配制 50g 溶质质量分数为 10%的氢氧化钠溶液实验过程中,下列操作属于规范操
作的是 ( )
A.抽取式面巾纸擦拭药匙
B.用托盘天平称取溶质时,将氢氧化钠直接放入托盘中
C.在量筒内配制溶液
D.配制完成的氢氧化钠溶液可以转移到细口瓶中并塞好橡胶塞
10.“液态阳光”是指利用太阳能等可再生能源制取绿色氢气,结合二氧化碳加氢技术制备
以甲醇 (CH OH)为代表的液态燃料。下列有关说法不.正.确.的是 ( )
A.“液态阳光”的应用具有减碳作用
B.煤经过加工合成的甲醇能称作“液态阳光”
C.甲醇可通过太阳能、水和二氧化碳合成,符合可持续发展要求
D.氢能属于可再生能源
第二部分 非选择题 (共 40 分)
(本部分共包括 4道小题)
11.(14 分)化学学习中倡导“做中学、用中学、创中学”,以发
现化学反应容器里的“星辰大海”。请回答下列问题。
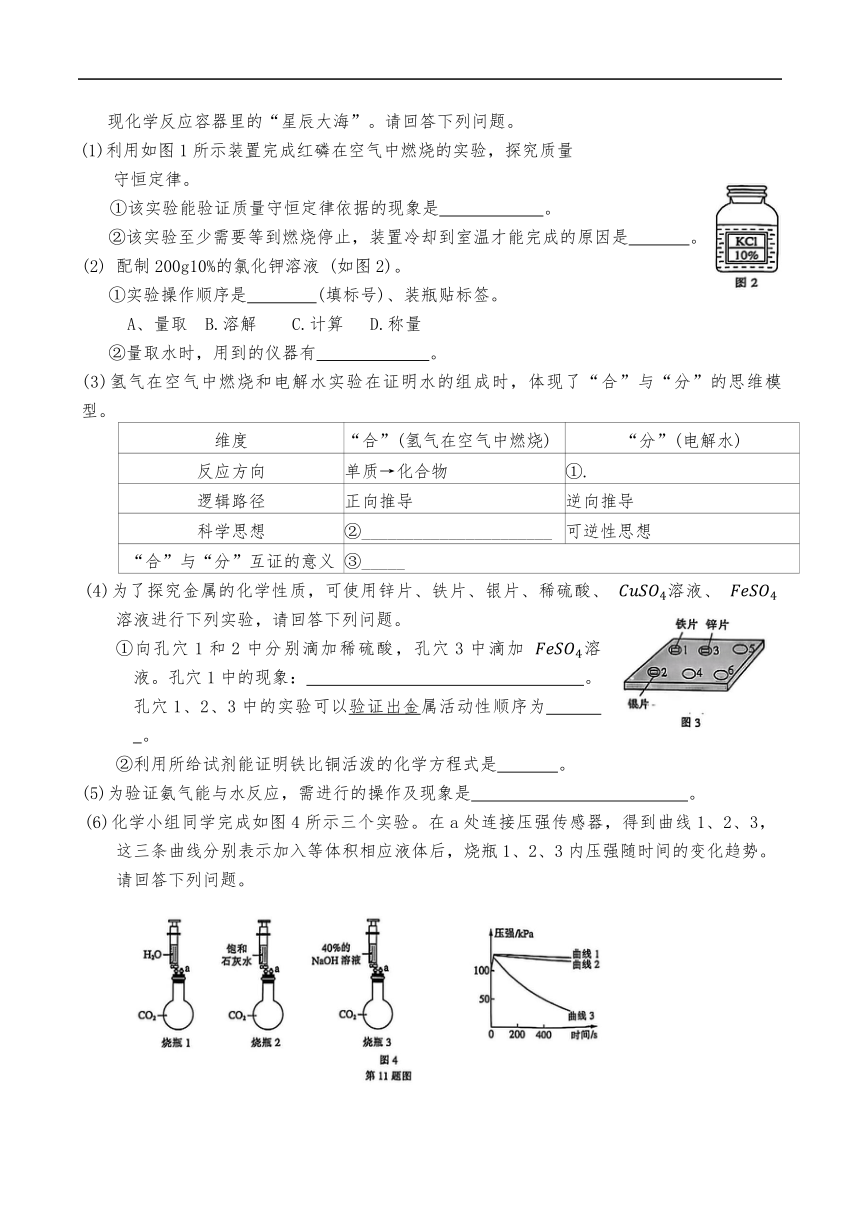
(1)利用如图 1所示装置完成红磷在空气中燃烧的实验,探究质量
守恒定律。
①该实验能验证质量守恒定律依据的现象是 。
②该实验至少需要等到燃烧停止,装置冷却到室温才能完成的原因是 。
(2) 配制 200g10%的氯化钾溶液 (如图 2)。
①实验操作顺序是 (填标号)、装瓶贴标签。
A、量取 B.溶解 C.计算 D.称量
②量取水时,用到的仪器有 。
(3)氢气在空气中燃烧和电解水实验在证明水的组成时,体现了“合”与“分”的思维模
型。
维度 “合”(氢气在空气中燃烧) “分”(电解水)
反应方向 单质→化合物 ①.
逻辑路径 正向推导 逆向推导
科学思想 ②______________________ 可逆性思想
“合”与“分”互证的意义 ③_____
(4)为了探究金属的化学性质,可使用锌片、铁片、银片、稀硫酸、 4溶液、 4
溶液进行下列实验,请回答下列问题。
①向孔穴 1 和 2 中分别滴加稀硫酸,孔穴 3 中滴加 4溶
液。孔穴 1中的现象: 。
孔穴 1、2、3 中的实验可以验证出金属活动性顺序为
。
②利用所给试剂能证明铁比铜活泼的化学方程式是 。
(5)为验证氨气能与水反应,需进行的操作及现象是 。
(6)化学小组同学完成如图 4 所示三个实验。在 a 处连接压强传感器,得到曲线 1、2、3,
这三条曲线分别表示加入等体积相应液体后,烧瓶 1、2、3内压强随时间的变化趋势。
请回答下列问题。
①请分析三个实验的起始阶段压强都快速增大的原因: 。
②能证明二氧化碳和氢氧化钠一定发生了化学反应的证据是 。
12.(7 分)阅读下面科普短文。
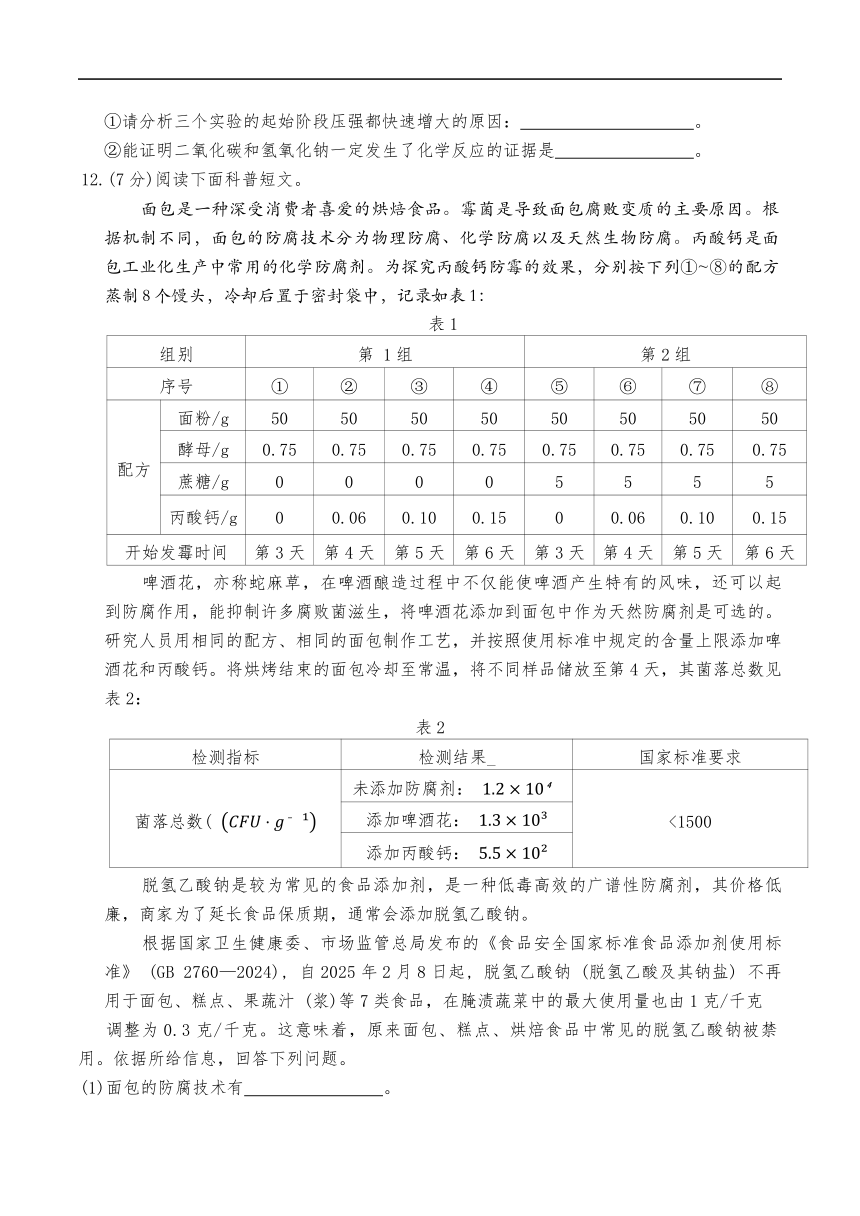
面包是一种深受消费者喜爱的烘焙食品。霉菌是导致面包腐败变质的主要原因。根
据机制不同,面包的防腐技术分为物理防腐、化学防腐以及天然生物防腐。丙酸钙是面
包工业化生产中常用的化学防腐剂。为探究丙酸钙防霉的效果,分别按下列①~⑧的配方
蒸制8个馒头,冷却后置于密封袋中,记录如表1:
表 1
组别 第 1组 第 2组
序号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
面粉/g 50 50 50 50 50 50 50 50
酵母/g 0.75 0.75 0.75 0.75 0.75 0.75 0.75 0.75
配方
蔗糖/g 0 0 0 0 5 5 5 5
丙酸钙/g 0 0.06 0.10 0.15 0 0.06 0.10 0.15
开始发霉时间 第 3天 第 4天 第 5天 第 6天 第 3天 第 4天 第 5天 第 6天
啤酒花,亦称蛇麻草,在啤酒酿造过程中不仅能使啤酒产生特有的风味,还可以起
到防腐作用,能抑制许多腐败菌滋生,将啤酒花添加到面包中作为天然防腐剂是可选的。
研究人员用相同的配方、相同的面包制作工艺,并按照使用标准中规定的含量上限添加啤
酒花和丙酸钙。将烘烤结束的面包冷却至常温,将不同样品储放至第 4 天,其菌落总数见
表 2:
表 2
检测指标 检测结果_ 国家标准要求
未添加防腐剂: 1.2 × 10
菌落总数( 添加啤酒花: 1.3 × 10 <1500
添加丙酸钙: 5.5 × 10
脱氢乙酸钠是较为常见的食品添加剂,是一种低毒高效的广谱性防腐剂,其价格低
廉,商家为了延长食品保质期,通常会添加脱氢乙酸钠。
根据国家卫生健康委、市场监管总局发布的《食品安全国家标准食品添加剂使用标
准》 (GB 2760—2024), 自 2025 年 2 月 8 日起, 脱氢乙酸钠 (脱氢乙酸及其钠盐) 不再
用于面包、糕点、果蔬汁 (浆)等 7类食品,在腌渍蔬菜中的最大使用量也由 1克/千克
调整为 0.3 克/千克。这意味着,原来面包、糕点、烘焙食品中常见的脱氢乙酸钠被禁
用。依据所给信息,回答下列问题。
(1)面包的防腐技术有 。
(2)面包中加入丙酸钙除了防腐,还可能具有 作用。
(3)分析表 1中第 2组实验数据,可以得出的结论是 。
(4)根据表 1,能证明“有无蔗糖对丙酸钙防霉效果无影响”的证据是 。
(5)根据表 1,可能影响丙酸钙防霉效果的因素有 。
(6)由表 2 可知,丙酸钙比啤酒花的抑菌防腐效果好,依据是 。
(7)根据短文中的介绍推测脱氢乙酸钠的一条化学性质: 。
13.(6 分)聚焦珊瑚礁破坏与保护。
【活动 1】珊瑚礁的形成原理
(1)海洋中的珊瑚虫通过一系列钙化作用形成石灰石外壳,这些石灰石经过压实、石化,形成
岛屿和礁石,珊瑚礁形成过程中发生了 (填“物理”或“化学”)变化。
(2)根据海水中含碳元素的微粒分布图可以获得的信息有 。
(答出一条即可)
【活动 2】珊瑚礁的破坏
3 2能引起海水酸化,其化学方程式为 。
(4)据预测海水的 pH 将于本世纪末降至 7:8,届时珊瑚礁可能消失的原因是
。 (答出一条即可)
【活动 3】珊瑚礁的保护
(5)保护珊瑚礁的关键是减少( 2的含量,请从两个不同角度提出措施: 、 。
14.(13 分)中国是茶叶的故乡, “围炉煮茶”已成为一种休闲生活方式。化学活动小组围绕
“茶”进行了项目式探究。
【任务 1】种植茶树
(1)茶树在 pH 为 4.5~6.5 的土壤中生长为佳,该土壤属于 (填“酸性”或“碱性”)
土壤。
(2)测定土壤酸碱度可使用 。
(3)种茶常施用的化学尿素 2 2 属于 (填“氮肥”或“复合肥料”)。
【任务 2】泡制茶汤
(4)选择茶具:现选用三种不同材质的茶具泡同一品牌龙井茶,测量茶汤中风味物质儿茶素
类和咖啡碱的含量。测量结果如下:
浸泡时间/ m 儿茶素类含量/(mg/g) 咖啡碱含量/(mg/g)
in 紫砂壶 瓷质盖碗 玻璃杯 紫砂壶 瓷质盖碗 玻璃杯
2 155 162 151 25 26 26
4 201 223 214 32 36 35
以下属于该实验需控制的变量是 (填标号)。
A.水温 B.水量 C.水样 D.煮水方式 E.茶叶用量
结论:不同材质的茶具对茶汤风味虽有一定影响,但差异不大,生活中按需选择即可。
(5)冲泡茶叶需高提水壶,水自高点下注,使茶叶在壶内翻滚散开,高冲的作用相当于实验基
本操作 (填标号)。
A.蒸发 B.搅拌 C.升华
【任务 3】探究茶垢剂
(6)茶垢剂的主要成分为过碳酸钠,化学式为 2 2 3 3 2 2。过碳酸钠是一种白色粉末,
常温下与水能反应生成) 2 3和 2 2。下列物质能使茶垢剂失效的是 (填
标号)。
A.硫酸 B.氢氧化钙 C.二氧化锰 D.氯化钠
(7)小组同学设计了如图装置,通过测定( 2质量来测定茶垢清洁剂中过碳酸钠的含
量。主要步骤:
a.检查装置气密性。
b.向锥形瓶中加入 10g 样品。
c.通入氮气一段时间后,称量装置 C 的质量为 132.0g。 (该碱石灰是由氢氧化钠和氧
化钙组成的混合固体)……
d.缓慢滴加适量稀硫酸至 A中。(假设茶垢清洁剂中其他成分不参与反应)
e.再通入氮气一段时间后,再次称量装置 C的质量为 134.2g。
请回答下列问题:
①实验中分液漏斗中放入稀硫酸比盐酸好的理由: 。
②确定向 A中滴加稀硫酸已足够的现象: 。
③浓硫酸的作用: 。
④反应前通入氮气的目的: 。
⑤反应结束后继续通入氮气的作用是 。
⑥装置 D中碱石灰的作用: 。
⑦计算茶垢清洁剂样品中过碳酸钠的质量分数为 。
1. D 2. A 3. C 4. D 5. A 6. B 7. B 8. D 9. D 10. B
11.(14 分) (1)①红磷燃烧产生大量白烟,反应前后天平保持平衡 ②红磷燃烧放热会使
瓶内压强增大,导致气球胀大产生浮力,影响测量结果
(2) ①CDAB ②量筒、胶头滴管
(3)①化合物→单质 ②化学反应前后元素种类不变 ③消除单一实验的偶然性 (或提高了
结论的可靠性)
(4)①铁表面有气泡产生,溶液由无色变为浅绿色 Zn>Fe>Ag
② + 4 = 4 +
(5)取 3 朵干燥的紫色石蕊纸花,向第一朵纸花喷水,将第二朵纸花放入盛有氨气的集气
瓶中,纸花均未变蓝;将第三朵纸花喷水后放入盛有氨气的集气瓶中,纸花变蓝,则证明氨
气能与水反应 (合理即可)
(6)①注入的液体压缩了烧瓶内的气体 ②对比曲线 1 和曲线 3 可知,二氧化碳和氢氧化
钠一定发生了化学反应
12.(7 分) (1)物理防腐、化学防腐以及天然生物防腐
(2) 补钙
(3)当面粉质量、蔗糖质量、酵母质量等其他条件相同时,丙酸钙质量越大,防霉效果越
好
(4)对比②⑥、③⑦、④⑧数据发现,有无蔗糖,面包开始发霉的时间均相同
(5)面粉的种类(答案合理即可)
(6)在实验研究范围内,当储存到第 4 天时,添加丙酸钙的面包菌落总数比添加啤酒花的
少
(7)脱氢乙酸钠化学性质稳定 (答案合理即可)
13. (6 分) (1) 化学
(2)当 pH 为 7.8 时,海水中含量最多的微观粒子为 HCO (答案合理即可)
3 2 + 2 = 2 3
(4)CaCO 能和酸反应,海水酸化能促进 CaCO 溶解,导致珊瑚礁减少 (答案合理即可)
(5)减少化石燃料的燃烧 植树造林 (答案合理即可)
14. (13 分) (1) 酸性
(2) pH 试纸 (或 pH 计)
(3) 氮肥
(4) ABCDE
(5) B
(6) ABC
(7)①盐酸具有挥发性
②向 A中滴加稀硫酸至不再产生气泡
③吸收水分,干燥气体
④为了排尽装置内的空气
⑤为了将装置内滞留的二氧化碳驱赶到装置 C中
⑥防止空气中二氧化碳和水蒸气进入装置 C中,对实验造成干扰
⑦78.5%
化 学 试 题
(本试卷共 14 道小题 满分 50 分)
考生注意:所有试题必须在答题卡上作答,在本试卷上作答无效。
可能用到的相对原子质量: H—1 C—12 O—16 Cl—35.5 Ca—40
第一部分 选择题 (共 10 分)
(本部分共包括 10 道小题,每小题 1分。下列每小题只有一个最符合题目要求的选项)
1.二十四节气蕴含丰富的文化内涵,反映了我国劳动人民的智慧。下列说法不.正.确.的是 ( )
A.清明,草木萌发,绿色植物通过光合作用能释放氧气
B.小满,农作物的颗粒逐渐饱满,农业上需合理使用农药化肥
C.大暑,炎热天气能加快食物发生化学变化而变质
D.冬至,传统习俗腌制腊肉、制作泡菜可以使用工业食盐
2.为深入打好蓝天、碧水、净土保卫战,持续优化生态环境,下列做法不提倡的是 ( )
A.工业“三废”直接排放 B.防止海洋垃圾污染
C.对垃圾进行分类回收 D.使用可降解塑料
3.安全离不开化学知识。下列实验操作正确的是( )
4.化学用语是化学学科的核心组成部分,是连接化学理论、实验与应用的纽带。下列有关化
学用语中说法正确的是 ()
A.H 表示氢元素显+1 价 B.2Si 表示两个硅元素
C.3NH 表示三个铵根 D.4H SO 表示四个亚硫酸分子
5.白醋是一种多功能的家居用品,下列关于白醋的叙述不.正.确.的是 ( )
A.食用工业级醋酸 B.在烹饪中调味增香
C.代替清洁剂去除水壶中的水垢 D.用来鉴别淀粉和纯碱
6.探究物质的燃烧条件能够实现能源高效率利用、减少污染物排
放、保障设备安全运行,-并推动技术创新。已知白磷着火点是 4
0℃。如图将两小块白磷固定在 U形管底部基座上,分别加入等体
积冷水和热水,白磷均不燃烧。一段时间后,将装置倒置。下列
说法正确的是 ( )
A.冷水的作用是提供热量和隔绝氧气
B.该实验能证明可燃物的燃烧需要与氧气接触
C.倒置后两块白磷均能燃烧产生大量白烟
D.该实验不能证明可燃物燃烧需要温度达到着火点
7.某同学在趣味实验“点水成冰”中用到了醋酸钠溶液。如图
是醋酸钠的溶解度曲线,下列说法正确的是 ( )
A.醋酸钠饱和溶液从 40℃降温到 10℃,有 29.4g 晶体析出
B.40℃时,配制醋酸钠溶液的溶质质量分数不能超过 39.6%
C.醋酸钠的溶解度是 65.5
D.将 60℃时醋酸钠溶液降温至 40℃,溶质质量分数一定减小
8.微粒观是化学学科的核心思想之一,是化学学习的基石。下列关于化学微粒观的认识中,
不正确的是 ( )
A.能直接构成物质的微观粒子有分子、原子和离子
B.化学变化是反应物的原子重新组合转变为生成物的过程
C.化学反应前后原子种类不变、原子数目不变、原子质量不变
D.分子可以再分,原子不能再分
9.在实验室配制 50g 溶质质量分数为 10%的氢氧化钠溶液实验过程中,下列操作属于规范操
作的是 ( )
A.抽取式面巾纸擦拭药匙
B.用托盘天平称取溶质时,将氢氧化钠直接放入托盘中
C.在量筒内配制溶液
D.配制完成的氢氧化钠溶液可以转移到细口瓶中并塞好橡胶塞
10.“液态阳光”是指利用太阳能等可再生能源制取绿色氢气,结合二氧化碳加氢技术制备
以甲醇 (CH OH)为代表的液态燃料。下列有关说法不.正.确.的是 ( )
A.“液态阳光”的应用具有减碳作用
B.煤经过加工合成的甲醇能称作“液态阳光”
C.甲醇可通过太阳能、水和二氧化碳合成,符合可持续发展要求
D.氢能属于可再生能源
第二部分 非选择题 (共 40 分)
(本部分共包括 4道小题)
11.(14 分)化学学习中倡导“做中学、用中学、创中学”,以发
现化学反应容器里的“星辰大海”。请回答下列问题。
(1)利用如图 1所示装置完成红磷在空气中燃烧的实验,探究质量
守恒定律。
①该实验能验证质量守恒定律依据的现象是 。
②该实验至少需要等到燃烧停止,装置冷却到室温才能完成的原因是 。
(2) 配制 200g10%的氯化钾溶液 (如图 2)。
①实验操作顺序是 (填标号)、装瓶贴标签。
A、量取 B.溶解 C.计算 D.称量
②量取水时,用到的仪器有 。
(3)氢气在空气中燃烧和电解水实验在证明水的组成时,体现了“合”与“分”的思维模
型。
维度 “合”(氢气在空气中燃烧) “分”(电解水)
反应方向 单质→化合物 ①.
逻辑路径 正向推导 逆向推导
科学思想 ②______________________ 可逆性思想
“合”与“分”互证的意义 ③_____
(4)为了探究金属的化学性质,可使用锌片、铁片、银片、稀硫酸、 4溶液、 4
溶液进行下列实验,请回答下列问题。
①向孔穴 1 和 2 中分别滴加稀硫酸,孔穴 3 中滴加 4溶
液。孔穴 1中的现象: 。
孔穴 1、2、3 中的实验可以验证出金属活动性顺序为
。
②利用所给试剂能证明铁比铜活泼的化学方程式是 。
(5)为验证氨气能与水反应,需进行的操作及现象是 。
(6)化学小组同学完成如图 4 所示三个实验。在 a 处连接压强传感器,得到曲线 1、2、3,
这三条曲线分别表示加入等体积相应液体后,烧瓶 1、2、3内压强随时间的变化趋势。
请回答下列问题。
①请分析三个实验的起始阶段压强都快速增大的原因: 。
②能证明二氧化碳和氢氧化钠一定发生了化学反应的证据是 。
12.(7 分)阅读下面科普短文。
面包是一种深受消费者喜爱的烘焙食品。霉菌是导致面包腐败变质的主要原因。根
据机制不同,面包的防腐技术分为物理防腐、化学防腐以及天然生物防腐。丙酸钙是面
包工业化生产中常用的化学防腐剂。为探究丙酸钙防霉的效果,分别按下列①~⑧的配方
蒸制8个馒头,冷却后置于密封袋中,记录如表1:
表 1
组别 第 1组 第 2组
序号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
面粉/g 50 50 50 50 50 50 50 50
酵母/g 0.75 0.75 0.75 0.75 0.75 0.75 0.75 0.75
配方
蔗糖/g 0 0 0 0 5 5 5 5
丙酸钙/g 0 0.06 0.10 0.15 0 0.06 0.10 0.15
开始发霉时间 第 3天 第 4天 第 5天 第 6天 第 3天 第 4天 第 5天 第 6天
啤酒花,亦称蛇麻草,在啤酒酿造过程中不仅能使啤酒产生特有的风味,还可以起
到防腐作用,能抑制许多腐败菌滋生,将啤酒花添加到面包中作为天然防腐剂是可选的。
研究人员用相同的配方、相同的面包制作工艺,并按照使用标准中规定的含量上限添加啤
酒花和丙酸钙。将烘烤结束的面包冷却至常温,将不同样品储放至第 4 天,其菌落总数见
表 2:
表 2
检测指标 检测结果_ 国家标准要求
未添加防腐剂: 1.2 × 10
菌落总数( 添加啤酒花: 1.3 × 10 <1500
添加丙酸钙: 5.5 × 10
脱氢乙酸钠是较为常见的食品添加剂,是一种低毒高效的广谱性防腐剂,其价格低
廉,商家为了延长食品保质期,通常会添加脱氢乙酸钠。
根据国家卫生健康委、市场监管总局发布的《食品安全国家标准食品添加剂使用标
准》 (GB 2760—2024), 自 2025 年 2 月 8 日起, 脱氢乙酸钠 (脱氢乙酸及其钠盐) 不再
用于面包、糕点、果蔬汁 (浆)等 7类食品,在腌渍蔬菜中的最大使用量也由 1克/千克
调整为 0.3 克/千克。这意味着,原来面包、糕点、烘焙食品中常见的脱氢乙酸钠被禁
用。依据所给信息,回答下列问题。
(1)面包的防腐技术有 。
(2)面包中加入丙酸钙除了防腐,还可能具有 作用。
(3)分析表 1中第 2组实验数据,可以得出的结论是 。
(4)根据表 1,能证明“有无蔗糖对丙酸钙防霉效果无影响”的证据是 。
(5)根据表 1,可能影响丙酸钙防霉效果的因素有 。
(6)由表 2 可知,丙酸钙比啤酒花的抑菌防腐效果好,依据是 。
(7)根据短文中的介绍推测脱氢乙酸钠的一条化学性质: 。
13.(6 分)聚焦珊瑚礁破坏与保护。
【活动 1】珊瑚礁的形成原理
(1)海洋中的珊瑚虫通过一系列钙化作用形成石灰石外壳,这些石灰石经过压实、石化,形成
岛屿和礁石,珊瑚礁形成过程中发生了 (填“物理”或“化学”)变化。
(2)根据海水中含碳元素的微粒分布图可以获得的信息有 。
(答出一条即可)
【活动 2】珊瑚礁的破坏
3 2能引起海水酸化,其化学方程式为 。
(4)据预测海水的 pH 将于本世纪末降至 7:8,届时珊瑚礁可能消失的原因是
。 (答出一条即可)
【活动 3】珊瑚礁的保护
(5)保护珊瑚礁的关键是减少( 2的含量,请从两个不同角度提出措施: 、 。
14.(13 分)中国是茶叶的故乡, “围炉煮茶”已成为一种休闲生活方式。化学活动小组围绕
“茶”进行了项目式探究。
【任务 1】种植茶树
(1)茶树在 pH 为 4.5~6.5 的土壤中生长为佳,该土壤属于 (填“酸性”或“碱性”)
土壤。
(2)测定土壤酸碱度可使用 。
(3)种茶常施用的化学尿素 2 2 属于 (填“氮肥”或“复合肥料”)。
【任务 2】泡制茶汤
(4)选择茶具:现选用三种不同材质的茶具泡同一品牌龙井茶,测量茶汤中风味物质儿茶素
类和咖啡碱的含量。测量结果如下:
浸泡时间/ m 儿茶素类含量/(mg/g) 咖啡碱含量/(mg/g)
in 紫砂壶 瓷质盖碗 玻璃杯 紫砂壶 瓷质盖碗 玻璃杯
2 155 162 151 25 26 26
4 201 223 214 32 36 35
以下属于该实验需控制的变量是 (填标号)。
A.水温 B.水量 C.水样 D.煮水方式 E.茶叶用量
结论:不同材质的茶具对茶汤风味虽有一定影响,但差异不大,生活中按需选择即可。
(5)冲泡茶叶需高提水壶,水自高点下注,使茶叶在壶内翻滚散开,高冲的作用相当于实验基
本操作 (填标号)。
A.蒸发 B.搅拌 C.升华
【任务 3】探究茶垢剂
(6)茶垢剂的主要成分为过碳酸钠,化学式为 2 2 3 3 2 2。过碳酸钠是一种白色粉末,
常温下与水能反应生成) 2 3和 2 2。下列物质能使茶垢剂失效的是 (填
标号)。
A.硫酸 B.氢氧化钙 C.二氧化锰 D.氯化钠
(7)小组同学设计了如图装置,通过测定( 2质量来测定茶垢清洁剂中过碳酸钠的含
量。主要步骤:
a.检查装置气密性。
b.向锥形瓶中加入 10g 样品。
c.通入氮气一段时间后,称量装置 C 的质量为 132.0g。 (该碱石灰是由氢氧化钠和氧
化钙组成的混合固体)……
d.缓慢滴加适量稀硫酸至 A中。(假设茶垢清洁剂中其他成分不参与反应)
e.再通入氮气一段时间后,再次称量装置 C的质量为 134.2g。
请回答下列问题:
①实验中分液漏斗中放入稀硫酸比盐酸好的理由: 。
②确定向 A中滴加稀硫酸已足够的现象: 。
③浓硫酸的作用: 。
④反应前通入氮气的目的: 。
⑤反应结束后继续通入氮气的作用是 。
⑥装置 D中碱石灰的作用: 。
⑦计算茶垢清洁剂样品中过碳酸钠的质量分数为 。
1. D 2. A 3. C 4. D 5. A 6. B 7. B 8. D 9. D 10. B
11.(14 分) (1)①红磷燃烧产生大量白烟,反应前后天平保持平衡 ②红磷燃烧放热会使
瓶内压强增大,导致气球胀大产生浮力,影响测量结果
(2) ①CDAB ②量筒、胶头滴管
(3)①化合物→单质 ②化学反应前后元素种类不变 ③消除单一实验的偶然性 (或提高了
结论的可靠性)
(4)①铁表面有气泡产生,溶液由无色变为浅绿色 Zn>Fe>Ag
② + 4 = 4 +
(5)取 3 朵干燥的紫色石蕊纸花,向第一朵纸花喷水,将第二朵纸花放入盛有氨气的集气
瓶中,纸花均未变蓝;将第三朵纸花喷水后放入盛有氨气的集气瓶中,纸花变蓝,则证明氨
气能与水反应 (合理即可)
(6)①注入的液体压缩了烧瓶内的气体 ②对比曲线 1 和曲线 3 可知,二氧化碳和氢氧化
钠一定发生了化学反应
12.(7 分) (1)物理防腐、化学防腐以及天然生物防腐
(2) 补钙
(3)当面粉质量、蔗糖质量、酵母质量等其他条件相同时,丙酸钙质量越大,防霉效果越
好
(4)对比②⑥、③⑦、④⑧数据发现,有无蔗糖,面包开始发霉的时间均相同
(5)面粉的种类(答案合理即可)
(6)在实验研究范围内,当储存到第 4 天时,添加丙酸钙的面包菌落总数比添加啤酒花的
少
(7)脱氢乙酸钠化学性质稳定 (答案合理即可)
13. (6 分) (1) 化学
(2)当 pH 为 7.8 时,海水中含量最多的微观粒子为 HCO (答案合理即可)
3 2 + 2 = 2 3
(4)CaCO 能和酸反应,海水酸化能促进 CaCO 溶解,导致珊瑚礁减少 (答案合理即可)
(5)减少化石燃料的燃烧 植树造林 (答案合理即可)
14. (13 分) (1) 酸性
(2) pH 试纸 (或 pH 计)
(3) 氮肥
(4) ABCDE
(5) B
(6) ABC
(7)①盐酸具有挥发性
②向 A中滴加稀硫酸至不再产生气泡
③吸收水分,干燥气体
④为了排尽装置内的空气
⑤为了将装置内滞留的二氧化碳驱赶到装置 C中
⑥防止空气中二氧化碳和水蒸气进入装置 C中,对实验造成干扰
⑦78.5%
同课章节目录
