2.2.1烯烃 课件(共20张PPT) 2024-2025学年人教版(2019)高中化学选择性必修3
文档属性
| 名称 | 2.2.1烯烃 课件(共20张PPT) 2024-2025学年人教版(2019)高中化学选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 22.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-11 00:00:00 | ||
图片预览






文档简介
(共20张PPT)
第二章 第二节 烯烃 炔烃
人教版高中化学选择性必修三
第1课时 烯烃
《格物粗谈》:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”
生活中的化学
乙烯
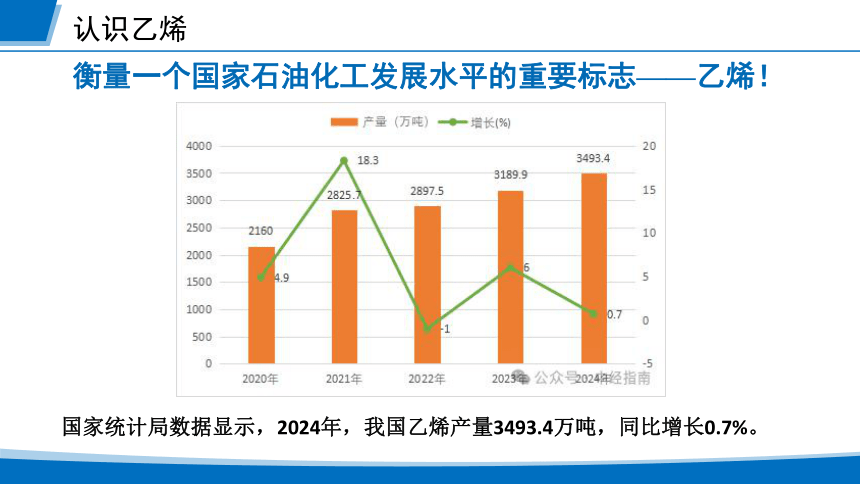
衡量一个国家石油化工发展水平的重要标志——乙烯!
认识乙烯
国家统计局数据显示,2024年,我国乙烯产量3493.4万吨,同比增长0.7%。
一、烯烃的结构特点
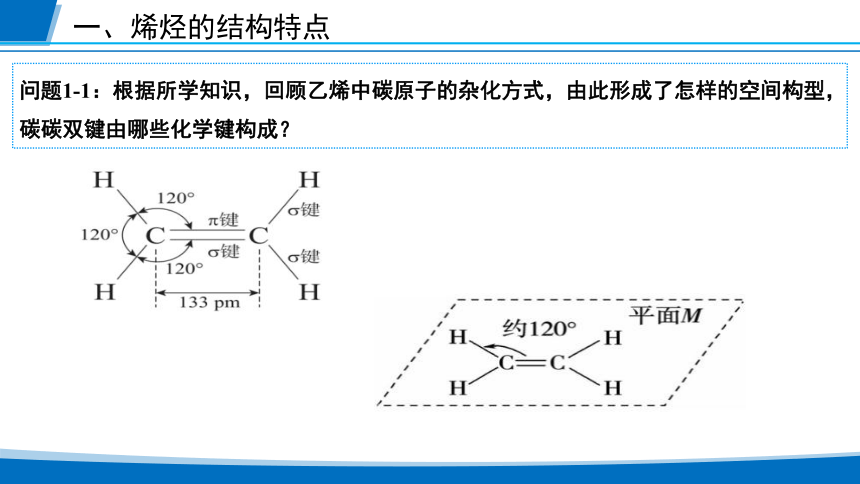
问题1-1:根据所学知识,回顾乙烯中碳原子的杂化方式,由此形成了怎样的空间构型,碳碳双键由哪些化学键构成?
问题1-2:结合教材p35图2-3,写出它们的分子式、官能团的名称,总结共同点。
一、烯烃的结构特点
1、烯烃:
分子里含有碳碳双键的不饱和链烃叫烯烃。
2、单烯烃:分子中只含有一个碳碳双键的链状烯烃称为“单烯烃”
分子式通式为:CnH2n(n 2)
一、烯烃的结构特点
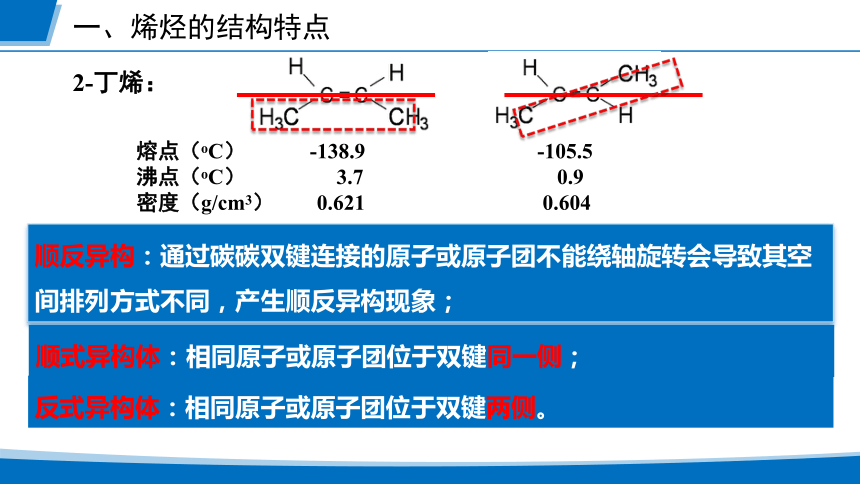
2-丁烯:
熔点(oC) -138.9 -105.5
沸点(oC) 3.7 0.9
密度(g/cm3) 0.621 0.604
顺反异构:通过碳碳双键连接的原子或原子团不能绕轴旋转会导致其空间排列方式不同,产生顺反异构现象;
顺式异构体:相同原子或原子团位于双键同一侧;
反式异构体:相同原子或原子团位于双键两侧。
问题1-3:所有烯烃都具有顺反异构吗?判断1-丁烯(H3C—CH2CH=CH2)是否存在顺反异构?思考产生顺反异构现象的条件是什么?
形成顺反异构的条件:
组成双键的每个碳原子必须连接两个不同的原子或原子团 。
无顺反异构
有顺反异构
一、烯烃的结构特点
一、烯烃的结构特点
【随堂检测】
下列物质中,存在顺反异构的是( )
A.CH2=CHCH2Cl
B.CH2=CClCH3
C.ClCH=CHCH3
C
问题1-4:回顾乙烯的化学性质,对比烷烃,烯烃可发生什么特殊的化学反应?为什么碳碳双键使得烯烃的化学性质较为活泼?
易氧化
能加成
能加聚
键轨道重叠程度小于 键,易断裂,属于反应活性部位!
二、烯烃的性质
2、烯烃的化学性质
二、烯烃的性质
思考1:回顾乙烯和溴单质的反应,讨论反应中官能团和化学键有哪些变化?
试剂 乙烯
溴
卤代烃
烯烃
加成反应化学键的断裂与生成:旧不饱和π键的断裂,新 键的形成
(1)加成反应特征:只进不出
试剂 乙烯
氯化氢
水
二、烯烃的性质
任务1-1:两人合作用球棍模型演示丙烯与氯化氢加成的过程,并展示产物的结构。
思考2:对比乙烯的加成反应,为什么丙烯和氯化氢的加成反应会有两种不同的产物?
甲基
双键碳原子的化学环境不同
两种加成产物
主?
副?
二、烯烃的性质
主
2-氯丙烷
受外界条件和基团间电子效应的影响下,加成反应的结果是:含双键的有机物分别与试剂中带相反电荷的原子或原子团结合,生产反应产物。
不对称烯烃的加成反应模型:
任务1-2:依据不对称烯烃发生加成反应的原理,写出丙烯和水反应的方程式,并判断出主、副反应。
二、烯烃的性质
试剂 丙烯
水 主反应:
副反应:
如何得到主产物1-丙醇?
任务1-3:请回顾乙烯的加聚反应,依次写出乙烯、丙烯的加聚反应。
二、烯烃的性质
单体
聚合度
链节
(2)加聚反应模型:
双键改单键,不饱和碳连成链,非H原子上下摆。
任务1-4:写出异丁烯(CH3 )2C=CH2发生加聚反应的化学方程式
二、烯烃的性质
b.烯烃都能使酸性KMnO4溶液褪色
二、烯烃的性质
(3)氧化反应
a.与氧气反应
烯烃与氧气、酸性KMnO4的反应较为复杂,产物众多,烯烃的氧化反应将在下一节课详细讲解!
二、烯烃的性质
任务1-5:乙烯有哪些物理性质?结合单烯烃的结构简式及熔沸点、相对密度数据,并类比烷烃的物理性质,总结烯烃物理性质的递变规律。
名称 结构式 熔点℃ 沸点℃ 相对密度
乙烯 H2C=CH2 -169. 1 -103.7 0.566
丙烯 H3C—HC=CH2 -185.3 -47.4 0.5193
1-丁烯 H3C—CH2CH2=CH2 -183.4 -6.3 0.5951
1-戊烯 CH3CH2CH2CH=CH2 -138 30 0.6405
升高
增大,< 水
(1)溶解性:难溶于水,易溶于有机溶剂
二、烯烃的性质
随着分子中碳原子数的递增,
(2)相对分子质量越大, 分子间作用力越强, 熔、沸点逐渐升高。
(3)密度逐渐增大,都小于水的密度。
(1)溶解性:不溶于水,易溶于有机溶剂
1、烯烃的物理性质
导致
影响
应用
反映
决定
二、烯烃的性质
有机反应较为复杂,在研究有机合成时,需要关注外界条件和基团间的电子效应对化学反应的影响。
课后作业
完成优佳学案配套检测卷p192-193页基础·巩固,
能力提升部分选做。
第二章 第二节 烯烃 炔烃
人教版高中化学选择性必修三
第1课时 烯烃
《格物粗谈》:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味”
生活中的化学
乙烯
衡量一个国家石油化工发展水平的重要标志——乙烯!
认识乙烯
国家统计局数据显示,2024年,我国乙烯产量3493.4万吨,同比增长0.7%。
一、烯烃的结构特点
问题1-1:根据所学知识,回顾乙烯中碳原子的杂化方式,由此形成了怎样的空间构型,碳碳双键由哪些化学键构成?
问题1-2:结合教材p35图2-3,写出它们的分子式、官能团的名称,总结共同点。
一、烯烃的结构特点
1、烯烃:
分子里含有碳碳双键的不饱和链烃叫烯烃。
2、单烯烃:分子中只含有一个碳碳双键的链状烯烃称为“单烯烃”
分子式通式为:CnH2n(n 2)
一、烯烃的结构特点
2-丁烯:
熔点(oC) -138.9 -105.5
沸点(oC) 3.7 0.9
密度(g/cm3) 0.621 0.604
顺反异构:通过碳碳双键连接的原子或原子团不能绕轴旋转会导致其空间排列方式不同,产生顺反异构现象;
顺式异构体:相同原子或原子团位于双键同一侧;
反式异构体:相同原子或原子团位于双键两侧。
问题1-3:所有烯烃都具有顺反异构吗?判断1-丁烯(H3C—CH2CH=CH2)是否存在顺反异构?思考产生顺反异构现象的条件是什么?
形成顺反异构的条件:
组成双键的每个碳原子必须连接两个不同的原子或原子团 。
无顺反异构
有顺反异构
一、烯烃的结构特点
一、烯烃的结构特点
【随堂检测】
下列物质中,存在顺反异构的是( )
A.CH2=CHCH2Cl
B.CH2=CClCH3
C.ClCH=CHCH3
C
问题1-4:回顾乙烯的化学性质,对比烷烃,烯烃可发生什么特殊的化学反应?为什么碳碳双键使得烯烃的化学性质较为活泼?
易氧化
能加成
能加聚
键轨道重叠程度小于 键,易断裂,属于反应活性部位!
二、烯烃的性质
2、烯烃的化学性质
二、烯烃的性质
思考1:回顾乙烯和溴单质的反应,讨论反应中官能团和化学键有哪些变化?
试剂 乙烯
溴
卤代烃
烯烃
加成反应化学键的断裂与生成:旧不饱和π键的断裂,新 键的形成
(1)加成反应特征:只进不出
试剂 乙烯
氯化氢
水
二、烯烃的性质
任务1-1:两人合作用球棍模型演示丙烯与氯化氢加成的过程,并展示产物的结构。
思考2:对比乙烯的加成反应,为什么丙烯和氯化氢的加成反应会有两种不同的产物?
甲基
双键碳原子的化学环境不同
两种加成产物
主?
副?
二、烯烃的性质
主
2-氯丙烷
受外界条件和基团间电子效应的影响下,加成反应的结果是:含双键的有机物分别与试剂中带相反电荷的原子或原子团结合,生产反应产物。
不对称烯烃的加成反应模型:
任务1-2:依据不对称烯烃发生加成反应的原理,写出丙烯和水反应的方程式,并判断出主、副反应。
二、烯烃的性质
试剂 丙烯
水 主反应:
副反应:
如何得到主产物1-丙醇?
任务1-3:请回顾乙烯的加聚反应,依次写出乙烯、丙烯的加聚反应。
二、烯烃的性质
单体
聚合度
链节
(2)加聚反应模型:
双键改单键,不饱和碳连成链,非H原子上下摆。
任务1-4:写出异丁烯(CH3 )2C=CH2发生加聚反应的化学方程式
二、烯烃的性质
b.烯烃都能使酸性KMnO4溶液褪色
二、烯烃的性质
(3)氧化反应
a.与氧气反应
烯烃与氧气、酸性KMnO4的反应较为复杂,产物众多,烯烃的氧化反应将在下一节课详细讲解!
二、烯烃的性质
任务1-5:乙烯有哪些物理性质?结合单烯烃的结构简式及熔沸点、相对密度数据,并类比烷烃的物理性质,总结烯烃物理性质的递变规律。
名称 结构式 熔点℃ 沸点℃ 相对密度
乙烯 H2C=CH2 -169. 1 -103.7 0.566
丙烯 H3C—HC=CH2 -185.3 -47.4 0.5193
1-丁烯 H3C—CH2CH2=CH2 -183.4 -6.3 0.5951
1-戊烯 CH3CH2CH2CH=CH2 -138 30 0.6405
升高
增大,< 水
(1)溶解性:难溶于水,易溶于有机溶剂
二、烯烃的性质
随着分子中碳原子数的递增,
(2)相对分子质量越大, 分子间作用力越强, 熔、沸点逐渐升高。
(3)密度逐渐增大,都小于水的密度。
(1)溶解性:不溶于水,易溶于有机溶剂
1、烯烃的物理性质
导致
影响
应用
反映
决定
二、烯烃的性质
有机反应较为复杂,在研究有机合成时,需要关注外界条件和基团间的电子效应对化学反应的影响。
课后作业
完成优佳学案配套检测卷p192-193页基础·巩固,
能力提升部分选做。
