2025年河南省驻马店市汝南县中考二模化学试卷(含答案)
文档属性
| 名称 | 2025年河南省驻马店市汝南县中考二模化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 460.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-10 00:00:00 | ||
图片预览



文档简介
2025年河南省驻马店市汝南县中考二模化学试题
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.下列变化属于物理变化的是
A.石灰水变质 B.铁的锈蚀 C.氢气燃烧 D.氢氧化钠的潮解
2.中国科学家为化学的发展作出了巨大贡献,其中为相对原子质量的测定作出卓越贡献的科学家是
A.李四光 B.侯德榜 C.张青莲 D.华罗庚
3.对下列宏观事实的微观解释,合理的是
A.醋与糖味道不同:不同种分子性质不同
B.金刚石与石墨的硬度不同:构成它们的原子不同
C.蔗糖在热水中溶解更快:温度升高使分子间隔增大
D.加压可将6000L氧气装入40L的钢瓶中:加压使分子变小
4.北斗卫星使用了中国自主研发的铷(Rb)原子钟,精度达到每300万年误差一秒。铷原子的结构示意图及其在元素周期表中的信息如图所示,下列说法错误的是
A.铷原子核内的质子数为37 B.铷原子的相对原子质量为85.47
C.铷原子在化学变化中容易失去1个电子 D.该元素排在第四周期
5.我省沁州黄小米不仅色泽金黄、味道香美,而且营养丰富。在种植过程中要增强小米的抗病虫和抗倒伏能力,可以施用( )
A.KCl B.NH4NO3 C.CO(NH2)2 D.Ca(H2PO4)2
6.糖类是人体最主要的能量来源,存在于许多食物中。下列食物中富含糖类的是
A.红烧鲤鱼 B.凉拌黄瓜 C.清炒蒜苗 D.炒米饭
7.2024年中国水周的主题为“精打细算用好水资源,从严从细管好水资源”。下列与水相关的说法错误的是
A.农业上提倡喷灌或滴灌
B.水由氢气和氧气组成
C.生活中可用煮沸的方法降低水的硬度
D.活性炭可吸附水中的异味和色素
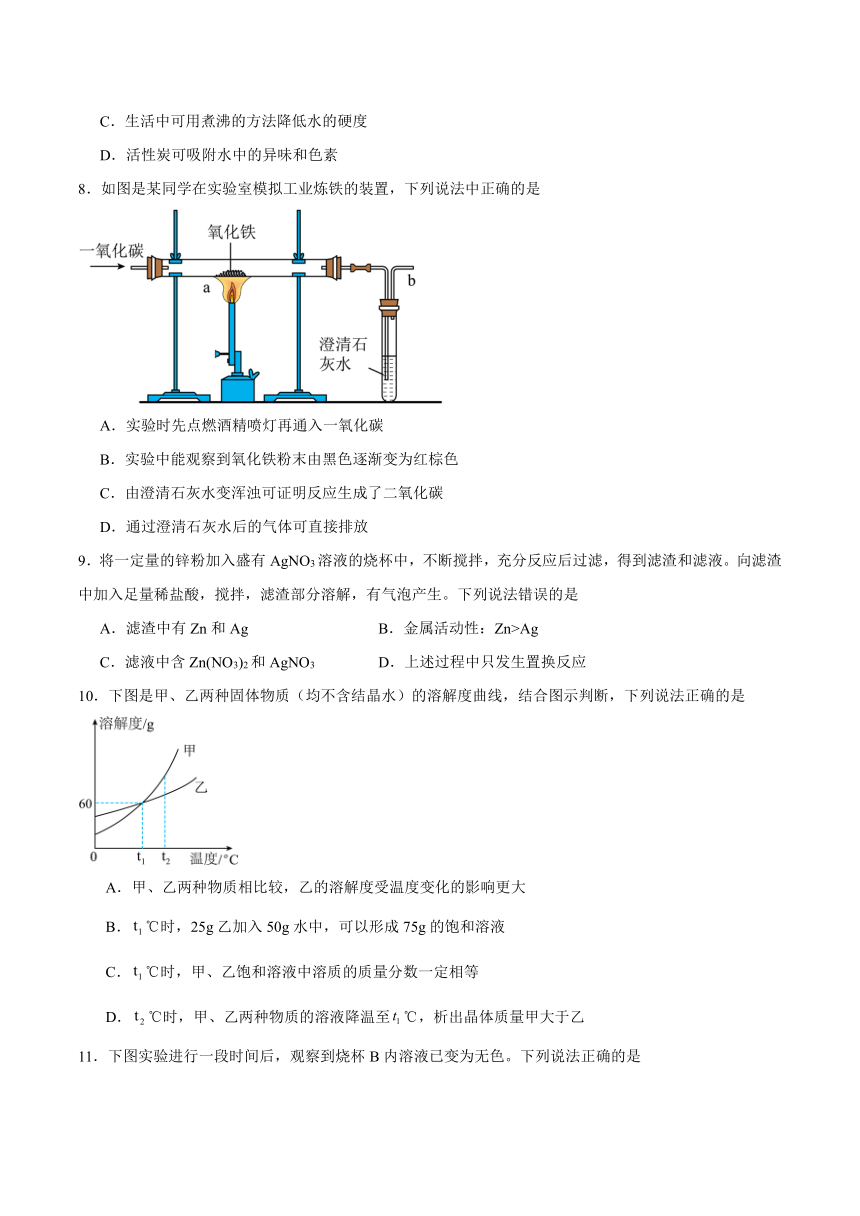
8.如图是某同学在实验室模拟工业炼铁的装置,下列说法中正确的是
A.实验时先点燃酒精喷灯再通入一氧化碳
B.实验中能观察到氧化铁粉末由黑色逐渐变为红棕色
C.由澄清石灰水变浑浊可证明反应生成了二氧化碳
D.通过澄清石灰水后的气体可直接排放
9.将一定量的锌粉加入盛有AgNO3溶液的烧杯中,不断搅拌,充分反应后过滤,得到滤渣和滤液。向滤渣中加入足量稀盐酸,搅拌,滤渣部分溶解,有气泡产生。下列说法错误的是
A.滤渣中有Zn和Ag B.金属活动性:Zn>Ag
C.滤液中含Zn(NO3)2和AgNO3 D.上述过程中只发生置换反应
10.下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,结合图示判断,下列说法正确的是
A.甲、乙两种物质相比较,乙的溶解度受温度变化的影响更大
B.℃时,25g乙加入50g水中,可以形成75g的饱和溶液
C.℃时,甲、乙饱和溶液中溶质的质量分数一定相等
D.℃时,甲、乙两种物质的溶液降温至℃,析出晶体质量甲大于乙
11.下图实验进行一段时间后,观察到烧杯B内溶液已变为无色。下列说法正确的是
A.实验能说明浓盐酸具有吸水性
B.烧杯A内溶液的溶质质量分数不变
C.烧杯B内溶液无色说明溶液呈中性
D.烧杯B内发生反应的实质是
12.小宁测得部分物品的pH如表所示,其中碱性最强的是
A.杨梅(PH≈3) B.蜜橘(PH≈4.5)
C.鸡蛋清(PH≈7.8) D.草木灰(PH≈11.5)
13.下列叙述能正确表示对应图像的是
A.等质量的铝片,铁片分别与足量且质量分数相同的稀硫酸反应
B.一定量的镁在装有空气的密闭容器里燃烧
C.向一定量硝酸钾的不饱和溶液中加入硝酸钾
D.向一定量的稀硫酸中不断加水稀释
14.实验室有部分被氧化的镁条8.0g与300.0g溶质质量分数为7.3%的稀盐酸恰好完全反应,该镁条中镁元素的质量为
A.7.8g B.7.2g C.6.0g D.2.4g
二、填空与简答
15.化学用语是学习化学的重要工具。
(1)空气中含量最高的元素,其元素符号是 ;
(2)钴酸锂(LiCoO2)常用作手机等电子设备的锂离子电池正极材料,其中Li的化合价为+1价,则Co的化合价为 。
16.古籍《天工开物》就有“煤饼烧石成灰”的记载。“烧石成灰”指高温条件下碳酸钙转化为生石灰,该反应的化学方程式为 。“灰”遇水成浆时反应的化学方程式为 。
17.中国传统文化中蕴含着许多化学知识。
(1)《富春山居图》是元代画家黄公望创作的水墨画,此画能够保存至今而不变色的原因是 。
(2)根据碳-14断定,中国的制陶工艺已有上万年的历史。碳-14是含有6个质子和8个中子的碳原子,其核外电子数是 。
(3)成语“钻木取火”说明燃烧的条件之一是需要 。
18.2024年1月,我国自主研制的第一架以氢内燃机为动力的通航飞机在辽宁成功首飞,氢气作为燃料的优点是 ,高纯度氢气可以通过电解水制得,反应的化学方程式为 ;水蒸气和高温铁屑反应是更为经济的制取氢气方法,化学方程式为,X化学式为 。
19.金属在人类文明中至关重要,请根据金属性质完成以下练习题。
(1)始建于明代的西安地标建筑——“钟楼”,外观为红柱绿瓦,蔚为壮观。红柱上红漆呈红色主要是因其含有一种铁的氧化物,该氧化物可能是 (填化学式)。
(2)生铁和钢都属于铁合金,主要区别是生铁的比钢的含碳量 (填“高”或“低”)。
(3)铝的活动性比铁强,铝制品在空气中却表现出良好的抗腐蚀性能,用化学方程式表示其原因 。
20.古籍中有记载制烧碱的方法,核心环节是纯碱和熟石灰的反应,该反应的化学方程式为 。制出的烧碱可配制成溶液用于制作叶脉书签,现配制200g溶质质量分数为10%的NaOH溶液,需NaOH的质量为 g,量水时俯视读数,则所配溶液溶质质量分数 (填“偏大”“偏小”或“不变”)。
21.燃气壁挂炉已成为家庭常用取暖设备。
(1)液态天然气变为气态时,体积扩大约600倍。请从微观角度解释该现象。
(2)打开壁挂炉点火开关、天然气燃烧。请写出反应的化学方程式。
22.利用如图装置探究燃烧的条件(白磷着火点为40℃,红磷的着火点为 试回答:
(1)通过比较图甲装置内 (填字母)两处的实验现象,可推导出燃烧条件之一是“温度需达到可燃物的着火点”。
(2)图乙中能正确反映气球内气压ρ随反应时间t而发生的变化的是 (填字母)。
23.A~F是初中化学常见的六种物质,已知A是人体胃液中的一种物质,可帮助消化;B、C、E在常温常压下为无色无味的气体,C、D、E为氧化物,F为固体。它们之间的转换关系如下图所示。(“→”表示一种物质可以转化为另一种物质,“—”表示相连两物质之间可以发生反应,部分反应物。生成物以及反应条件省略)。请回答下列问题:
(1)物质A的化学式是 ;
(2)物质F的用途是 (任写一种即可)。
(3)实验室制取气体B的化学反应方程式为: 。
三、实验题
24.实验室用如图装置制取一瓶干燥的氧气。
(1)甲装置中发生反应的化学方程式为 。
(2)乙装置中液体是 (填试剂名称)。
(3)能用丙装置收集氧气,是因为氧气的密度 (填大于或小于)空气。
四、综合应用题
25.酸、碱、盐物质与人类日常生活和工农业生产关系十分密切。
(1)物质是由微观粒子构成的,氯化钠的构成微粒是 (用化学用语填写)。
(2)侯德榜是我国制碱工业的先驱。这里的“碱”化学式为 ,它属于 (填“酸”、“碱”或“盐”)
(3)如图是向氢氧化钠溶液中逐滴滴加稀硫酸时,用温度传感器测定溶液温度的变化曲线。
①该反应的化学方程式为 。
②该反应属于 (填“吸热”或“放热”)反应。
(4)某同学用如图所示装置探究氢氧化钠与二氧化碳的反应。
步骤1:夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。
步骤2:一段时间后,打开弹簧夹,观察现象。
①写出步骤1发生反应的化学方程式 。
②步骤2打开弹簧夹后观察到的现象是 。
(5)小佳同学向盛有铜与氧化铜粉末共22g的固体混合物中加入100g稀硫酸恰好完全反应,过滤得到滤液和6g滤渣,请计算所用稀硫酸中溶质的质量分数?
《2025年河南省驻马店市汝南县中考二模化学试题》参考答案
1.D
2.C
3.A
4.D
5.A
6.D
7.B
8.C
9.C
10.C
11.D
12.D
13.C
14.B
15.(1)N
(2)+3
16. CaO+H2O=Ca(OH)2
17.(1)常温下碳的化学性质稳定
(2)6
(3)温度达到可燃物的着火点
18. 热值高(合理即可) Fe3O4
19.(1)Fe2O3
(2)高
(3)4Al+3O2=2Al2O3
20. 20 偏大
21.(1)分子间有间隔,温度升高,间隔变大
(2)
22.(1)a和b
(2)B
23.(1)HCl
(2)作燃料(合理即可)
(3)
24.(1)
(2)浓硫酸
(3)大于
25.(1)Na+、Cl-(或Na+和Cl-,合理即可)
(2) 盐
(3) 放热
(4) 烧杯中氯化钙溶液倒流进锥形瓶内,产生白色沉淀
(5)解:固体混合物中氧化铜的质量为:22g-6g=16g。
设100g稀硫酸中溶质的质量为x。
x=19.6g
稀硫酸中溶质的质量分数为:
答:所用稀硫酸中溶质的质量分数为19.6%。
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.下列变化属于物理变化的是
A.石灰水变质 B.铁的锈蚀 C.氢气燃烧 D.氢氧化钠的潮解
2.中国科学家为化学的发展作出了巨大贡献,其中为相对原子质量的测定作出卓越贡献的科学家是
A.李四光 B.侯德榜 C.张青莲 D.华罗庚
3.对下列宏观事实的微观解释,合理的是
A.醋与糖味道不同:不同种分子性质不同
B.金刚石与石墨的硬度不同:构成它们的原子不同
C.蔗糖在热水中溶解更快:温度升高使分子间隔增大
D.加压可将6000L氧气装入40L的钢瓶中:加压使分子变小
4.北斗卫星使用了中国自主研发的铷(Rb)原子钟,精度达到每300万年误差一秒。铷原子的结构示意图及其在元素周期表中的信息如图所示,下列说法错误的是
A.铷原子核内的质子数为37 B.铷原子的相对原子质量为85.47
C.铷原子在化学变化中容易失去1个电子 D.该元素排在第四周期
5.我省沁州黄小米不仅色泽金黄、味道香美,而且营养丰富。在种植过程中要增强小米的抗病虫和抗倒伏能力,可以施用( )
A.KCl B.NH4NO3 C.CO(NH2)2 D.Ca(H2PO4)2
6.糖类是人体最主要的能量来源,存在于许多食物中。下列食物中富含糖类的是
A.红烧鲤鱼 B.凉拌黄瓜 C.清炒蒜苗 D.炒米饭
7.2024年中国水周的主题为“精打细算用好水资源,从严从细管好水资源”。下列与水相关的说法错误的是
A.农业上提倡喷灌或滴灌
B.水由氢气和氧气组成
C.生活中可用煮沸的方法降低水的硬度
D.活性炭可吸附水中的异味和色素
8.如图是某同学在实验室模拟工业炼铁的装置,下列说法中正确的是
A.实验时先点燃酒精喷灯再通入一氧化碳
B.实验中能观察到氧化铁粉末由黑色逐渐变为红棕色
C.由澄清石灰水变浑浊可证明反应生成了二氧化碳
D.通过澄清石灰水后的气体可直接排放
9.将一定量的锌粉加入盛有AgNO3溶液的烧杯中,不断搅拌,充分反应后过滤,得到滤渣和滤液。向滤渣中加入足量稀盐酸,搅拌,滤渣部分溶解,有气泡产生。下列说法错误的是
A.滤渣中有Zn和Ag B.金属活动性:Zn>Ag
C.滤液中含Zn(NO3)2和AgNO3 D.上述过程中只发生置换反应
10.下图是甲、乙两种固体物质(均不含结晶水)的溶解度曲线,结合图示判断,下列说法正确的是
A.甲、乙两种物质相比较,乙的溶解度受温度变化的影响更大
B.℃时,25g乙加入50g水中,可以形成75g的饱和溶液
C.℃时,甲、乙饱和溶液中溶质的质量分数一定相等
D.℃时,甲、乙两种物质的溶液降温至℃,析出晶体质量甲大于乙
11.下图实验进行一段时间后,观察到烧杯B内溶液已变为无色。下列说法正确的是
A.实验能说明浓盐酸具有吸水性
B.烧杯A内溶液的溶质质量分数不变
C.烧杯B内溶液无色说明溶液呈中性
D.烧杯B内发生反应的实质是
12.小宁测得部分物品的pH如表所示,其中碱性最强的是
A.杨梅(PH≈3) B.蜜橘(PH≈4.5)
C.鸡蛋清(PH≈7.8) D.草木灰(PH≈11.5)
13.下列叙述能正确表示对应图像的是
A.等质量的铝片,铁片分别与足量且质量分数相同的稀硫酸反应
B.一定量的镁在装有空气的密闭容器里燃烧
C.向一定量硝酸钾的不饱和溶液中加入硝酸钾
D.向一定量的稀硫酸中不断加水稀释
14.实验室有部分被氧化的镁条8.0g与300.0g溶质质量分数为7.3%的稀盐酸恰好完全反应,该镁条中镁元素的质量为
A.7.8g B.7.2g C.6.0g D.2.4g
二、填空与简答
15.化学用语是学习化学的重要工具。
(1)空气中含量最高的元素,其元素符号是 ;
(2)钴酸锂(LiCoO2)常用作手机等电子设备的锂离子电池正极材料,其中Li的化合价为+1价,则Co的化合价为 。
16.古籍《天工开物》就有“煤饼烧石成灰”的记载。“烧石成灰”指高温条件下碳酸钙转化为生石灰,该反应的化学方程式为 。“灰”遇水成浆时反应的化学方程式为 。
17.中国传统文化中蕴含着许多化学知识。
(1)《富春山居图》是元代画家黄公望创作的水墨画,此画能够保存至今而不变色的原因是 。
(2)根据碳-14断定,中国的制陶工艺已有上万年的历史。碳-14是含有6个质子和8个中子的碳原子,其核外电子数是 。
(3)成语“钻木取火”说明燃烧的条件之一是需要 。
18.2024年1月,我国自主研制的第一架以氢内燃机为动力的通航飞机在辽宁成功首飞,氢气作为燃料的优点是 ,高纯度氢气可以通过电解水制得,反应的化学方程式为 ;水蒸气和高温铁屑反应是更为经济的制取氢气方法,化学方程式为,X化学式为 。
19.金属在人类文明中至关重要,请根据金属性质完成以下练习题。
(1)始建于明代的西安地标建筑——“钟楼”,外观为红柱绿瓦,蔚为壮观。红柱上红漆呈红色主要是因其含有一种铁的氧化物,该氧化物可能是 (填化学式)。
(2)生铁和钢都属于铁合金,主要区别是生铁的比钢的含碳量 (填“高”或“低”)。
(3)铝的活动性比铁强,铝制品在空气中却表现出良好的抗腐蚀性能,用化学方程式表示其原因 。
20.古籍中有记载制烧碱的方法,核心环节是纯碱和熟石灰的反应,该反应的化学方程式为 。制出的烧碱可配制成溶液用于制作叶脉书签,现配制200g溶质质量分数为10%的NaOH溶液,需NaOH的质量为 g,量水时俯视读数,则所配溶液溶质质量分数 (填“偏大”“偏小”或“不变”)。
21.燃气壁挂炉已成为家庭常用取暖设备。
(1)液态天然气变为气态时,体积扩大约600倍。请从微观角度解释该现象。
(2)打开壁挂炉点火开关、天然气燃烧。请写出反应的化学方程式。
22.利用如图装置探究燃烧的条件(白磷着火点为40℃,红磷的着火点为 试回答:
(1)通过比较图甲装置内 (填字母)两处的实验现象,可推导出燃烧条件之一是“温度需达到可燃物的着火点”。
(2)图乙中能正确反映气球内气压ρ随反应时间t而发生的变化的是 (填字母)。
23.A~F是初中化学常见的六种物质,已知A是人体胃液中的一种物质,可帮助消化;B、C、E在常温常压下为无色无味的气体,C、D、E为氧化物,F为固体。它们之间的转换关系如下图所示。(“→”表示一种物质可以转化为另一种物质,“—”表示相连两物质之间可以发生反应,部分反应物。生成物以及反应条件省略)。请回答下列问题:
(1)物质A的化学式是 ;
(2)物质F的用途是 (任写一种即可)。
(3)实验室制取气体B的化学反应方程式为: 。
三、实验题
24.实验室用如图装置制取一瓶干燥的氧气。
(1)甲装置中发生反应的化学方程式为 。
(2)乙装置中液体是 (填试剂名称)。
(3)能用丙装置收集氧气,是因为氧气的密度 (填大于或小于)空气。
四、综合应用题
25.酸、碱、盐物质与人类日常生活和工农业生产关系十分密切。
(1)物质是由微观粒子构成的,氯化钠的构成微粒是 (用化学用语填写)。
(2)侯德榜是我国制碱工业的先驱。这里的“碱”化学式为 ,它属于 (填“酸”、“碱”或“盐”)
(3)如图是向氢氧化钠溶液中逐滴滴加稀硫酸时,用温度传感器测定溶液温度的变化曲线。
①该反应的化学方程式为 。
②该反应属于 (填“吸热”或“放热”)反应。
(4)某同学用如图所示装置探究氢氧化钠与二氧化碳的反应。
步骤1:夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。
步骤2:一段时间后,打开弹簧夹,观察现象。
①写出步骤1发生反应的化学方程式 。
②步骤2打开弹簧夹后观察到的现象是 。
(5)小佳同学向盛有铜与氧化铜粉末共22g的固体混合物中加入100g稀硫酸恰好完全反应,过滤得到滤液和6g滤渣,请计算所用稀硫酸中溶质的质量分数?
《2025年河南省驻马店市汝南县中考二模化学试题》参考答案
1.D
2.C
3.A
4.D
5.A
6.D
7.B
8.C
9.C
10.C
11.D
12.D
13.C
14.B
15.(1)N
(2)+3
16. CaO+H2O=Ca(OH)2
17.(1)常温下碳的化学性质稳定
(2)6
(3)温度达到可燃物的着火点
18. 热值高(合理即可) Fe3O4
19.(1)Fe2O3
(2)高
(3)4Al+3O2=2Al2O3
20. 20 偏大
21.(1)分子间有间隔,温度升高,间隔变大
(2)
22.(1)a和b
(2)B
23.(1)HCl
(2)作燃料(合理即可)
(3)
24.(1)
(2)浓硫酸
(3)大于
25.(1)Na+、Cl-(或Na+和Cl-,合理即可)
(2) 盐
(3) 放热
(4) 烧杯中氯化钙溶液倒流进锥形瓶内,产生白色沉淀
(5)解:固体混合物中氧化铜的质量为:22g-6g=16g。
设100g稀硫酸中溶质的质量为x。
x=19.6g
稀硫酸中溶质的质量分数为:
答:所用稀硫酸中溶质的质量分数为19.6%。
同课章节目录
