广东省肇庆鼎湖中学2023-2024学年高二下学期期末统考模拟测试化学试卷(含答案)
文档属性
| 名称 | 广东省肇庆鼎湖中学2023-2024学年高二下学期期末统考模拟测试化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-10 00:00:00 | ||
图片预览




文档简介
广东省肇庆市肇庆鼎湖中学2023-2024学年高二下学期期末统考模拟测试化学试题
一、单选题
1.下列物品不是由合成有机高分子材料制成的是
物品
选项 A.宇宙飞船返回舱的涤纶降落伞 B.纯羊毛上衣 C.家用净水器中的聚酰胺超滤膜 D.聚氯乙烯塑胶羽毛球场地板
A.A B.B C.C D.D
2.化学符号是化学学科进行思维的最基本的工具,下列微粒的化学符号表述正确的是
A.基态Zn原子的价层电子排布图:
B.丙酮的球棍模型:
C.乙酸甲酯的结构简式:C3H6O2
D.NH3的电子式:
3.下列过程中,共价键被破坏的是
A.干冰升华 B.食盐溶于水 C.乙烯燃烧 D.钢铁熔化
4.下列有关晶体的说法正确的是
A.共价晶体的熔点一定高于金属晶体
B.白磷是分子晶体,石英是共价晶体
C.圆柱形容器中结出的冰是圆柱形的,体现了晶体的自范性
D.共价晶体中只含有共价键,离子晶体中只含有离子键
5.CH4、NH3、H2O和HF是第二周期常见元素的简单氢化物。下列说法不正确的是
A.H-F是s-pσ键
B.H2O属于极性分子,CH4属于非极性分子
C.CH4、NH3、H2O和HF的沸点依次升高
D.NH3中H-N-H的键角大于H2O中H-O-H的键角
6.化学与生产、生活密切相关。下列生产生活中的实际应用,涉及的相应化学原理不正确的是
选项 实际应用 化学原理
A 聚丙烯酰胺可作“尿不湿”吸水材料 聚丙烯酰胺中的氨基具有亲水性
B 用汽油可洗掉衣服上的油漆 物质“相似相溶”
C CH3CH2Cl可作冷冻镇痛剂 CH3CH2Cl能发生消去反应
D 节日燃放的焰火 电子发生跃迁
A.A B.B C.C D.D
7.冠醚与碱金属离子结合形成超分子,可以用于制备新型的电池材料。部分冠醚的结构简式如图所示。下列说法不正确的是
A.1 mol 15-冠-5含有5NA个C-C
B.18-冠-6与15-冠-5互为同素异形体
C.冠醚只含有醚键1种官能团
D.冠醚通过不同大小的空穴适配不同的碱金属离子,体现超分子“分子识别”的特征
8.化学为甲流防控提供了强有力的支撑。下列说法正确的是
A.甲流疫苗中含有的卵清蛋白属于小分子化合物
B.75%的酒精能有效杀灭甲流病毒,主要利用了乙醇的强氧化性
C.医用输液瓶主要原料为聚乙烯,其结构简式为
D.甲流患者痊愈后可适当摄入淀粉和肉类食物,为身体补充能量
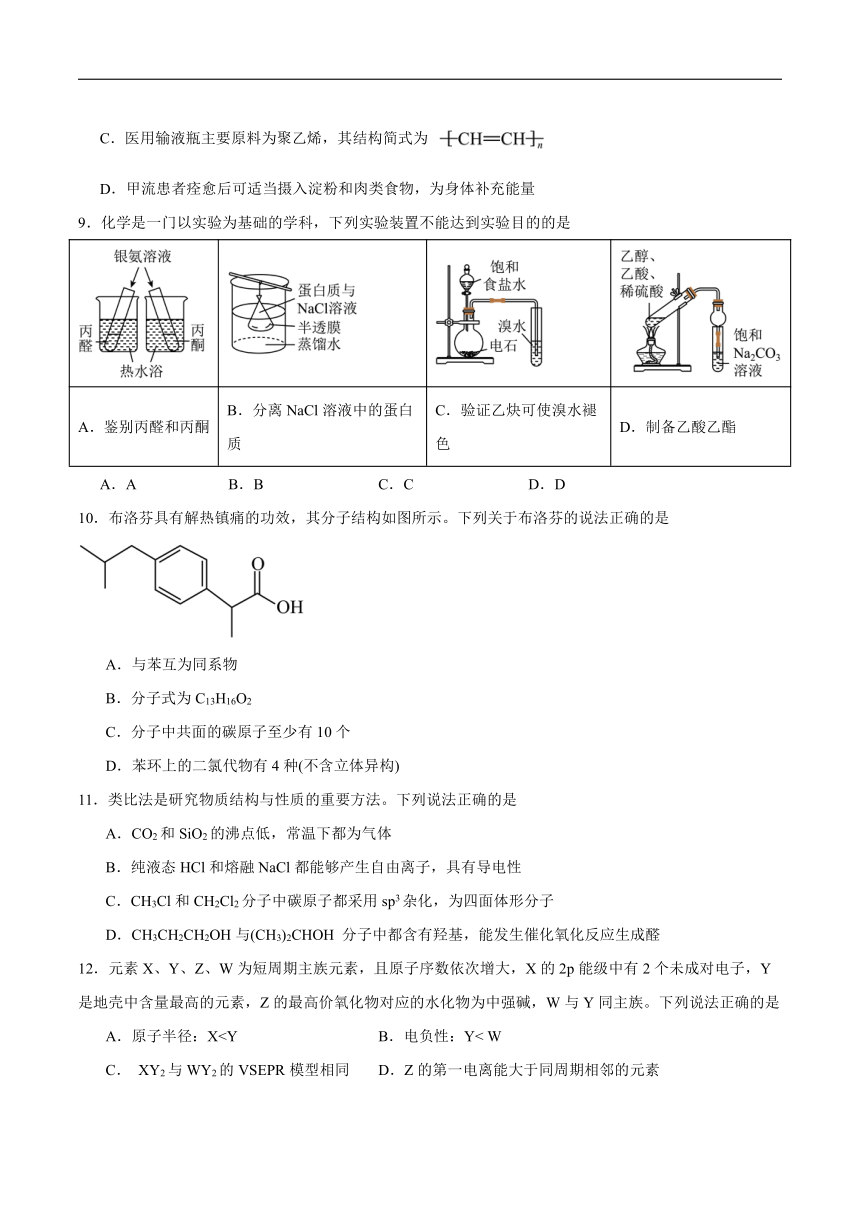
9.化学是一门以实验为基础的学科,下列实验装置不能达到实验目的的是
A.鉴别丙醛和丙酮 B.分离NaCl溶液中的蛋白质 C.验证乙炔可使溴水褪色 D.制备乙酸乙酯
A.A B.B C.C D.D
10.布洛芬具有解热镇痛的功效,其分子结构如图所示。下列关于布洛芬的说法正确的是
A.与苯互为同系物
B.分子式为C13H16O2
C.分子中共面的碳原子至少有10个
D.苯环上的二氯代物有4种(不含立体异构)
11.类比法是研究物质结构与性质的重要方法。下列说法正确的是
A.CO2和SiO2的沸点低,常温下都为气体
B.纯液态HCl和熔融NaCl都能够产生自由离子,具有导电性
C.CH3Cl和CH2Cl2分子中碳原子都采用sp3杂化,为四面体形分子
D.CH3CH2CH2OH与(CH3)2CHOH 分子中都含有羟基,能发生催化氧化反应生成醛
12.元素X、Y、Z、W为短周期主族元素,且原子序数依次增大,X的2p能级中有2个未成对电子,Y是地壳中含量最高的元素,Z的最高价氧化物对应的水化物为中强碱,W与Y同主族。下列说法正确的是
A.原子半径:XC. XY2与WY2的VSEPR模型相同 D.Z的第一电离能大于同周期相邻的元素
13.“下列对实验事实的解释不正确的是
选项 实验事实 解释
A 乙酸的酸性弱于甲酸 乙酸中“-CH3” 是推电子基团,羧基中羟基的极性较小,酸性较弱
B HF的稳定性强于HCl H-F的键长比H-Cl短,键能较大,分子更稳定
C 对羟基苯甲酸的沸点高于邻羟基苯甲酸 对羟基苯甲酸分子间存在氢键
D I2的熔点高于Br2 碘原子的电负性大于溴原子
A.A B.B C.C D.D
14.有机物Z是一种常见的医药中间体,可由有机物X和Y在一定条件下反应制得。下列说法不正确的是
A.有机物X中含有1个手性碳原子
B.该反应的类型为加成反应
C.有机物Y难溶于水
D.有机物Z能发生加成反应、取代反应
15.有机物A是一种常见的黄酮类化合物,具有抗肿瘤、抗病毒的功能,其分子结构如图所示。下列关于有机物A的说法不正确的是
A.有4种官能团
B.不能发生水解反应
C.能与NaHCO3溶液反应产生CO2
D.1 mol有机物A最多能与5 mol Br2发生反应
16.下列实验操作能达到实验目的的是
选项 实验操作 实验目的
A 向苯中加入适量酸性高锰酸钾溶液,振荡,观察溶液是否褪色 检验苯分子中是否含碳碳双键
B 向盛有CH3CH2Br的试管中加入适量NaOH溶液,加热并充分反应后,再加入几滴AgNO3溶液 验证CH3CH2Br的水解产物中有NaBr
C 向装有苯和苯酚混合物的分液漏斗中加入足量溴水,充分反应后分液 除去苯中混有的苯酚
D 向盛有少量淀粉溶液的试管中加入几滴稀硫酸,加热一段时间后,加入几滴新制Cu(OH)2悬浊液,继续加热 验证淀粉的水解产物中有葡萄糖
A.A B.B C.C D.D
二、解答题
17.苯甲酸甲酯( )常用作合成树脂和橡胶的溶剂以及聚酯纤维的助染剂。某化学实验小组以苯甲酸( )和甲醇(CH3OH) 为原料,利用如图所示的装置制备苯甲酸甲酯。
已知:各物质的沸点以及25℃时在水中的溶解度如下表所示。
物质 苯甲酸 甲醇 苯甲酸甲酯
沸点/℃ 249 64.7 199.6
溶解度 微溶于水 与水互溶 难溶于水
回答下列问题:
(1)仪器A的名称为 ,仪器B的作用是 ,冷却水方向为 (填“上”或“下”,下同)口进 口出。
(2)向仪器A中加入12.2 g苯甲酸和足量甲醇,再小心加入2 mL浓硫酸和几块碎瓷片,点燃酒精灯加热一段时间,得到苯甲酸甲酯粗产品。
①写出该反应的化学方程式: 。
②浓硫酸的作用有 。
(3)将仪器A中反应后的液体转移到烧杯中,依次使用水洗、饱和Na2CO3溶液洗、水洗,每次洗涤后,将有机层和水层分离的操作是 。
(4)洗涤后,利用蒸馏装置将有机层进行蒸馏,收集 ℃的馏分。
(5)若蒸馏后,最终收集得到10.88 g产品,则本实验中苯甲酸甲酯的产率为 。
18.钴素有“工业的牙齿”“工业味精”之称,自我国大力推广锂离子电池等新能源以来,钴的消耗量逐年攀升。一种从废旧锂电池中回收钻资源的工艺流程如图所示。
回答下列问题:
(1)钴在元素周期表的位置为 ;下列基态或激发态Mn原子价层电子排布图中,能量最高的是 (填标号)。
A. B. C.
(2)已知电解熔融CoCl2也能制备金属钴,则CoCl2的晶体类型是 。CoCl2熔点为735 ℃,CoF2熔点为1 200℃,试分析CoCl2的熔点比CoF2的熔点低的原因: 。
(3)步骤④中,为了检测固体上是否有Ni2+残留,可将最后一次洗涤液加入氨水和丁二酮肟(镍试剂)的混合物中。若有残留,则会生成一种含镍的整合物沉淀,其结构如图所示。
该螯合物中,碳原子采用的杂化方式有 ;该物质结构中存在的作用力有极性共价键、非极性共价键、 。
(4)工业上利用CoO生产钴蓝。钴蓝是一种无毒、耐高温的颜料,可用于制作蓝色钴玻璃,其主要成分是Co(AlO2)2,阴离子的空间结构为 。
19.五水硫酸铜(CuSO4·5H2O),俗名蓝矾、胆矾,具有催吐、解毒、祛腐的作用。回答下列问题:
(1)基态硫原子的价层电子排布式为 。
(2)CuSO4·5H2O可写作[Cu(H2O)4]SO4·5H2O,其中 为配位体,配位数为 。
(3)铜的某种氧化物是一种新型的半导体光催化剂,晶胞结构如图所示,其化学式为 。
①晶胞中O2-周围距离最近且相等的O2-共有 个,设A原子坐标为(0,0,0),B原子坐标为(1,1,1),则C原子坐标为 。
②已知该晶体密度为ρ g/cm3,阿伏加德罗常数用NA表示,则晶胞的棱长为 nm(列出计算式即可)。
20.丁苯酞是我国自主研发的一种治疗缺血性脑梗死的药物,其合成路线如图所示。
已知:
回答下列问题:
(1)有机物A的名称为 ;A→B的反应类型为 。
(2)反应1的条件是 ;有机物C的官能团名称为 。
(3)写出反应2的化学方程式: 。
(4)有机物G通过分子内脱水可得到丁苯酞,写出G的结构简式: 。
(5)有机物H与F的组成元素相同,且相对分子质量比F小28,写出符合下列条件的H的其中一种同分异构体: 。
①能与FeCl3溶液发生显色反应;②核磁共振氢谱有4 组峰,且峰面积之比为6:2:2:1
(6)参考题中信息和所学知识,写出以CH3CH2Br为原料制备CH3CH2CH(OH)CH3的合成路线 (其他无机试剂任选)。
参考答案
1.B
2.B
3.C
4.B
5.C
6.C
7.B
8.D
9.C
10.D
11.C
12.D
13.D
14.A
15.C
16.A
17.(1) 圆底烧瓶 冷凝回流反应物 下 上
(2) +CH3OH+H2O 催化剂、吸水剂
(3)分液
(4)199.6
(5)80%
18.(1) 第四周期Ⅷ族 A
(2) 离子晶体 同为离子晶体,离子所带电荷数相同,且r(C1-)>r(F-),CoCl2中的离子键较弱,熔点较低
(3) sp2杂化和sp3杂化 氢键、配位键
(4)直线形
19.(1)3s23p4
(2) H2O 4
(3) Cu2O 8 (,,) ×107
20.(1) 邻溴甲苯(或2-溴甲苯) 取代反应
(2) NaOH水溶液、加热 羟基、碳溴键
(3)CH2=C(CH3)2+HBr→(CH3)3CBr
(4)
(5)或或
(6)
一、单选题
1.下列物品不是由合成有机高分子材料制成的是
物品
选项 A.宇宙飞船返回舱的涤纶降落伞 B.纯羊毛上衣 C.家用净水器中的聚酰胺超滤膜 D.聚氯乙烯塑胶羽毛球场地板
A.A B.B C.C D.D
2.化学符号是化学学科进行思维的最基本的工具,下列微粒的化学符号表述正确的是
A.基态Zn原子的价层电子排布图:
B.丙酮的球棍模型:
C.乙酸甲酯的结构简式:C3H6O2
D.NH3的电子式:
3.下列过程中,共价键被破坏的是
A.干冰升华 B.食盐溶于水 C.乙烯燃烧 D.钢铁熔化
4.下列有关晶体的说法正确的是
A.共价晶体的熔点一定高于金属晶体
B.白磷是分子晶体,石英是共价晶体
C.圆柱形容器中结出的冰是圆柱形的,体现了晶体的自范性
D.共价晶体中只含有共价键,离子晶体中只含有离子键
5.CH4、NH3、H2O和HF是第二周期常见元素的简单氢化物。下列说法不正确的是
A.H-F是s-pσ键
B.H2O属于极性分子,CH4属于非极性分子
C.CH4、NH3、H2O和HF的沸点依次升高
D.NH3中H-N-H的键角大于H2O中H-O-H的键角
6.化学与生产、生活密切相关。下列生产生活中的实际应用,涉及的相应化学原理不正确的是
选项 实际应用 化学原理
A 聚丙烯酰胺可作“尿不湿”吸水材料 聚丙烯酰胺中的氨基具有亲水性
B 用汽油可洗掉衣服上的油漆 物质“相似相溶”
C CH3CH2Cl可作冷冻镇痛剂 CH3CH2Cl能发生消去反应
D 节日燃放的焰火 电子发生跃迁
A.A B.B C.C D.D
7.冠醚与碱金属离子结合形成超分子,可以用于制备新型的电池材料。部分冠醚的结构简式如图所示。下列说法不正确的是
A.1 mol 15-冠-5含有5NA个C-C
B.18-冠-6与15-冠-5互为同素异形体
C.冠醚只含有醚键1种官能团
D.冠醚通过不同大小的空穴适配不同的碱金属离子,体现超分子“分子识别”的特征
8.化学为甲流防控提供了强有力的支撑。下列说法正确的是
A.甲流疫苗中含有的卵清蛋白属于小分子化合物
B.75%的酒精能有效杀灭甲流病毒,主要利用了乙醇的强氧化性
C.医用输液瓶主要原料为聚乙烯,其结构简式为
D.甲流患者痊愈后可适当摄入淀粉和肉类食物,为身体补充能量
9.化学是一门以实验为基础的学科,下列实验装置不能达到实验目的的是
A.鉴别丙醛和丙酮 B.分离NaCl溶液中的蛋白质 C.验证乙炔可使溴水褪色 D.制备乙酸乙酯
A.A B.B C.C D.D
10.布洛芬具有解热镇痛的功效,其分子结构如图所示。下列关于布洛芬的说法正确的是
A.与苯互为同系物
B.分子式为C13H16O2
C.分子中共面的碳原子至少有10个
D.苯环上的二氯代物有4种(不含立体异构)
11.类比法是研究物质结构与性质的重要方法。下列说法正确的是
A.CO2和SiO2的沸点低,常温下都为气体
B.纯液态HCl和熔融NaCl都能够产生自由离子,具有导电性
C.CH3Cl和CH2Cl2分子中碳原子都采用sp3杂化,为四面体形分子
D.CH3CH2CH2OH与(CH3)2CHOH 分子中都含有羟基,能发生催化氧化反应生成醛
12.元素X、Y、Z、W为短周期主族元素,且原子序数依次增大,X的2p能级中有2个未成对电子,Y是地壳中含量最高的元素,Z的最高价氧化物对应的水化物为中强碱,W与Y同主族。下列说法正确的是
A.原子半径:X
13.“下列对实验事实的解释不正确的是
选项 实验事实 解释
A 乙酸的酸性弱于甲酸 乙酸中“-CH3” 是推电子基团,羧基中羟基的极性较小,酸性较弱
B HF的稳定性强于HCl H-F的键长比H-Cl短,键能较大,分子更稳定
C 对羟基苯甲酸的沸点高于邻羟基苯甲酸 对羟基苯甲酸分子间存在氢键
D I2的熔点高于Br2 碘原子的电负性大于溴原子
A.A B.B C.C D.D
14.有机物Z是一种常见的医药中间体,可由有机物X和Y在一定条件下反应制得。下列说法不正确的是
A.有机物X中含有1个手性碳原子
B.该反应的类型为加成反应
C.有机物Y难溶于水
D.有机物Z能发生加成反应、取代反应
15.有机物A是一种常见的黄酮类化合物,具有抗肿瘤、抗病毒的功能,其分子结构如图所示。下列关于有机物A的说法不正确的是
A.有4种官能团
B.不能发生水解反应
C.能与NaHCO3溶液反应产生CO2
D.1 mol有机物A最多能与5 mol Br2发生反应
16.下列实验操作能达到实验目的的是
选项 实验操作 实验目的
A 向苯中加入适量酸性高锰酸钾溶液,振荡,观察溶液是否褪色 检验苯分子中是否含碳碳双键
B 向盛有CH3CH2Br的试管中加入适量NaOH溶液,加热并充分反应后,再加入几滴AgNO3溶液 验证CH3CH2Br的水解产物中有NaBr
C 向装有苯和苯酚混合物的分液漏斗中加入足量溴水,充分反应后分液 除去苯中混有的苯酚
D 向盛有少量淀粉溶液的试管中加入几滴稀硫酸,加热一段时间后,加入几滴新制Cu(OH)2悬浊液,继续加热 验证淀粉的水解产物中有葡萄糖
A.A B.B C.C D.D
二、解答题
17.苯甲酸甲酯( )常用作合成树脂和橡胶的溶剂以及聚酯纤维的助染剂。某化学实验小组以苯甲酸( )和甲醇(CH3OH) 为原料,利用如图所示的装置制备苯甲酸甲酯。
已知:各物质的沸点以及25℃时在水中的溶解度如下表所示。
物质 苯甲酸 甲醇 苯甲酸甲酯
沸点/℃ 249 64.7 199.6
溶解度 微溶于水 与水互溶 难溶于水
回答下列问题:
(1)仪器A的名称为 ,仪器B的作用是 ,冷却水方向为 (填“上”或“下”,下同)口进 口出。
(2)向仪器A中加入12.2 g苯甲酸和足量甲醇,再小心加入2 mL浓硫酸和几块碎瓷片,点燃酒精灯加热一段时间,得到苯甲酸甲酯粗产品。
①写出该反应的化学方程式: 。
②浓硫酸的作用有 。
(3)将仪器A中反应后的液体转移到烧杯中,依次使用水洗、饱和Na2CO3溶液洗、水洗,每次洗涤后,将有机层和水层分离的操作是 。
(4)洗涤后,利用蒸馏装置将有机层进行蒸馏,收集 ℃的馏分。
(5)若蒸馏后,最终收集得到10.88 g产品,则本实验中苯甲酸甲酯的产率为 。
18.钴素有“工业的牙齿”“工业味精”之称,自我国大力推广锂离子电池等新能源以来,钴的消耗量逐年攀升。一种从废旧锂电池中回收钻资源的工艺流程如图所示。
回答下列问题:
(1)钴在元素周期表的位置为 ;下列基态或激发态Mn原子价层电子排布图中,能量最高的是 (填标号)。
A. B. C.
(2)已知电解熔融CoCl2也能制备金属钴,则CoCl2的晶体类型是 。CoCl2熔点为735 ℃,CoF2熔点为1 200℃,试分析CoCl2的熔点比CoF2的熔点低的原因: 。
(3)步骤④中,为了检测固体上是否有Ni2+残留,可将最后一次洗涤液加入氨水和丁二酮肟(镍试剂)的混合物中。若有残留,则会生成一种含镍的整合物沉淀,其结构如图所示。
该螯合物中,碳原子采用的杂化方式有 ;该物质结构中存在的作用力有极性共价键、非极性共价键、 。
(4)工业上利用CoO生产钴蓝。钴蓝是一种无毒、耐高温的颜料,可用于制作蓝色钴玻璃,其主要成分是Co(AlO2)2,阴离子的空间结构为 。
19.五水硫酸铜(CuSO4·5H2O),俗名蓝矾、胆矾,具有催吐、解毒、祛腐的作用。回答下列问题:
(1)基态硫原子的价层电子排布式为 。
(2)CuSO4·5H2O可写作[Cu(H2O)4]SO4·5H2O,其中 为配位体,配位数为 。
(3)铜的某种氧化物是一种新型的半导体光催化剂,晶胞结构如图所示,其化学式为 。
①晶胞中O2-周围距离最近且相等的O2-共有 个,设A原子坐标为(0,0,0),B原子坐标为(1,1,1),则C原子坐标为 。
②已知该晶体密度为ρ g/cm3,阿伏加德罗常数用NA表示,则晶胞的棱长为 nm(列出计算式即可)。
20.丁苯酞是我国自主研发的一种治疗缺血性脑梗死的药物,其合成路线如图所示。
已知:
回答下列问题:
(1)有机物A的名称为 ;A→B的反应类型为 。
(2)反应1的条件是 ;有机物C的官能团名称为 。
(3)写出反应2的化学方程式: 。
(4)有机物G通过分子内脱水可得到丁苯酞,写出G的结构简式: 。
(5)有机物H与F的组成元素相同,且相对分子质量比F小28,写出符合下列条件的H的其中一种同分异构体: 。
①能与FeCl3溶液发生显色反应;②核磁共振氢谱有4 组峰,且峰面积之比为6:2:2:1
(6)参考题中信息和所学知识,写出以CH3CH2Br为原料制备CH3CH2CH(OH)CH3的合成路线 (其他无机试剂任选)。
参考答案
1.B
2.B
3.C
4.B
5.C
6.C
7.B
8.D
9.C
10.D
11.C
12.D
13.D
14.A
15.C
16.A
17.(1) 圆底烧瓶 冷凝回流反应物 下 上
(2) +CH3OH+H2O 催化剂、吸水剂
(3)分液
(4)199.6
(5)80%
18.(1) 第四周期Ⅷ族 A
(2) 离子晶体 同为离子晶体,离子所带电荷数相同,且r(C1-)>r(F-),CoCl2中的离子键较弱,熔点较低
(3) sp2杂化和sp3杂化 氢键、配位键
(4)直线形
19.(1)3s23p4
(2) H2O 4
(3) Cu2O 8 (,,) ×107
20.(1) 邻溴甲苯(或2-溴甲苯) 取代反应
(2) NaOH水溶液、加热 羟基、碳溴键
(3)CH2=C(CH3)2+HBr→(CH3)3CBr
(4)
(5)或或
(6)
同课章节目录
