安徽省桐城中学2024-2025学年高二下学期五月份阶段性考试化学(A)试卷(图片版,含解析)
文档属性
| 名称 | 安徽省桐城中学2024-2025学年高二下学期五月份阶段性考试化学(A)试卷(图片版,含解析) |  | |
| 格式 | |||
| 文件大小 | 6.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-10 17:17:52 | ||
图片预览



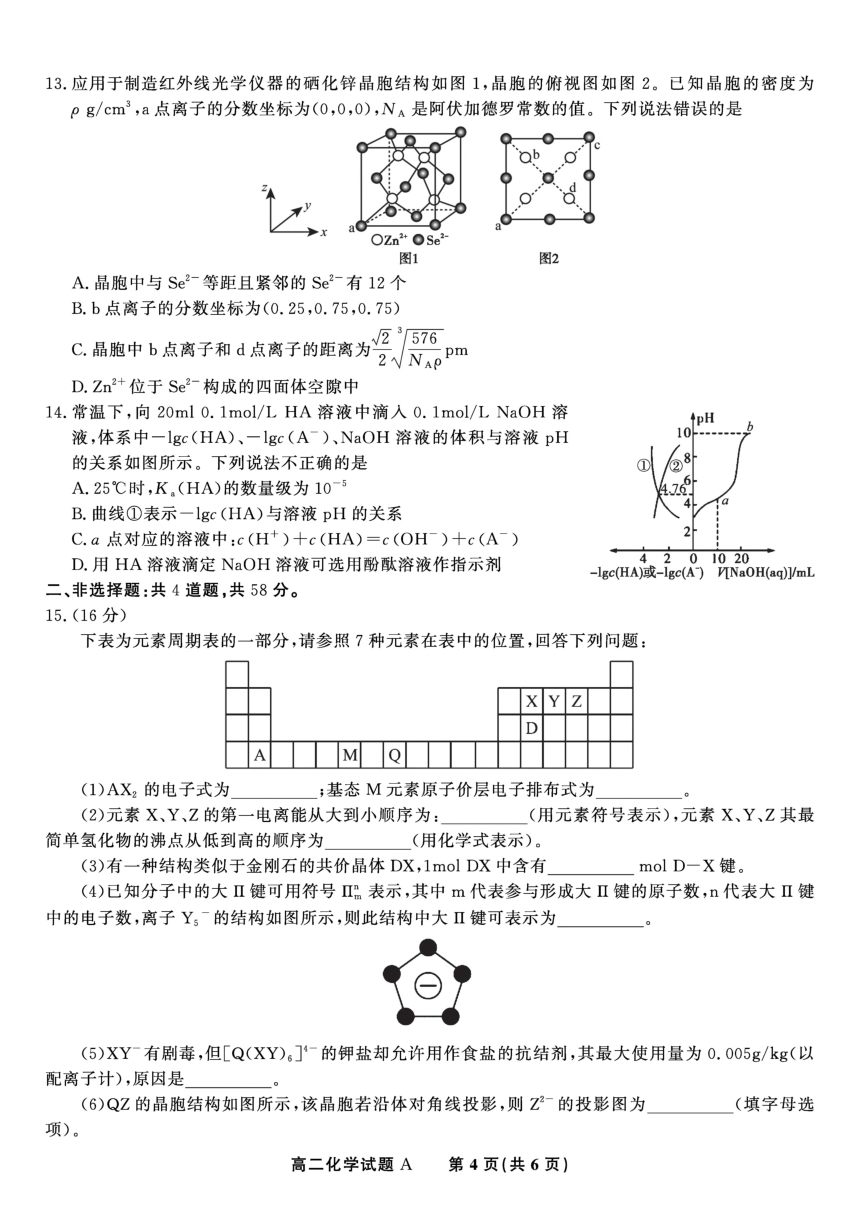
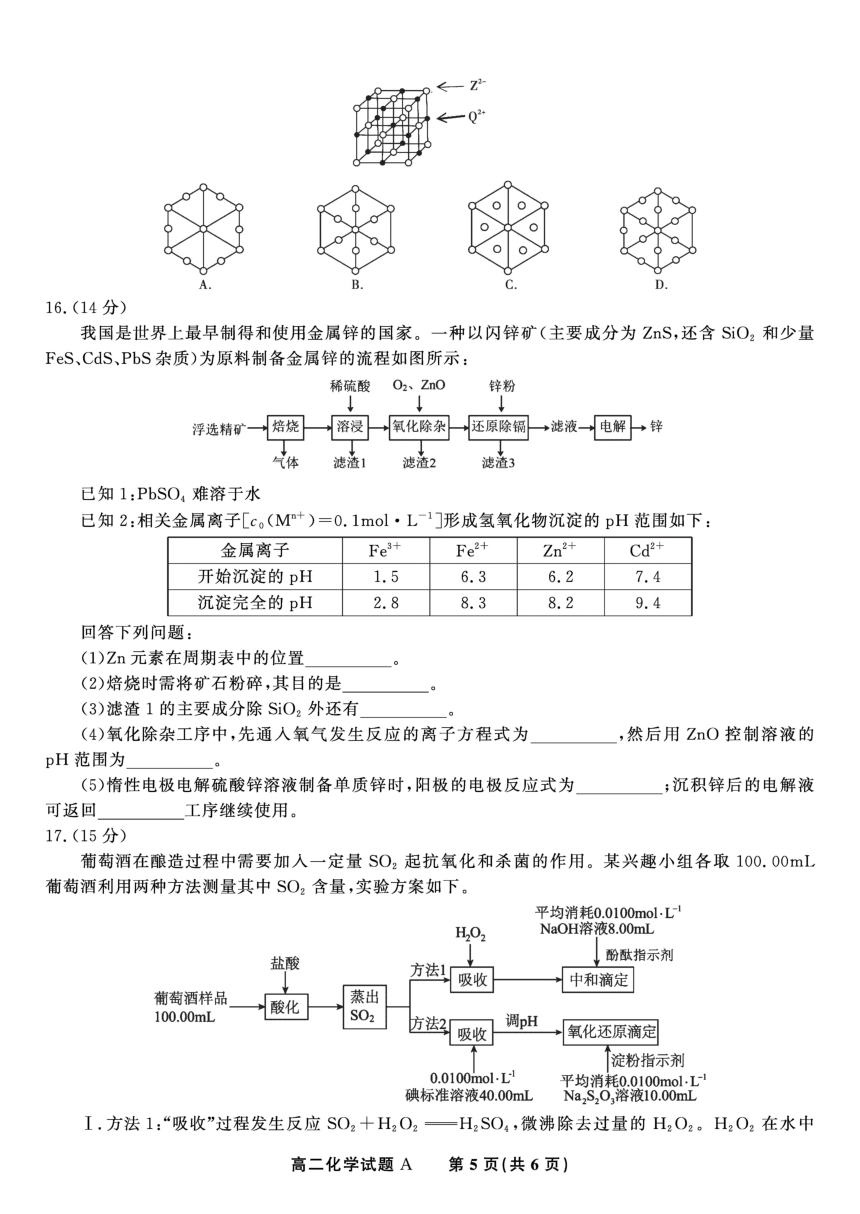
文档简介
高二化学参考答案A
一、 选择题(每小题只有一个正确选项, 每小题3分,14小题共42分) 。
题号 1 2 3 4 5 6 7 8
答案 B A D B D c D C
题号 9 10 11 12 13 14
答案 A C C D C C
1. B【知识点】 石 墨的性质、 干冰的性质、 原子核外电子的跃迁,氢键
【解析】 A.铅笔芯的主要成分为石墨,A正确; B. 干冰是固态的二氧化碳,干冰升华时,吸收大量
的热,使周围温度降低,大量的水蒸气凝结成了小液滴,形成“云雾”效果,升华为物理变化,共价键
没有断裂, B错误C. 焰火、 激光、 霓虹灯光都与原子核外电子跃迁释放能量有关, C正确D.天然气
水合物是巨大的潜在能源,水分子以氢键相连构成的笼容纳甲烷、 乙烷等气体,D正确 。
2. A【知识点】 原子轨道式,基团的结构简式,价层电子对互斥理论,共价键的类型
【解 析 】 A. K能层只有 1个能级 1s,不存在 1p能 级,A错误B.异丙基的结构简式 :
, B正确; C.NH 中心N原子的价层电子对数为4,,属于 sp 杂化,有 1个孤电子
对,VSEPR模型四面体形, C正确; D. Cl 分子中的共价键是由2个氯原子各提供1个未成对电子
的3p原子轨道重叠形成的p-po键。 D正确。
3. D【知识点】 乙烯的结构特点和性质,核磁共振氢谱图,同分异构体的判断
【解析】 A. 乙烯分子中的六个原子共面, A正确; B. 环戊烯 ,核磁共振氢谱有3组峰, B
正确; C. 由于CH -CH=CH 只有三种氢,所以有三种一氯代物: CH Cl-CH=CH 、 CH -CCl=
CH 、 CH -CH=CHCl,其中CH -CH=CHC1有顺式和反式两种结构,所以分子式为C H Cl链状有机
物的同分异构体共有4种,C正确; D.乙烯和溴水发生加成反应,乙烯被酸性高锰酸钾溶液氧化产生
新的杂质气体CO ,D正确。
4. B【知识点】 限定条件下的离子共存
【解析】 A. 甲基橙变红说明溶液为强酸性(pH≤3.1)。 此时,ClO-和NO 在酸性条件下具有强氧化
性,会与 Fe +发生氧化还原反应 ,生成 Fe +等产物,无法大量共存,A错误 ; B. 常温下,
. 则 c(O H-)=0.1 mol/L· C(H)=10 *m01L. 此时溶液为碱性, 在碱性条件下
Co;-、 Na+、 CH COO-、 NO 不发生反应,可大量共存,B正确; C. 加入Al能放出H 的溶液可能
为非氧化性酸性或强碱性溶液,酸性条件下H+与HCO 反应生成,碱性条件下OH-与HCO 、 NH
反应,不能大量共存, C错误; D. 水电离的c(H+)=10- mol/L,说明溶液可能为酸性或碱性。 酸
性: [Al(OH) ]会与H+反应生成Al +; 碱性: Fe +会与OH-生成Fe(OH) 沉淀, D错误。
5. D【知识点】 外界条件对反应速率及化学平衡的影响
【解析】 A. 该反应的正反应放热,同一压强下,降低温度,平衡正向移动, CO的平衡转化率增大,
化学参考答案A 第1页 (共4页)
一、 选择题(每小题只有一个正确选项, 每小题3分,14小题共42分) 。
题号 1 2 3 4 5 6 7 8
答案 B A D B D c D C
题号 9 10 11 12 13 14
答案 A C C D C C
1. B【知识点】 石 墨的性质、 干冰的性质、 原子核外电子的跃迁,氢键
【解析】 A.铅笔芯的主要成分为石墨,A正确; B. 干冰是固态的二氧化碳,干冰升华时,吸收大量
的热,使周围温度降低,大量的水蒸气凝结成了小液滴,形成“云雾”效果,升华为物理变化,共价键
没有断裂, B错误C. 焰火、 激光、 霓虹灯光都与原子核外电子跃迁释放能量有关, C正确D.天然气
水合物是巨大的潜在能源,水分子以氢键相连构成的笼容纳甲烷、 乙烷等气体,D正确 。
2. A【知识点】 原子轨道式,基团的结构简式,价层电子对互斥理论,共价键的类型
【解 析 】 A. K能层只有 1个能级 1s,不存在 1p能 级,A错误B.异丙基的结构简式 :
, B正确; C.NH 中心N原子的价层电子对数为4,,属于 sp 杂化,有 1个孤电子
对,VSEPR模型四面体形, C正确; D. Cl 分子中的共价键是由2个氯原子各提供1个未成对电子
的3p原子轨道重叠形成的p-po键。 D正确。
3. D【知识点】 乙烯的结构特点和性质,核磁共振氢谱图,同分异构体的判断
【解析】 A. 乙烯分子中的六个原子共面, A正确; B. 环戊烯 ,核磁共振氢谱有3组峰, B
正确; C. 由于CH -CH=CH 只有三种氢,所以有三种一氯代物: CH Cl-CH=CH 、 CH -CCl=
CH 、 CH -CH=CHCl,其中CH -CH=CHC1有顺式和反式两种结构,所以分子式为C H Cl链状有机
物的同分异构体共有4种,C正确; D.乙烯和溴水发生加成反应,乙烯被酸性高锰酸钾溶液氧化产生
新的杂质气体CO ,D正确。
4. B【知识点】 限定条件下的离子共存
【解析】 A. 甲基橙变红说明溶液为强酸性(pH≤3.1)。 此时,ClO-和NO 在酸性条件下具有强氧化
性,会与 Fe +发生氧化还原反应 ,生成 Fe +等产物,无法大量共存,A错误 ; B. 常温下,
. 则 c(O H-)=0.1 mol/L· C(H)=10 *m01L. 此时溶液为碱性, 在碱性条件下
Co;-、 Na+、 CH COO-、 NO 不发生反应,可大量共存,B正确; C. 加入Al能放出H 的溶液可能
为非氧化性酸性或强碱性溶液,酸性条件下H+与HCO 反应生成,碱性条件下OH-与HCO 、 NH
反应,不能大量共存, C错误; D. 水电离的c(H+)=10- mol/L,说明溶液可能为酸性或碱性。 酸
性: [Al(OH) ]会与H+反应生成Al +; 碱性: Fe +会与OH-生成Fe(OH) 沉淀, D错误。
5. D【知识点】 外界条件对反应速率及化学平衡的影响
【解析】 A. 该反应的正反应放热,同一压强下,降低温度,平衡正向移动, CO的平衡转化率增大,
化学参考答案A 第1页 (共4页)
同课章节目录
