人教版高中化学选修四课件 3.4 难溶电解质的溶解平衡 课件(共41张PPT)
文档属性
| 名称 | 人教版高中化学选修四课件 3.4 难溶电解质的溶解平衡 课件(共41张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 945.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-20 00:00:00 | ||
图片预览










文档简介
课件41张PPT。 难溶电解质的溶解平衡
习惯上,将溶解度小于0.01克的电解质称为难溶电解质。难溶电解质的溶解度尽管很小,但不会等于0 ,没有绝对不溶的物质。化学上通常认为残留在溶液中的离子浓度小于10-5mol/L时,沉淀达到完全。
课堂练习练习1:下列说法中正确的是( )
A.不溶于水的物质溶解度为0
B.绝对不溶解的物质是不存在的
C.某离子被沉淀完全是指该离子在溶液中的浓度为0
D.物质的溶解性为难溶,则该物质不溶于水B在饱和NaCl溶液中加入浓盐酸解释: 在NaCl的饱和溶液中,存在溶解平衡NaCl(s) Na+(aq) + Cl-(aq)NaCl饱和溶液中有固体析出 可溶的电解质溶液中存在溶解平衡,那么难溶的电解质在水中是否也存在溶解平衡呢?【现象】 加浓盐酸会使c(Cl- )增加,平衡向左移动,因而有NaCl晶体析出。 溶解
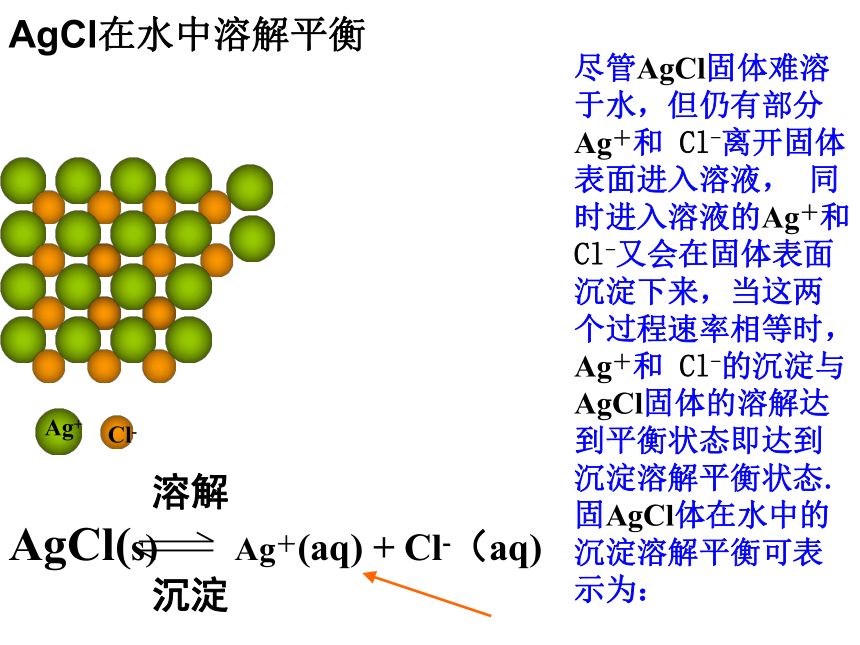
AgCl(s) Ag+(aq) + Cl-(aq)
沉淀
AgCl在水中溶解平衡尽管AgCl固体难溶于水,但仍有部分Ag+和 Cl-离开固体表面进入溶液, 同时进入溶液的Ag+和 Cl-又会在固体表面沉淀下来,当这两个过程速率相等时,Ag+和 Cl-的沉淀与AgCl固体的溶解达到平衡状态即达到沉淀溶解平衡状态. 固AgCl体在水中的沉淀溶解平衡可表示为:
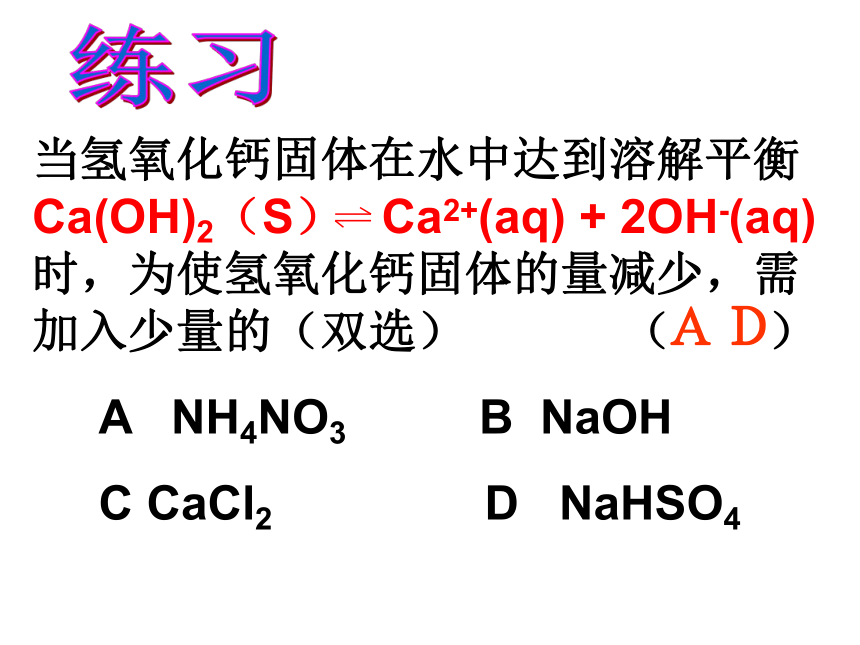
一、沉淀溶解平衡练:书写碳酸钙溶解平衡的表达式 一定温度下,当沉淀溶解的速率和沉淀生成的速率相等时,形成电解质的饱和溶液,达到平衡状态,我们把这种平衡称为沉淀溶解平衡 。 2、表达式:1、概念:沉淀溶解平衡表达式:对比电离方程式:PbI2:AgCl:Cu(OH)2: 动:动态平衡,溶解和沉淀仍在进行 定:溶液中各离子浓度保持不变 变:当条件改变时,溶解平衡将发生移动逆:溶解和沉淀互为可逆过程 逆、动、等、定、变3、特征:沉淀溶解平衡和化学平衡、电离平衡一样,符合平衡的基本特征、满足平衡的变化基本规律。 4、影响难溶电解质溶解平衡的因素a、浓度:加水,平衡向溶解方向移动。b、温度:升温,多数平衡向溶解方向移动。c、同离子效应:增加与难溶电解质相同的离子,平衡向沉淀方向移动。d、化学反应:反应消耗难溶电解质的离子,平衡向溶解方向移动。①内因:电解质本身的性质 练习AD二、沉淀反应的应用1、沉淀的生成(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。(2)沉淀的方法① 调pH值如:工业原料氯化铵中混有氯化铁,使其溶解于水,再加氨水调 pH值至7~8,可使Fe3+转变为Fe(OH)3沉淀而除去。Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+ ② 加沉淀剂
如:沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂Cu2++S2-= CuS↓
Hg2++S2-= HgS↓2. 沉淀的溶解
原理:不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就达到使沉淀溶解的目的。
例:CaCO3(s) CO32-(aq) + Ca2+(aq)
HCO3-+H++H+H2CO3H2O + CO2强酸是常用的溶解难溶电解质的试剂。如可溶解难溶氢氧化物,难溶碳酸盐、某些难溶硫化物等。除酸外,某些盐溶液也可用来溶解沉淀。[思考]:写出氢氧化镁沉淀溶解平衡的表达式. 1、若使氢氧化镁沉淀溶解,可以采取什么方法?所依据的原理是什么?
2、现提供以下试剂,请你设计可行的实验方案。蒸馏水、盐酸、饱和NH4Cl溶液、NaOH溶液、NaCl溶液、Na2CO3溶液、 FeCl3溶液。Mg(OH)2(s) Mg2+(aq)+2OH-(aq)讨论溶解沉淀 根据勒夏特列原理,使沉淀溶解平衡向溶解方向移动固体无明显溶解现象,溶液变浅红迅速溶解逐渐溶解Mg(OH)2 + 2HCl = MgCl2 + 2H2OMg(OH)2 + 2NH4Cl = MgCl2 + 2NH3·H2O完成实验,记录现象,写出反应的化学方程式。有红褐色沉淀生成说明溶解实验方案:分别向氢氧化镁沉淀中加入蒸馏水、酸、
盐,根据实验现象,得出结论。在溶液中存在Mg(OH)2的溶解平衡:
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq) 加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。 加入NH4Cl时,NH4+与OH-结合,生成弱电解质NH3·H2O(它在水中比Mg(OH)2更难电离出OH-),使c(OH-)减小,平衡右移,从而使Mg(OH)2的沉淀溶解平衡向溶解方向移动。【思考与交流】: 应用平衡移动原理分析、解释实验中发生的反应,并试从中找出使沉淀溶解的规律。【解释】[思考]:白色的氢氧化镁沉淀加入氯化铁溶液后,
为什么会有红褐色沉淀生成?
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq),3、沉淀的转化【实验3-4】有白色沉淀析出白色沉淀转化为黄色黄色沉淀转化为黑色AgClAgIAg2S(实验3-4、3-5 沉淀转化)AgClAgIAg2SMg(OH)2Fe(OH)3[讨论]:从实验中可以得到什么结论?实验说明:沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
沉淀一般从溶解度小的向溶解度更小的方向转化。沉淀的转化示意图KI = I- + K++AgI(s)s(AgCl)=1.5×10-4gs(AgI)=3.7×10-7gs(Ag2S)=1.3×10-16g沉淀从溶解度小的向溶解度更小的方向转化。沉淀的转化示意图KI = I- + K++AgI(s)s(AgCl)=1.5×10-4gs(AgI)=3.7×10-7gs(Ag2S)=1.3×10-16g沉淀从溶解度小的向溶解度更小的方向转化。龋齿应用2、预防龋齿 龋齿的形成
1. 牙釉质:主要成分为Ca5(PO4)3OH(羟基磷灰石);是一种难溶电解质。
2. 残留在牙齿上的糖发酵会产生H+。
生活中的问题沉淀的溶解Ca5(PO4)3OH 5Ca2++ 3PO43- + OH-3H+3HPO42-++H+H2OCa5(PO4)3OH+F- Ca5(PO4)3F + OH-沉淀的转化 龋齿的预防 氟离子会与 Ca5(PO4)3OH (羟基磷灰石)反应生成Ca5(PO4)3F (氟磷灰石) 。 练习、向5mLNaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色。根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A.AgCl=AgI=Ag2S
B.AgCl C.AgCl>AgI> Ag2S
D.AgI>AgCI> Ag2S【小结】:沉淀的生成、溶解、转化实质上都是沉淀溶解平衡的移动的过程,其基本依据主要有:
①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
③加入相同离子,平衡向沉淀方向移动。
④加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子,使平衡向溶解的方向移动。1、定义:在一定温度下,难溶电解质在溶液中达到沉淀溶解平衡时。其离子浓度幂的乘积为一个常数,称之为溶度积常数,简称溶度积,用Ksp表示。科学视野 、溶度积常数( Ksp )注意:
①书写溶度积表达式时不考虑固体的浓度
②溶度积常数有单位(通常不写)溶液过饱和,有沉淀析出溶液饱和,沉淀与溶解处于平衡状态溶液未饱和,可继续溶解该难溶电解质溶液中有关离子浓度幂的乘积—离子积QC2、溶度积规则溶液过饱和 ,有沉淀生成处于沉淀溶解平衡 溶液不饱和,若加入固体将溶解 在100mL 0.01mol/LKCl 溶液中,加入 1mL 0.01mol/LAgNO3溶液,下列说法正确的是(AgCl 的Ksp=1.8×10-10) ( )
A、有AgCl沉淀析出 B、无AgCl沉淀
C、无法确定 D、有沉淀但不是AgClAc(Cl-)=(0.01×0.1) ÷0.101 = 9.9×10-3mol/Lc(Ag+)=(0.01×0.001) ÷0.101 = 9.9×10-5mol/LQc =9.9×10-3×9.9×10-5 = 9.8×10-7 > Ksp练习3、影响Ksp的因素 难溶电解质本身的性质和温度温度:升温,多数平衡向溶解方向移动, Ksp 增大。 写出下列难溶物的溶度积表达式 Ksp反映了难溶电解质在水中的溶解能力.一定的温度下,相同类型的难溶电解质的Ksp越小,溶解度越小,越难溶解 4、溶度积Ksp的物理意义练习、下列情况下,有无CaCO3沉淀生成?
(1)往盛有1.0 L纯水中加入0.1 mL浓度为0.01 mol /L 的CaCl2和Na2CO3;
(2)改变CaCl2和Na2CO3的浓度为1.0 mol /L 呢? C(Ca2+)= C(CO32-)= 0.1?10-3 ? 0.01/1.0 = 10-6 mol /L Qc = C(Ca2+)×C(CO32-) = 10-12 < Ksp,CaCO3=4.96 ?10-9
因此无 CaCO3沉淀生成。C(Ca2+)×C(CO32-) = 10-4 mol /L
Qc = C(Ca2+)×C(CO32-) = 10-8 > Ksp,CaCO3
因此有CaCO3沉淀生成。
练习 如果溶液中Fe3+和Mg2+的浓度均为0.10 mol/L,
使Fe3+完全沉淀而使Mg2+不沉淀的pH条件是什么?
(沉淀完全是指该离子的浓度降低到10-5 以下,氢氧化铁的Ksp为 4.0 ×10-39氢氧化镁的Ksp为 1.8 ×10-11)
pH ≥ 3.2解: Fe(OH)3 Fe3+ + 3OH-
Ksp = C(Fe3+)×C 3 (OH-) = 4.0 ×10-39
Fe3+ 沉淀完全时的C(OH-)为:Mg2+开始沉淀的pH值为: pH ≤9.1因此, 只要控制pH值在3.2 ~ 9.1之间即可使Fe3+定量沉淀而使Mg2+不沉淀。例3:已知Ksp,AgCl=1.8?10-10, Ksp,Ag2CrO4=9.0?10-12,试 求AgCl和Ag2CrO4的溶解度(用g/L表示)解:(1)设AgCl的溶解度为S1(mol/L),则:
AgCl(s) Ag+(aq) + Cl-(aq)
平衡 S1 S1 (2)设Ag2CrO4的溶解度为S2(mol/L),则:
Ag2CrO4(s) 2Ag+(aq) + CrO42-(aq)
平 2S2 S2在水中:AgCl溶解度小于Ag2CrO4的溶解度
由以上例题的结果可得到如下结论:
①同种类型的难溶电解质,在一定温度下,Ksp越大则溶解度越大。
②不同类型则不能用Ksp的大小来比较溶解度的大小,必须经过换算才能得出结论。练习7:现将足量AgCl固体分别放入下列物质中,AgCl溶解度由大到小的排列顺序为( )①20ml0.01mol/LKCl溶液②30ml0.02mol/LCaCl2溶液③40ml0.03mol/LHCl溶液④10ml蒸馏水
⑤50ml0.05mol/LAgNO3溶液
A、 ①﹥②﹥③﹥④﹥⑤
B 、④﹥①﹥③﹥②﹥⑤
C、 ⑤﹥④﹥②﹥①﹥③
D 、④﹥③﹥⑤﹥②﹥①
B练习:在饱和澄清石灰水中加入生石灰反应后,恢复至原来温度下列说法正确的是( )
A.溶液中钙离子浓度变大
B.溶液中氢氧化钙的质量分数增大
C.溶液的pH不变
D.溶液中钙离子的物质的量减少.
C D练习:为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入一种试剂,下列不宜选用的试剂是( )
A.NaOH B.MgCO3
C.氨水 D.MgO E.Mg(OH)2AC练习:以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2。根据上述实验事实,可推知MnS具有的相关性质是( )
A.具有吸附性
B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS
D.溶解度小于CuS、PbS、CdSC
习惯上,将溶解度小于0.01克的电解质称为难溶电解质。难溶电解质的溶解度尽管很小,但不会等于0 ,没有绝对不溶的物质。化学上通常认为残留在溶液中的离子浓度小于10-5mol/L时,沉淀达到完全。
课堂练习练习1:下列说法中正确的是( )
A.不溶于水的物质溶解度为0
B.绝对不溶解的物质是不存在的
C.某离子被沉淀完全是指该离子在溶液中的浓度为0
D.物质的溶解性为难溶,则该物质不溶于水B在饱和NaCl溶液中加入浓盐酸解释: 在NaCl的饱和溶液中,存在溶解平衡NaCl(s) Na+(aq) + Cl-(aq)NaCl饱和溶液中有固体析出 可溶的电解质溶液中存在溶解平衡,那么难溶的电解质在水中是否也存在溶解平衡呢?【现象】 加浓盐酸会使c(Cl- )增加,平衡向左移动,因而有NaCl晶体析出。 溶解
AgCl(s) Ag+(aq) + Cl-(aq)
沉淀
AgCl在水中溶解平衡尽管AgCl固体难溶于水,但仍有部分Ag+和 Cl-离开固体表面进入溶液, 同时进入溶液的Ag+和 Cl-又会在固体表面沉淀下来,当这两个过程速率相等时,Ag+和 Cl-的沉淀与AgCl固体的溶解达到平衡状态即达到沉淀溶解平衡状态. 固AgCl体在水中的沉淀溶解平衡可表示为:
一、沉淀溶解平衡练:书写碳酸钙溶解平衡的表达式 一定温度下,当沉淀溶解的速率和沉淀生成的速率相等时,形成电解质的饱和溶液,达到平衡状态,我们把这种平衡称为沉淀溶解平衡 。 2、表达式:1、概念:沉淀溶解平衡表达式:对比电离方程式:PbI2:AgCl:Cu(OH)2: 动:动态平衡,溶解和沉淀仍在进行 定:溶液中各离子浓度保持不变 变:当条件改变时,溶解平衡将发生移动逆:溶解和沉淀互为可逆过程 逆、动、等、定、变3、特征:沉淀溶解平衡和化学平衡、电离平衡一样,符合平衡的基本特征、满足平衡的变化基本规律。 4、影响难溶电解质溶解平衡的因素a、浓度:加水,平衡向溶解方向移动。b、温度:升温,多数平衡向溶解方向移动。c、同离子效应:增加与难溶电解质相同的离子,平衡向沉淀方向移动。d、化学反应:反应消耗难溶电解质的离子,平衡向溶解方向移动。①内因:电解质本身的性质 练习AD二、沉淀反应的应用1、沉淀的生成(1)应用:生成难溶电解质的沉淀,是工业生产、环保工程和科学研究中除杂或提纯物质的重要方法之一。(2)沉淀的方法① 调pH值如:工业原料氯化铵中混有氯化铁,使其溶解于水,再加氨水调 pH值至7~8,可使Fe3+转变为Fe(OH)3沉淀而除去。Fe3+ + 3NH3?H2O=Fe(OH)3↓+3NH4+ ② 加沉淀剂
如:沉淀Cu2+、Hg2+等,以Na2S、H2S做沉淀剂Cu2++S2-= CuS↓
Hg2++S2-= HgS↓2. 沉淀的溶解
原理:不断移去溶解平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就达到使沉淀溶解的目的。
例:CaCO3(s) CO32-(aq) + Ca2+(aq)
HCO3-+H++H+H2CO3H2O + CO2强酸是常用的溶解难溶电解质的试剂。如可溶解难溶氢氧化物,难溶碳酸盐、某些难溶硫化物等。除酸外,某些盐溶液也可用来溶解沉淀。[思考]:写出氢氧化镁沉淀溶解平衡的表达式. 1、若使氢氧化镁沉淀溶解,可以采取什么方法?所依据的原理是什么?
2、现提供以下试剂,请你设计可行的实验方案。蒸馏水、盐酸、饱和NH4Cl溶液、NaOH溶液、NaCl溶液、Na2CO3溶液、 FeCl3溶液。Mg(OH)2(s) Mg2+(aq)+2OH-(aq)讨论溶解沉淀 根据勒夏特列原理,使沉淀溶解平衡向溶解方向移动固体无明显溶解现象,溶液变浅红迅速溶解逐渐溶解Mg(OH)2 + 2HCl = MgCl2 + 2H2OMg(OH)2 + 2NH4Cl = MgCl2 + 2NH3·H2O完成实验,记录现象,写出反应的化学方程式。有红褐色沉淀生成说明溶解实验方案:分别向氢氧化镁沉淀中加入蒸馏水、酸、
盐,根据实验现象,得出结论。在溶液中存在Mg(OH)2的溶解平衡:
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq) 加入盐酸时,H+中和OH-,使c(OH-)减小,平衡右移,从而使Mg(OH)2溶解。 加入NH4Cl时,NH4+与OH-结合,生成弱电解质NH3·H2O(它在水中比Mg(OH)2更难电离出OH-),使c(OH-)减小,平衡右移,从而使Mg(OH)2的沉淀溶解平衡向溶解方向移动。【思考与交流】: 应用平衡移动原理分析、解释实验中发生的反应,并试从中找出使沉淀溶解的规律。【解释】[思考]:白色的氢氧化镁沉淀加入氯化铁溶液后,
为什么会有红褐色沉淀生成?
Mg(OH)2(s) ?Mg2+(aq)+2OH-(aq),3、沉淀的转化【实验3-4】有白色沉淀析出白色沉淀转化为黄色黄色沉淀转化为黑色AgClAgIAg2S(实验3-4、3-5 沉淀转化)AgClAgIAg2SMg(OH)2Fe(OH)3[讨论]:从实验中可以得到什么结论?实验说明:沉淀可以从溶解度小的向溶解度更小的方向转化,两者差别越大,转化越容易。
沉淀一般从溶解度小的向溶解度更小的方向转化。沉淀的转化示意图KI = I- + K++AgI(s)s(AgCl)=1.5×10-4gs(AgI)=3.7×10-7gs(Ag2S)=1.3×10-16g沉淀从溶解度小的向溶解度更小的方向转化。沉淀的转化示意图KI = I- + K++AgI(s)s(AgCl)=1.5×10-4gs(AgI)=3.7×10-7gs(Ag2S)=1.3×10-16g沉淀从溶解度小的向溶解度更小的方向转化。龋齿应用2、预防龋齿 龋齿的形成
1. 牙釉质:主要成分为Ca5(PO4)3OH(羟基磷灰石);是一种难溶电解质。
2. 残留在牙齿上的糖发酵会产生H+。
生活中的问题沉淀的溶解Ca5(PO4)3OH 5Ca2++ 3PO43- + OH-3H+3HPO42-++H+H2OCa5(PO4)3OH+F- Ca5(PO4)3F + OH-沉淀的转化 龋齿的预防 氟离子会与 Ca5(PO4)3OH (羟基磷灰石)反应生成Ca5(PO4)3F (氟磷灰石) 。 练习、向5mLNaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色。根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
A.AgCl=AgI=Ag2S
B.AgCl
D.AgI>AgCI> Ag2S【小结】:沉淀的生成、溶解、转化实质上都是沉淀溶解平衡的移动的过程,其基本依据主要有:
①浓度:加水,平衡向溶解方向移动。
②温度:升温,多数平衡向溶解方向移动。
③加入相同离子,平衡向沉淀方向移动。
④加入可与体系中某些离子反应生成更难溶或更难电离或气体的离子,使平衡向溶解的方向移动。1、定义:在一定温度下,难溶电解质在溶液中达到沉淀溶解平衡时。其离子浓度幂的乘积为一个常数,称之为溶度积常数,简称溶度积,用Ksp表示。科学视野 、溶度积常数( Ksp )注意:
①书写溶度积表达式时不考虑固体的浓度
②溶度积常数有单位(通常不写)溶液过饱和,有沉淀析出溶液饱和,沉淀与溶解处于平衡状态溶液未饱和,可继续溶解该难溶电解质溶液中有关离子浓度幂的乘积—离子积QC2、溶度积规则溶液过饱和 ,有沉淀生成处于沉淀溶解平衡 溶液不饱和,若加入固体将溶解 在100mL 0.01mol/LKCl 溶液中,加入 1mL 0.01mol/LAgNO3溶液,下列说法正确的是(AgCl 的Ksp=1.8×10-10) ( )
A、有AgCl沉淀析出 B、无AgCl沉淀
C、无法确定 D、有沉淀但不是AgClAc(Cl-)=(0.01×0.1) ÷0.101 = 9.9×10-3mol/Lc(Ag+)=(0.01×0.001) ÷0.101 = 9.9×10-5mol/LQc =9.9×10-3×9.9×10-5 = 9.8×10-7 > Ksp练习3、影响Ksp的因素 难溶电解质本身的性质和温度温度:升温,多数平衡向溶解方向移动, Ksp 增大。 写出下列难溶物的溶度积表达式 Ksp反映了难溶电解质在水中的溶解能力.一定的温度下,相同类型的难溶电解质的Ksp越小,溶解度越小,越难溶解 4、溶度积Ksp的物理意义练习、下列情况下,有无CaCO3沉淀生成?
(1)往盛有1.0 L纯水中加入0.1 mL浓度为0.01 mol /L 的CaCl2和Na2CO3;
(2)改变CaCl2和Na2CO3的浓度为1.0 mol /L 呢? C(Ca2+)= C(CO32-)= 0.1?10-3 ? 0.01/1.0 = 10-6 mol /L Qc = C(Ca2+)×C(CO32-) = 10-12 < Ksp,CaCO3=4.96 ?10-9
因此无 CaCO3沉淀生成。C(Ca2+)×C(CO32-) = 10-4 mol /L
Qc = C(Ca2+)×C(CO32-) = 10-8 > Ksp,CaCO3
因此有CaCO3沉淀生成。
练习 如果溶液中Fe3+和Mg2+的浓度均为0.10 mol/L,
使Fe3+完全沉淀而使Mg2+不沉淀的pH条件是什么?
(沉淀完全是指该离子的浓度降低到10-5 以下,氢氧化铁的Ksp为 4.0 ×10-39氢氧化镁的Ksp为 1.8 ×10-11)
pH ≥ 3.2解: Fe(OH)3 Fe3+ + 3OH-
Ksp = C(Fe3+)×C 3 (OH-) = 4.0 ×10-39
Fe3+ 沉淀完全时的C(OH-)为:Mg2+开始沉淀的pH值为: pH ≤9.1因此, 只要控制pH值在3.2 ~ 9.1之间即可使Fe3+定量沉淀而使Mg2+不沉淀。例3:已知Ksp,AgCl=1.8?10-10, Ksp,Ag2CrO4=9.0?10-12,试 求AgCl和Ag2CrO4的溶解度(用g/L表示)解:(1)设AgCl的溶解度为S1(mol/L),则:
AgCl(s) Ag+(aq) + Cl-(aq)
平衡 S1 S1 (2)设Ag2CrO4的溶解度为S2(mol/L),则:
Ag2CrO4(s) 2Ag+(aq) + CrO42-(aq)
平 2S2 S2在水中:AgCl溶解度小于Ag2CrO4的溶解度
由以上例题的结果可得到如下结论:
①同种类型的难溶电解质,在一定温度下,Ksp越大则溶解度越大。
②不同类型则不能用Ksp的大小来比较溶解度的大小,必须经过换算才能得出结论。练习7:现将足量AgCl固体分别放入下列物质中,AgCl溶解度由大到小的排列顺序为( )①20ml0.01mol/LKCl溶液②30ml0.02mol/LCaCl2溶液③40ml0.03mol/LHCl溶液④10ml蒸馏水
⑤50ml0.05mol/LAgNO3溶液
A、 ①﹥②﹥③﹥④﹥⑤
B 、④﹥①﹥③﹥②﹥⑤
C、 ⑤﹥④﹥②﹥①﹥③
D 、④﹥③﹥⑤﹥②﹥①
B练习:在饱和澄清石灰水中加入生石灰反应后,恢复至原来温度下列说法正确的是( )
A.溶液中钙离子浓度变大
B.溶液中氢氧化钙的质量分数增大
C.溶液的pH不变
D.溶液中钙离子的物质的量减少.
C D练习:为除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入一种试剂,下列不宜选用的试剂是( )
A.NaOH B.MgCO3
C.氨水 D.MgO E.Mg(OH)2AC练习:以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2。根据上述实验事实,可推知MnS具有的相关性质是( )
A.具有吸附性
B.溶解度与CuS、PbS、CdS等相同
C.溶解度大于CuS、PbS、CdS
D.溶解度小于CuS、PbS、CdSC
