2025年辽宁省抚顺市新抚区中考四模化学试题(PDF版、含答案)
文档属性
| 名称 | 2025年辽宁省抚顺市新抚区中考四模化学试题(PDF版、含答案) |

|
|
| 格式 | |||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-11 00:00:00 | ||
图片预览


文档简介
2024—2025 学年度(下)学期教学质量检测
九年级化学试卷(四)
(本试卷共 14 道题,满分 50 分)
温馨提示:请在答题卡规定答题区域内作答,在本试卷上作答无效
可能用到的近似相对原子质量: H-1 C-12 N-14 O-16 Na-23 Cl-35.5
第一部分 选择题(共 10 分)
(本部分共包括 10 道小题,每小题 1分。每小题只有一个最符合题目要求的选项)
1.化学用语是学习化学的工具,选项表示两个铝离子的是
3+ 3+ 2+
A. 2Al B. 2Al C. Al D. 2Al
2.下列实验操作正确的是
3.张青莲院士主持测定的锑、铈等元素的相对原子质量新值,被采用为国际新标准。
铈元素在元素周期表中的信息如图,其相对原子质量为
A. 58 B. 82.1
C. 140.1 D. 198.1
4.高铁列车依靠车顶的受电弓滑板与接触网持续摩擦获取电力,石墨可用于制造受电弓滑
板。这一应用与石墨的下列性质无关的是
A. 金属光泽 B. 滑腻感 C.导电性 D.熔点高
5.我国 2035 年远景目标之一是“推进绿色发展,促进人与自然和谐共生”。下列做法不
符合该目标的是
A.进行生活垃圾分类和定时定点投放
B.合理施用化肥,可以提高农作物产量
C.工业污水经处理达标后,可用作生活用水
D.鼓励简约的生活方式,节能节电、倡导绿色出行
九年级化学试卷 第 1页(共 6页)
6.学会用化学方法守护生命,让安全的警钟时刻长鸣。下列做法不当的是
A.燃气泄露,点火检查 B.煤炉取暖,注意通风
C.高原游玩,携带氧气 D.营地篝火,用水浇灭
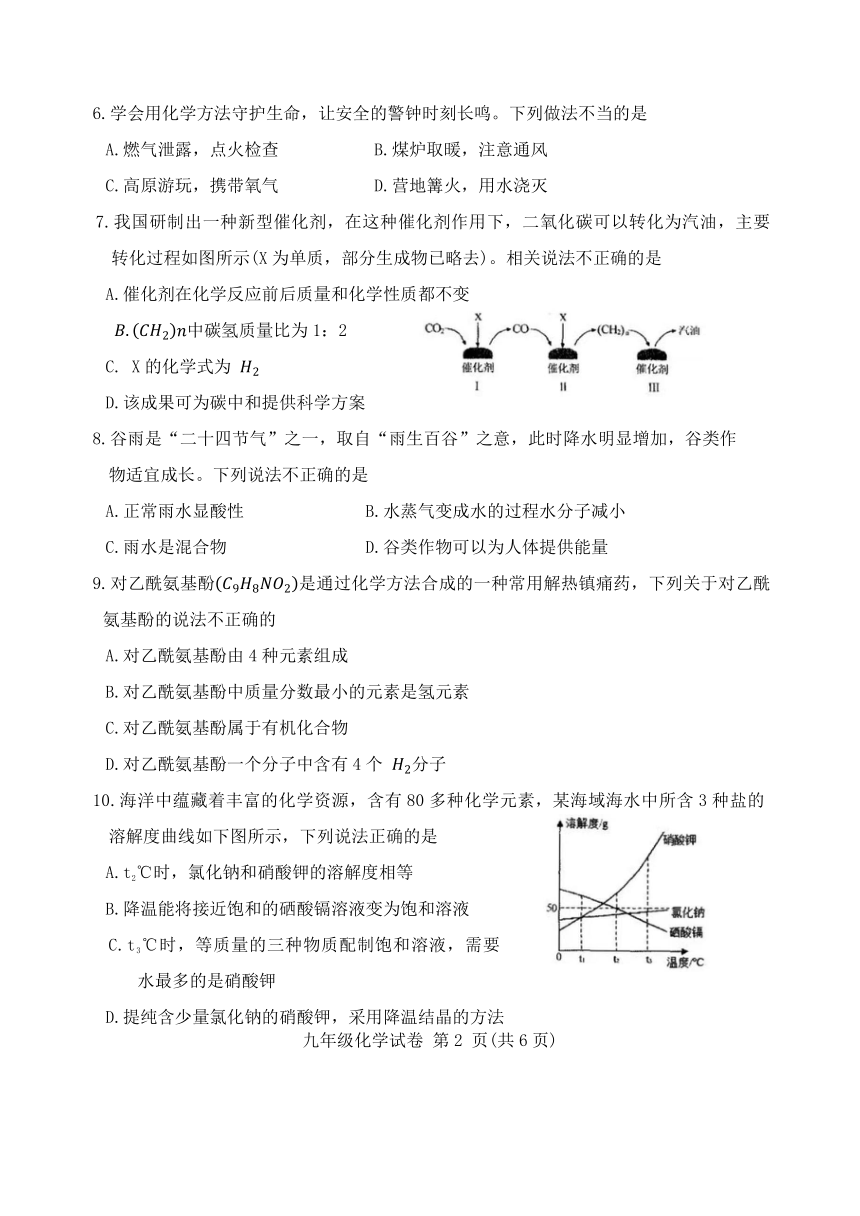
7.我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要
转化过程如图所示(X 为单质,部分生成物已略去)。相关说法不正确的是
A.催化剂在化学反应前后质量和化学性质都不变
. 2 中碳氢质量比为 1:2
C. X 的化学式为 2
D.该成果可为碳中和提供科学方案
8.谷雨是“二十四节气”之一,取自“雨生百谷”之意,此时降水明显增加,谷类作
物适宜成长。下列说法不正确的是
A.正常雨水显酸性 B.水蒸气变成水的过程水分子减小
C.雨水是混合物 D.谷类作物可以为人体提供能量
9.对乙酰氨基酚 9 8 2 是通过化学方法合成的一种常用解热镇痛药,下列关于对乙酰
氨基酚的说法不正确的
A.对乙酰氨基酚由 4种元素组成
B.对乙酰氨基酚中质量分数最小的元素是氢元素
C.对乙酰氨基酚属于有机化合物
D.对乙酰氨基酚一个分子中含有 4个 2分子
10.海洋中蕴藏着丰富的化学资源,含有 80 多种化学元素,某海域海水中所含 3 种盐的
溶解度曲线如下图所示,下列说法正确的是
A.t2℃时,氯化钠和硝酸钾的溶解度相等
B.降温能将接近饱和的硒酸镉溶液变为饱和溶液
C.t3℃时,等质量的三种物质配制饱和溶液,需要
水最多的是硝酸钾
D.提纯含少量氯化钠的硝酸钾,采用降温结晶的方法
九年级化学试卷 第 2 页(共 6页)
第二部分 非选择题(共 40 分)
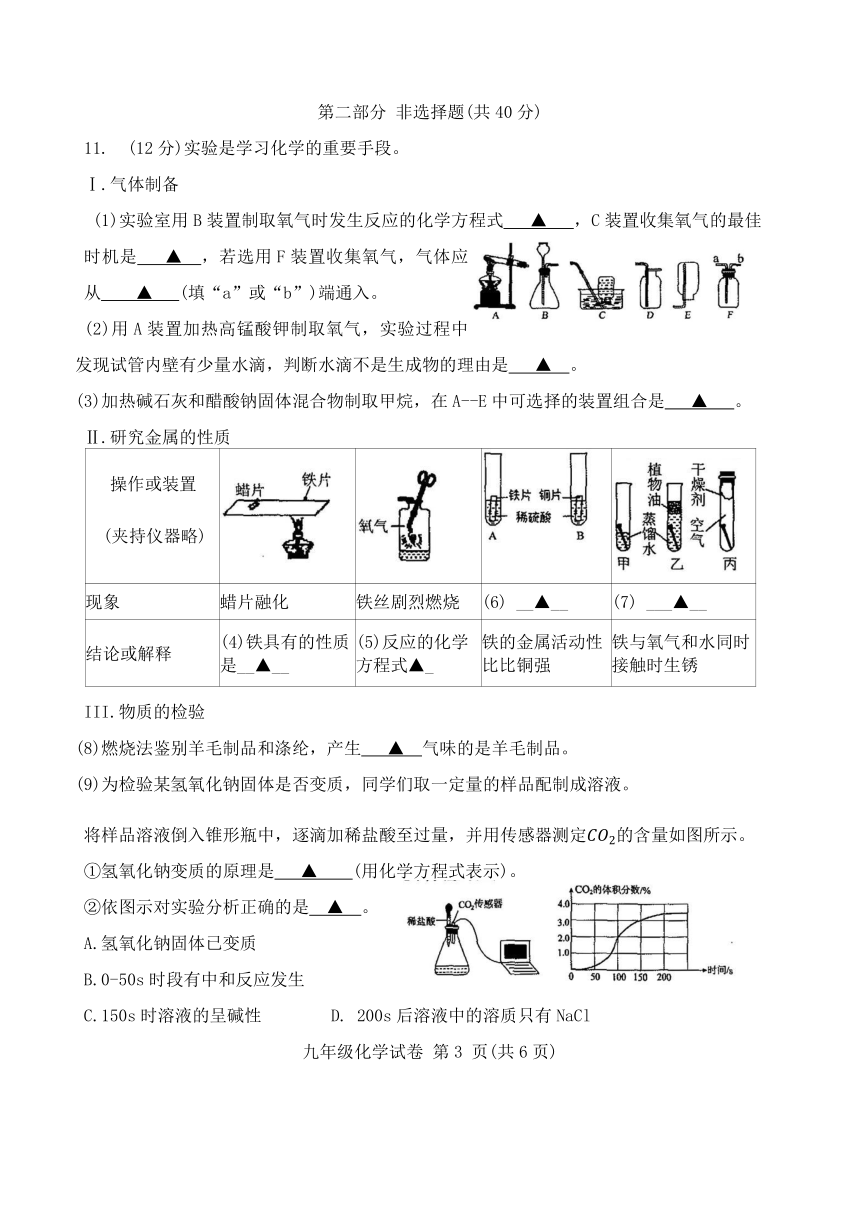
11. (12 分)实验是学习化学的重要手段。
Ⅰ.气体制备
(1)实验室用 B 装置制取氧气时发生反应的化学方程式 ▲ ,C 装置收集氧气的最佳
时机是 ▲ ,若选用 F 装置收集氧气,气体应
从 ▲ (填“a”或“b”)端通入。
(2)用 A 装置加热高锰酸钾制取氧气,实验过程中
发现试管内壁有少量水滴,判断水滴不是生成物的理由是 ▲ 。
(3)加热碱石灰和醋酸钠固体混合物制取甲烷,在 A--E 中可选择的装置组合是 ▲ 。
Ⅱ.研究金属的性质
操作或装置
(夹持仪器略)
现象 蜡片融化 铁丝剧烈燃烧 (6) __▲__ (7) ___▲__
(4)铁具有的性质 (5)反应的化学 铁的金属活动性 铁与氧气和水同时
结论或解释
是__▲__ 方程式▲_ 比比铜强 接触时生锈
III.物质的检验
(8)燃烧法鉴别羊毛制品和涤纶,产生 ▲ 气味的是羊毛制品。
(9)为检验某氢氧化钠固体是否变质,同学们取一定量的样品配制成溶液。
将样品溶液倒入锥形瓶中,逐滴加稀盐酸至过量,并用传感器测定 2的含量如图所示。
①氢氧化钠变质的原理是 ▲ (用化学方程式表示)。
②依图示对实验分析正确的是 ▲ 。
A.氢氧化钠固体已变质
B.0-50s 时段有中和反应发生
C.150s 时溶液的呈碱性 D. 200s 后溶液中的溶质只有 NaCl
九年级化学试卷 第 3 页(共 6页)
12. (8 分)阅读科普短文,回答相关问题。
氨气 3 主要来自于人工合成,有助解决全球粮食短缺问题,并广泛应用于国防、
能源等领域。弗里茨·哈伯因发明了由氮气和氢气合成氨气的方
法荣获 1918 年诺贝尔化学奖,合
成氨的原理和过程如图 1所示。
在铁催化作用下,用体积比
为 1:3 的氮气和氢气合成氨,当
容器中氨的含量不再发生变化时
(平衡时),测得氨的含量分别与温度和压强的关系如图 2所示。
通常状况下,氨气是无色有刺激性气味气体,常温加压即可液化,研究发现 3作
为燃料,是一种比 H 更理想的能源。在相同条件下的物性参数如下表:
物性参数 颜色、气味 沸点 /° 溶解性 燃烧热 KJ/L
无色、无味 252.9 难溶于水 12.77
无色、刺激性 33.5 极易溶于水 17.10
我国在绿氨合成领域也不断突破,中科院科研团队借助一种固体催化剂 LDH,在常温
常压和可见光条件下,用氮气和水合成氨气和一种供给呼吸的气体,直接应用于船舶发动
机的燃烧测试。与传统合成氨相比,该过程无需高温高压且不消耗和依赖化石燃料。
(1)从微粒的角度分析,氨气变成液氨过程中,分子 ▲ (填“是”或“否”)发生变
化。
(2)图 1 从“合成塔”中出来的气体是 ▲ (填“纯净物”或“混合物”)。
(3)结合图 2分析,进行该合成氨反应,若使平衡时氨含量高达到 40%,你建议工厂选择的
合成氨的最佳条件是 ▲ 。 A. 300℃、低压 B. 500℃、高压
(4)氨燃料相较于化石燃料的使用,可有效减缓 ▲ 效应加剧 。
(5)对比表中数据,你认为氨气有希望替代氢气成为理想燃料的理由有(写 2 条)
▲ 、 ▲ 。
(6)①科研团队用氮气和水合成氨气的化学方程式为 ▲ ;
②与传统工业合成氨相比,该新工艺的显著优势有 ▲ 。
A.反应条件更温和 B.无需使用催化剂 C.原料成本更低
九年级化学试卷 第 4 页(共 6页)
13. (10 分)化学在社会发展中发挥着重要的作用。
Ⅰ.【化学与航空航天】
(1)2025 年 3 月 30 日,国产大飞机 C919 首航沈阳桃仙机场,C919 机身使用了先进的铝锂
合金,铝锂合金具备的优良性能是 ▲ 。
(2)从 1999 年到 2025 年,神舟一号到神舟二十号飞船见证了我
国载人航天事业的辉煌。
①飞船的太阳翼可将太阳能转化为 ▲ 能。
②“神十六”航天员曾在燃烧科学实验柜中以甲烷为燃料进行在轨点火燃烧实验,观察
到甲烷火焰与地面对照实验的火焰相比,显得短而圆且微弱。下列分析正确的是 ▲ 。
A.空间站甲烷燃烧,不需要氧气
B.空间站失重条件下燃烧的热气流向四周扩散,地面上热气流向上扩散
C.空间站失重条件下空气流动性差,甲烷燃烧的火焰比较微弱
(3)氢氧化锂(LiOH) 在航天器中用于吸收 CO2(LiOH 化学性质与 NaOH 相似, 20 时 LiOH 溶
解度为 12.8g)。工业上用电解法制得 LiOH 溶液,再蒸发结晶可得 LiOH 晶体。
①LiOH 溶液的 pH ▲ (填“>”、“=”或“<”) 7。
②20℃时电解法制得的 500gLiOH 溶液中,溶质的质量分数为 10%,将该溶液蒸发溶剂至
剩余水的质量为 200g,温度恢复至 20 ,此时溶液中溶质的质量分数是 ▲ 。
Ⅱ.【化学与科技生产】
中国芯彰显中国“智”造,制备高纯硅(芯片的基材)的工艺流程如图:
(4)硅元素在地壳中的含量仅次于 ▲ 。
(5) 操作Ⅰ的名称是 ▲ 。
(6)反应Ⅰ的基本反应类型是 ▲ ,反应Ⅱ需在无氧气环境中进行,原因是 ▲ 。
(7)上述生产流程中,可以循环利用的物质是 ▲ (填化学式)。
九年级化学试卷 第 5 页(共 6页)
14. (10 分)在范旭东和侯德榜等化学工业先驱的共同努力下,我国拥有了第一批民族化工
企业,侯德榜先生“碱”济天下,发明“侯氏制碱法”,打破了当时欧美对制碱业的垄
断,将制碱与制氨有机结合起来,同时生产纯碱和氯化铵两种产品,大大提高了原料的利
用率。
资料 1: 20℃时, NaCl、NaHCO3、NH4Cl 的溶解度分别为 36.0g、9.6g、37.2g
资料 2:氨气极易溶于饱和食盐水,形成的溶液呈碱性
(1)“侯氏制碱法”的产品是 ▲ 。
2 3中 N的化合价为 ▲ ;NH4Cl 的用途是 ▲ 。
(3)制碱工艺中的关键反应为: + 2 + 3 + 2 = 3 ↓+
4 。20 时,在实验室条件下按图示装置模拟该反应(其它装置略 …
去,实验时从左侧导管通入 2,从右侧导管通入 3) 。
① 向 200g 水中加入 ▲ gNaCl 固体配制成 NaCl 的饱和溶液。
②若条件控制得当,①中 NaCl 完全反应,理论上可得到 3的质量是 ▲ g。
③操作时先通入 3后,再通入 2的原因是 ▲ 。
④充分反应后烧杯中有晶体析出,出现的晶体主要成分是 3而不是 4 ,其原因是
▲ 。
【纯碱的应用】
“侯氏制碱法”的碱即纯碱,其水溶液显碱性,可以清洗油污,溶液碱性越强,去油
污效果越好。为探究纯碱溶液去油污效果的影响因素,分别测定不同温度下,不同浓度的
纯碱溶液的 pH,结果如下:
序号 1 2 3 4 5 6 7 8 9
浓度 2% 2% 2% 6% 6% 6% 10% 10% 10%
温度/℃ 20 40 60 20 40 60 20 40 60
pH 10.09 11.13 11.18 11.10 11.19 11.30 11.15 11.23 11.35
(4)实验中,去油污效果最好的溶液是 ▲ 。
(5)得出“纯碱溶液浓度是影响去油污效果的因素”的结论,依据的实验组合是 ▲
(填实验序号)。
)
(6)在一定温度范围内,纯碱溶液去油污效果与温度的关系是 ▲ 。
九年级化学试卷(四)
(本试卷共 14 道题,满分 50 分)
温馨提示:请在答题卡规定答题区域内作答,在本试卷上作答无效
可能用到的近似相对原子质量: H-1 C-12 N-14 O-16 Na-23 Cl-35.5
第一部分 选择题(共 10 分)
(本部分共包括 10 道小题,每小题 1分。每小题只有一个最符合题目要求的选项)
1.化学用语是学习化学的工具,选项表示两个铝离子的是
3+ 3+ 2+
A. 2Al B. 2Al C. Al D. 2Al
2.下列实验操作正确的是
3.张青莲院士主持测定的锑、铈等元素的相对原子质量新值,被采用为国际新标准。
铈元素在元素周期表中的信息如图,其相对原子质量为
A. 58 B. 82.1
C. 140.1 D. 198.1
4.高铁列车依靠车顶的受电弓滑板与接触网持续摩擦获取电力,石墨可用于制造受电弓滑
板。这一应用与石墨的下列性质无关的是
A. 金属光泽 B. 滑腻感 C.导电性 D.熔点高
5.我国 2035 年远景目标之一是“推进绿色发展,促进人与自然和谐共生”。下列做法不
符合该目标的是
A.进行生活垃圾分类和定时定点投放
B.合理施用化肥,可以提高农作物产量
C.工业污水经处理达标后,可用作生活用水
D.鼓励简约的生活方式,节能节电、倡导绿色出行
九年级化学试卷 第 1页(共 6页)
6.学会用化学方法守护生命,让安全的警钟时刻长鸣。下列做法不当的是
A.燃气泄露,点火检查 B.煤炉取暖,注意通风
C.高原游玩,携带氧气 D.营地篝火,用水浇灭
7.我国研制出一种新型催化剂,在这种催化剂作用下,二氧化碳可以转化为汽油,主要
转化过程如图所示(X 为单质,部分生成物已略去)。相关说法不正确的是
A.催化剂在化学反应前后质量和化学性质都不变
. 2 中碳氢质量比为 1:2
C. X 的化学式为 2
D.该成果可为碳中和提供科学方案
8.谷雨是“二十四节气”之一,取自“雨生百谷”之意,此时降水明显增加,谷类作
物适宜成长。下列说法不正确的是
A.正常雨水显酸性 B.水蒸气变成水的过程水分子减小
C.雨水是混合物 D.谷类作物可以为人体提供能量
9.对乙酰氨基酚 9 8 2 是通过化学方法合成的一种常用解热镇痛药,下列关于对乙酰
氨基酚的说法不正确的
A.对乙酰氨基酚由 4种元素组成
B.对乙酰氨基酚中质量分数最小的元素是氢元素
C.对乙酰氨基酚属于有机化合物
D.对乙酰氨基酚一个分子中含有 4个 2分子
10.海洋中蕴藏着丰富的化学资源,含有 80 多种化学元素,某海域海水中所含 3 种盐的
溶解度曲线如下图所示,下列说法正确的是
A.t2℃时,氯化钠和硝酸钾的溶解度相等
B.降温能将接近饱和的硒酸镉溶液变为饱和溶液
C.t3℃时,等质量的三种物质配制饱和溶液,需要
水最多的是硝酸钾
D.提纯含少量氯化钠的硝酸钾,采用降温结晶的方法
九年级化学试卷 第 2 页(共 6页)
第二部分 非选择题(共 40 分)
11. (12 分)实验是学习化学的重要手段。
Ⅰ.气体制备
(1)实验室用 B 装置制取氧气时发生反应的化学方程式 ▲ ,C 装置收集氧气的最佳
时机是 ▲ ,若选用 F 装置收集氧气,气体应
从 ▲ (填“a”或“b”)端通入。
(2)用 A 装置加热高锰酸钾制取氧气,实验过程中
发现试管内壁有少量水滴,判断水滴不是生成物的理由是 ▲ 。
(3)加热碱石灰和醋酸钠固体混合物制取甲烷,在 A--E 中可选择的装置组合是 ▲ 。
Ⅱ.研究金属的性质
操作或装置
(夹持仪器略)
现象 蜡片融化 铁丝剧烈燃烧 (6) __▲__ (7) ___▲__
(4)铁具有的性质 (5)反应的化学 铁的金属活动性 铁与氧气和水同时
结论或解释
是__▲__ 方程式▲_ 比比铜强 接触时生锈
III.物质的检验
(8)燃烧法鉴别羊毛制品和涤纶,产生 ▲ 气味的是羊毛制品。
(9)为检验某氢氧化钠固体是否变质,同学们取一定量的样品配制成溶液。
将样品溶液倒入锥形瓶中,逐滴加稀盐酸至过量,并用传感器测定 2的含量如图所示。
①氢氧化钠变质的原理是 ▲ (用化学方程式表示)。
②依图示对实验分析正确的是 ▲ 。
A.氢氧化钠固体已变质
B.0-50s 时段有中和反应发生
C.150s 时溶液的呈碱性 D. 200s 后溶液中的溶质只有 NaCl
九年级化学试卷 第 3 页(共 6页)
12. (8 分)阅读科普短文,回答相关问题。
氨气 3 主要来自于人工合成,有助解决全球粮食短缺问题,并广泛应用于国防、
能源等领域。弗里茨·哈伯因发明了由氮气和氢气合成氨气的方
法荣获 1918 年诺贝尔化学奖,合
成氨的原理和过程如图 1所示。
在铁催化作用下,用体积比
为 1:3 的氮气和氢气合成氨,当
容器中氨的含量不再发生变化时
(平衡时),测得氨的含量分别与温度和压强的关系如图 2所示。
通常状况下,氨气是无色有刺激性气味气体,常温加压即可液化,研究发现 3作
为燃料,是一种比 H 更理想的能源。在相同条件下的物性参数如下表:
物性参数 颜色、气味 沸点 /° 溶解性 燃烧热 KJ/L
无色、无味 252.9 难溶于水 12.77
无色、刺激性 33.5 极易溶于水 17.10
我国在绿氨合成领域也不断突破,中科院科研团队借助一种固体催化剂 LDH,在常温
常压和可见光条件下,用氮气和水合成氨气和一种供给呼吸的气体,直接应用于船舶发动
机的燃烧测试。与传统合成氨相比,该过程无需高温高压且不消耗和依赖化石燃料。
(1)从微粒的角度分析,氨气变成液氨过程中,分子 ▲ (填“是”或“否”)发生变
化。
(2)图 1 从“合成塔”中出来的气体是 ▲ (填“纯净物”或“混合物”)。
(3)结合图 2分析,进行该合成氨反应,若使平衡时氨含量高达到 40%,你建议工厂选择的
合成氨的最佳条件是 ▲ 。 A. 300℃、低压 B. 500℃、高压
(4)氨燃料相较于化石燃料的使用,可有效减缓 ▲ 效应加剧 。
(5)对比表中数据,你认为氨气有希望替代氢气成为理想燃料的理由有(写 2 条)
▲ 、 ▲ 。
(6)①科研团队用氮气和水合成氨气的化学方程式为 ▲ ;
②与传统工业合成氨相比,该新工艺的显著优势有 ▲ 。
A.反应条件更温和 B.无需使用催化剂 C.原料成本更低
九年级化学试卷 第 4 页(共 6页)
13. (10 分)化学在社会发展中发挥着重要的作用。
Ⅰ.【化学与航空航天】
(1)2025 年 3 月 30 日,国产大飞机 C919 首航沈阳桃仙机场,C919 机身使用了先进的铝锂
合金,铝锂合金具备的优良性能是 ▲ 。
(2)从 1999 年到 2025 年,神舟一号到神舟二十号飞船见证了我
国载人航天事业的辉煌。
①飞船的太阳翼可将太阳能转化为 ▲ 能。
②“神十六”航天员曾在燃烧科学实验柜中以甲烷为燃料进行在轨点火燃烧实验,观察
到甲烷火焰与地面对照实验的火焰相比,显得短而圆且微弱。下列分析正确的是 ▲ 。
A.空间站甲烷燃烧,不需要氧气
B.空间站失重条件下燃烧的热气流向四周扩散,地面上热气流向上扩散
C.空间站失重条件下空气流动性差,甲烷燃烧的火焰比较微弱
(3)氢氧化锂(LiOH) 在航天器中用于吸收 CO2(LiOH 化学性质与 NaOH 相似, 20 时 LiOH 溶
解度为 12.8g)。工业上用电解法制得 LiOH 溶液,再蒸发结晶可得 LiOH 晶体。
①LiOH 溶液的 pH ▲ (填“>”、“=”或“<”) 7。
②20℃时电解法制得的 500gLiOH 溶液中,溶质的质量分数为 10%,将该溶液蒸发溶剂至
剩余水的质量为 200g,温度恢复至 20 ,此时溶液中溶质的质量分数是 ▲ 。
Ⅱ.【化学与科技生产】
中国芯彰显中国“智”造,制备高纯硅(芯片的基材)的工艺流程如图:
(4)硅元素在地壳中的含量仅次于 ▲ 。
(5) 操作Ⅰ的名称是 ▲ 。
(6)反应Ⅰ的基本反应类型是 ▲ ,反应Ⅱ需在无氧气环境中进行,原因是 ▲ 。
(7)上述生产流程中,可以循环利用的物质是 ▲ (填化学式)。
九年级化学试卷 第 5 页(共 6页)
14. (10 分)在范旭东和侯德榜等化学工业先驱的共同努力下,我国拥有了第一批民族化工
企业,侯德榜先生“碱”济天下,发明“侯氏制碱法”,打破了当时欧美对制碱业的垄
断,将制碱与制氨有机结合起来,同时生产纯碱和氯化铵两种产品,大大提高了原料的利
用率。
资料 1: 20℃时, NaCl、NaHCO3、NH4Cl 的溶解度分别为 36.0g、9.6g、37.2g
资料 2:氨气极易溶于饱和食盐水,形成的溶液呈碱性
(1)“侯氏制碱法”的产品是 ▲ 。
2 3中 N的化合价为 ▲ ;NH4Cl 的用途是 ▲ 。
(3)制碱工艺中的关键反应为: + 2 + 3 + 2 = 3 ↓+
4 。20 时,在实验室条件下按图示装置模拟该反应(其它装置略 …
去,实验时从左侧导管通入 2,从右侧导管通入 3) 。
① 向 200g 水中加入 ▲ gNaCl 固体配制成 NaCl 的饱和溶液。
②若条件控制得当,①中 NaCl 完全反应,理论上可得到 3的质量是 ▲ g。
③操作时先通入 3后,再通入 2的原因是 ▲ 。
④充分反应后烧杯中有晶体析出,出现的晶体主要成分是 3而不是 4 ,其原因是
▲ 。
【纯碱的应用】
“侯氏制碱法”的碱即纯碱,其水溶液显碱性,可以清洗油污,溶液碱性越强,去油
污效果越好。为探究纯碱溶液去油污效果的影响因素,分别测定不同温度下,不同浓度的
纯碱溶液的 pH,结果如下:
序号 1 2 3 4 5 6 7 8 9
浓度 2% 2% 2% 6% 6% 6% 10% 10% 10%
温度/℃ 20 40 60 20 40 60 20 40 60
pH 10.09 11.13 11.18 11.10 11.19 11.30 11.15 11.23 11.35
(4)实验中,去油污效果最好的溶液是 ▲ 。
(5)得出“纯碱溶液浓度是影响去油污效果的因素”的结论,依据的实验组合是 ▲
(填实验序号)。
)
(6)在一定温度范围内,纯碱溶液去油污效果与温度的关系是 ▲ 。
同课章节目录
