2025年湖北省黄石市阳新县城区四校中考第二次模拟考试化学试卷(含答案)
文档属性
| 名称 | 2025年湖北省黄石市阳新县城区四校中考第二次模拟考试化学试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-12 00:00:00 | ||
图片预览


文档简介
阳新县城区四校2025年中考第二次模拟考试
化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Ca-40
一、选择题(共13个题,共18分。1-8题,每题1分;9-13题,每题2分。在每题给出的四个选项中,只有一项符合题目要求)
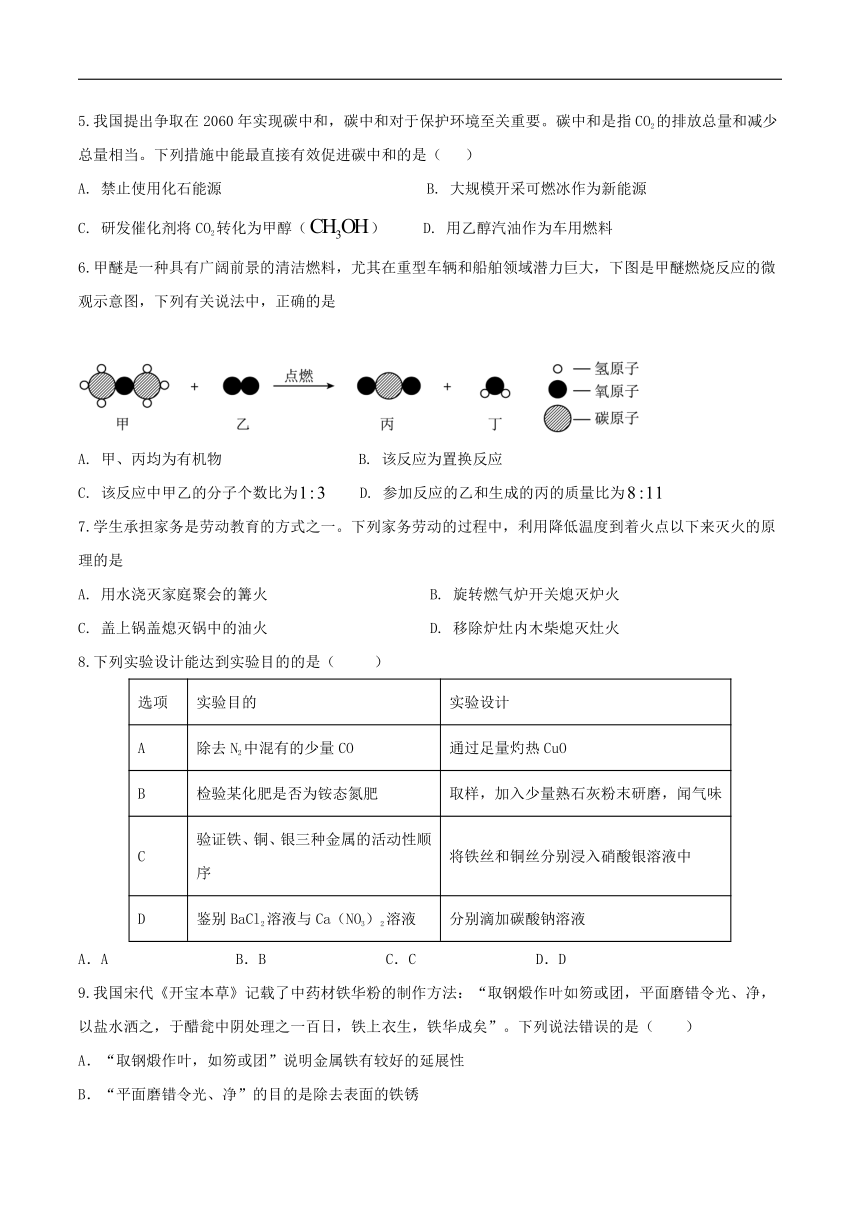
1.2024年春晚节目《瓷影》,以舞绘型,展现青白瓷跨越千年的独特魅力,下列关于青白瓷的制作过程中,属于化学变化的是( )
揉泥 B.烧窑
C.做坯 D.画坯
2.端午节吃粽子是中华民族的传统习俗。广西的肉粽味道鲜美,其原料有:糯米、五花肉、植物油、食盐和食用纯碱等。其中富含糖类的是( )
A.糯米 B.五花肉
C.植物油 D.食盐
3.2023年中国空间站正式进入运营阶段,空间站内可利用以下反应为航天员提供氧气:4KO2+4CO2+2H2O=4KHCO3+3O2。下列说法错误的是( )
A. KO2属于氧化物 B. H2O的相对分子质量为18
C. KHCO3中含有两种金属元素 D. 3O2表示3个氧分子
4.规范的操作方法是实验安全和成功的重要保证。下列实验操作中正确的是( )
A.点燃酒精灯 B.量取液体
C.倾倒液体 D.滴加液体
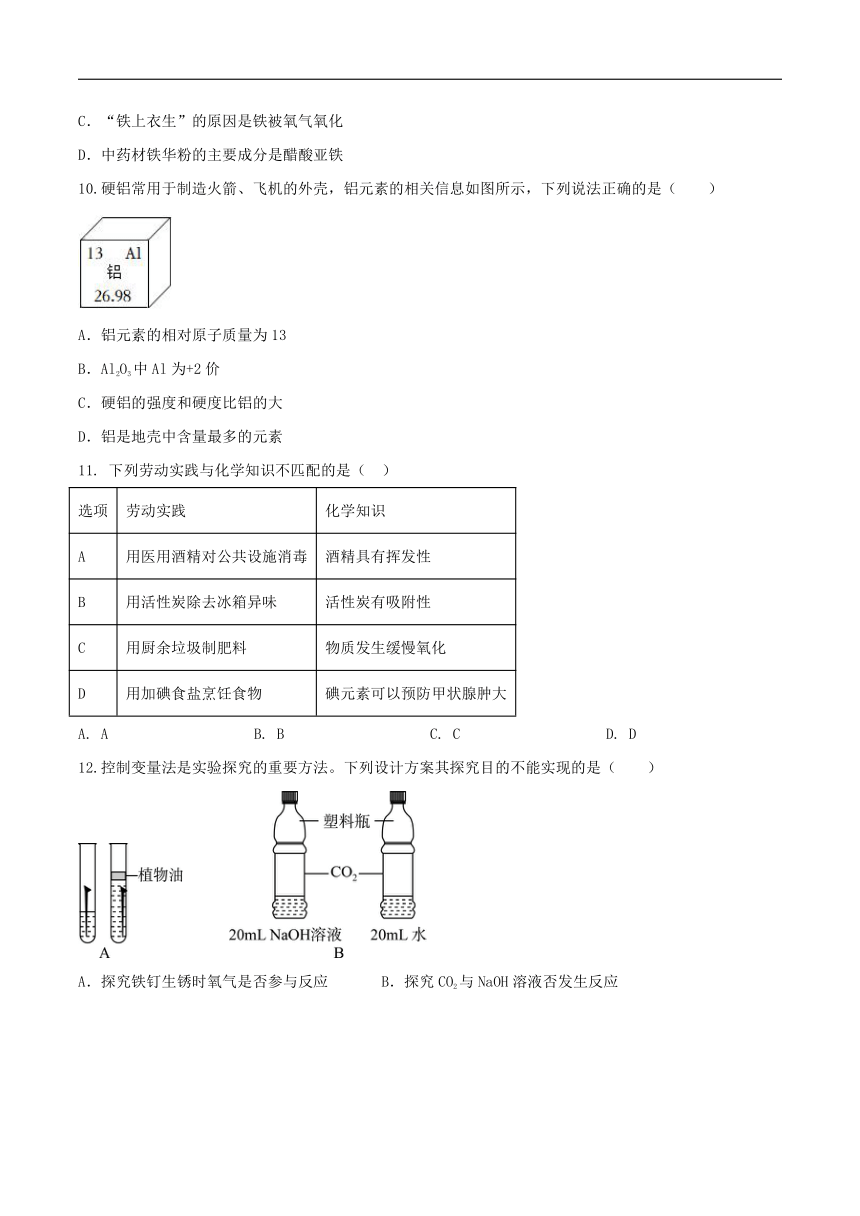
5.我国提出争取在2060年实现碳中和,碳中和对于保护环境至关重要。碳中和是指CO2的排放总量和减少总量相当。下列措施中能最直接有效促进碳中和的是( )
A. 禁止使用化石能源 B. 大规模开采可燃冰作为新能源
C. 研发催化剂将CO2转化为甲醇() D. 用乙醇汽油作为车用燃料
6.甲醚是一种具有广阔前景的清洁燃料,尤其在重型车辆和船舶领域潜力巨大,下图是甲醚燃烧反应的微观示意图,下列有关说法中,正确的是
A. 甲、丙均为有机物 B. 该反应为置换反应
C. 该反应中甲乙的分子个数比为 D. 参加反应的乙和生成的丙的质量比为
7.学生承担家务是劳动教育的方式之一。下列家务劳动的过程中,利用降低温度到着火点以下来灭火的原理的是
A. 用水浇灭家庭聚会的篝火 B. 旋转燃气炉开关熄灭炉火
C. 盖上锅盖熄灭锅中的油火 D. 移除炉灶内木柴熄灭灶火
8.下列实验设计能达到实验目的的是( )
选项 实验目的 实验设计
A 除去N2中混有的少量CO 通过足量灼热CuO
B 检验某化肥是否为铵态氮肥 取样,加入少量熟石灰粉末研磨,闻气味
C 验证铁、铜、银三种金属的活动性顺序 将铁丝和铜丝分别浸入硝酸银溶液中
D 鉴别BaCl2溶液与Ca(NO3)2溶液 分别滴加碳酸钠溶液
A.A B.B C.C D.D
9.我国宋代《开宝本草》记载了中药材铁华粉的制作方法:“取钢煅作叶如笏或团,平面磨错令光、净,以盐水洒之,于醋瓮中阴处理之一百日,铁上衣生,铁华成矣”。下列说法错误的是( )
A.“取钢煅作叶,如笏或团”说明金属铁有较好的延展性
B.“平面磨错令光、净”的目的是除去表面的铁锈
C.“铁上衣生”的原因是铁被氧气氧化
D.中药材铁华粉的主要成分是醋酸亚铁
10.硬铝常用于制造火箭、飞机的外壳,铝元素的相关信息如图所示,下列说法正确的是( )
A.铝元素的相对原子质量为13
B.Al2O3中Al为+2价
C.硬铝的强度和硬度比铝的大
D.铝是地壳中含量最多的元素
11. 下列劳动实践与化学知识不匹配的是( )
选项 劳动实践 化学知识
A 用医用酒精对公共设施消毒 酒精具有挥发性
B 用活性炭除去冰箱异味 活性炭有吸附性
C 用厨余垃圾制肥料 物质发生缓慢氧化
D 用加碘食盐烹饪食物 碘元素可以预防甲状腺肿大
A. A B. B C. C D. D
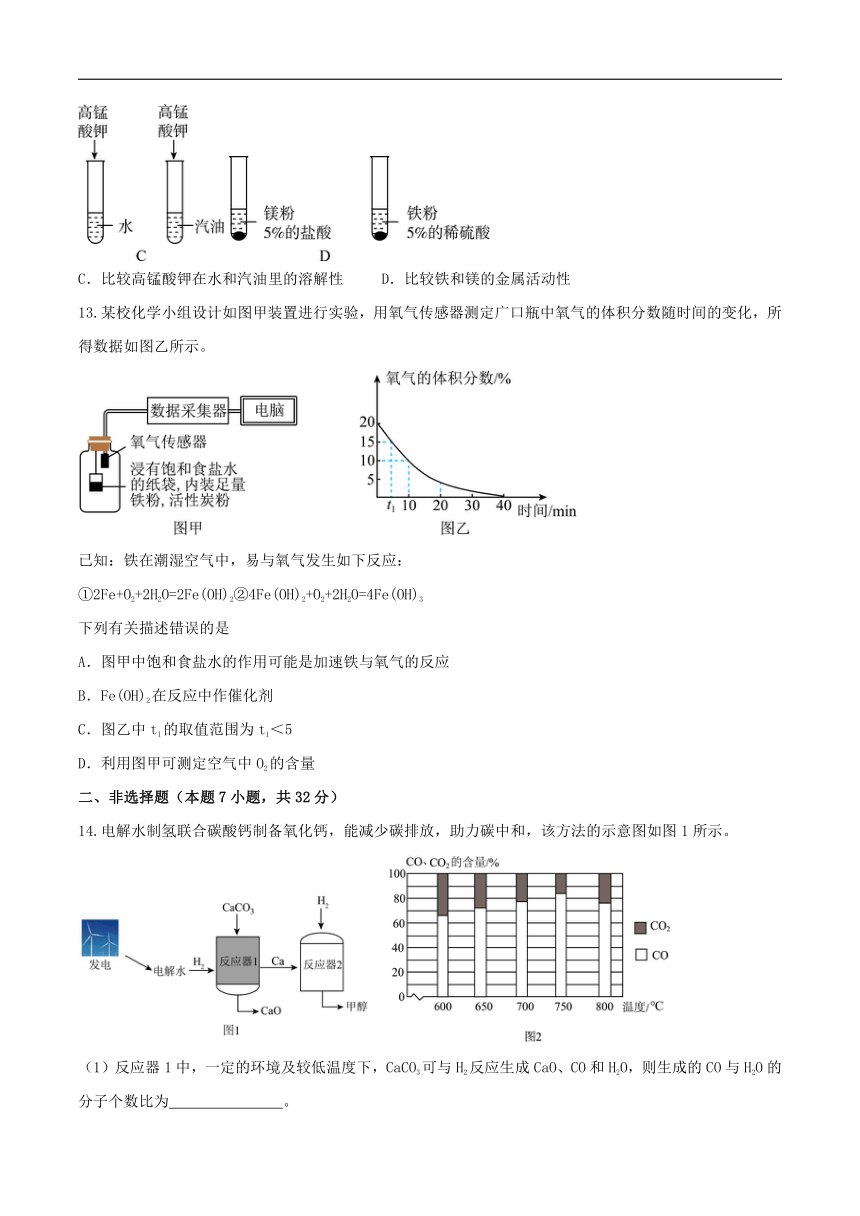
12.控制变量法是实验探究的重要方法。下列设计方案其探究目的不能实现的是( )
A.探究铁钉生锈时氧气是否参与反应 B.探究CO2与NaOH溶液否发生反应
C.比较高锰酸钾在水和汽油里的溶解性 D.比较铁和镁的金属活动性
13.某校化学小组设计如图甲装置进行实验,用氧气传感器测定广口瓶中氧气的体积分数随时间的变化,所得数据如图乙所示。
已知:铁在潮湿空气中,易与氧气发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2②4Fe(OH)2+O2+2H2O=4Fe(OH)3
下列有关描述错误的是
A.图甲中饱和食盐水的作用可能是加速铁与氧气的反应
B.Fe(OH)2在反应中作催化剂
C.图乙中t1的取值范围为t1<5
D.利用图甲可测定空气中O2的含量
二、非选择题(本题7小题,共32分)
14.电解水制氢联合碳酸钙制备氧化钙,能减少碳排放,助力碳中和,该方法的示意图如图1所示。
(1)反应器1中,一定的环境及较低温度下,CaCO3可与H2反应生成CaO、CO和H2O,则生成的CO与H2O的分子个数比为 。
(2)随着温度升高,反应器1中还会生成CO2,且生成CO、CO2的含量随反应温度的变化如图2所示, ℃时 ,抑制CO2生成的效果最好。
(3)反应器2中,一定条件下,CO与H2能发生化合反应生成甲醇(CH3OH),反应化学方程式为 。
(4)在900℃以上分解CaCO3也可以制备CaO,相比之下,电解水制氢联合碳酸钙制备氧化钙的优点有 (写一条即可)。
15.阅读科普短文,回答下列问题。
塑料方便了生活,但是由于难以降解也给环境带来了“白色污染”,危害人类的健康,寻找塑料的替代品已迫在眉睫。科学家从饱含淀粉质的玉米中制取乳酸(C3H6O3),再经过聚合反应生产出颗粒状高分子材料聚乳酸,被称为玉米塑料。提取玉米中的淀粉是该工艺的关键环节,玉米粒中70%以上为淀粉,科学家采用湿法(浸泡)提取玉米淀粉,在50℃时,相同浸泡液中(水、0.5%亚硫酸钠溶液、0.5%乳酸溶液按8:1:1配比),测定浸泡时间与玉米淀粉提取率的关系如图1。玉米塑料可替代塑料广泛应用于食品包装、一次性产品、工程、日用、农业、医疗等领域,它将变成盒子、瓶子和手机等产品。玉米塑料制品废弃后可被环境中的微生物完全分解,成为自然界碳循环的组成部分,如图2。
(1)写出一条减少“白色污染”的措施: 。
(2)乳酸中碳、氢、氧的原子个数比为 (填最简整数比).
(3)由图1分析可知,浸泡时间与玉米淀粉提取率的关系是 。
(4)玉米塑料制品废弃后最终被环境中的微生物完全分解,生成的物质是 。
(5)玉米塑料在自然环境中循环,主要发生化学变化的是______。(填字母序号)
A.玉米进行光合作用 B.玉米淀粉制取乳酸
C.玉米塑料降解或焚烧 D.从玉米中提取出玉米淀粉
16.保险粉(化学式为Na2S2O4),在工农业生产中有广泛的用途。Na2S2O4制备流程如下:
查阅资料:Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在下,Na2S2O4在水中溶解度显著下降。
(1)ZnS2O4中硫元素的化合价是 。
(2)反应I的原理为:Zn+2SO2=ZnS2O4,该反应类型为 。该反应中将Zn研磨成粉末的目的是 。
(3)反应II为复分解反应,该反应的化学方程式为 。
(4)操作a过程需要用到的玻璃仪器是烧杯、玻璃棒、 。
(5)滤液中含有Na2S2O4,为使Na2S2O4结晶析出,要加入NaCl的原因 ,还需要加入少量NaOH的原因是 。
(6)Zn(OH)2在加热的条件下分解为两种氧化物,该反应的化学方程式为 。
17.小明用石灰石测定某稀盐酸中溶质的质量分数,进行了如图甲所示的实验。随着实验的进行烧杯内物质的质量变化如图乙所示。请计算:
(1)产生二氧化碳的总质量为 g。
(2)稀盐酸中溶质的质量分数。
18.实验室用如图所示装置制取CO2气体,并进行相关性质研究。
(1)仪器a的名称是 。
(2)连接装置A、B,向锥形瓶内逐滴加入稀盐酸。
①锥形瓶内发生反应的化学方程式为 。
②若装置B用来干燥CO2,装置B中应盛放的试剂是 。
(3)将纯净干燥的CO2缓慢通入装置C,观察到现象:a.玻璃管内的干燥纸花始终未变色;b.塑料瓶内的下方纸花先变红色,上方纸花后变红色。
根据上述现象,得出关于CO2性质的结论是: (写一条即可)。
19.某化学活动小组的同学在一次实验中进行如下图所示实验。
【观察与表达】U形管左侧有白色沉淀生成,右侧产生的现象是 。
实验后,小组同学用胶塞塞紧U形管两端,充分振荡,发现管内仍有白色固体残留。将混合物过滤后,同学们对滤液中溶质的成分产生了兴趣,于是继续进行探究。
【提出问题】滤液中可能含有哪些溶质?
【猜想与假设】同学们讨论后对滤液中含有的溶质成分做出以下几种猜想:
猜想①:
猜想②:、
猜想③:、
猜想④:、
猜想⑤:、、
【分析与交流】
(1)小红指出猜想④不成立,因为振荡后U形管内的白色固体一定是 ,故滤液中溶质一定不含。
(2)小兰指出猜想⑤也一定不成立,理由是 (用化学方程式表示)。
【实验探究】为探究滤液中的溶质,同学们设计了如下实验。
实验方案 实验现象 实验结论
小兰组 取少量滤液于试管中,加入足量溶液和稀硝酸 产生 猜想①成立
小红组 取少量滤液于试管中,加入足量 (填化学式)溶液 无明显现象
【反思评价】老师指出,小兰组的实验方案是错误的,原因是 。
【归纳总结】确定反应后溶液中的溶质成分,除了要考虑生成物外,还要考虑反应物是否有剩余。
20.2024年,我国在人工智能、航空航天、地壳探测以及科技创新等方面取得了令人瞩目的成就,既彰显了我国科技力量的强大,也为我国未来发展奠定了坚实的基础。请结合图文信息,完成下面小题的相关问题。
(1)芯片是人工智能的核心,制造芯片的重要材料是硅。硅属于 (填“金属”或“非金属”)元素,硅原子的结构示意图如图,其中x的值为 。
(2)嫦娥六号探测器圆满完成人类首次月背采样后,顺利返回地球。月壤样品中含有氧化铝、氧化铁等,其中一种物质的化学式为 。月壤中含有大量氦-3,地球上有大量氦-4,氦-3与氦-4都属于氦元素,其结构中的相同之处是 。
(3)我国深地塔科1井钻探深度已突破万米。钻头中含有金刚石,构成它的微观粒子是 。在钻探时要不断注水,使钻头降温,若不降温,钻头可能会烧毁,其原因是 (用化学方程式解释)。
(4)科技创新在污染治理和生态环境保护方面发挥重要作用。采用先进的膜分离技术对污水进行处理,膜材料能像筛子一样把水中的污染物除掉。膜材料应该具有的性质是 该材料属于 材料。污水经分级处理后,可用于
参考答案
1.B
2.A
3.C
4.C
5.C
6.C
7.C
8.B
9.C
10.D
11.A
12.D
13.B
14.(1)1:1 (2)750 (3)
(4)减少CO2的排放(或节约能源、缓解温室效应)
15.(1)回收废弃塑料(合理即可)
(2)1:2:1
(3)在50℃时,相同浸泡液中,在12h~72h的浸泡时间内,玉米淀粉提取率先升高后降低
(4)二氧化碳和水
(5)ABC
16.(1)+3
(2)化合反应 增大反应物的接触面积,使反应更快更充分
(3)
(4)漏斗
(5)加入NaCl后Na2S2O4在水中溶解度显著下降 Na2S2O4在碱性溶液中稳定
(6)
17.(1)8.8
(2)14.6%
答:稀盐酸中溶质的质量分数为14.6%。
18.(1)分液漏斗
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸
(3)CO2与水反应生成碳酸或CO2密度比空气大
19.产生气泡 碳酸钡
白色沉淀 H2SO4 氯化钠、氯化钡与硝酸银反应都会产生氯化银白色沉淀,不能证明猜想一成立(合理即可)
20.(1) 非金属 4
(2) Al2O3或Fe2O3 质子数相同
(3) 碳原子
(4) 不溶于水且孔径较小 合成 业生产(或农业灌溉,或园林绿化,合理即可)
化学试题
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 Ca-40
一、选择题(共13个题,共18分。1-8题,每题1分;9-13题,每题2分。在每题给出的四个选项中,只有一项符合题目要求)
1.2024年春晚节目《瓷影》,以舞绘型,展现青白瓷跨越千年的独特魅力,下列关于青白瓷的制作过程中,属于化学变化的是( )
揉泥 B.烧窑
C.做坯 D.画坯
2.端午节吃粽子是中华民族的传统习俗。广西的肉粽味道鲜美,其原料有:糯米、五花肉、植物油、食盐和食用纯碱等。其中富含糖类的是( )
A.糯米 B.五花肉
C.植物油 D.食盐
3.2023年中国空间站正式进入运营阶段,空间站内可利用以下反应为航天员提供氧气:4KO2+4CO2+2H2O=4KHCO3+3O2。下列说法错误的是( )
A. KO2属于氧化物 B. H2O的相对分子质量为18
C. KHCO3中含有两种金属元素 D. 3O2表示3个氧分子
4.规范的操作方法是实验安全和成功的重要保证。下列实验操作中正确的是( )
A.点燃酒精灯 B.量取液体
C.倾倒液体 D.滴加液体
5.我国提出争取在2060年实现碳中和,碳中和对于保护环境至关重要。碳中和是指CO2的排放总量和减少总量相当。下列措施中能最直接有效促进碳中和的是( )
A. 禁止使用化石能源 B. 大规模开采可燃冰作为新能源
C. 研发催化剂将CO2转化为甲醇() D. 用乙醇汽油作为车用燃料
6.甲醚是一种具有广阔前景的清洁燃料,尤其在重型车辆和船舶领域潜力巨大,下图是甲醚燃烧反应的微观示意图,下列有关说法中,正确的是
A. 甲、丙均为有机物 B. 该反应为置换反应
C. 该反应中甲乙的分子个数比为 D. 参加反应的乙和生成的丙的质量比为
7.学生承担家务是劳动教育的方式之一。下列家务劳动的过程中,利用降低温度到着火点以下来灭火的原理的是
A. 用水浇灭家庭聚会的篝火 B. 旋转燃气炉开关熄灭炉火
C. 盖上锅盖熄灭锅中的油火 D. 移除炉灶内木柴熄灭灶火
8.下列实验设计能达到实验目的的是( )
选项 实验目的 实验设计
A 除去N2中混有的少量CO 通过足量灼热CuO
B 检验某化肥是否为铵态氮肥 取样,加入少量熟石灰粉末研磨,闻气味
C 验证铁、铜、银三种金属的活动性顺序 将铁丝和铜丝分别浸入硝酸银溶液中
D 鉴别BaCl2溶液与Ca(NO3)2溶液 分别滴加碳酸钠溶液
A.A B.B C.C D.D
9.我国宋代《开宝本草》记载了中药材铁华粉的制作方法:“取钢煅作叶如笏或团,平面磨错令光、净,以盐水洒之,于醋瓮中阴处理之一百日,铁上衣生,铁华成矣”。下列说法错误的是( )
A.“取钢煅作叶,如笏或团”说明金属铁有较好的延展性
B.“平面磨错令光、净”的目的是除去表面的铁锈
C.“铁上衣生”的原因是铁被氧气氧化
D.中药材铁华粉的主要成分是醋酸亚铁
10.硬铝常用于制造火箭、飞机的外壳,铝元素的相关信息如图所示,下列说法正确的是( )
A.铝元素的相对原子质量为13
B.Al2O3中Al为+2价
C.硬铝的强度和硬度比铝的大
D.铝是地壳中含量最多的元素
11. 下列劳动实践与化学知识不匹配的是( )
选项 劳动实践 化学知识
A 用医用酒精对公共设施消毒 酒精具有挥发性
B 用活性炭除去冰箱异味 活性炭有吸附性
C 用厨余垃圾制肥料 物质发生缓慢氧化
D 用加碘食盐烹饪食物 碘元素可以预防甲状腺肿大
A. A B. B C. C D. D
12.控制变量法是实验探究的重要方法。下列设计方案其探究目的不能实现的是( )
A.探究铁钉生锈时氧气是否参与反应 B.探究CO2与NaOH溶液否发生反应
C.比较高锰酸钾在水和汽油里的溶解性 D.比较铁和镁的金属活动性
13.某校化学小组设计如图甲装置进行实验,用氧气传感器测定广口瓶中氧气的体积分数随时间的变化,所得数据如图乙所示。
已知:铁在潮湿空气中,易与氧气发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2②4Fe(OH)2+O2+2H2O=4Fe(OH)3
下列有关描述错误的是
A.图甲中饱和食盐水的作用可能是加速铁与氧气的反应
B.Fe(OH)2在反应中作催化剂
C.图乙中t1的取值范围为t1<5
D.利用图甲可测定空气中O2的含量
二、非选择题(本题7小题,共32分)
14.电解水制氢联合碳酸钙制备氧化钙,能减少碳排放,助力碳中和,该方法的示意图如图1所示。
(1)反应器1中,一定的环境及较低温度下,CaCO3可与H2反应生成CaO、CO和H2O,则生成的CO与H2O的分子个数比为 。
(2)随着温度升高,反应器1中还会生成CO2,且生成CO、CO2的含量随反应温度的变化如图2所示, ℃时 ,抑制CO2生成的效果最好。
(3)反应器2中,一定条件下,CO与H2能发生化合反应生成甲醇(CH3OH),反应化学方程式为 。
(4)在900℃以上分解CaCO3也可以制备CaO,相比之下,电解水制氢联合碳酸钙制备氧化钙的优点有 (写一条即可)。
15.阅读科普短文,回答下列问题。
塑料方便了生活,但是由于难以降解也给环境带来了“白色污染”,危害人类的健康,寻找塑料的替代品已迫在眉睫。科学家从饱含淀粉质的玉米中制取乳酸(C3H6O3),再经过聚合反应生产出颗粒状高分子材料聚乳酸,被称为玉米塑料。提取玉米中的淀粉是该工艺的关键环节,玉米粒中70%以上为淀粉,科学家采用湿法(浸泡)提取玉米淀粉,在50℃时,相同浸泡液中(水、0.5%亚硫酸钠溶液、0.5%乳酸溶液按8:1:1配比),测定浸泡时间与玉米淀粉提取率的关系如图1。玉米塑料可替代塑料广泛应用于食品包装、一次性产品、工程、日用、农业、医疗等领域,它将变成盒子、瓶子和手机等产品。玉米塑料制品废弃后可被环境中的微生物完全分解,成为自然界碳循环的组成部分,如图2。
(1)写出一条减少“白色污染”的措施: 。
(2)乳酸中碳、氢、氧的原子个数比为 (填最简整数比).
(3)由图1分析可知,浸泡时间与玉米淀粉提取率的关系是 。
(4)玉米塑料制品废弃后最终被环境中的微生物完全分解,生成的物质是 。
(5)玉米塑料在自然环境中循环,主要发生化学变化的是______。(填字母序号)
A.玉米进行光合作用 B.玉米淀粉制取乳酸
C.玉米塑料降解或焚烧 D.从玉米中提取出玉米淀粉
16.保险粉(化学式为Na2S2O4),在工农业生产中有广泛的用途。Na2S2O4制备流程如下:
查阅资料:Na2S2O4在碱性溶液中稳定,在中性和酸性溶液中极不稳定;在NaCl存在下,Na2S2O4在水中溶解度显著下降。
(1)ZnS2O4中硫元素的化合价是 。
(2)反应I的原理为:Zn+2SO2=ZnS2O4,该反应类型为 。该反应中将Zn研磨成粉末的目的是 。
(3)反应II为复分解反应,该反应的化学方程式为 。
(4)操作a过程需要用到的玻璃仪器是烧杯、玻璃棒、 。
(5)滤液中含有Na2S2O4,为使Na2S2O4结晶析出,要加入NaCl的原因 ,还需要加入少量NaOH的原因是 。
(6)Zn(OH)2在加热的条件下分解为两种氧化物,该反应的化学方程式为 。
17.小明用石灰石测定某稀盐酸中溶质的质量分数,进行了如图甲所示的实验。随着实验的进行烧杯内物质的质量变化如图乙所示。请计算:
(1)产生二氧化碳的总质量为 g。
(2)稀盐酸中溶质的质量分数。
18.实验室用如图所示装置制取CO2气体,并进行相关性质研究。
(1)仪器a的名称是 。
(2)连接装置A、B,向锥形瓶内逐滴加入稀盐酸。
①锥形瓶内发生反应的化学方程式为 。
②若装置B用来干燥CO2,装置B中应盛放的试剂是 。
(3)将纯净干燥的CO2缓慢通入装置C,观察到现象:a.玻璃管内的干燥纸花始终未变色;b.塑料瓶内的下方纸花先变红色,上方纸花后变红色。
根据上述现象,得出关于CO2性质的结论是: (写一条即可)。
19.某化学活动小组的同学在一次实验中进行如下图所示实验。
【观察与表达】U形管左侧有白色沉淀生成,右侧产生的现象是 。
实验后,小组同学用胶塞塞紧U形管两端,充分振荡,发现管内仍有白色固体残留。将混合物过滤后,同学们对滤液中溶质的成分产生了兴趣,于是继续进行探究。
【提出问题】滤液中可能含有哪些溶质?
【猜想与假设】同学们讨论后对滤液中含有的溶质成分做出以下几种猜想:
猜想①:
猜想②:、
猜想③:、
猜想④:、
猜想⑤:、、
【分析与交流】
(1)小红指出猜想④不成立,因为振荡后U形管内的白色固体一定是 ,故滤液中溶质一定不含。
(2)小兰指出猜想⑤也一定不成立,理由是 (用化学方程式表示)。
【实验探究】为探究滤液中的溶质,同学们设计了如下实验。
实验方案 实验现象 实验结论
小兰组 取少量滤液于试管中,加入足量溶液和稀硝酸 产生 猜想①成立
小红组 取少量滤液于试管中,加入足量 (填化学式)溶液 无明显现象
【反思评价】老师指出,小兰组的实验方案是错误的,原因是 。
【归纳总结】确定反应后溶液中的溶质成分,除了要考虑生成物外,还要考虑反应物是否有剩余。
20.2024年,我国在人工智能、航空航天、地壳探测以及科技创新等方面取得了令人瞩目的成就,既彰显了我国科技力量的强大,也为我国未来发展奠定了坚实的基础。请结合图文信息,完成下面小题的相关问题。
(1)芯片是人工智能的核心,制造芯片的重要材料是硅。硅属于 (填“金属”或“非金属”)元素,硅原子的结构示意图如图,其中x的值为 。
(2)嫦娥六号探测器圆满完成人类首次月背采样后,顺利返回地球。月壤样品中含有氧化铝、氧化铁等,其中一种物质的化学式为 。月壤中含有大量氦-3,地球上有大量氦-4,氦-3与氦-4都属于氦元素,其结构中的相同之处是 。
(3)我国深地塔科1井钻探深度已突破万米。钻头中含有金刚石,构成它的微观粒子是 。在钻探时要不断注水,使钻头降温,若不降温,钻头可能会烧毁,其原因是 (用化学方程式解释)。
(4)科技创新在污染治理和生态环境保护方面发挥重要作用。采用先进的膜分离技术对污水进行处理,膜材料能像筛子一样把水中的污染物除掉。膜材料应该具有的性质是 该材料属于 材料。污水经分级处理后,可用于
参考答案
1.B
2.A
3.C
4.C
5.C
6.C
7.C
8.B
9.C
10.D
11.A
12.D
13.B
14.(1)1:1 (2)750 (3)
(4)减少CO2的排放(或节约能源、缓解温室效应)
15.(1)回收废弃塑料(合理即可)
(2)1:2:1
(3)在50℃时,相同浸泡液中,在12h~72h的浸泡时间内,玉米淀粉提取率先升高后降低
(4)二氧化碳和水
(5)ABC
16.(1)+3
(2)化合反应 增大反应物的接触面积,使反应更快更充分
(3)
(4)漏斗
(5)加入NaCl后Na2S2O4在水中溶解度显著下降 Na2S2O4在碱性溶液中稳定
(6)
17.(1)8.8
(2)14.6%
答:稀盐酸中溶质的质量分数为14.6%。
18.(1)分液漏斗
(2)CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸
(3)CO2与水反应生成碳酸或CO2密度比空气大
19.产生气泡 碳酸钡
白色沉淀 H2SO4 氯化钠、氯化钡与硝酸银反应都会产生氯化银白色沉淀,不能证明猜想一成立(合理即可)
20.(1) 非金属 4
(2) Al2O3或Fe2O3 质子数相同
(3) 碳原子
(4) 不溶于水且孔径较小 合成 业生产(或农业灌溉,或园林绿化,合理即可)
同课章节目录
