浙江省七彩阳光新高考研究联盟2024-2025学年高一下学期期中联考化学试卷(PDF版,含答案)
文档属性
| 名称 | 浙江省七彩阳光新高考研究联盟2024-2025学年高一下学期期中联考化学试卷(PDF版,含答案) |  | |
| 格式 | |||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-12 20:43:07 | ||
图片预览


文档简介
绝密★考试结束前
2024 学年第二学期浙江“七彩阳光”新高考研究联盟期中联考
高一年级化学学科 试题
考生须知:
1.本卷共 6 页满分 100 分,考试时间 90 分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27
S 32 Cl 35.5 Ca 40 Mn 55 Fe 56 Cu 64 Ba 137
选择题部分
一、选择题(本大题共 20小题,每小题 3分,共 60分。每小题列出的四个备选项中只有一个是符合题目要求的,
不选,多选,错选均不得分)
1.按物质的组成进行分类,KMnO4属于
A.氧化物 B.酸 C.盐 D.碱
2.下列实验图标符合“热烫”有关提示的是
A. B. C. D.
3.化学反应速率的常用单位是
A.mol/L B.L/mol C.mol/(L·s) D.L/(mol·s)
4.下列物质不.属.于.无机非金属材料的是
A.光导纤维 B.PVC塑料 C.水泥 D.氮化硅陶瓷
5.反应 H3PO2+4Ag++2H2O=4Ag+H3PO4+4H+中,氧化剂是
A.H3PO4 B.Ag+ C.H2O D.H3PO2
6.下列化学用语表示正确的是
A.过氧化钠的电子式: B.氯化钠的分子式:NaCl
C.乙烷的结构式:CH3CH3 D.氨的空间填充模型:
7.下列说法不.正.确.的是
A.在食品中添加适量二氧化硫可以起到漂白、防腐和抗氧化等作用
B.合成氨在很大程度上解决了地球上因粮食不足而导致的饥饿问题
C.石墨烯是仅一个碳原子直径厚度的单层石墨,有电阻率低的特性
D.沼气、水煤气、凡士林、石蜡都是烷烃,烷烃中甲烷含氢量最高
高一化学学科 试题 第 1页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
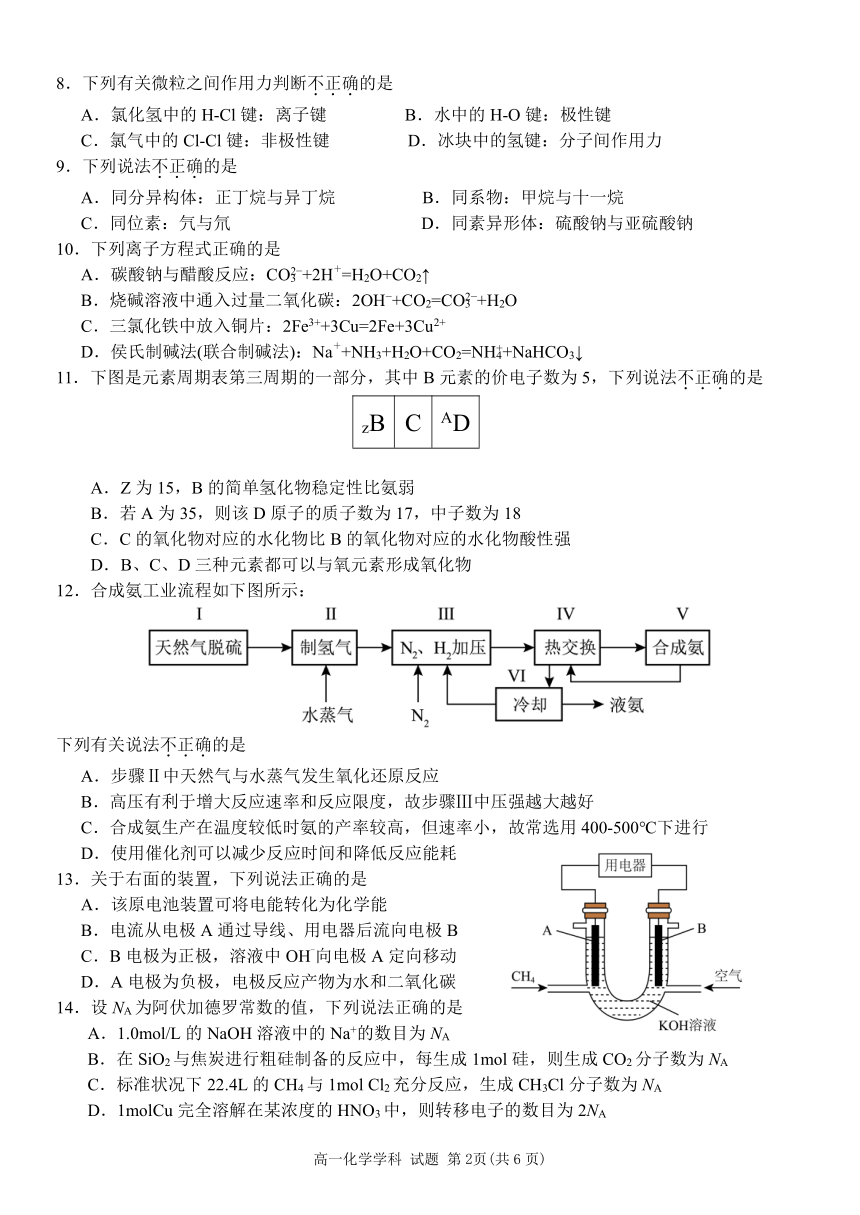
8.下列有关微粒之间作用力判断不.正.确.的是
A.氯化氢中的 H-Cl键:离子键 B.水中的 H-O键:极性键
C.氯气中的 Cl-Cl键:非极性键 D.冰块中的氢键:分子间作用力
9.下列说法不.正.确.的是
A.同分异构体:正丁烷与异丁烷 B.同系物:甲烷与十一烷
C.同位素:氕与氘 D.同素异形体:硫酸钠与亚硫酸钠
10.下列离子方程式正确的是
A +.碳酸钠与醋酸反应:CO23 +2H =H2O+CO2↑
B.烧碱溶液中通入过量二氧化碳:2OH +CO2=CO32 +H2O
C.三氯化铁中放入铜片:2Fe3++3Cu=2Fe+3Cu2+
D +.侯氏制碱法(联合制碱法):Na +NH3+H2O+CO2=NH4++NaHCO3↓
11.下图是元素周期表第三周期的一部分,其中 B元素的价电子数为 5,下列说法不.正.确.的是
zB C AD
A.Z为 15,B的简单氢化物稳定性比氨弱
B.若 A为 35,则该 D原子的质子数为 17,中子数为 18
C.C的氧化物对应的水化物比 B的氧化物对应的水化物酸性强
D.B、C、D三种元素都可以与氧元素形成氧化物
12.合成氨工业流程如下图所示:
下列有关说法不.正.确.的是
A.步骤Ⅱ中天然气与水蒸气发生氧化还原反应
B.高压有利于增大反应速率和反应限度,故步骤Ⅲ中压强越大越好
C.合成氨生产在温度较低时氨的产率较高,但速率小,故常选用 400-500℃下进行
D.使用催化剂可以减少反应时间和降低反应能耗
13.关于右面的装置,下列说法正确的是
A.该原电池装置可将电能转化为化学能
B.电流从电极 A通过导线、用电器后流向电极 B
C B -. 电极为正极,溶液中 OH向电极 A定向移动
D.A电极为负极,电极反应产物为水和二氧化碳
14.设 NA为阿伏加德罗常数的值,下列说法正确的是
A.1.0mol/L的 NaOH溶液中的 Na+的数目为 NA
B.在 SiO2与焦炭进行粗硅制备的反应中,每生成 1mol硅,则生成 CO2分子数为 NA
C.标准状况下 22.4L的 CH4与 1mol Cl2充分反应,生成 CH3Cl分子数为 NA
D.1molCu完全溶解在某浓度的 HNO3中,则转移电子的数目为 2NA
高一化学学科 试题 第 2页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
15.下列实验装置中,无法达到相应实验目的的是
A.装置甲可制备氢氧化亚铁沉淀 B.装置乙可进行粗盐的提纯
C.装置丙可观察钠的焰色试验 D.装置丁可探究浓度对化学反应速率的影响
16.下列对化学学科思想的理解正确的是
A.氧化钠是碱性氧化物,过氧化钠也是碱性氧化物
B.探究催化剂对反应速率的影响时,需要控制温度、浓度等其他变量因素一致
C.氯与溴是同一主族元素,氯单质在常温下是气态,则溴单质在常温下也是气态
D.实验室制取气体装置的一般顺序:发生装置→收集装置→除杂装置→尾气处理装置
17.发动机在高速运转时会发生 N2(g)和 O2(g)的化合反应,其能量变化如图所示,
下列说法不.正.确.的是
A.断开 1molN2(g)中的化学键需要吸收 946kJ的能量
B.2molNO(g)完全分解成 N2(g)和 O2(g)放出 180kJ的能量
C.1molN2(g)和 1molO2(g)的总能量高于 2molNO(g)总能量
D.该反应的反应物的总键能大于生成物的总键能
18.某兴趣小组验证浓硫酸与木炭反应的产物,实验设计如下:
木炭
下列说法不.正.确.的是
A.浓硫酸与木炭的反应方程式:C + 2H2SO4(浓) =CO2↑+ 2SO2↑ + 2H2O
B.装置的连接顺序:Ⅰ→Ⅲ→Ⅳ→Ⅱ
C.酸性 KMnO4溶液的作用是除去产物中的 SO2
D.仅根据澄清石灰水变浑浊并不能证明产物中有 CO2
高一化学学科 试题 第 3页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
19.在恒温恒容密闭体系中发生:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列选项能说明已经达到平
衡状态的是
A.v(CO2)=v(H2O) B.容器内密度不变
C.c(CO2)=c(H2O) D.c(H2O)/c(CO2)值不变
20.下列实验事实与对应的结论都正确的是
实验事实 结论
A 新制氯水滴到蓝色石蕊试纸上先变红后褪色 新制氯水无酸性,只有漂白性
一定量 Fe粉与水蒸气反应后的混合物溶于稀 生成的 Fe3+可能与多余的 Fe 粉反
B
硫酸,再向溶液中滴加 KSCN无明显变化 应,全部变成了 Fe2+
C 浓硫酸与铜共热后的溶液不显蓝色 浓硫酸与铜共热不生成 Cu2+
D 打磨过的铝片投入到浓硝酸中没有明显变化 铝片与浓硝酸不反应
非选择题部分
二、非选择题(本大题共 5小题,共 40分)
21.请回答:
(1)CH3CH2CH3的名称为 ▲ 。
(2)CH4与 Cl2在光照条件下生成 CH3Cl的反应类型是 ▲ 。
(3)通过增加炼铁高炉的高度来增加 CO参与反应的时间,不能改变高炉尾气中 CO气体的比例,
不能减少有害气体的排放,其原因是 ▲ 。
22.某实验小组用打磨并称重后的两种金属片在硫酸铜溶液中进行如下实验,
硫酸铜溶液
装置以稳定的电流强度 I安培持续放电 t秒后,溶液仍呈现蓝色。
取出铜片,洗涤、干燥、称量,铜片增重 ag。
提示:电流强度定义为单位时间流过的电量,计算公式:I=Q/t
请回答下列问题:
(1)电子流入的电极材料是 ▲ (填“铜片”或“铝片”)。
(2)写出该原电池的总反应 ▲ 。
(3)铝片减轻的质量是 ▲ g(小数部分保留两位有效数字)。
(4)设 NA为阿伏加德罗常数的数值,则每个电子所带的电量是 ▲ C(库仑)。
高一化学学科 试题 第 4页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
23.工业上氨气经过一系列反应制得硝酸。流程如图所示:
(1)NO2气体的颜色 ▲ ,浓 HNO3见光或加热易分解为 ▲ 和 H2O。
(2)NH3发生催化氧化生成 NO的反应方程式为 ▲ 。
(3)尾气中含有氮氧化物 NO、NO2,可用 NaOH溶液吸收,发生的反应有:
2NaOH+2NO2=NaNO3+NaNO2+H2O,
NaOH+NO+NO2= ▲ +H2O(只填化学式,无需配平) 。
(4)用不同浓度的 NaOH溶液吸收 NO2含量不同的尾气,测得氮氧化物吸收率与 NaOH 溶液浓度
的关系如图所示:
依据测得的关系图,下列措施一定能提高氮氧化物吸收率的是 ▲ (填序号)。
A.增大 NaOH溶液的浓度 B.提高尾气中 NO2的含量
C.在 NaOH 溶液加入 H2O2 D.用热的 NaOH溶液吸收
高一化学学科 试题 第 5页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
24.某化学兴趣小组设计了如下实验流程,用该工厂的废金属屑(主要成分为 Cu、Fe 和 Al,少量
Al2O3和 Fe2O3)制取氯化铝(AlCl3)、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
请回答:
(1)试剂 X的名称 ▲ ,溶液 D中主要溶质的化学式是 ▲ 。
(2)固体 C溶于 NaOH溶液的化学方程式为 ▲ 。
(3)溶液 E经过蒸发浓缩、冷却结晶、 ▲ 、洗涤、干燥等系列操作制得绿矾晶体。
(4)实验兴趣小组利用以下流程制取消毒净水两用剂 Na2FeO4,
写出上述流程中发生的离子方程式 ▲ 。
25.利用催化技术可将汽车尾气中的 CO和 NO转化为 CO2和 N2,
反应的化学方程式为:2NO+2CO 2CO2+N2。
某温度下,在 2L容积不变的密闭容器中通入 CO和 NO,测得不同时间 CO的物质的量如下:
时间/s 0 1 2 3 …
n(CO)/mol 3.60 3.05 2.85 2.75 …
(1)比较下列时间段平均反应速率最快的是 ▲ 。
A.0→1s B. 1s→2s C.2s→3s
(2)在 2s时,容器中的 CO2物质的量为 ▲ mol。
(3)用 N2的浓度变化表示 0~3s的平均反应速率为 ▲ mol L-1 s-1(保留 3位有效数字)。
高一化学学科 试题 第 6页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
2024学年第二学期浙江“七彩阳光”新高考研究联盟期中联考
高一年级化学学科评分标准及参考答案
一、选择题(本大题共 20小题,每小题 3分,共 60分。每小题列出的四个备选项中只有一个是符
合题目要求的,不选、多选、错选均不得分)
1 2 3 4 5 6 7 8 9 10
C C C B B D D A D D
11 12 13 14 15 16 17 18 19 20
C B C D D B C B D B
二、非选择题部分(本大题共 5小题,共 40分)
21.(6分)
(1)(2分)丙烷 ;
(2)(2分)取代反应 (只写“取代”也给分) ;
(3)(2分)可逆反应(给 1分) CO不能完全转化(给 1分) (只写“反应存在限度”或“达到
平衡状态”均给 2分) 。
22.(8分)
(1)(2分)铜片 ;
(2)(2分)2Al+3Cu2+=2Al3++3Cu (写化学方程式、离子方程式均给分) ;
(3)(2分)0.28a (用分数“9a/32”表示也给分);
(4)(2分)32It/aNA (写“64It/2aNA”不扣分,“M(Cu)It/2aNA”只给 1分)。
23.(10分)
(1)(2分)红棕色; (2分)NO2 O2 (每个 1分,多写只看前两个)
(2)(2分)4NH3+5O2=4NO+6H2O (化学式正确未配平给 1分,反应条件不写不扣分?)
(3)(2分)NaNO2
(4)(2分)BC (选对 1个给 1分,错选、多选、不选不给分)
24.(10分)
(1)(2分)硫酸 (写“稀硫酸”给 2分,写“浓硫酸”不给分,写化学式不给分);
(2分)NaHCO3 (写名称或俗称的不给分);
(2)(2分)Al(OH)3+NaOH=Na[Al(OH)4]
(化学式正确未配平给 1分,写“Al(OH)3+NaOH=NaAlO2+2H2O”的也给 2分)
(3)(2分)过滤
(4)(2分)2Fe(OH)3+3ClO-+4OH-=2FeO24 +3Cl-+5H2O (化学式正确未配平给 1分,写化学方程
式的不给分)
25.(6分)
(1)(2分)A (只选一个,错选、多选、不选不给分)
(2)(2分)0.75 (复写单位不扣分)
(3)(2分)0.0708 (有效数字保留不正确扣 1分,复写单位不扣分)
高一化学学科 评分标准及参考答案 第 1 页 共 1 页
{#{QQABbQaEggAIAAJAABhCEwVSCAOQkBCAAQoOQAAQMAAAAAFABCA=}#}
2024 学年第二学期浙江“七彩阳光”新高考研究联盟期中联考
高一年级化学学科 试题
考生须知:
1.本卷共 6 页满分 100 分,考试时间 90 分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27
S 32 Cl 35.5 Ca 40 Mn 55 Fe 56 Cu 64 Ba 137
选择题部分
一、选择题(本大题共 20小题,每小题 3分,共 60分。每小题列出的四个备选项中只有一个是符合题目要求的,
不选,多选,错选均不得分)
1.按物质的组成进行分类,KMnO4属于
A.氧化物 B.酸 C.盐 D.碱
2.下列实验图标符合“热烫”有关提示的是
A. B. C. D.
3.化学反应速率的常用单位是
A.mol/L B.L/mol C.mol/(L·s) D.L/(mol·s)
4.下列物质不.属.于.无机非金属材料的是
A.光导纤维 B.PVC塑料 C.水泥 D.氮化硅陶瓷
5.反应 H3PO2+4Ag++2H2O=4Ag+H3PO4+4H+中,氧化剂是
A.H3PO4 B.Ag+ C.H2O D.H3PO2
6.下列化学用语表示正确的是
A.过氧化钠的电子式: B.氯化钠的分子式:NaCl
C.乙烷的结构式:CH3CH3 D.氨的空间填充模型:
7.下列说法不.正.确.的是
A.在食品中添加适量二氧化硫可以起到漂白、防腐和抗氧化等作用
B.合成氨在很大程度上解决了地球上因粮食不足而导致的饥饿问题
C.石墨烯是仅一个碳原子直径厚度的单层石墨,有电阻率低的特性
D.沼气、水煤气、凡士林、石蜡都是烷烃,烷烃中甲烷含氢量最高
高一化学学科 试题 第 1页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
8.下列有关微粒之间作用力判断不.正.确.的是
A.氯化氢中的 H-Cl键:离子键 B.水中的 H-O键:极性键
C.氯气中的 Cl-Cl键:非极性键 D.冰块中的氢键:分子间作用力
9.下列说法不.正.确.的是
A.同分异构体:正丁烷与异丁烷 B.同系物:甲烷与十一烷
C.同位素:氕与氘 D.同素异形体:硫酸钠与亚硫酸钠
10.下列离子方程式正确的是
A +.碳酸钠与醋酸反应:CO23 +2H =H2O+CO2↑
B.烧碱溶液中通入过量二氧化碳:2OH +CO2=CO32 +H2O
C.三氯化铁中放入铜片:2Fe3++3Cu=2Fe+3Cu2+
D +.侯氏制碱法(联合制碱法):Na +NH3+H2O+CO2=NH4++NaHCO3↓
11.下图是元素周期表第三周期的一部分,其中 B元素的价电子数为 5,下列说法不.正.确.的是
zB C AD
A.Z为 15,B的简单氢化物稳定性比氨弱
B.若 A为 35,则该 D原子的质子数为 17,中子数为 18
C.C的氧化物对应的水化物比 B的氧化物对应的水化物酸性强
D.B、C、D三种元素都可以与氧元素形成氧化物
12.合成氨工业流程如下图所示:
下列有关说法不.正.确.的是
A.步骤Ⅱ中天然气与水蒸气发生氧化还原反应
B.高压有利于增大反应速率和反应限度,故步骤Ⅲ中压强越大越好
C.合成氨生产在温度较低时氨的产率较高,但速率小,故常选用 400-500℃下进行
D.使用催化剂可以减少反应时间和降低反应能耗
13.关于右面的装置,下列说法正确的是
A.该原电池装置可将电能转化为化学能
B.电流从电极 A通过导线、用电器后流向电极 B
C B -. 电极为正极,溶液中 OH向电极 A定向移动
D.A电极为负极,电极反应产物为水和二氧化碳
14.设 NA为阿伏加德罗常数的值,下列说法正确的是
A.1.0mol/L的 NaOH溶液中的 Na+的数目为 NA
B.在 SiO2与焦炭进行粗硅制备的反应中,每生成 1mol硅,则生成 CO2分子数为 NA
C.标准状况下 22.4L的 CH4与 1mol Cl2充分反应,生成 CH3Cl分子数为 NA
D.1molCu完全溶解在某浓度的 HNO3中,则转移电子的数目为 2NA
高一化学学科 试题 第 2页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
15.下列实验装置中,无法达到相应实验目的的是
A.装置甲可制备氢氧化亚铁沉淀 B.装置乙可进行粗盐的提纯
C.装置丙可观察钠的焰色试验 D.装置丁可探究浓度对化学反应速率的影响
16.下列对化学学科思想的理解正确的是
A.氧化钠是碱性氧化物,过氧化钠也是碱性氧化物
B.探究催化剂对反应速率的影响时,需要控制温度、浓度等其他变量因素一致
C.氯与溴是同一主族元素,氯单质在常温下是气态,则溴单质在常温下也是气态
D.实验室制取气体装置的一般顺序:发生装置→收集装置→除杂装置→尾气处理装置
17.发动机在高速运转时会发生 N2(g)和 O2(g)的化合反应,其能量变化如图所示,
下列说法不.正.确.的是
A.断开 1molN2(g)中的化学键需要吸收 946kJ的能量
B.2molNO(g)完全分解成 N2(g)和 O2(g)放出 180kJ的能量
C.1molN2(g)和 1molO2(g)的总能量高于 2molNO(g)总能量
D.该反应的反应物的总键能大于生成物的总键能
18.某兴趣小组验证浓硫酸与木炭反应的产物,实验设计如下:
木炭
下列说法不.正.确.的是
A.浓硫酸与木炭的反应方程式:C + 2H2SO4(浓) =CO2↑+ 2SO2↑ + 2H2O
B.装置的连接顺序:Ⅰ→Ⅲ→Ⅳ→Ⅱ
C.酸性 KMnO4溶液的作用是除去产物中的 SO2
D.仅根据澄清石灰水变浑浊并不能证明产物中有 CO2
高一化学学科 试题 第 3页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
19.在恒温恒容密闭体系中发生:CO2(g)+3H2(g) CH3OH(g)+H2O(g),下列选项能说明已经达到平
衡状态的是
A.v(CO2)=v(H2O) B.容器内密度不变
C.c(CO2)=c(H2O) D.c(H2O)/c(CO2)值不变
20.下列实验事实与对应的结论都正确的是
实验事实 结论
A 新制氯水滴到蓝色石蕊试纸上先变红后褪色 新制氯水无酸性,只有漂白性
一定量 Fe粉与水蒸气反应后的混合物溶于稀 生成的 Fe3+可能与多余的 Fe 粉反
B
硫酸,再向溶液中滴加 KSCN无明显变化 应,全部变成了 Fe2+
C 浓硫酸与铜共热后的溶液不显蓝色 浓硫酸与铜共热不生成 Cu2+
D 打磨过的铝片投入到浓硝酸中没有明显变化 铝片与浓硝酸不反应
非选择题部分
二、非选择题(本大题共 5小题,共 40分)
21.请回答:
(1)CH3CH2CH3的名称为 ▲ 。
(2)CH4与 Cl2在光照条件下生成 CH3Cl的反应类型是 ▲ 。
(3)通过增加炼铁高炉的高度来增加 CO参与反应的时间,不能改变高炉尾气中 CO气体的比例,
不能减少有害气体的排放,其原因是 ▲ 。
22.某实验小组用打磨并称重后的两种金属片在硫酸铜溶液中进行如下实验,
硫酸铜溶液
装置以稳定的电流强度 I安培持续放电 t秒后,溶液仍呈现蓝色。
取出铜片,洗涤、干燥、称量,铜片增重 ag。
提示:电流强度定义为单位时间流过的电量,计算公式:I=Q/t
请回答下列问题:
(1)电子流入的电极材料是 ▲ (填“铜片”或“铝片”)。
(2)写出该原电池的总反应 ▲ 。
(3)铝片减轻的质量是 ▲ g(小数部分保留两位有效数字)。
(4)设 NA为阿伏加德罗常数的数值,则每个电子所带的电量是 ▲ C(库仑)。
高一化学学科 试题 第 4页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
23.工业上氨气经过一系列反应制得硝酸。流程如图所示:
(1)NO2气体的颜色 ▲ ,浓 HNO3见光或加热易分解为 ▲ 和 H2O。
(2)NH3发生催化氧化生成 NO的反应方程式为 ▲ 。
(3)尾气中含有氮氧化物 NO、NO2,可用 NaOH溶液吸收,发生的反应有:
2NaOH+2NO2=NaNO3+NaNO2+H2O,
NaOH+NO+NO2= ▲ +H2O(只填化学式,无需配平) 。
(4)用不同浓度的 NaOH溶液吸收 NO2含量不同的尾气,测得氮氧化物吸收率与 NaOH 溶液浓度
的关系如图所示:
依据测得的关系图,下列措施一定能提高氮氧化物吸收率的是 ▲ (填序号)。
A.增大 NaOH溶液的浓度 B.提高尾气中 NO2的含量
C.在 NaOH 溶液加入 H2O2 D.用热的 NaOH溶液吸收
高一化学学科 试题 第 5页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
24.某化学兴趣小组设计了如下实验流程,用该工厂的废金属屑(主要成分为 Cu、Fe 和 Al,少量
Al2O3和 Fe2O3)制取氯化铝(AlCl3)、绿矾晶体(FeSO4·7H2O)和胆矾晶体(CuSO4·5H2O)。
请回答:
(1)试剂 X的名称 ▲ ,溶液 D中主要溶质的化学式是 ▲ 。
(2)固体 C溶于 NaOH溶液的化学方程式为 ▲ 。
(3)溶液 E经过蒸发浓缩、冷却结晶、 ▲ 、洗涤、干燥等系列操作制得绿矾晶体。
(4)实验兴趣小组利用以下流程制取消毒净水两用剂 Na2FeO4,
写出上述流程中发生的离子方程式 ▲ 。
25.利用催化技术可将汽车尾气中的 CO和 NO转化为 CO2和 N2,
反应的化学方程式为:2NO+2CO 2CO2+N2。
某温度下,在 2L容积不变的密闭容器中通入 CO和 NO,测得不同时间 CO的物质的量如下:
时间/s 0 1 2 3 …
n(CO)/mol 3.60 3.05 2.85 2.75 …
(1)比较下列时间段平均反应速率最快的是 ▲ 。
A.0→1s B. 1s→2s C.2s→3s
(2)在 2s时,容器中的 CO2物质的量为 ▲ mol。
(3)用 N2的浓度变化表示 0~3s的平均反应速率为 ▲ mol L-1 s-1(保留 3位有效数字)。
高一化学学科 试题 第 6页(共 6 页)
{#{QQABSYSxwwC4gEQACJaaBUlsC0gQsIMSLYouAQCeKERLgQFABAA=}#}
2024学年第二学期浙江“七彩阳光”新高考研究联盟期中联考
高一年级化学学科评分标准及参考答案
一、选择题(本大题共 20小题,每小题 3分,共 60分。每小题列出的四个备选项中只有一个是符
合题目要求的,不选、多选、错选均不得分)
1 2 3 4 5 6 7 8 9 10
C C C B B D D A D D
11 12 13 14 15 16 17 18 19 20
C B C D D B C B D B
二、非选择题部分(本大题共 5小题,共 40分)
21.(6分)
(1)(2分)丙烷 ;
(2)(2分)取代反应 (只写“取代”也给分) ;
(3)(2分)可逆反应(给 1分) CO不能完全转化(给 1分) (只写“反应存在限度”或“达到
平衡状态”均给 2分) 。
22.(8分)
(1)(2分)铜片 ;
(2)(2分)2Al+3Cu2+=2Al3++3Cu (写化学方程式、离子方程式均给分) ;
(3)(2分)0.28a (用分数“9a/32”表示也给分);
(4)(2分)32It/aNA (写“64It/2aNA”不扣分,“M(Cu)It/2aNA”只给 1分)。
23.(10分)
(1)(2分)红棕色; (2分)NO2 O2 (每个 1分,多写只看前两个)
(2)(2分)4NH3+5O2=4NO+6H2O (化学式正确未配平给 1分,反应条件不写不扣分?)
(3)(2分)NaNO2
(4)(2分)BC (选对 1个给 1分,错选、多选、不选不给分)
24.(10分)
(1)(2分)硫酸 (写“稀硫酸”给 2分,写“浓硫酸”不给分,写化学式不给分);
(2分)NaHCO3 (写名称或俗称的不给分);
(2)(2分)Al(OH)3+NaOH=Na[Al(OH)4]
(化学式正确未配平给 1分,写“Al(OH)3+NaOH=NaAlO2+2H2O”的也给 2分)
(3)(2分)过滤
(4)(2分)2Fe(OH)3+3ClO-+4OH-=2FeO24 +3Cl-+5H2O (化学式正确未配平给 1分,写化学方程
式的不给分)
25.(6分)
(1)(2分)A (只选一个,错选、多选、不选不给分)
(2)(2分)0.75 (复写单位不扣分)
(3)(2分)0.0708 (有效数字保留不正确扣 1分,复写单位不扣分)
高一化学学科 评分标准及参考答案 第 1 页 共 1 页
{#{QQABbQaEggAIAAJAABhCEwVSCAOQkBCAAQoOQAAQMAAAAAFABCA=}#}
同课章节目录
