山东省枣庄市2023-2024学年高二下学期7月期末教学质量检测化学试卷(含答案)
文档属性
| 名称 | 山东省枣庄市2023-2024学年高二下学期7月期末教学质量检测化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-13 00:00:00 | ||
图片预览


文档简介
山东省枣庄市2023-2024学年高二下学期7月期末考试化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学品在日常生产生活中有着重要的应用,下列说法错误的是
A.五氧化二磷用作食品干燥剂 B.二氧化硫用作葡萄酒的添加剂
C.新制的氢氧化铜悬浊液用于尿糖的检验 D.活性炭用于室内装修污染气体甲醛的去除
2.晶体是材料科学研究中非常重要的材料类型,下列说法错误的是
A.金属晶体中含有离子,但不存在离子键 B.共价晶体中共价键越强,晶体的熔点越高
C.分子晶体中分子间作用力越大,该物质越稳定 D.离子晶体中一定存在离子键,可能存在共价键
3.某烃能与完全加成,产物上的氢原子最多能被取代,则该烃可能为
A.丙烷 B.2-丁烯 C.1,3-丁二烯 D.丙炔
4.下列分子中,所有原子都满足最外层8电子稳定结构的是
A.六氟化硫 B.五氯化磷 C.三氯化硼 D.二氯化二硫
5.绿原酸是咖啡的热水提取液成分之一,结构简式如图所示:
下列关于绿原酸说法正确的是
A.分子式为 B.分子存在3个手性碳原子
C.与溶液反应产生紫色沉淀 D.绿原酸与足量溴水反应,最多消耗
6.花炮以土硝、硫黄和炭为主要药剂,采用传统手工技艺制成。下列说法正确的是
A.中含有个键
B.土硝中阴离子的空间结构与分子相同
C.钠的焰色试验呈黄色是因为电子由低能级跃迁至高能级
D.金刚石、石墨、互为同素异形体且化学性质和晶体类型都相同
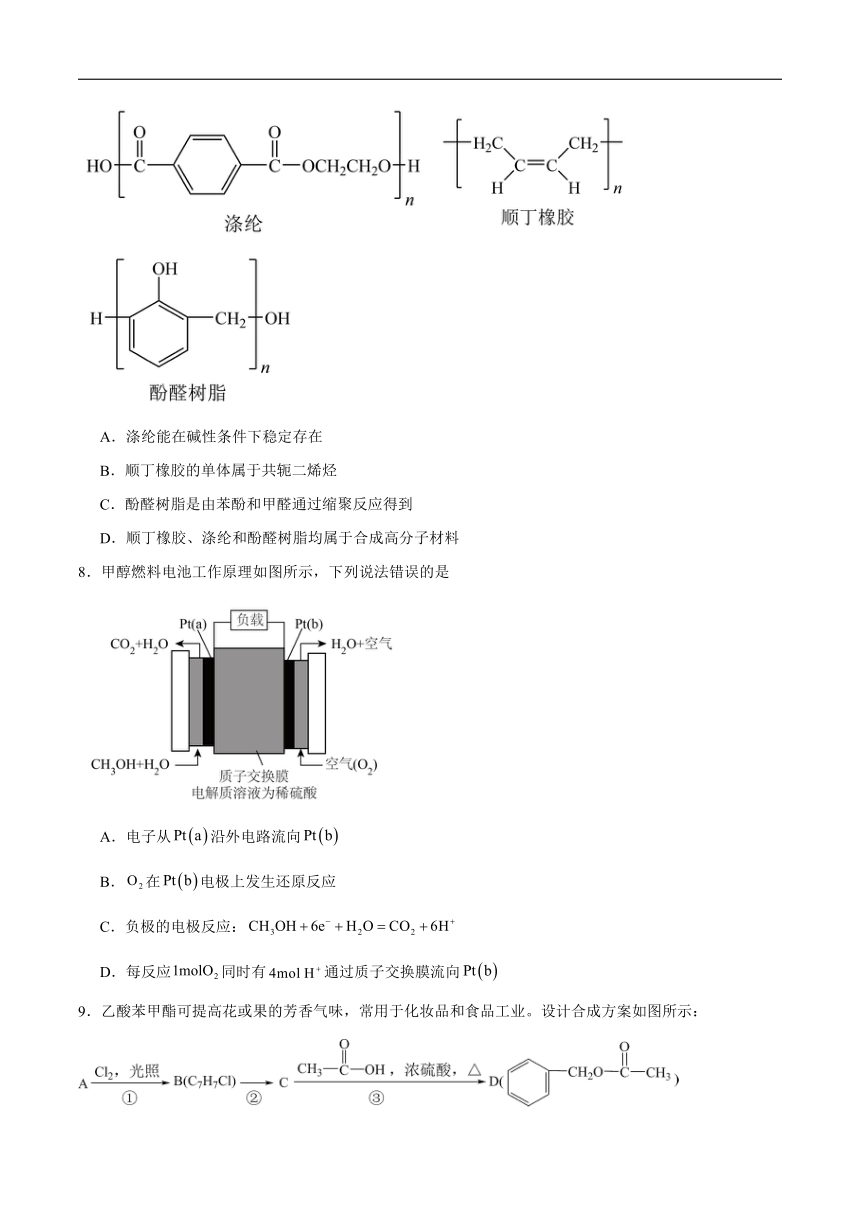
7.关于下列三种常见高分子材料说法错误的是
A.涤纶能在碱性条件下稳定存在
B.顺丁橡胶的单体属于共轭二烯烃
C.酚醛树脂是由苯酚和甲醛通过缩聚反应得到
D.顺丁橡胶、涤纶和酚醛树脂均属于合成高分子材料
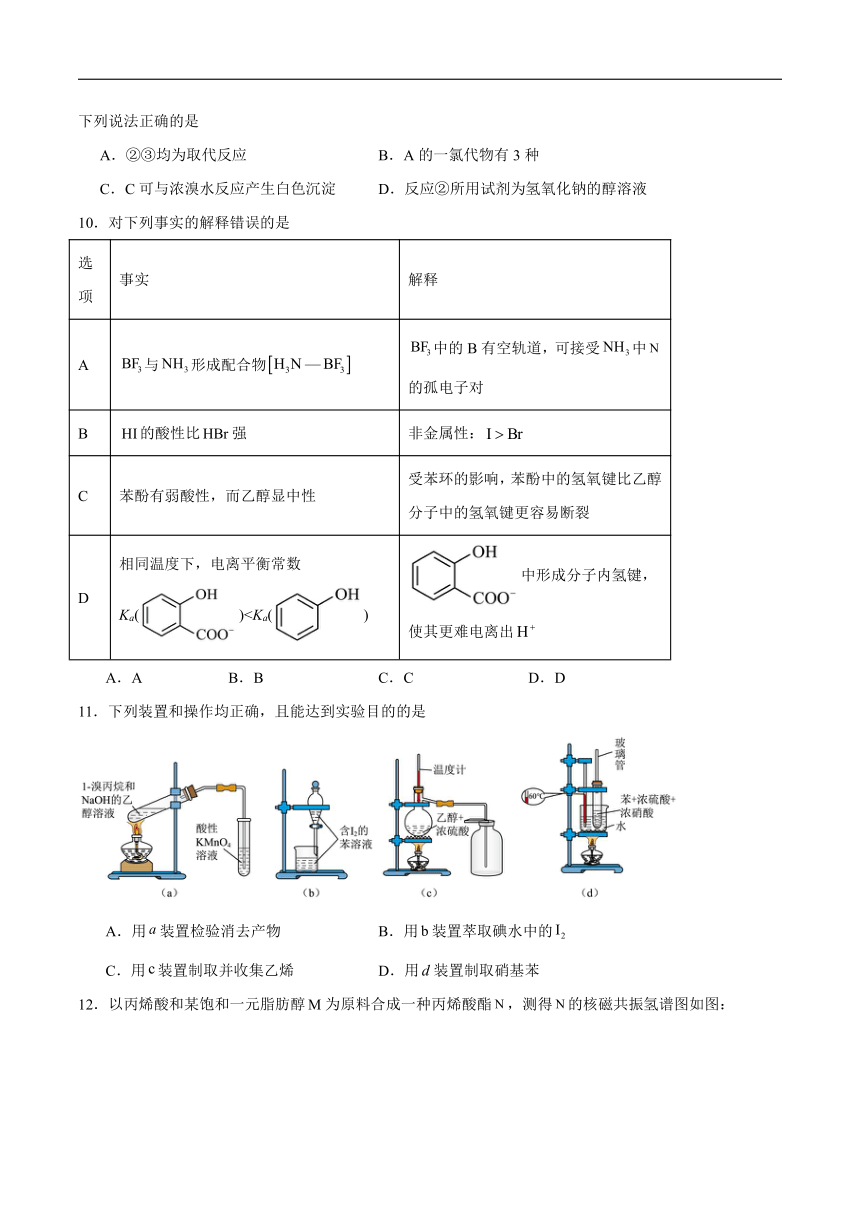
8.甲醇燃料电池工作原理如图所示,下列说法错误的是
A.电子从沿外电路流向
B.在电极上发生还原反应
C.负极的电极反应:
D.每反应同时有通过质子交换膜流向
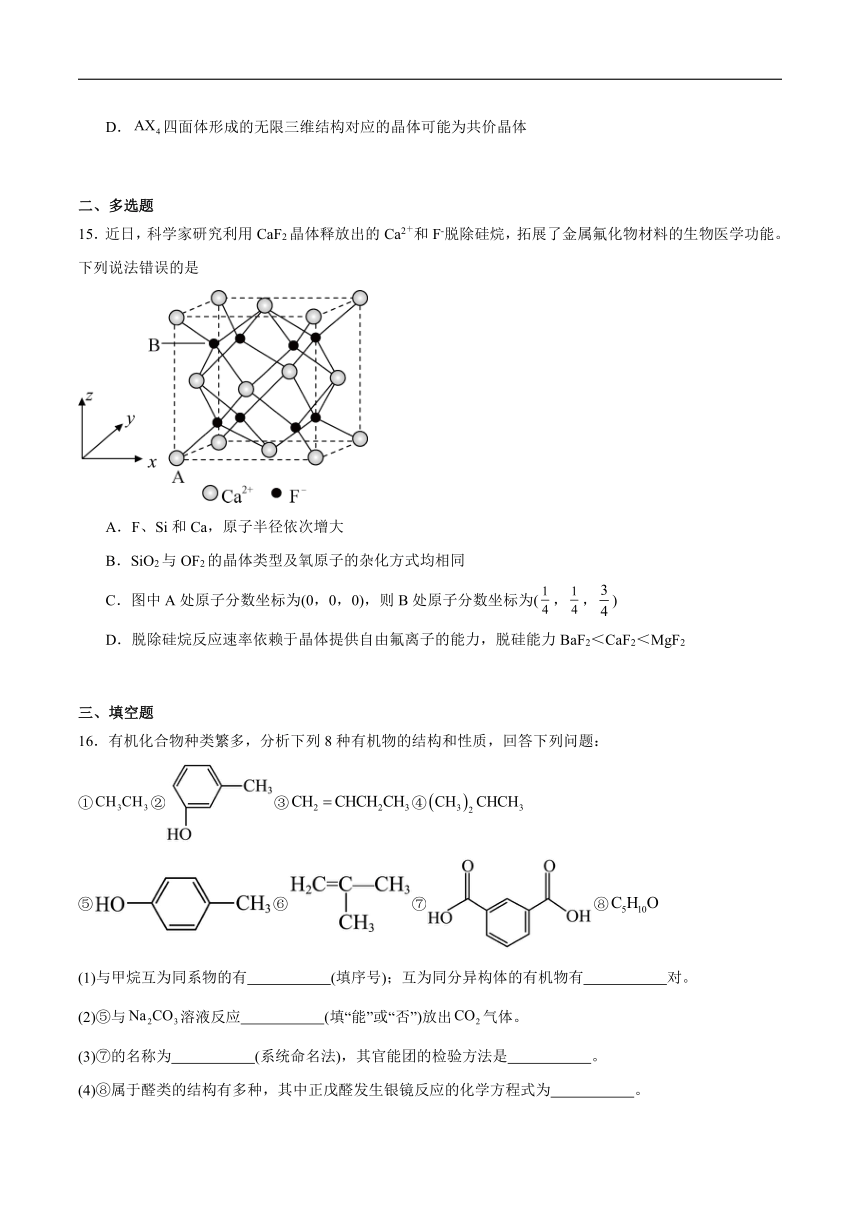
9.乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品和食品工业。设计合成方案如图所示:
下列说法正确的是
A.②③均为取代反应 B.A的一氯代物有3种
C.C可与浓溴水反应产生白色沉淀 D.反应②所用试剂为氢氧化钠的醇溶液
10.对下列事实的解释错误的是
选项 事实 解释
A 与形成配合物 中的B有空轨道,可接受中的孤电子对
B 的酸性比强 非金属性:
C 苯酚有弱酸性,而乙醇显中性 受苯环的影响,苯酚中的氢氧键比乙醇分子中的氢氧键更容易断裂
D 相同温度下,电离平衡常数Ka()A.A B.B C.C D.D
11.下列装置和操作均正确,且能达到实验目的的是
A.用装置检验消去产物 B.用装置萃取碘水中的
C.用装置制取并收集乙烯 D.用装置制取硝基苯
12.以丙烯酸和某饱和一元脂肪醇为原料合成一种丙烯酸酯,测得的核磁共振氢谱图如图:
下列说法正确的是
A.丙烯酸分子存在顺反异构 B.的沸点比乙醚的高
C.和丁醚互为同分异构体 D.发生消去反应的有机产物可能有两种
13.某饲料添加剂结构如图,均为前四周期元素且原子序数递增。处于同一周期,基态原子各能级电子数相同,基态原子价电子排布式为。下列说法正确的是
A.元素位于周期表的区 B.两种微粒的质子数相同
C.简单气态氢化物的稳定性: D.同周期基态原子第一电离能大于的元素有2种
14.四面体()在无机化合物中很常见。按图所示方式相连,可形成一系列“超四面体”(、…),下列说法正确的是
A.超四面体系列的各物质最简式相同
B.每个面都是正三角形,键角为
C.、、等硅的化合物均可形成超四面体系列
D.四面体形成的无限三维结构对应的晶体可能为共价晶体
二、多选题
15.近日,科学家研究利用CaF2晶体释放出的Ca2+和F-脱除硅烷,拓展了金属氟化物材料的生物医学功能。下列说法错误的是
A.F、Si和Ca,原子半径依次增大
B.SiO2与OF2的晶体类型及氧原子的杂化方式均相同
C.图中A处原子分数坐标为(0,0,0),则B处原子分数坐标为(,,)
D.脱除硅烷反应速率依赖于晶体提供自由氟离子的能力,脱硅能力BaF2<CaF2<MgF2
三、填空题
16.有机化合物种类繁多,分析下列8种有机物的结构和性质,回答下列问题:
①②③④
⑤⑥⑦⑧
(1)与甲烷互为同系物的有 (填序号);互为同分异构体的有机物有 对。
(2)⑤与溶液反应 (填“能”或“否”)放出气体。
(3)⑦的名称为 (系统命名法),其官能团的检验方法是 。
(4)⑧属于醛类的结构有多种,其中正戊醛发生银镜反应的化学方程式为 。
17.硼族元素可形成多种结构和性质特殊的化合物,回答下列问题:
(1)硼酸为一元酸,与足量的氢氧化钠溶液反应得到,反应的离子方程式为 ,的空间构型为 ;硼酸和甲醇反应制得硼酸三甲酯,沸点: (填“”或“”或“”),原因是 。
(2)过硼酸钠被用于洗衣粉中作增白剂,其阴离子结构如图所示,该阴离子组成元素中电负性由大到小的顺序为 ,硼原子的杂化方式为 ,该物质可用于增白的原因是 。
(3)科学家利用和过量碳在高温条件下合成出一种坚硬物质,结构如图所示,该物质的化学式为 ,晶胞参数:(单位),。若为阿伏加 德罗常数的值,则该晶体的密度为 。
四、解答题
18.锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是,含少量等杂质)为原料采用多种方法,最终电解溶液冶炼锌,流程如图所示。
已知:①是两性氢氧化物,易溶于溶液,也溶于氨水。发生反应:
②常温下,几种金属离子转化成氢氧化物沉淀的见表:
金属离子 开始沉淀的 完全沉淀的
6.5 9.7
5.4 8.0
2.3 4.1
回答下列问题:
(1)中采用杂化,则有 种结构;中的键角 (填“大于”“小于”或“等于”)中的键角。
(2)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入,除生成外,还能回收非金属单质。参与反应的离子方程为 。“氧压酸浸”中增大化学反应速率的措施有 (填一条即可)。
(3)“氧化,调”中调节的范围为 ;加入试剂宜选用 (填标号)。
A.氨水B.氢氧化钠溶液C.氧化锌D.硫酸溶液
(4)“电解沉积”中锌在 极生成(填“阴”或“阳”)。
19.某化学兴趣小组设计图甲装置制备苯甲酸异丙酯,其反应原理如下:
物质的性质数据如下表所示:
物质 相对分子质量 密度 沸点 水溶性
苯甲酸 122 1.27 249 微溶
异丙醇 60 0.79 82 易溶
苯甲酸异丙酯 164 1.08 218 不溶
实验步骤:
步骤ⅰ、在图甲干燥的仪器中加入苯甲酸、异丙醇和浓硫酸,再加入几粒沸石;
步骤ⅱ、加热至左右保持恒温半小时;
步骤ⅲ、将图甲的仪器中的液体混合物进行如下操作得到粗产品:
步骤ⅳ。将粗产品用图乙所示装置进行精制。回答下列问题:
(1)仪器的名称为 ;仪器的容积为 (填标号)。
A.
(2)步骤ⅰ中加入过量异丙醇的目的是 。
(3)步骤ⅱ中可采用的加热方式为 ,判断实验完成的现象为 。
(4)步骤ⅲ操作Ⅰ中③水洗是为了除去 (填化学式)。
(5)步骤ⅳ操作时应收集的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为 (填名称);若得到苯甲酸异丙酯,则该实验中苯甲酸异丙酯的产率为 (保留3位有效数字)。
20.链状烃A是一种有机化工原料,由A制备D和P的合成路线如图所示(部分条件略去):
已知:
①②
回答下列问题:
(1)A的结构简式是 ;B中官能团名称是 。
(2)的化学方程式为 ,反应类型为 。
(3)B的同分异构体中,满足①分子中含有一个羧基②能使溴的四氯化碳溶液褪色③三种不同化学环境的氢原子个数比为三个条件的是 (填结构简式)。
(4)等物质的量的P分别与足量反应,则消耗三者的物质的量之比为 。
(5)根据题目信息,以1,3-丁二烯为原料制备乙基环己烷的合成路线为 (无机试剂任选)。
山东省枣庄市2023-2024学年高二下学期7月期末考试化学试题参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 A C C D D B A C A B
题号 11 12 13 14 15
答案 D B C D BD
16.(1) ①④ 2
(2)否
(3) 1,3-苯二甲酸 取少量该物质于试管中,滴入碳酸氢钠溶液,若有气泡生成,则证明含有羧基(合理即可)
(4)
17.(1) 正四面体形 < 二者均为分子晶体,硼酸能形成分子间氢键,硼酸三甲酯不能形成分子间氢键
(2) O>B>H sp3 过硼酸根中含有过氧键,具有强氧化性,具有漂白性
(3) B4C
18.(1) 1 小于
(2) 搅拌、适当升温、适当增加酸的浓度等
(3) C
(4)阴极
19.(1) 蒸馏烧瓶 B
(2)使酯化反应正反应方向进行,提高苯甲酸的转化率
(3) 水浴加热 油水分离器中水面保持稳定(或油水分离器中水层高度保持不变)
(4)Na2CO3
(5) 苯甲酸 87.8
20.(1) CH2=CHCH3 碳碳双键、酯基
(2) 加成反应
(3)(CH3)2C=CHCOOH
(4)2∶1∶1
(5)
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.化学品在日常生产生活中有着重要的应用,下列说法错误的是
A.五氧化二磷用作食品干燥剂 B.二氧化硫用作葡萄酒的添加剂
C.新制的氢氧化铜悬浊液用于尿糖的检验 D.活性炭用于室内装修污染气体甲醛的去除
2.晶体是材料科学研究中非常重要的材料类型,下列说法错误的是
A.金属晶体中含有离子,但不存在离子键 B.共价晶体中共价键越强,晶体的熔点越高
C.分子晶体中分子间作用力越大,该物质越稳定 D.离子晶体中一定存在离子键,可能存在共价键
3.某烃能与完全加成,产物上的氢原子最多能被取代,则该烃可能为
A.丙烷 B.2-丁烯 C.1,3-丁二烯 D.丙炔
4.下列分子中,所有原子都满足最外层8电子稳定结构的是
A.六氟化硫 B.五氯化磷 C.三氯化硼 D.二氯化二硫
5.绿原酸是咖啡的热水提取液成分之一,结构简式如图所示:
下列关于绿原酸说法正确的是
A.分子式为 B.分子存在3个手性碳原子
C.与溶液反应产生紫色沉淀 D.绿原酸与足量溴水反应,最多消耗
6.花炮以土硝、硫黄和炭为主要药剂,采用传统手工技艺制成。下列说法正确的是
A.中含有个键
B.土硝中阴离子的空间结构与分子相同
C.钠的焰色试验呈黄色是因为电子由低能级跃迁至高能级
D.金刚石、石墨、互为同素异形体且化学性质和晶体类型都相同
7.关于下列三种常见高分子材料说法错误的是
A.涤纶能在碱性条件下稳定存在
B.顺丁橡胶的单体属于共轭二烯烃
C.酚醛树脂是由苯酚和甲醛通过缩聚反应得到
D.顺丁橡胶、涤纶和酚醛树脂均属于合成高分子材料
8.甲醇燃料电池工作原理如图所示,下列说法错误的是
A.电子从沿外电路流向
B.在电极上发生还原反应
C.负极的电极反应:
D.每反应同时有通过质子交换膜流向
9.乙酸苯甲酯可提高花或果的芳香气味,常用于化妆品和食品工业。设计合成方案如图所示:
下列说法正确的是
A.②③均为取代反应 B.A的一氯代物有3种
C.C可与浓溴水反应产生白色沉淀 D.反应②所用试剂为氢氧化钠的醇溶液
10.对下列事实的解释错误的是
选项 事实 解释
A 与形成配合物 中的B有空轨道,可接受中的孤电子对
B 的酸性比强 非金属性:
C 苯酚有弱酸性,而乙醇显中性 受苯环的影响,苯酚中的氢氧键比乙醇分子中的氢氧键更容易断裂
D 相同温度下,电离平衡常数Ka()
11.下列装置和操作均正确,且能达到实验目的的是
A.用装置检验消去产物 B.用装置萃取碘水中的
C.用装置制取并收集乙烯 D.用装置制取硝基苯
12.以丙烯酸和某饱和一元脂肪醇为原料合成一种丙烯酸酯,测得的核磁共振氢谱图如图:
下列说法正确的是
A.丙烯酸分子存在顺反异构 B.的沸点比乙醚的高
C.和丁醚互为同分异构体 D.发生消去反应的有机产物可能有两种
13.某饲料添加剂结构如图,均为前四周期元素且原子序数递增。处于同一周期,基态原子各能级电子数相同,基态原子价电子排布式为。下列说法正确的是
A.元素位于周期表的区 B.两种微粒的质子数相同
C.简单气态氢化物的稳定性: D.同周期基态原子第一电离能大于的元素有2种
14.四面体()在无机化合物中很常见。按图所示方式相连,可形成一系列“超四面体”(、…),下列说法正确的是
A.超四面体系列的各物质最简式相同
B.每个面都是正三角形,键角为
C.、、等硅的化合物均可形成超四面体系列
D.四面体形成的无限三维结构对应的晶体可能为共价晶体
二、多选题
15.近日,科学家研究利用CaF2晶体释放出的Ca2+和F-脱除硅烷,拓展了金属氟化物材料的生物医学功能。下列说法错误的是
A.F、Si和Ca,原子半径依次增大
B.SiO2与OF2的晶体类型及氧原子的杂化方式均相同
C.图中A处原子分数坐标为(0,0,0),则B处原子分数坐标为(,,)
D.脱除硅烷反应速率依赖于晶体提供自由氟离子的能力,脱硅能力BaF2<CaF2<MgF2
三、填空题
16.有机化合物种类繁多,分析下列8种有机物的结构和性质,回答下列问题:
①②③④
⑤⑥⑦⑧
(1)与甲烷互为同系物的有 (填序号);互为同分异构体的有机物有 对。
(2)⑤与溶液反应 (填“能”或“否”)放出气体。
(3)⑦的名称为 (系统命名法),其官能团的检验方法是 。
(4)⑧属于醛类的结构有多种,其中正戊醛发生银镜反应的化学方程式为 。
17.硼族元素可形成多种结构和性质特殊的化合物,回答下列问题:
(1)硼酸为一元酸,与足量的氢氧化钠溶液反应得到,反应的离子方程式为 ,的空间构型为 ;硼酸和甲醇反应制得硼酸三甲酯,沸点: (填“”或“”或“”),原因是 。
(2)过硼酸钠被用于洗衣粉中作增白剂,其阴离子结构如图所示,该阴离子组成元素中电负性由大到小的顺序为 ,硼原子的杂化方式为 ,该物质可用于增白的原因是 。
(3)科学家利用和过量碳在高温条件下合成出一种坚硬物质,结构如图所示,该物质的化学式为 ,晶胞参数:(单位),。若为阿伏加 德罗常数的值,则该晶体的密度为 。
四、解答题
18.锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是,含少量等杂质)为原料采用多种方法,最终电解溶液冶炼锌,流程如图所示。
已知:①是两性氢氧化物,易溶于溶液,也溶于氨水。发生反应:
②常温下,几种金属离子转化成氢氧化物沉淀的见表:
金属离子 开始沉淀的 完全沉淀的
6.5 9.7
5.4 8.0
2.3 4.1
回答下列问题:
(1)中采用杂化,则有 种结构;中的键角 (填“大于”“小于”或“等于”)中的键角。
(2)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入,除生成外,还能回收非金属单质。参与反应的离子方程为 。“氧压酸浸”中增大化学反应速率的措施有 (填一条即可)。
(3)“氧化,调”中调节的范围为 ;加入试剂宜选用 (填标号)。
A.氨水B.氢氧化钠溶液C.氧化锌D.硫酸溶液
(4)“电解沉积”中锌在 极生成(填“阴”或“阳”)。
19.某化学兴趣小组设计图甲装置制备苯甲酸异丙酯,其反应原理如下:
物质的性质数据如下表所示:
物质 相对分子质量 密度 沸点 水溶性
苯甲酸 122 1.27 249 微溶
异丙醇 60 0.79 82 易溶
苯甲酸异丙酯 164 1.08 218 不溶
实验步骤:
步骤ⅰ、在图甲干燥的仪器中加入苯甲酸、异丙醇和浓硫酸,再加入几粒沸石;
步骤ⅱ、加热至左右保持恒温半小时;
步骤ⅲ、将图甲的仪器中的液体混合物进行如下操作得到粗产品:
步骤ⅳ。将粗产品用图乙所示装置进行精制。回答下列问题:
(1)仪器的名称为 ;仪器的容积为 (填标号)。
A.
(2)步骤ⅰ中加入过量异丙醇的目的是 。
(3)步骤ⅱ中可采用的加热方式为 ,判断实验完成的现象为 。
(4)步骤ⅲ操作Ⅰ中③水洗是为了除去 (填化学式)。
(5)步骤ⅳ操作时应收集的馏分,如果温度计水银球位置偏上,则收集的精制产品中可能混有的杂质为 (填名称);若得到苯甲酸异丙酯,则该实验中苯甲酸异丙酯的产率为 (保留3位有效数字)。
20.链状烃A是一种有机化工原料,由A制备D和P的合成路线如图所示(部分条件略去):
已知:
①②
回答下列问题:
(1)A的结构简式是 ;B中官能团名称是 。
(2)的化学方程式为 ,反应类型为 。
(3)B的同分异构体中,满足①分子中含有一个羧基②能使溴的四氯化碳溶液褪色③三种不同化学环境的氢原子个数比为三个条件的是 (填结构简式)。
(4)等物质的量的P分别与足量反应,则消耗三者的物质的量之比为 。
(5)根据题目信息,以1,3-丁二烯为原料制备乙基环己烷的合成路线为 (无机试剂任选)。
山东省枣庄市2023-2024学年高二下学期7月期末考试化学试题参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 A C C D D B A C A B
题号 11 12 13 14 15
答案 D B C D BD
16.(1) ①④ 2
(2)否
(3) 1,3-苯二甲酸 取少量该物质于试管中,滴入碳酸氢钠溶液,若有气泡生成,则证明含有羧基(合理即可)
(4)
17.(1) 正四面体形 < 二者均为分子晶体,硼酸能形成分子间氢键,硼酸三甲酯不能形成分子间氢键
(2) O>B>H sp3 过硼酸根中含有过氧键,具有强氧化性,具有漂白性
(3) B4C
18.(1) 1 小于
(2) 搅拌、适当升温、适当增加酸的浓度等
(3) C
(4)阴极
19.(1) 蒸馏烧瓶 B
(2)使酯化反应正反应方向进行,提高苯甲酸的转化率
(3) 水浴加热 油水分离器中水面保持稳定(或油水分离器中水层高度保持不变)
(4)Na2CO3
(5) 苯甲酸 87.8
20.(1) CH2=CHCH3 碳碳双键、酯基
(2) 加成反应
(3)(CH3)2C=CHCOOH
(4)2∶1∶1
(5)
同课章节目录
