2026届高考化学一轮复习 第3章 物质及其变化 第1节 物质的分类及转化 课件(44张PPT)
文档属性
| 名称 | 2026届高考化学一轮复习 第3章 物质及其变化 第1节 物质的分类及转化 课件(44张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-15 00:00:00 | ||
图片预览










文档简介
(共44张PPT)
第1节 物质的分类及转化
第3章
课标要求
1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类;能依据物质类别和元素价态列举某种元素的典型代表物。
2.认识同类物质具有相似的性质,一定条件下各类物质可以相互转化。
3.认识胶体是一种常见的分散系。能举例说明胶体的典型特征。
备考指导
高考中本节的考点主要有两个:一是以生产、生活、社会、科技中的物质为载体或以传统文化、古籍中的描述等为素材,考查物质的组成、分类、性质、用途及变化;二是以重要的新闻背景、新科技产品为题材考查胶体的性质、制备及应用。
内容索引
01
02
03
第一环节 必备知识落实
第二环节 关键能力形成
第三环节 核心素养提升
第一环节 必备知识落实
知识点1
物质的组成与分类
知识筛查
1.元素、物质及粒子间的关系
(1)构成物质的微观粒子。
①原子:原子是化学变化中的最小粒子。原子是由原子核和核外电子构成的,原子核又是由质子和中子构成的(1H除外)。
②分子:分子是保持物质化学性质的最小粒子。一般分子由原子通过共价键构成,但稀有气体是单原子分子。
③离子:离子是带电荷的原子或原子团。离子有阳离子和阴离子之分。
(2)元素与物质的组成。
①宏观上物质是由元素组成的。
②元素在物质中的存在形态。
游离态:元素以单质形式存在的状态。
化合态:元素以化合物形式存在的状态。
③同素异形体。
定义:同种元素形成的性质不同的单质叫同素异形体。
性质差异:物理性质差别较大,一般情况下同素异形体之间的转化属于化学变化。
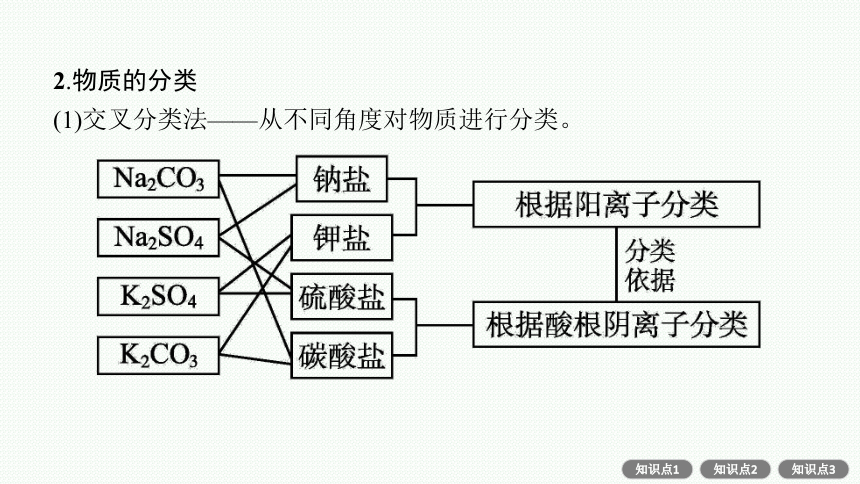
2.物质的分类
(1)交叉分类法——从不同角度对物质进行分类。
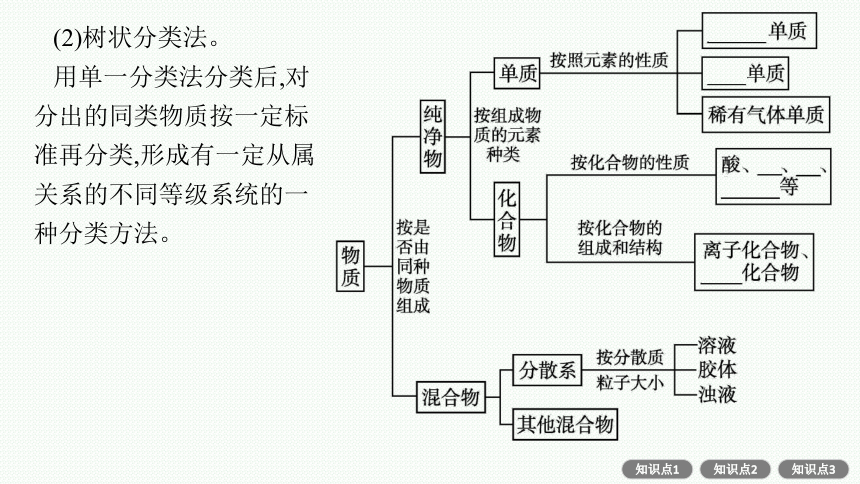
(2)树状分类法。
用单一分类法分类后,对分出的同类物质按一定标准再分类,形成有一定从属关系的不同等级系统的一种分类方法。
知识巩固
1.判断正误,正确的画“√”,错误的画“×”。
(1)非金属氧化物一定是酸性氧化物。( )
(2)酸性氧化物不一定是非金属氧化物。( )
(3)金属氧化物一定是碱性氧化物。( )
(4)碱性氧化物一定是金属氧化物。( )
(5)Na2O和Na2O2均能与H2O反应生成NaOH,故两者都是碱性氧化物。( )
(6)同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子。( )
×
√
×
√
×
√
(7)能与碱反应生成盐和水的氧化物一定是酸性氧化物。( )
(8)由同一种元素组成的物质一定是同一种物质。( )
(9)HCOOH分子中含有两个氢原子,所以是二元酸。( )
(10)盐一定由金属离子和酸根离子构成。( )
×
×
×
×
2.(2024新课标卷)文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是( )。
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸钙
解析:羊毛的主要成分为蛋白质,可用于制毛笔,A项正确;松木可用于制墨,墨的主要成分是单质碳,B项正确;竹子的主要成分为纤维素,竹子可用于造纸,故纸的主要成分是纤维素,C项正确;大理石的主要成分是CaCO3,D项错误。
D
知识点2
物质的性质与变化
知识筛查
1.物理变化与化学变化
(1)宏观角度。
物理变化没有新物质生成,化学变化有新物质生成。
(2)微观角度。
化学变化过程中同时伴随着旧化学键的断裂和新化学键的形成。只有旧化学键断裂而没有新化学键形成的过程不是化学变化,如NaCl晶体的熔化。
(3)两者关系。
化学变化中一定伴随着物理变化,物理变化过程中一定没有化学变化。
(4)物质变化与性质的关系。
①图示。
②应用下列用途体现物质
物理性质的是ae;体现物质
化学性质的是bcd。
a.用铝箔包装物品
b.NaHCO3作为食品工业的膨松剂
c.浓氨水检验输送氯气的管道是否泄漏
d.SO2漂白纸浆
e.液态丙烷作制冷剂
2.化学反应的分类
知识巩固
1.判断正误,正确的画“√”,错误的画“×”。
(1)臭氧变成氧气是物理变化。( )
(2)将蓝色的硫酸铜晶体放入浓硫酸中只发生物理变化。( )
(3)发光发热的变化都是化学变化。( )
(4)煤的气化、液化、干馏都是物理变化。( )
(5)分馏、蒸馏、蒸发、萃取、分液、过滤都是物理变化。( )
(6)加热I2或NH4Cl晶体,固体从试管底部跑到上部均属于物理变化。( )
×
×
×
×
√
×
(7)向蛋白质溶液中滴加CuSO4溶液或Na2SO4溶液产生沉淀均属于化学变化。( )
(8)向紫色石蕊溶液中加入活性炭后,溶液褪色,发生的是化学变化。( )
(9)用铂丝蘸取NaCl溶液进行焰色试验是化学变化。( )
(10)核裂变、核聚变均有新物质生成,均属于化学变化。( )
×
×
×
×
2.(2024吉林卷)家务劳动中蕴含着丰富的化学知识。下列相关解释错误的是( )。
A.用过氧碳酸钠漂白衣物:Na2CO4具有较强氧化性
B.酿米酒需晾凉米饭后加酒曲:乙醇受热易挥发
C.用柠檬酸去除水垢:柠檬酸酸性强于碳酸
D.用碱液清洗厨房油污:油脂可碱性水解
解析:过氧碳酸钠中的过氧键具有强氧化性,可用于漂白衣物,A项正确;酿米酒晾凉米饭是为了防止酒曲酶(主要成分为蛋白质)受热变性,变性后失去催化效果,B项错误;水垢的主要成分有CaCO3等,柠檬酸可以除去水垢说明柠檬酸的酸性比碳酸强,C项正确;油脂是高级脂肪酸甘油酯,在碱性条件下能够促进油脂的水解,去除油污效果更好,D项正确。
B
知识点3
分散系 胶体
知识筛查
1.分散系
(1)定义:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。
(2)分类。
2.胶体
(1)性质与应用。
(2)Fe(OH)3胶体的制备。(夹持装置省略)
向沸水中逐滴加入FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,即制得Fe(OH)3胶体,化学方程式为FeCl3+3H2O Fe(OH)3(胶体)+3HCl。
特别提醒(1)胶体中的胶粒带电荷,但胶体不带电荷,整个分散系仍呈电中性。
(2)区分胶体和其他分散系的方法是丁达尔效应,而胶体与其他分散系的本质区别是分散质粒子直径为1~100 nm。
(3)Fe(OH)3胶体粒子是“分子”的集合体,因此,Fe(OH)3胶体粒子的数目要远远小于原FeCl3溶液中Fe3+的数目。
知识巩固
判断正误,正确的画“√”,错误的画“×”。
(1)将NaOH浓溶液滴入FeCl3饱和溶液中,制备Fe(OH)3胶体。( )
(2)稀豆浆、硅酸、氯化铁溶液均为胶体。( )
(3)H+、K+、S2-、Br-能在Fe(OH)3胶体中大量共存。( )
(4)向沸水中逐滴加入FeCl3饱和溶液,可制得Fe(OH)3胶体。( )
(5)向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O Al(OH)3(胶体)+3H+。( )
(6)沸水中滴加适量FeCl3饱和溶液,形成带电荷的胶体,导电能力增强。( )
(7)葡萄糖注射液不能产生丁达尔效应,不属于胶体。( )
×
×
×
√
√
×
√
第二环节 关键能力形成
能力点1
根据一定的标准给物质分类的能力
整合建构
物质分类的3个“误区”
(1)误认为由相同元素组成的物质一定是纯净物。若某物质是由一种元素组成的单质混合而成,则属于混合物。如O2、O3组成的混合气体就是混合物,由12C和13C组成的石墨则是纯净物。
(2)误认为溶液呈酸性的物质一定是酸,溶液呈碱性的物质一定是碱。如NaHSO4、CuSO4、NH4Cl等物质的溶液呈酸性,但这些物质均属于盐。Na2CO3溶液、NaHCO3溶液呈碱性,Na2CO3、NaHCO3均属于盐。
(3)误认为能与酸反应生成盐和水的氧化物就是碱性氧化物,如Na2O2不属于碱性氧化物。
问题引领
(1)如何区别纯净物与混合物
(2)如何区别酸性氧化物与碱性氧化物
点拨(1)纯净物、混合物的判断方法。
常见混合物:①分散系(如溶液、胶体、浊液等);②高分子(如蛋白质、纤维素、聚合物、淀粉等);③常见特殊名称的混合物,如石油、石油的各种馏分、煤、漂白粉、碱石灰、福尔马林、油脂、天然气、水煤气、铝热剂、氨水、氯水、王水等。
(2)酸性氧化物和碱性氧化物。
①酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸或碱,如SiO2、Fe2O3。②能与酸反应生成盐和水的氧化物不一定是碱性氧化物,如Al2O3。③能与碱反应生成盐和水的氧化物不一定是酸性氧化物,如Al2O3。④碱性氧化物都是金属氧化物,但金属氧化物不一定都是碱性氧化物,如Mn2O7为酸性氧化物,Al2O3为两性氧化物,Na2O2为过氧化物。⑤酸性氧化物不一定是非金属氧化物,如Mn2O7;非金属氧化物也不一定是酸性氧化物,如CO、NO。
训练突破
1.下列各组物质的分类正确的是( )。
①混合物:液氯、氨水、水玻璃、福尔马林、聚乙烯 ②电解质:明矾、冰醋酸、石膏、纯碱 ③CO2、NO2、P2O5均为酸性氧化物 ④同位素: 1H+、2H2、3H ⑤同素异形体:C60、C80、金刚石、石墨 ⑥同系物: CH2O2、C2H4O2、C3H6O2、C4H8O2 ⑦化合物:CaCl2、NaOH、HCl、HD ⑧在熔化状态下能导电的化合物为离子化合物
A.②⑤⑧ B.①②⑤⑦⑧
C.②⑤⑥⑦⑧ D.①③④⑥⑦
A
解析:液氯属于纯净物,故①错误。明矾、冰醋酸、石膏、纯碱溶于水自身电离出阳离子与阴离子,属于电解质,故②正确。NO2不是酸性氧化物,故③错误。同位素研究的对象是原子,1H+是离子,2H2属于单质,故④错误。C60、C80、金刚石、石墨是碳元素组成的结构不同的单质,互为同素异形体,故⑤正确。C2H4O2、C3H6O2、C4H8O2存在同分异构体,结构不一定相似,CH2O2、C2H4O2、C3H6O2、C4H8O2不一定属于同系物,故⑥错误。HD是单质,故⑦错误。共价化合物在熔化状态下不导电,在熔化状态下能导电的化合物为离子化合物,故⑧正确。综上所述,A项正确。
2.下列说法正确的是( )。
A.水银、磁铁矿、淀粉、纤维素都是混合物
B.SiO2、Mn2O7为酸性氧化物,Na2O2、MgO为碱性氧化物
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
D
解析:水银是Hg,是纯净物,A项错误。Na2O2不是碱性氧化物,B项错误。Mg、Al、Cu可以分别用电解法、电解法和热还原法冶炼得到,C项错误。天然气属于化石能源,沼气为可再生能源,由植物秸秆等在沼气池中发酵得到,水煤气由碳与水蒸气反应得到,是二次能源,D项正确。
能力点2
运用胶体的特征分析、解释与胶体有关的问题的能力
整合建构
问题引领
溶液、胶体、浊液三种分散系的区别和联系是什么
点拨
分散系 溶液 胶体 浊液
分散质粒子直径 小于 1 nm 1~100 nm 大于 100 nm
分散质粒子 单个小分子或离子 高分子或多分子集合体 巨大数目的分子或离子集合体
性 质 外观 透明、均一 均一 不透明、不均一
稳定性 稳定 介于溶液与 浊液之间 不稳定
能否透过滤纸 能 能 不能
能否透过半透膜 能 不能 不能
鉴别 无丁达尔效应 有丁达尔效应 静置分层或沉淀
训练突破
下列叙述正确的是( )。
A.胶体区别于其他分散系的本质特征是胶体能产生丁达尔效应
B.浓硫酸具有吸水性,可以干燥NH3、SO2、CO2
C.Fe(OH)3胶体带正电荷
D.化合物分为酸、碱、盐和氧化物利用的是树状分类法
D
解析:胶体区别于其他分散系的本质特征是分散质粒子直径在1~100 nm之间,A项错误。NH3能与浓硫酸反应,浓硫酸不能干燥NH3,B项错误。Fe(OH)3胶体粒子带正电荷,Fe(OH)3胶体不带电荷,C项错误。利用树状分类法,可将化合物分为酸、碱、盐和氧化物,D项正确。
第三环节 核心素养提升
【高考真题剖析】
【例题】 (2023辽宁卷)科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是( )。
A.利用CO2合成了脂肪酸:实现了无机小分子向有机高分子的转变
B.发现了月壤中的“嫦娥石
[(Ca8Y)Fe(PO4)7]”:其成分属于无机盐
C.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
A
解析:脂肪酸分子不是有机高分子,A项错误;嫦娥石中无碳元素,为无机物,结构中含有 ,为无机盐,B项正确;太阳能电池将太阳能直接转化为电能,C项正确;聚四氟乙烯性质稳定,具有很好的耐腐蚀性,D项正确。
【核心素养考查点剖析】本题是一道有关化学与生产、科技的题目,较好地考查了考生“宏观辨识与微观探析”素养,考查考生能否“从不同层次认识物质的多样性,并对物质进行分类”;能否“从元素和原子、分子水平认识物质的组成、结构、性质和变化”;同时考查了考生的“科学态度与社会责任”,考查考生深刻认识化学对创造更多物质财富、满足人民日益增长的美好生活需要的重大贡献。
【典题训练】
1.(2022浙江卷)下列消毒剂的有效成分属于盐的是( )。
A.高锰酸钾溶液
B.过氧乙酸溶液
C.双氧水
D.医用酒精
解析:高锰酸钾溶液的有效成分是高锰酸钾,属于盐,A项符合题意;过氧乙酸溶液的有效成分是过氧乙酸,属于有机酸,B项不符合题意;双氧水的有效成分是过氧化氢,属于过氧化物,C项不符合题意;医用酒精的有效成分是乙醇,属于醇类,D项不符合题意。
A
2.下列说法正确的是( )。
A.MgO和Al2O3都属于两性氧化物
B.悬浊液和乳浊液的分散质均为液态
C.Fe3O4和Pb3O4中的金属都呈现两种价态
D.葡萄糖溶液和淀粉溶液都具有丁达尔效应
C
解析:MgO是碱性氧化物,A项错误。悬浊液的分散质是固体小颗粒,B项错误。Fe3O4可表示为FeO·Fe2O3,铁元素化合价为+2、+3价;Pb3O4可表示为2PbO·PbO2,铅元素化合价为+2、+4价,因此两种化合物中的金属都呈现两种价态,C项正确。葡萄糖溶液不具有丁达尔效应,D项错误。
3.(2023全国甲)化学与生活密切相关,下列说法正确的是( )。
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C.SO2可用于丝织品漂白是由于其能氧化丝织品中有色成分
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
B
解析:苯甲酸钠具有杀菌、抑菌作用,常用作食品防腐剂,且苯甲酸钠水解,其溶液显碱性,A项错误;豆浆中胶体粒子能对光线产生散射作用,从而产生丁达尔效应,B项正确;SO2能与某些有色物质化合为不稳定的无色物质,体现其漂白性,C项错误;维生素C具有强还原性,易与水果罐头中的氧气等氧化性物质反应,从而起到抗氧化的作用,D项错误。
4.(2023新课标卷)化学在文物的研究和修复中有重要作用。下列说法错误的是( )。
A.竹简的成分之一纤维素属于天然高分子
B.龟甲的成分之一羟基磷灰石属于无机物
C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)2
D.古壁画颜料中所用的铁红,其成分为Fe2O3
C
解析:竹简的成分之一纤维素的分子式为(C6H10O5)n,属于天然高分子化合物,A项正确;羟基磷灰石,又称碱式磷酸钙,属于无机盐,B项正确;熟石灰的成分是Ca(OH)2,而熟石膏的化学式为2CaSO4·H2O,C项错误;Fe2O3为红棕色,是红色颜料的成分,俗称铁红,D项正确。
5.(2024湖北卷)劳动人民的发明创造是中华优秀传统文化的组成部分。下列化学原理描述错误的是( )。
C
选项 发明 关键操作 化学原理
A 制墨 松木在窑内焖烧 发生不完全燃烧
B 陶瓷 黏土高温烧结 形成新的化学键
C 造纸 草木灰水浸泡树皮 促进纤维素溶解
D 火药 硫黄、硝石和木炭混合,点燃 发生氧化还原反应
解析:松木在窑内焖烧产生烟尘(发生不完全燃烧得到松烟),加胶和其他辅料再定型得到墨,A项正确;黏土高温烧结过程中发生一系列物理、化学变化形成陶瓷,化学变化的过程中有新的化学键形成,B项正确;草木灰的主要成分为碳酸钾,浸泡后的水溶液呈碱性,可用于分离树皮等原料中的胶质,纤维素不能在K2CO3溶液中发生水解反应,因此草木灰水浸泡树皮,并不能促进纤维素溶解,C项错误;硫黄、硝石和木炭混合点燃,发生反应: S+2KNO3+3C K2S+N2↑+3CO2↑,该反应为氧化还原反应,D项正确。
【新情境模拟训练】
某同学在实验室进行了如图所示的实验,下列说法中正确的是( )。
A.氯化铁溶液是电解质
B.Z中红褐色透明液体中
分散质不能透过滤纸
C.Y中反应的离子方程式为
3CaCO3+2Fe3++3H2O══
2Fe(OH)3(胶体)+3CO2↑+3Ca2+
D.X、Z中分散系都能产生丁达尔效应
C
解析:氯化铁溶液是混合物,是电解质溶液,不属于电解质,A项错误。Z中红褐色透明液体为胶体,其分散质能透过滤纸,B项错误。铁离子水解使溶液显酸性,Y中反应的离子方程式为3CaCO3+2Fe3++3H2O══2Fe(OH)3(胶体)+3CO2↑+3Ca2+,C项正确。Z中分散系是胶体,能产生丁达尔效应;X中分散系是溶液,不能产生丁达尔效应,D项错误。
第1节 物质的分类及转化
第3章
课标要求
1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类;能依据物质类别和元素价态列举某种元素的典型代表物。
2.认识同类物质具有相似的性质,一定条件下各类物质可以相互转化。
3.认识胶体是一种常见的分散系。能举例说明胶体的典型特征。
备考指导
高考中本节的考点主要有两个:一是以生产、生活、社会、科技中的物质为载体或以传统文化、古籍中的描述等为素材,考查物质的组成、分类、性质、用途及变化;二是以重要的新闻背景、新科技产品为题材考查胶体的性质、制备及应用。
内容索引
01
02
03
第一环节 必备知识落实
第二环节 关键能力形成
第三环节 核心素养提升
第一环节 必备知识落实
知识点1
物质的组成与分类
知识筛查
1.元素、物质及粒子间的关系
(1)构成物质的微观粒子。
①原子:原子是化学变化中的最小粒子。原子是由原子核和核外电子构成的,原子核又是由质子和中子构成的(1H除外)。
②分子:分子是保持物质化学性质的最小粒子。一般分子由原子通过共价键构成,但稀有气体是单原子分子。
③离子:离子是带电荷的原子或原子团。离子有阳离子和阴离子之分。
(2)元素与物质的组成。
①宏观上物质是由元素组成的。
②元素在物质中的存在形态。
游离态:元素以单质形式存在的状态。
化合态:元素以化合物形式存在的状态。
③同素异形体。
定义:同种元素形成的性质不同的单质叫同素异形体。
性质差异:物理性质差别较大,一般情况下同素异形体之间的转化属于化学变化。
2.物质的分类
(1)交叉分类法——从不同角度对物质进行分类。
(2)树状分类法。
用单一分类法分类后,对分出的同类物质按一定标准再分类,形成有一定从属关系的不同等级系统的一种分类方法。
知识巩固
1.判断正误,正确的画“√”,错误的画“×”。
(1)非金属氧化物一定是酸性氧化物。( )
(2)酸性氧化物不一定是非金属氧化物。( )
(3)金属氧化物一定是碱性氧化物。( )
(4)碱性氧化物一定是金属氧化物。( )
(5)Na2O和Na2O2均能与H2O反应生成NaOH,故两者都是碱性氧化物。( )
(6)同一种元素可能有多种不同原子,同一种原子也可能形成不同的离子。( )
×
√
×
√
×
√
(7)能与碱反应生成盐和水的氧化物一定是酸性氧化物。( )
(8)由同一种元素组成的物质一定是同一种物质。( )
(9)HCOOH分子中含有两个氢原子,所以是二元酸。( )
(10)盐一定由金属离子和酸根离子构成。( )
×
×
×
×
2.(2024新课标卷)文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是( )。
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸钙
解析:羊毛的主要成分为蛋白质,可用于制毛笔,A项正确;松木可用于制墨,墨的主要成分是单质碳,B项正确;竹子的主要成分为纤维素,竹子可用于造纸,故纸的主要成分是纤维素,C项正确;大理石的主要成分是CaCO3,D项错误。
D
知识点2
物质的性质与变化
知识筛查
1.物理变化与化学变化
(1)宏观角度。
物理变化没有新物质生成,化学变化有新物质生成。
(2)微观角度。
化学变化过程中同时伴随着旧化学键的断裂和新化学键的形成。只有旧化学键断裂而没有新化学键形成的过程不是化学变化,如NaCl晶体的熔化。
(3)两者关系。
化学变化中一定伴随着物理变化,物理变化过程中一定没有化学变化。
(4)物质变化与性质的关系。
①图示。
②应用下列用途体现物质
物理性质的是ae;体现物质
化学性质的是bcd。
a.用铝箔包装物品
b.NaHCO3作为食品工业的膨松剂
c.浓氨水检验输送氯气的管道是否泄漏
d.SO2漂白纸浆
e.液态丙烷作制冷剂
2.化学反应的分类
知识巩固
1.判断正误,正确的画“√”,错误的画“×”。
(1)臭氧变成氧气是物理变化。( )
(2)将蓝色的硫酸铜晶体放入浓硫酸中只发生物理变化。( )
(3)发光发热的变化都是化学变化。( )
(4)煤的气化、液化、干馏都是物理变化。( )
(5)分馏、蒸馏、蒸发、萃取、分液、过滤都是物理变化。( )
(6)加热I2或NH4Cl晶体,固体从试管底部跑到上部均属于物理变化。( )
×
×
×
×
√
×
(7)向蛋白质溶液中滴加CuSO4溶液或Na2SO4溶液产生沉淀均属于化学变化。( )
(8)向紫色石蕊溶液中加入活性炭后,溶液褪色,发生的是化学变化。( )
(9)用铂丝蘸取NaCl溶液进行焰色试验是化学变化。( )
(10)核裂变、核聚变均有新物质生成,均属于化学变化。( )
×
×
×
×
2.(2024吉林卷)家务劳动中蕴含着丰富的化学知识。下列相关解释错误的是( )。
A.用过氧碳酸钠漂白衣物:Na2CO4具有较强氧化性
B.酿米酒需晾凉米饭后加酒曲:乙醇受热易挥发
C.用柠檬酸去除水垢:柠檬酸酸性强于碳酸
D.用碱液清洗厨房油污:油脂可碱性水解
解析:过氧碳酸钠中的过氧键具有强氧化性,可用于漂白衣物,A项正确;酿米酒晾凉米饭是为了防止酒曲酶(主要成分为蛋白质)受热变性,变性后失去催化效果,B项错误;水垢的主要成分有CaCO3等,柠檬酸可以除去水垢说明柠檬酸的酸性比碳酸强,C项正确;油脂是高级脂肪酸甘油酯,在碱性条件下能够促进油脂的水解,去除油污效果更好,D项正确。
B
知识点3
分散系 胶体
知识筛查
1.分散系
(1)定义:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物,叫做分散系。
(2)分类。
2.胶体
(1)性质与应用。
(2)Fe(OH)3胶体的制备。(夹持装置省略)
向沸水中逐滴加入FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,即制得Fe(OH)3胶体,化学方程式为FeCl3+3H2O Fe(OH)3(胶体)+3HCl。
特别提醒(1)胶体中的胶粒带电荷,但胶体不带电荷,整个分散系仍呈电中性。
(2)区分胶体和其他分散系的方法是丁达尔效应,而胶体与其他分散系的本质区别是分散质粒子直径为1~100 nm。
(3)Fe(OH)3胶体粒子是“分子”的集合体,因此,Fe(OH)3胶体粒子的数目要远远小于原FeCl3溶液中Fe3+的数目。
知识巩固
判断正误,正确的画“√”,错误的画“×”。
(1)将NaOH浓溶液滴入FeCl3饱和溶液中,制备Fe(OH)3胶体。( )
(2)稀豆浆、硅酸、氯化铁溶液均为胶体。( )
(3)H+、K+、S2-、Br-能在Fe(OH)3胶体中大量共存。( )
(4)向沸水中逐滴加入FeCl3饱和溶液,可制得Fe(OH)3胶体。( )
(5)向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O Al(OH)3(胶体)+3H+。( )
(6)沸水中滴加适量FeCl3饱和溶液,形成带电荷的胶体,导电能力增强。( )
(7)葡萄糖注射液不能产生丁达尔效应,不属于胶体。( )
×
×
×
√
√
×
√
第二环节 关键能力形成
能力点1
根据一定的标准给物质分类的能力
整合建构
物质分类的3个“误区”
(1)误认为由相同元素组成的物质一定是纯净物。若某物质是由一种元素组成的单质混合而成,则属于混合物。如O2、O3组成的混合气体就是混合物,由12C和13C组成的石墨则是纯净物。
(2)误认为溶液呈酸性的物质一定是酸,溶液呈碱性的物质一定是碱。如NaHSO4、CuSO4、NH4Cl等物质的溶液呈酸性,但这些物质均属于盐。Na2CO3溶液、NaHCO3溶液呈碱性,Na2CO3、NaHCO3均属于盐。
(3)误认为能与酸反应生成盐和水的氧化物就是碱性氧化物,如Na2O2不属于碱性氧化物。
问题引领
(1)如何区别纯净物与混合物
(2)如何区别酸性氧化物与碱性氧化物
点拨(1)纯净物、混合物的判断方法。
常见混合物:①分散系(如溶液、胶体、浊液等);②高分子(如蛋白质、纤维素、聚合物、淀粉等);③常见特殊名称的混合物,如石油、石油的各种馏分、煤、漂白粉、碱石灰、福尔马林、油脂、天然气、水煤气、铝热剂、氨水、氯水、王水等。
(2)酸性氧化物和碱性氧化物。
①酸性氧化物、碱性氧化物不一定都能与水反应生成相应的酸或碱,如SiO2、Fe2O3。②能与酸反应生成盐和水的氧化物不一定是碱性氧化物,如Al2O3。③能与碱反应生成盐和水的氧化物不一定是酸性氧化物,如Al2O3。④碱性氧化物都是金属氧化物,但金属氧化物不一定都是碱性氧化物,如Mn2O7为酸性氧化物,Al2O3为两性氧化物,Na2O2为过氧化物。⑤酸性氧化物不一定是非金属氧化物,如Mn2O7;非金属氧化物也不一定是酸性氧化物,如CO、NO。
训练突破
1.下列各组物质的分类正确的是( )。
①混合物:液氯、氨水、水玻璃、福尔马林、聚乙烯 ②电解质:明矾、冰醋酸、石膏、纯碱 ③CO2、NO2、P2O5均为酸性氧化物 ④同位素: 1H+、2H2、3H ⑤同素异形体:C60、C80、金刚石、石墨 ⑥同系物: CH2O2、C2H4O2、C3H6O2、C4H8O2 ⑦化合物:CaCl2、NaOH、HCl、HD ⑧在熔化状态下能导电的化合物为离子化合物
A.②⑤⑧ B.①②⑤⑦⑧
C.②⑤⑥⑦⑧ D.①③④⑥⑦
A
解析:液氯属于纯净物,故①错误。明矾、冰醋酸、石膏、纯碱溶于水自身电离出阳离子与阴离子,属于电解质,故②正确。NO2不是酸性氧化物,故③错误。同位素研究的对象是原子,1H+是离子,2H2属于单质,故④错误。C60、C80、金刚石、石墨是碳元素组成的结构不同的单质,互为同素异形体,故⑤正确。C2H4O2、C3H6O2、C4H8O2存在同分异构体,结构不一定相似,CH2O2、C2H4O2、C3H6O2、C4H8O2不一定属于同系物,故⑥错误。HD是单质,故⑦错误。共价化合物在熔化状态下不导电,在熔化状态下能导电的化合物为离子化合物,故⑧正确。综上所述,A项正确。
2.下列说法正确的是( )。
A.水银、磁铁矿、淀粉、纤维素都是混合物
B.SiO2、Mn2O7为酸性氧化物,Na2O2、MgO为碱性氧化物
C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到
D.天然气、沼气和水煤气分别属于化石能源、可再生能源和二次能源
D
解析:水银是Hg,是纯净物,A项错误。Na2O2不是碱性氧化物,B项错误。Mg、Al、Cu可以分别用电解法、电解法和热还原法冶炼得到,C项错误。天然气属于化石能源,沼气为可再生能源,由植物秸秆等在沼气池中发酵得到,水煤气由碳与水蒸气反应得到,是二次能源,D项正确。
能力点2
运用胶体的特征分析、解释与胶体有关的问题的能力
整合建构
问题引领
溶液、胶体、浊液三种分散系的区别和联系是什么
点拨
分散系 溶液 胶体 浊液
分散质粒子直径 小于 1 nm 1~100 nm 大于 100 nm
分散质粒子 单个小分子或离子 高分子或多分子集合体 巨大数目的分子或离子集合体
性 质 外观 透明、均一 均一 不透明、不均一
稳定性 稳定 介于溶液与 浊液之间 不稳定
能否透过滤纸 能 能 不能
能否透过半透膜 能 不能 不能
鉴别 无丁达尔效应 有丁达尔效应 静置分层或沉淀
训练突破
下列叙述正确的是( )。
A.胶体区别于其他分散系的本质特征是胶体能产生丁达尔效应
B.浓硫酸具有吸水性,可以干燥NH3、SO2、CO2
C.Fe(OH)3胶体带正电荷
D.化合物分为酸、碱、盐和氧化物利用的是树状分类法
D
解析:胶体区别于其他分散系的本质特征是分散质粒子直径在1~100 nm之间,A项错误。NH3能与浓硫酸反应,浓硫酸不能干燥NH3,B项错误。Fe(OH)3胶体粒子带正电荷,Fe(OH)3胶体不带电荷,C项错误。利用树状分类法,可将化合物分为酸、碱、盐和氧化物,D项正确。
第三环节 核心素养提升
【高考真题剖析】
【例题】 (2023辽宁卷)科技是第一生产力,我国科学家在诸多领域取得新突破,下列说法错误的是( )。
A.利用CO2合成了脂肪酸:实现了无机小分子向有机高分子的转变
B.发现了月壤中的“嫦娥石
[(Ca8Y)Fe(PO4)7]”:其成分属于无机盐
C.研制了高效率钙钛矿太阳能电池,其能量转化形式:太阳能→电能
D.革新了海水原位电解制氢工艺:其关键材料多孔聚四氟乙烯耐腐蚀
A
解析:脂肪酸分子不是有机高分子,A项错误;嫦娥石中无碳元素,为无机物,结构中含有 ,为无机盐,B项正确;太阳能电池将太阳能直接转化为电能,C项正确;聚四氟乙烯性质稳定,具有很好的耐腐蚀性,D项正确。
【核心素养考查点剖析】本题是一道有关化学与生产、科技的题目,较好地考查了考生“宏观辨识与微观探析”素养,考查考生能否“从不同层次认识物质的多样性,并对物质进行分类”;能否“从元素和原子、分子水平认识物质的组成、结构、性质和变化”;同时考查了考生的“科学态度与社会责任”,考查考生深刻认识化学对创造更多物质财富、满足人民日益增长的美好生活需要的重大贡献。
【典题训练】
1.(2022浙江卷)下列消毒剂的有效成分属于盐的是( )。
A.高锰酸钾溶液
B.过氧乙酸溶液
C.双氧水
D.医用酒精
解析:高锰酸钾溶液的有效成分是高锰酸钾,属于盐,A项符合题意;过氧乙酸溶液的有效成分是过氧乙酸,属于有机酸,B项不符合题意;双氧水的有效成分是过氧化氢,属于过氧化物,C项不符合题意;医用酒精的有效成分是乙醇,属于醇类,D项不符合题意。
A
2.下列说法正确的是( )。
A.MgO和Al2O3都属于两性氧化物
B.悬浊液和乳浊液的分散质均为液态
C.Fe3O4和Pb3O4中的金属都呈现两种价态
D.葡萄糖溶液和淀粉溶液都具有丁达尔效应
C
解析:MgO是碱性氧化物,A项错误。悬浊液的分散质是固体小颗粒,B项错误。Fe3O4可表示为FeO·Fe2O3,铁元素化合价为+2、+3价;Pb3O4可表示为2PbO·PbO2,铅元素化合价为+2、+4价,因此两种化合物中的金属都呈现两种价态,C项正确。葡萄糖溶液不具有丁达尔效应,D项错误。
3.(2023全国甲)化学与生活密切相关,下列说法正确的是( )。
A.苯甲酸钠可作为食品防腐剂是由于其具有酸性
B.豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C.SO2可用于丝织品漂白是由于其能氧化丝织品中有色成分
D.维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
B
解析:苯甲酸钠具有杀菌、抑菌作用,常用作食品防腐剂,且苯甲酸钠水解,其溶液显碱性,A项错误;豆浆中胶体粒子能对光线产生散射作用,从而产生丁达尔效应,B项正确;SO2能与某些有色物质化合为不稳定的无色物质,体现其漂白性,C项错误;维生素C具有强还原性,易与水果罐头中的氧气等氧化性物质反应,从而起到抗氧化的作用,D项错误。
4.(2023新课标卷)化学在文物的研究和修复中有重要作用。下列说法错误的是( )。
A.竹简的成分之一纤维素属于天然高分子
B.龟甲的成分之一羟基磷灰石属于无机物
C.古陶瓷修复所用的熟石膏,其成分为Ca(OH)2
D.古壁画颜料中所用的铁红,其成分为Fe2O3
C
解析:竹简的成分之一纤维素的分子式为(C6H10O5)n,属于天然高分子化合物,A项正确;羟基磷灰石,又称碱式磷酸钙,属于无机盐,B项正确;熟石灰的成分是Ca(OH)2,而熟石膏的化学式为2CaSO4·H2O,C项错误;Fe2O3为红棕色,是红色颜料的成分,俗称铁红,D项正确。
5.(2024湖北卷)劳动人民的发明创造是中华优秀传统文化的组成部分。下列化学原理描述错误的是( )。
C
选项 发明 关键操作 化学原理
A 制墨 松木在窑内焖烧 发生不完全燃烧
B 陶瓷 黏土高温烧结 形成新的化学键
C 造纸 草木灰水浸泡树皮 促进纤维素溶解
D 火药 硫黄、硝石和木炭混合,点燃 发生氧化还原反应
解析:松木在窑内焖烧产生烟尘(发生不完全燃烧得到松烟),加胶和其他辅料再定型得到墨,A项正确;黏土高温烧结过程中发生一系列物理、化学变化形成陶瓷,化学变化的过程中有新的化学键形成,B项正确;草木灰的主要成分为碳酸钾,浸泡后的水溶液呈碱性,可用于分离树皮等原料中的胶质,纤维素不能在K2CO3溶液中发生水解反应,因此草木灰水浸泡树皮,并不能促进纤维素溶解,C项错误;硫黄、硝石和木炭混合点燃,发生反应: S+2KNO3+3C K2S+N2↑+3CO2↑,该反应为氧化还原反应,D项正确。
【新情境模拟训练】
某同学在实验室进行了如图所示的实验,下列说法中正确的是( )。
A.氯化铁溶液是电解质
B.Z中红褐色透明液体中
分散质不能透过滤纸
C.Y中反应的离子方程式为
3CaCO3+2Fe3++3H2O══
2Fe(OH)3(胶体)+3CO2↑+3Ca2+
D.X、Z中分散系都能产生丁达尔效应
C
解析:氯化铁溶液是混合物,是电解质溶液,不属于电解质,A项错误。Z中红褐色透明液体为胶体,其分散质能透过滤纸,B项错误。铁离子水解使溶液显酸性,Y中反应的离子方程式为3CaCO3+2Fe3++3H2O══2Fe(OH)3(胶体)+3CO2↑+3Ca2+,C项正确。Z中分散系是胶体,能产生丁达尔效应;X中分散系是溶液,不能产生丁达尔效应,D项错误。
同课章节目录
