四川省广元市川师大万达中学2023-2024学年高二下学期6月期末模拟考试化学试卷(含答案)
文档属性
| 名称 | 四川省广元市川师大万达中学2023-2024学年高二下学期6月期末模拟考试化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 792.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-18 00:00:00 | ||
图片预览



文档简介
四川省广元市川师大万达中学2023-2024学年高二下学期6月期末模拟考试化学试题
一、单选题
1.生活中的化学无处不在,下列关于生活中的化学描述正确的是
A.玛瑙、水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐
B.人体细胞和细胞器的双分子膜属于一种可以自组装的超分子
C.《本草纲目》中“凡坏酸之酒,皆可蒸烧”,所用的分离方法是蒸发
D.N95型口罩的核心材料是聚丙烯,它能使溴水褪色
2.我们生活的衣食住行都离不开有机化合物,下列说法不正确的是
A.甲烷是一种清洁能源,是天然气的主要成分
B.用溶液浸泡过的藻土可使水果保鲜,是利用了乙烯的还原性
C.乙炔用于焊接或切割金属,是因为乙炔燃烧时放出大量的热
D.聚氯乙烯(PVC)塑料,可用于制作食品包装袋
3.1, 3-丁二烯(CH2=CH-CH=CH2)和1-丁炔(CHC-CH2-CH3)在下列哪一种检测仪上显示出的信号是完全相同的
A.元素分析仪 B.质谱仪 C.红外光谱仪 D.核磁共振仪
4.下列化学用语表述正确的是
A.异丁烷的球棍模型: B.羟基的电子式:
C.硝基苯的结构简式: D. 的系统命名:2-乙基丁烷
5.下列有关分子结构和性质的说法正确的是
A.冰融化时,H2O分子中H—O键发生断裂
B.NH3比PH3稳定是因为NH3分子间存在氢键
C.H2O2易溶于水难溶于CCl4可用“相似相溶”原理解释
D.臭氧是含有非极性键的极性分子
6.阿伏加德罗常数的值为NA,下列说法正确的是
A.12 g 金刚石中C—C键的数目为4 NA
B.12 g 石墨烯中含有0.5 NA个六元环
C.标准状况下,22.4 L 氯仿中所含分子数为NA
D.1 mol CaC2含有的阴阳离子总数为3 NA
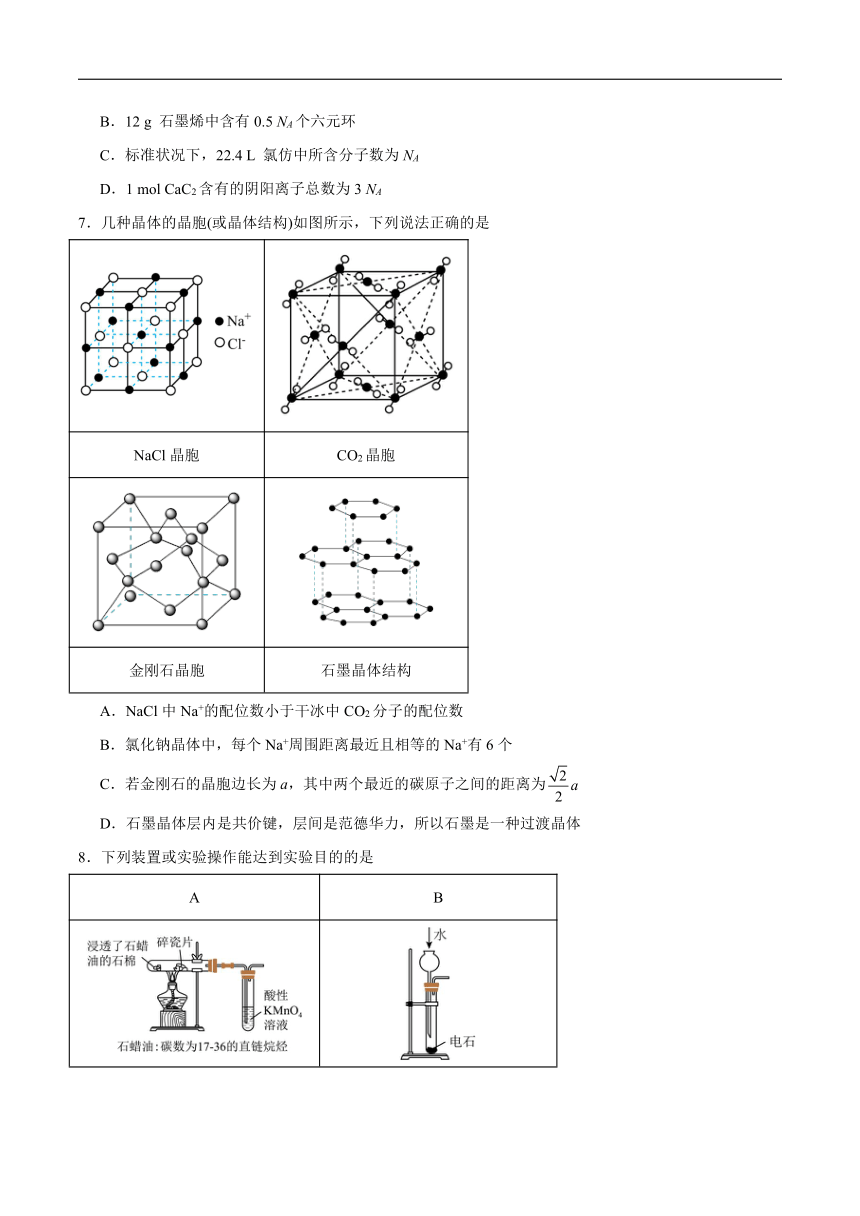
7.几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
NaCl晶胞 CO2晶胞
金刚石晶胞 石墨晶体结构
A.NaCl中Na+的配位数小于干冰中CO2分子的配位数
B.氯化钠晶体中,每个Na+周围距离最近且相等的Na+有6个
C.若金刚石的晶胞边长为a,其中两个最近的碳原子之间的距离为
D.石墨晶体层内是共价键,层间是范德华力,所以石墨是一种过渡晶体
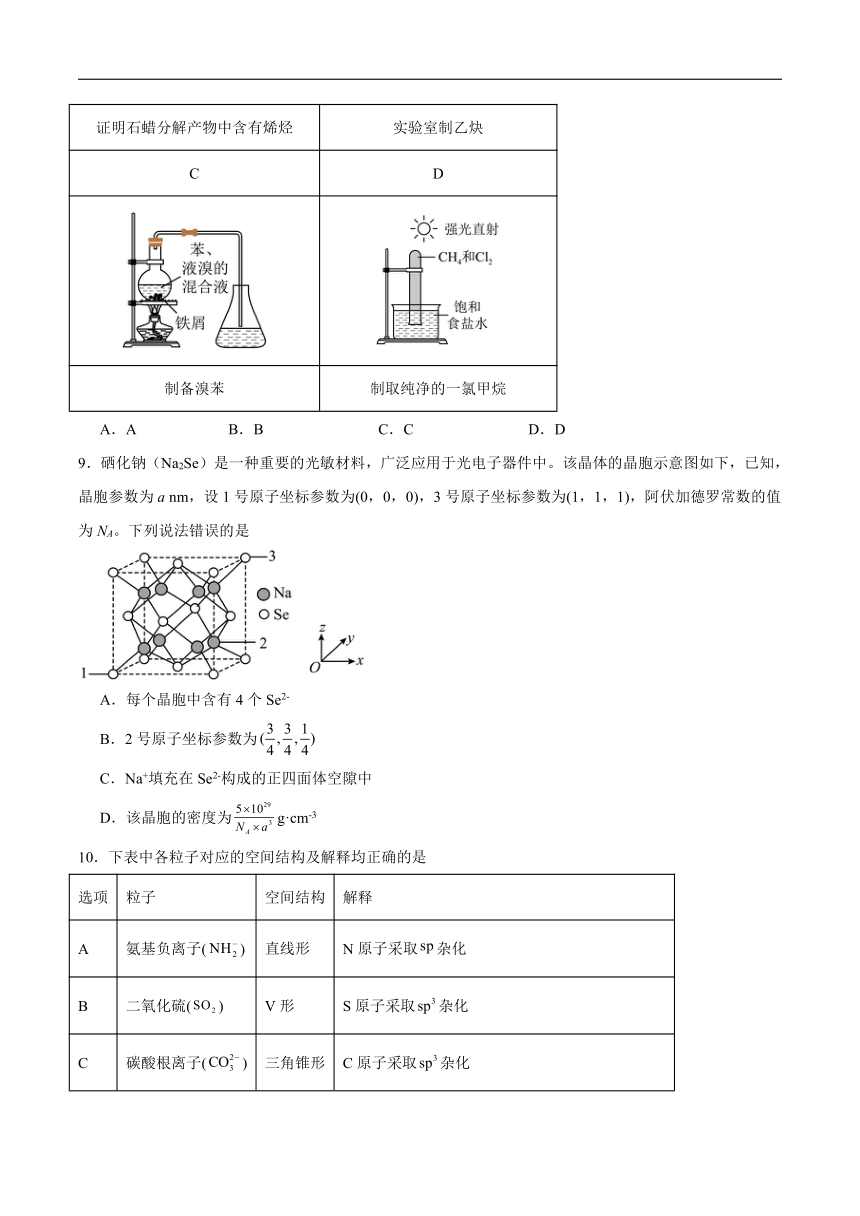
8.下列装置或实验操作能达到实验目的的是
A B
证明石蜡分解产物中含有烯烃 实验室制乙炔
C D
制备溴苯 制取纯净的一氯甲烷
A.A B.B C.C D.D
9.硒化钠(Na2Se)是一种重要的光敏材料,广泛应用于光电子器件中。该晶体的晶胞示意图如下,已知,晶胞参数为a nm,设1号原子坐标参数为(0,0,0),3号原子坐标参数为(1,1,1),阿伏加德罗常数的值为NA。下列说法错误的是
A.每个晶胞中含有4个Se2-
B.2号原子坐标参数为
C.Na+填充在Se2-构成的正四面体空隙中
D.该晶胞的密度为g·cm-3
10.下表中各粒子对应的空间结构及解释均正确的是
选项 粒子 空间结构 解释
A 氨基负离子() 直线形 N原子采取杂化
B 二氧化硫() V形 S原子采取杂化
C 碳酸根离子() 三角锥形 C原子采取杂化
D 乙炔() 直线形 C原子采取杂化且C原子的价电子均参与成键
A.A B.B C.C D.D
11.下列有机反应所属反应类型判断不正确的
A.取代反应
B.还原反应
C. 加成反应
D. 加成反应
12.冠醚是一类皇冠状的分子,可有不同大小的空穴适配不同大小的碱金属离子。18-冠-6可以通过图示方法制备。下列说法错误的是
A.18-冠-6分子中都采用sp3杂化
B.反应(1)比反应(2)原子利用率更高
C.冠醚的空穴结构对离子有选择作用,在有机反应中可作催化剂
D.制取方法中(1)为取代反应,另一种产物为
13.下列除去杂质的方法不正确的是
选项 物质 杂质 试剂 主要操作
A 乙炔 、 溶液 洗气
B 溴苯 溴 溶液 分液
C 乙烷 乙烯 溶液 洗气
D 蒸馏
A.A B.B C.C D.D
14.五羰基铁[]是一种具有三角双锥结构的黄色黏稠状液体,结构如图所示,已知其熔点为﹣20 ℃,沸点为103 ℃。下列推测不合理的是
A.五羰基铁晶体属于分子晶体
B.五羰基铁不溶于水,易溶于苯
C.五羰基铁隔绝空气受热分解生成Fe和CO
D.每个粒子中含σ键的个数为20
二、解答题
15.秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供 ,配位原子是 ,1 mol [Cu(H2O)4]2+中σ键的数目为 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式 ,再向溶液中加入乙醇,会析出深蓝色晶体 (写出化学式)。
(3)“中国蓝”“中国紫”中存在四面体结构,其中Si原子采取的杂化方式为 。
(4)BaO的熔沸点 MgO(填“>”“<”“=”),原因是 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为 g·cm-3。
16.苯胺是一种重要的精细化工原料,在染料、医药等行业中具有广泛的应用。
物质 相对分子质量 沸点/℃ 密度/(g·mL-1) 溶解性
硝基苯 123 210.9 1.23 不溶于水,易溶于乙醇、乙醚
苯胺 93 184.4 1.02 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化
(1)实验室以苯为原料制取苯胺,其反应原理如下:
第一步: ;
第二步: + 3H2 + 2H2O
(2)制取硝基苯
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶中装有一定比例的浓硫酸和浓硝酸混合物。
①下列说法中正确的是 (填字母)。
A.配制混酸时,将浓硝酸沿杯壁缓缓加入浓硫酸中,并不断搅拌、冷却
B.浓硫酸可以降低该反应的活化能
C. 温度控制在50~60 ℃原因之一是减少副反应的发生
D.制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤
②制备硝基苯时使用了恒压滴液漏斗,其作用是 ;
③粗硝基苯中有少量浓硫酸、浓硝酸,可选用的除杂试剂是 ;
(3)制取苯胺
步骤1:组装好实验装置并检查气密性;
步骤2:先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计;
步骤3:打开活塞K,通入H2一段时间;
步骤4:利用油浴加热;
步骤5:反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰;
步骤6:调整好温度计的位置,继续加热,收集182~186 ℃馏分,得到较纯苯胺。
回答下列问题:
①步骤4中油浴加热的优点是 ;
②步骤5中加入生石灰的作用是 ;
③步骤6中,仪器A的名称是 ,冷凝水的流向为 → (填字母);
④若实验中硝基苯用量为10 mL,最后得到苯胺5.6 g,苯胺的产率为 (精确到0.1%)。
17.钴及其化合物广泛应用于航天、电池、磁性合金等高科技领域,我国钴资源贫乏,再生钴资源的回收利用是解决钴资源供给的重要途径。一种利用含钴废料(主要成分为,含少量、有机物)制取的工艺流程如图:
已知该工艺条件下,有关金属离子开始沉淀和沉淀完全的,回答下列问题:
金属离子
开始沉淀的 7.5 1.8 3.4 9.1 6.5
沉淀完全的 9.5 3.2 4.7 11.1 8.5
(1)“焙烧”的主要目的是 。
(2)“浸取”过程中发生反应的离子方程式为 。
(3)“沉淀”时先加入溶液,的作用主要是 ;再加入溶液调节为5.0,此时滤液中的 。
(4)“萃取”用到的玻璃仪器主要有 、烧杯,萃取原理可表述为:(水层)(有机层)(有机层)(水层)。已知萃取率随变化如图所示,分析其变化原因 。水相中含有的阳离子有 。
(5)“沉钴”可得到,反应的离子方程式为 。
18.光固化是高效、环保、节能的材料表面处理技术。化合物E是一种广泛应用于光固化产品的光引发剂,可采用异丁酸(A)为原料,按如图路线合成:
回答下列问题:
(1)写出化合物E的分子式: ,其含氧官能团名称为 。
(2)用系统命名法对A命名: ;在异丁酸的同分异构体中,属于酯类的化合物数目为 ,写出其中含有4种处于不同化学环境氢原子的异构体的结构简式: 。
(3)为实现C→D的转化,试剂X为 (填序号)。
a.HBr b.NaBr c.
(4)D→E的反应类型为 。
(5)在紫外光照射下,少量化合物E能引发甲基丙烯酸甲酯()快速聚合,写出该聚合反应的方程式: 。
(6)已知: R=烷基或羧基
参照以上合成路线和条件,利用甲苯和苯及必要的无机试剂,在方框中完成制备化合物F的合成路线。
参考答案
1.B
2.D
3.A
4.B
5.C
6.B
7.A
8.A
9.D
10.D
11.C
12.B
13.C
14.D
15.(1) 空轨道 O 12NA
(2) Cu(OH)2+4NH3= [Cu(NH3)4]2++2OH-或Cu(OH)2+4NH3·H2O= [Cu(NH3)4]2++2OH-+4H2O [Cu(NH3)4]SO4·H2O
(3)sp3杂化
(4) < MgO和BaO都是离子晶体,Mg2+和Ba2+所带电荷相同,前者半径更小,MgO离子键更强,熔沸点更高
(5) 6
16.(1)+HNO3+H2O
(2) BC 平衡气压,使苯顺利流下 NaOH溶液
(3) 加热温度恒定、受热均匀,加热温度较高 吸收反应生成的水 (直形)冷凝管 a b 60.2%
17.(1)除去废料中的有机物
(2)
(3) 将氧化为,以便后续转换为除去 或
(4) 分液漏斗 当时,随着升高,溶液中减小,平衡向正反应方向移动,更多的与萃取剂反应;当时,随着升高,溶液中增大,与形成沉淀 、、
(5)
18.(1) 酮羰基、羟基
(2) 2 甲基丙酸 4
(3)c
(4)取代反应(或水解反应)
(5)
(6)
一、单选题
1.生活中的化学无处不在,下列关于生活中的化学描述正确的是
A.玛瑙、水晶、钻石、红宝石等装饰品的主要成分都是硅酸盐
B.人体细胞和细胞器的双分子膜属于一种可以自组装的超分子
C.《本草纲目》中“凡坏酸之酒,皆可蒸烧”,所用的分离方法是蒸发
D.N95型口罩的核心材料是聚丙烯,它能使溴水褪色
2.我们生活的衣食住行都离不开有机化合物,下列说法不正确的是
A.甲烷是一种清洁能源,是天然气的主要成分
B.用溶液浸泡过的藻土可使水果保鲜,是利用了乙烯的还原性
C.乙炔用于焊接或切割金属,是因为乙炔燃烧时放出大量的热
D.聚氯乙烯(PVC)塑料,可用于制作食品包装袋
3.1, 3-丁二烯(CH2=CH-CH=CH2)和1-丁炔(CHC-CH2-CH3)在下列哪一种检测仪上显示出的信号是完全相同的
A.元素分析仪 B.质谱仪 C.红外光谱仪 D.核磁共振仪
4.下列化学用语表述正确的是
A.异丁烷的球棍模型: B.羟基的电子式:
C.硝基苯的结构简式: D. 的系统命名:2-乙基丁烷
5.下列有关分子结构和性质的说法正确的是
A.冰融化时,H2O分子中H—O键发生断裂
B.NH3比PH3稳定是因为NH3分子间存在氢键
C.H2O2易溶于水难溶于CCl4可用“相似相溶”原理解释
D.臭氧是含有非极性键的极性分子
6.阿伏加德罗常数的值为NA,下列说法正确的是
A.12 g 金刚石中C—C键的数目为4 NA
B.12 g 石墨烯中含有0.5 NA个六元环
C.标准状况下,22.4 L 氯仿中所含分子数为NA
D.1 mol CaC2含有的阴阳离子总数为3 NA
7.几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
NaCl晶胞 CO2晶胞
金刚石晶胞 石墨晶体结构
A.NaCl中Na+的配位数小于干冰中CO2分子的配位数
B.氯化钠晶体中,每个Na+周围距离最近且相等的Na+有6个
C.若金刚石的晶胞边长为a,其中两个最近的碳原子之间的距离为
D.石墨晶体层内是共价键,层间是范德华力,所以石墨是一种过渡晶体
8.下列装置或实验操作能达到实验目的的是
A B
证明石蜡分解产物中含有烯烃 实验室制乙炔
C D
制备溴苯 制取纯净的一氯甲烷
A.A B.B C.C D.D
9.硒化钠(Na2Se)是一种重要的光敏材料,广泛应用于光电子器件中。该晶体的晶胞示意图如下,已知,晶胞参数为a nm,设1号原子坐标参数为(0,0,0),3号原子坐标参数为(1,1,1),阿伏加德罗常数的值为NA。下列说法错误的是
A.每个晶胞中含有4个Se2-
B.2号原子坐标参数为
C.Na+填充在Se2-构成的正四面体空隙中
D.该晶胞的密度为g·cm-3
10.下表中各粒子对应的空间结构及解释均正确的是
选项 粒子 空间结构 解释
A 氨基负离子() 直线形 N原子采取杂化
B 二氧化硫() V形 S原子采取杂化
C 碳酸根离子() 三角锥形 C原子采取杂化
D 乙炔() 直线形 C原子采取杂化且C原子的价电子均参与成键
A.A B.B C.C D.D
11.下列有机反应所属反应类型判断不正确的
A.取代反应
B.还原反应
C. 加成反应
D. 加成反应
12.冠醚是一类皇冠状的分子,可有不同大小的空穴适配不同大小的碱金属离子。18-冠-6可以通过图示方法制备。下列说法错误的是
A.18-冠-6分子中都采用sp3杂化
B.反应(1)比反应(2)原子利用率更高
C.冠醚的空穴结构对离子有选择作用,在有机反应中可作催化剂
D.制取方法中(1)为取代反应,另一种产物为
13.下列除去杂质的方法不正确的是
选项 物质 杂质 试剂 主要操作
A 乙炔 、 溶液 洗气
B 溴苯 溴 溶液 分液
C 乙烷 乙烯 溶液 洗气
D 蒸馏
A.A B.B C.C D.D
14.五羰基铁[]是一种具有三角双锥结构的黄色黏稠状液体,结构如图所示,已知其熔点为﹣20 ℃,沸点为103 ℃。下列推测不合理的是
A.五羰基铁晶体属于分子晶体
B.五羰基铁不溶于水,易溶于苯
C.五羰基铁隔绝空气受热分解生成Fe和CO
D.每个粒子中含σ键的个数为20
二、解答题
15.秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。通过对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(BaCuSixOy) 。
回答下列问题:
(1)“中国蓝”的发色与硫酸铜溶液呈天蓝色类似,都是由于形成了[Cu(H2O)4]2+,该配离子中Cu2+提供 ,配位原子是 ,1 mol [Cu(H2O)4]2+中σ键的数目为 。
(2)写出向硫酸铜溶液里逐滴加入氨水过程中沉淀溶解的离子方程式 ,再向溶液中加入乙醇,会析出深蓝色晶体 (写出化学式)。
(3)“中国蓝”“中国紫”中存在四面体结构,其中Si原子采取的杂化方式为 。
(4)BaO的熔沸点 MgO(填“>”“<”“=”),原因是 。
(5)立方CuO晶胞结构如图所示。其中Cu2+的配位数为 。NA代表阿伏加德罗常数的值,晶胞参数为a pm,则其晶体密度为 g·cm-3。
16.苯胺是一种重要的精细化工原料,在染料、医药等行业中具有广泛的应用。
物质 相对分子质量 沸点/℃ 密度/(g·mL-1) 溶解性
硝基苯 123 210.9 1.23 不溶于水,易溶于乙醇、乙醚
苯胺 93 184.4 1.02 微溶于水,易溶于乙醇、乙醚;还原性强、易被氧化
(1)实验室以苯为原料制取苯胺,其反应原理如下:
第一步: ;
第二步: + 3H2 + 2H2O
(2)制取硝基苯
实验步骤:实验室采用如图所示装置制取硝基苯,恒压滴液漏斗中装有一定量的苯,三颈烧瓶中装有一定比例的浓硫酸和浓硝酸混合物。
①下列说法中正确的是 (填字母)。
A.配制混酸时,将浓硝酸沿杯壁缓缓加入浓硫酸中,并不断搅拌、冷却
B.浓硫酸可以降低该反应的活化能
C. 温度控制在50~60 ℃原因之一是减少副反应的发生
D.制得的粗硝基苯可以先用乙醇萃取,分液后再洗涤
②制备硝基苯时使用了恒压滴液漏斗,其作用是 ;
③粗硝基苯中有少量浓硫酸、浓硝酸,可选用的除杂试剂是 ;
(3)制取苯胺
步骤1:组装好实验装置并检查气密性;
步骤2:先向三颈烧瓶中加入沸石及硝基苯,再取下恒压滴液漏斗,换上温度计;
步骤3:打开活塞K,通入H2一段时间;
步骤4:利用油浴加热;
步骤5:反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰;
步骤6:调整好温度计的位置,继续加热,收集182~186 ℃馏分,得到较纯苯胺。
回答下列问题:
①步骤4中油浴加热的优点是 ;
②步骤5中加入生石灰的作用是 ;
③步骤6中,仪器A的名称是 ,冷凝水的流向为 → (填字母);
④若实验中硝基苯用量为10 mL,最后得到苯胺5.6 g,苯胺的产率为 (精确到0.1%)。
17.钴及其化合物广泛应用于航天、电池、磁性合金等高科技领域,我国钴资源贫乏,再生钴资源的回收利用是解决钴资源供给的重要途径。一种利用含钴废料(主要成分为,含少量、有机物)制取的工艺流程如图:
已知该工艺条件下,有关金属离子开始沉淀和沉淀完全的,回答下列问题:
金属离子
开始沉淀的 7.5 1.8 3.4 9.1 6.5
沉淀完全的 9.5 3.2 4.7 11.1 8.5
(1)“焙烧”的主要目的是 。
(2)“浸取”过程中发生反应的离子方程式为 。
(3)“沉淀”时先加入溶液,的作用主要是 ;再加入溶液调节为5.0,此时滤液中的 。
(4)“萃取”用到的玻璃仪器主要有 、烧杯,萃取原理可表述为:(水层)(有机层)(有机层)(水层)。已知萃取率随变化如图所示,分析其变化原因 。水相中含有的阳离子有 。
(5)“沉钴”可得到,反应的离子方程式为 。
18.光固化是高效、环保、节能的材料表面处理技术。化合物E是一种广泛应用于光固化产品的光引发剂,可采用异丁酸(A)为原料,按如图路线合成:
回答下列问题:
(1)写出化合物E的分子式: ,其含氧官能团名称为 。
(2)用系统命名法对A命名: ;在异丁酸的同分异构体中,属于酯类的化合物数目为 ,写出其中含有4种处于不同化学环境氢原子的异构体的结构简式: 。
(3)为实现C→D的转化,试剂X为 (填序号)。
a.HBr b.NaBr c.
(4)D→E的反应类型为 。
(5)在紫外光照射下,少量化合物E能引发甲基丙烯酸甲酯()快速聚合,写出该聚合反应的方程式: 。
(6)已知: R=烷基或羧基
参照以上合成路线和条件,利用甲苯和苯及必要的无机试剂,在方框中完成制备化合物F的合成路线。
参考答案
1.B
2.D
3.A
4.B
5.C
6.B
7.A
8.A
9.D
10.D
11.C
12.B
13.C
14.D
15.(1) 空轨道 O 12NA
(2) Cu(OH)2+4NH3= [Cu(NH3)4]2++2OH-或Cu(OH)2+4NH3·H2O= [Cu(NH3)4]2++2OH-+4H2O [Cu(NH3)4]SO4·H2O
(3)sp3杂化
(4) < MgO和BaO都是离子晶体,Mg2+和Ba2+所带电荷相同,前者半径更小,MgO离子键更强,熔沸点更高
(5) 6
16.(1)+HNO3+H2O
(2) BC 平衡气压,使苯顺利流下 NaOH溶液
(3) 加热温度恒定、受热均匀,加热温度较高 吸收反应生成的水 (直形)冷凝管 a b 60.2%
17.(1)除去废料中的有机物
(2)
(3) 将氧化为,以便后续转换为除去 或
(4) 分液漏斗 当时,随着升高,溶液中减小,平衡向正反应方向移动,更多的与萃取剂反应;当时,随着升高,溶液中增大,与形成沉淀 、、
(5)
18.(1) 酮羰基、羟基
(2) 2 甲基丙酸 4
(3)c
(4)取代反应(或水解反应)
(5)
(6)
同课章节目录
