2025年安徽省合肥市安师联盟中考安心卷化学试卷(含答案)
文档属性
| 名称 | 2025年安徽省合肥市安师联盟中考安心卷化学试卷(含答案) | 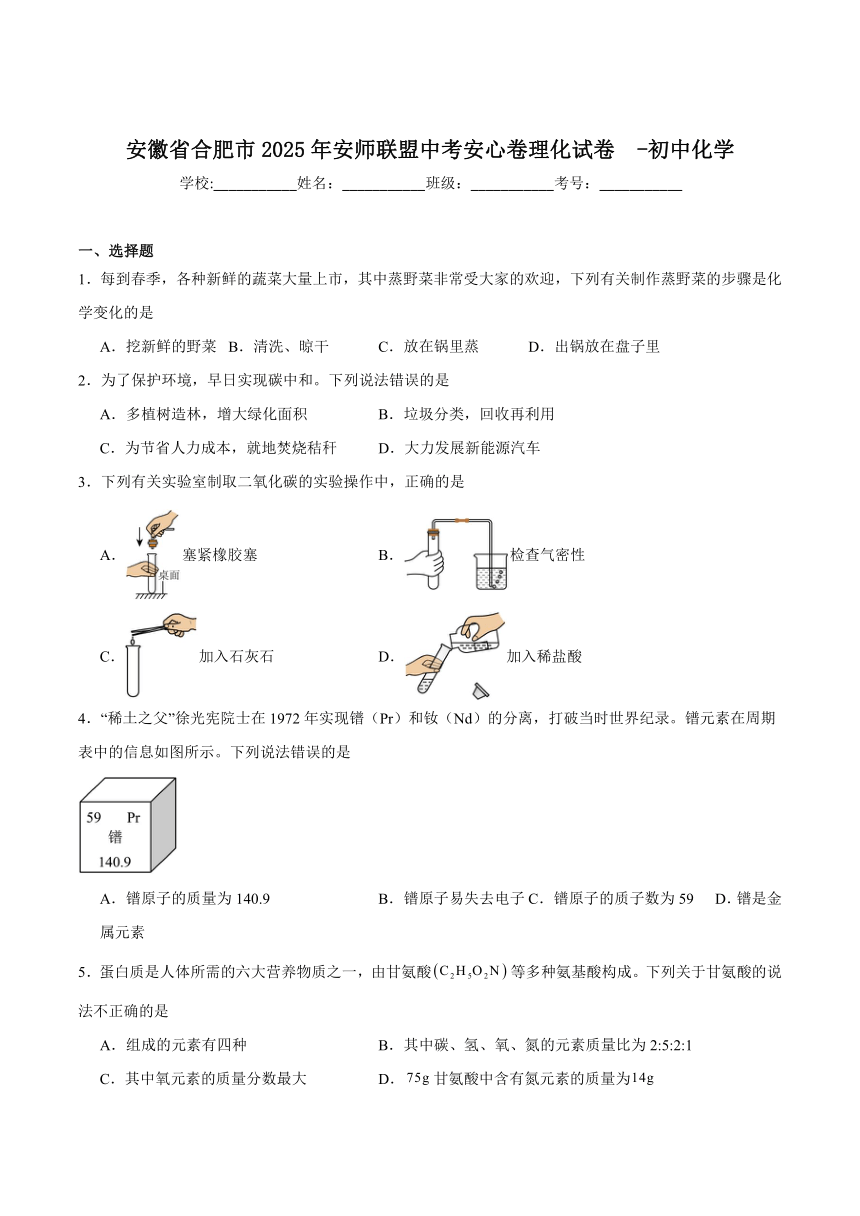 | |
| 格式 | docx | ||
| 文件大小 | 661.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-19 15:55:33 | ||
图片预览



文档简介
安徽省合肥市2025年安师联盟中考安心卷理化试卷 -初中化学
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.每到春季,各种新鲜的蔬菜大量上市,其中蒸野菜非常受大家的欢迎,下列有关制作蒸野菜的步骤是化学变化的是
A.挖新鲜的野菜 B.清洗、晾干 C.放在锅里蒸 D.出锅放在盘子里
2.为了保护环境,早日实现碳中和。下列说法错误的是
A.多植树造林,增大绿化面积 B.垃圾分类,回收再利用
C.为节省人力成本,就地焚烧秸秆 D.大力发展新能源汽车
3.下列有关实验室制取二氧化碳的实验操作中,正确的是
A.塞紧橡胶塞 B.检查气密性
C.加入石灰石 D.加入稀盐酸
4.“稀土之父”徐光宪院士在1972年实现镨(Pr)和钕(Nd)的分离,打破当时世界纪录。镨元素在周期表中的信息如图所示。下列说法错误的是
A.镨原子的质量为140.9 B.镨原子易失去电子 C.镨原子的质子数为59 D.镨是金属元素
5.蛋白质是人体所需的六大营养物质之一,由甘氨酸等多种氨基酸构成。下列关于甘氨酸的说法不正确的是
A.组成的元素有四种 B.其中碳、氢、氧、氮的元素质量比为2:5:2:1
C.其中氧元素的质量分数最大 D.甘氨酸中含有氮元素的质量为
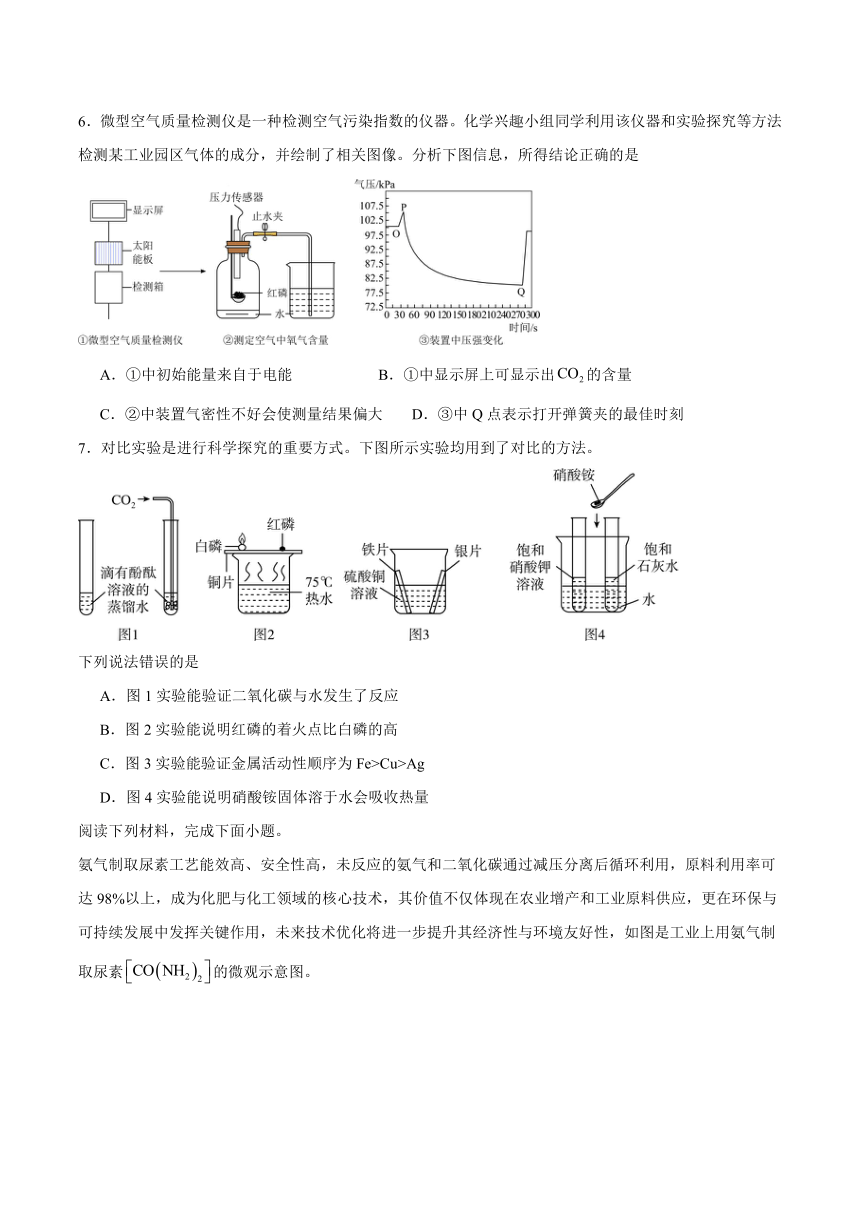
6.微型空气质量检测仪是一种检测空气污染指数的仪器。化学兴趣小组同学利用该仪器和实验探究等方法检测某工业园区气体的成分,并绘制了相关图像。分析下图信息,所得结论正确的是
A.①中初始能量来自于电能 B.①中显示屏上可显示出的含量
C.②中装置气密性不好会使测量结果偏大 D.③中Q点表示打开弹簧夹的最佳时刻
7.对比实验是进行科学探究的重要方式。下图所示实验均用到了对比的方法。
下列说法错误的是
A.图1实验能验证二氧化碳与水发生了反应
B.图2实验能说明红磷的着火点比白磷的高
C.图3实验能验证金属活动性顺序为Fe>Cu>Ag
D.图4实验能说明硝酸铵固体溶于水会吸收热量
阅读下列材料,完成下面小题。
氨气制取尿素工艺能效高、安全性高,未反应的氨气和二氧化碳通过减压分离后循环利用,原料利用率可达98%以上,成为化肥与化工领域的核心技术,其价值不仅体现在农业增产和工业原料供应,更在环保与可持续发展中发挥关键作用,未来技术优化将进一步提升其经济性与环境友好性,如图是工业上用氨气制取尿素的微观示意图。
8.下列有关说法不正确的是
A.该反应实现了无机物向有机物的转化 B.参加反应的甲、乙分子的个数比为2:1
C.该反应前后元素种类和质量不变 D.该反应是置换反应
9.下列有关该工艺的说法不正确的是
A.尿素是氮肥,能促进植物叶片浓绿 B.化肥能促进植物的生成,可以大量使用化肥
C.该工艺减少温室气体排放,助力碳中和目标 D.回收未反应的NH3和CO2可减少排放,符合绿色生产要求
10.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 除去CO2中少量的CO 在氧气中点燃
B 除去NaCl溶液中的Na2CO3溶液 取样,滴加适量的溶液
C 检验稀盐酸中是否含有硫酸 取样,滴加少量溶液
D 鉴别H2和CH4 分别点燃,在火焰上方罩一个干燥的烧杯
A.A B.B C.C D.D
11.逻辑推理是一种重要的化学思维方法,以下推理合理的是
A.纯碱溶液的pH>7,但pH>7的溶液不一定是碱溶液
B.酸碱中和反应属于复分解反应,则复分解反应一定是中和反应
C.金属离子与酸根离子组成的化合物叫盐,则盐中一定含金属离子
D.碳酸盐与盐酸反应产生气体,则与盐酸反应生成气体的物质一定是碳酸盐
12.下图为甲、乙、丙三种固体物质(不形成结晶水合物)在水中随温度变化的溶解度曲线,下列说法不正确的是
A.在t2℃时,甲和丙的溶解度相等
B.t1℃时,可以通过加水,将乙溶液的状态由M点变为N点
C.t3℃时,将40g甲放入50g水中,充分溶解后所得溶液的质量为90g
D.t3℃时,将125g丙的饱和溶液降温至t1℃,应再加入15g丙才能恰好达到饱和状态
二、填空与简答
13.我国是茶文化的发源地。唐代陆羽《茶经》中记载:“风炉以铜铁铸之……底一窗以为通飚漏烬之所……风能兴火,火能熟水。”“漉水囊……其格以生铜铸之、”
(1)“铜铁”属于 (填“金属”或“合成”)材料。
(2)“飚”(即风)提供燃烧所需的 。“烬”中含钾盐。农业上可用作 。
(3)“火能熟水”说明燃烧 (填“吸收”或“放出”)热量。
(4)茶香四溢,从分子角度解释其原因是 。
14.某工业废水,含有大量的ZnSO4和少量的CuSO4以及污泥。化学兴趣小组的同学想从中回收金属铜和硫酸锌晶体,他们设计了如下方案。
(1)操作a、b的名称是 ,用到的玻璃仪器有 (写一种)。
(2)步骤Ⅰ中加入过量的金属X的目的是 。
(3)步骤Ⅱ中发生反应的化学方程式是 。
(4)若溶液1和溶液2中溶质ZnSO4的质量分数分别表示为x和y,则x与y的大小关系是 。
三、实验题
15.结合图示实验装置,回答下列问题。
(1)图中仪器②的名称是 。
(2)实验室用A装置制取氧气,反应的化学方程式为 ;实验室制取氢气可选用D装置,也可用C装置替代,选用C装置的优点是 ;若用H装置收集氢气应从 (填“a”或“b”)端通入。
(3)常温下块状电石与水剧烈反应生成乙炔(C2H2)气体,已知乙炔难溶于水。实验室要用该反应制取乙炔气体,选用的发生和收集装置是 (填装置序号)。
四、科学探究题
16.学习了常见的碱,某同学想在实验室里用NaOH溶液制取Na2CO3溶液。
【查阅资料】①NaOH溶液中通入过量CO2,会发生两步反应且无明显现象。
第一步:生成Na2CO3;第二步:生成可溶于水的NaHCO3,反应原理为:Na2CO3+H2O+CO2=2NaHCO3。
②NaHCO3溶液煮沸时不会发生分解。
③NaHCO3+NaOH=Na2CO3+H2O。
④可溶于水。
【制取步骤】①量取两份50mL相同浓度的NaOH溶液备用。
②用一份50mLNaOH溶液吸收过量的CO2气体,至CO2气体不再溶解。
③小心煮沸②溶液1~2分钟。
④________________________,即得Na2CO3溶液。
【实验探究】为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与该同学一起完成下列实验探究:
实验步骤 实验现象 实验结论
取少量制得的溶液于试管中,加入过量的 ⑤ 溶液 产生白色沉淀 制得的溶液中含有Na2CO3
将上步实验所得混合物进行过滤,将滤液分成两份 取其中一份加入足量的 ⑥ 无气泡产生 制得的溶液中不含 ⑦
取另外一份加入MgCl2溶液 ⑧ 制得的溶液中不含NaOH
【实验结论】所制得的溶液为纯净的Na2CO3溶液。
(1)学习了氢氧化钠的知识,写出一个氢氧化钠在生活中的用途: 。
(2)将步骤④补充完整: 。
(3)将实验探究中各空格补充完整:⑤ ,⑥ ,⑦ ,⑧ 。
【评价与反思】
(4)有人认为将实验步骤③④的顺序对调更合理,你认为是否可行?并说明理由: 。
(5)实验探究中加入MgCl2溶液检验溶液中不含NaOH,除了用MgCl2溶液还可以用 检验,现象是 。
五、计算题
17.实验室中有一包石灰石,化学活动小组同学为测定该石灰石中CaCO3(杂质不与酸反应也不溶于水)的含量,取20g样品于烧杯中,向其中加入足量的稀盐酸,测得生成的气体与加入稀盐酸的质量关系如图所示,请回答下列问题。
(1)求石灰石中碳酸钙的质量分数。
(2)若所得结果比实际值偏小,则可能的原因是 。
《安徽省合肥市2025年安师联盟中考安心卷理化试卷 -初中化学》参考答案
1.C
2.C
3.B
4.A
5.B
6.D
7.A
8.D 9.B
10.C
11.A
12.C
13.(1)金属材料
(2) 空气或氧气 钾肥
(3)放出
(4)分子在不断运动
14.(1) 过滤 玻璃棒/漏斗/烧杯
(2)确保Cu2+完全被置换(或把CuSO4反应完)
(3)
(4)
15.(1)长颈漏斗
(2) 可以控制反应的发生与停止 a
(3)BE
16.(1)除油污(或作清洁剂)
(2)在得到的③的溶液中加入另一份50mLNaOH溶液,使其充分混合
(3) CaCl2(或BaCl2) 稀盐酸 NaHCO3 无明显现象
(4)不可行,如果对调,溶液中过量的CO2会与NaOH反应,消耗NaOH,使NaHCO3不能全部转化为Na2CO3
(5) 酚酞溶液 若溶液变红,则说明制得的溶液中含NaOH(合理即可)
17.(1)解:设石灰石中碳酸钙的质量为x。
x=10g
石灰石中碳酸钙的质量分数为:
答:石灰石中碳酸钙的质量分数为50%。
(2)有部分二氧化碳溶解在水中(答案合理即可)
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.每到春季,各种新鲜的蔬菜大量上市,其中蒸野菜非常受大家的欢迎,下列有关制作蒸野菜的步骤是化学变化的是
A.挖新鲜的野菜 B.清洗、晾干 C.放在锅里蒸 D.出锅放在盘子里
2.为了保护环境,早日实现碳中和。下列说法错误的是
A.多植树造林,增大绿化面积 B.垃圾分类,回收再利用
C.为节省人力成本,就地焚烧秸秆 D.大力发展新能源汽车
3.下列有关实验室制取二氧化碳的实验操作中,正确的是
A.塞紧橡胶塞 B.检查气密性
C.加入石灰石 D.加入稀盐酸
4.“稀土之父”徐光宪院士在1972年实现镨(Pr)和钕(Nd)的分离,打破当时世界纪录。镨元素在周期表中的信息如图所示。下列说法错误的是
A.镨原子的质量为140.9 B.镨原子易失去电子 C.镨原子的质子数为59 D.镨是金属元素
5.蛋白质是人体所需的六大营养物质之一,由甘氨酸等多种氨基酸构成。下列关于甘氨酸的说法不正确的是
A.组成的元素有四种 B.其中碳、氢、氧、氮的元素质量比为2:5:2:1
C.其中氧元素的质量分数最大 D.甘氨酸中含有氮元素的质量为
6.微型空气质量检测仪是一种检测空气污染指数的仪器。化学兴趣小组同学利用该仪器和实验探究等方法检测某工业园区气体的成分,并绘制了相关图像。分析下图信息,所得结论正确的是
A.①中初始能量来自于电能 B.①中显示屏上可显示出的含量
C.②中装置气密性不好会使测量结果偏大 D.③中Q点表示打开弹簧夹的最佳时刻
7.对比实验是进行科学探究的重要方式。下图所示实验均用到了对比的方法。
下列说法错误的是
A.图1实验能验证二氧化碳与水发生了反应
B.图2实验能说明红磷的着火点比白磷的高
C.图3实验能验证金属活动性顺序为Fe>Cu>Ag
D.图4实验能说明硝酸铵固体溶于水会吸收热量
阅读下列材料,完成下面小题。
氨气制取尿素工艺能效高、安全性高,未反应的氨气和二氧化碳通过减压分离后循环利用,原料利用率可达98%以上,成为化肥与化工领域的核心技术,其价值不仅体现在农业增产和工业原料供应,更在环保与可持续发展中发挥关键作用,未来技术优化将进一步提升其经济性与环境友好性,如图是工业上用氨气制取尿素的微观示意图。
8.下列有关说法不正确的是
A.该反应实现了无机物向有机物的转化 B.参加反应的甲、乙分子的个数比为2:1
C.该反应前后元素种类和质量不变 D.该反应是置换反应
9.下列有关该工艺的说法不正确的是
A.尿素是氮肥,能促进植物叶片浓绿 B.化肥能促进植物的生成,可以大量使用化肥
C.该工艺减少温室气体排放,助力碳中和目标 D.回收未反应的NH3和CO2可减少排放,符合绿色生产要求
10.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
A 除去CO2中少量的CO 在氧气中点燃
B 除去NaCl溶液中的Na2CO3溶液 取样,滴加适量的溶液
C 检验稀盐酸中是否含有硫酸 取样,滴加少量溶液
D 鉴别H2和CH4 分别点燃,在火焰上方罩一个干燥的烧杯
A.A B.B C.C D.D
11.逻辑推理是一种重要的化学思维方法,以下推理合理的是
A.纯碱溶液的pH>7,但pH>7的溶液不一定是碱溶液
B.酸碱中和反应属于复分解反应,则复分解反应一定是中和反应
C.金属离子与酸根离子组成的化合物叫盐,则盐中一定含金属离子
D.碳酸盐与盐酸反应产生气体,则与盐酸反应生成气体的物质一定是碳酸盐
12.下图为甲、乙、丙三种固体物质(不形成结晶水合物)在水中随温度变化的溶解度曲线,下列说法不正确的是
A.在t2℃时,甲和丙的溶解度相等
B.t1℃时,可以通过加水,将乙溶液的状态由M点变为N点
C.t3℃时,将40g甲放入50g水中,充分溶解后所得溶液的质量为90g
D.t3℃时,将125g丙的饱和溶液降温至t1℃,应再加入15g丙才能恰好达到饱和状态
二、填空与简答
13.我国是茶文化的发源地。唐代陆羽《茶经》中记载:“风炉以铜铁铸之……底一窗以为通飚漏烬之所……风能兴火,火能熟水。”“漉水囊……其格以生铜铸之、”
(1)“铜铁”属于 (填“金属”或“合成”)材料。
(2)“飚”(即风)提供燃烧所需的 。“烬”中含钾盐。农业上可用作 。
(3)“火能熟水”说明燃烧 (填“吸收”或“放出”)热量。
(4)茶香四溢,从分子角度解释其原因是 。
14.某工业废水,含有大量的ZnSO4和少量的CuSO4以及污泥。化学兴趣小组的同学想从中回收金属铜和硫酸锌晶体,他们设计了如下方案。
(1)操作a、b的名称是 ,用到的玻璃仪器有 (写一种)。
(2)步骤Ⅰ中加入过量的金属X的目的是 。
(3)步骤Ⅱ中发生反应的化学方程式是 。
(4)若溶液1和溶液2中溶质ZnSO4的质量分数分别表示为x和y,则x与y的大小关系是 。
三、实验题
15.结合图示实验装置,回答下列问题。
(1)图中仪器②的名称是 。
(2)实验室用A装置制取氧气,反应的化学方程式为 ;实验室制取氢气可选用D装置,也可用C装置替代,选用C装置的优点是 ;若用H装置收集氢气应从 (填“a”或“b”)端通入。
(3)常温下块状电石与水剧烈反应生成乙炔(C2H2)气体,已知乙炔难溶于水。实验室要用该反应制取乙炔气体,选用的发生和收集装置是 (填装置序号)。
四、科学探究题
16.学习了常见的碱,某同学想在实验室里用NaOH溶液制取Na2CO3溶液。
【查阅资料】①NaOH溶液中通入过量CO2,会发生两步反应且无明显现象。
第一步:生成Na2CO3;第二步:生成可溶于水的NaHCO3,反应原理为:Na2CO3+H2O+CO2=2NaHCO3。
②NaHCO3溶液煮沸时不会发生分解。
③NaHCO3+NaOH=Na2CO3+H2O。
④可溶于水。
【制取步骤】①量取两份50mL相同浓度的NaOH溶液备用。
②用一份50mLNaOH溶液吸收过量的CO2气体,至CO2气体不再溶解。
③小心煮沸②溶液1~2分钟。
④________________________,即得Na2CO3溶液。
【实验探究】为了检验制得的溶液是否为纯净的Na2CO3溶液,请你与该同学一起完成下列实验探究:
实验步骤 实验现象 实验结论
取少量制得的溶液于试管中,加入过量的 ⑤ 溶液 产生白色沉淀 制得的溶液中含有Na2CO3
将上步实验所得混合物进行过滤,将滤液分成两份 取其中一份加入足量的 ⑥ 无气泡产生 制得的溶液中不含 ⑦
取另外一份加入MgCl2溶液 ⑧ 制得的溶液中不含NaOH
【实验结论】所制得的溶液为纯净的Na2CO3溶液。
(1)学习了氢氧化钠的知识,写出一个氢氧化钠在生活中的用途: 。
(2)将步骤④补充完整: 。
(3)将实验探究中各空格补充完整:⑤ ,⑥ ,⑦ ,⑧ 。
【评价与反思】
(4)有人认为将实验步骤③④的顺序对调更合理,你认为是否可行?并说明理由: 。
(5)实验探究中加入MgCl2溶液检验溶液中不含NaOH,除了用MgCl2溶液还可以用 检验,现象是 。
五、计算题
17.实验室中有一包石灰石,化学活动小组同学为测定该石灰石中CaCO3(杂质不与酸反应也不溶于水)的含量,取20g样品于烧杯中,向其中加入足量的稀盐酸,测得生成的气体与加入稀盐酸的质量关系如图所示,请回答下列问题。
(1)求石灰石中碳酸钙的质量分数。
(2)若所得结果比实际值偏小,则可能的原因是 。
《安徽省合肥市2025年安师联盟中考安心卷理化试卷 -初中化学》参考答案
1.C
2.C
3.B
4.A
5.B
6.D
7.A
8.D 9.B
10.C
11.A
12.C
13.(1)金属材料
(2) 空气或氧气 钾肥
(3)放出
(4)分子在不断运动
14.(1) 过滤 玻璃棒/漏斗/烧杯
(2)确保Cu2+完全被置换(或把CuSO4反应完)
(3)
(4)
15.(1)长颈漏斗
(2) 可以控制反应的发生与停止 a
(3)BE
16.(1)除油污(或作清洁剂)
(2)在得到的③的溶液中加入另一份50mLNaOH溶液,使其充分混合
(3) CaCl2(或BaCl2) 稀盐酸 NaHCO3 无明显现象
(4)不可行,如果对调,溶液中过量的CO2会与NaOH反应,消耗NaOH,使NaHCO3不能全部转化为Na2CO3
(5) 酚酞溶液 若溶液变红,则说明制得的溶液中含NaOH(合理即可)
17.(1)解:设石灰石中碳酸钙的质量为x。
x=10g
石灰石中碳酸钙的质量分数为:
答:石灰石中碳酸钙的质量分数为50%。
(2)有部分二氧化碳溶解在水中(答案合理即可)
同课章节目录
