3.1.1 氯气的发现与制备 课后练(含解析)高中化学 必修1(苏教版2019)
文档属性
| 名称 | 3.1.1 氯气的发现与制备 课后练(含解析)高中化学 必修1(苏教版2019) |
|
|
| 格式 | doc | ||
| 文件大小 | 551.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-06-28 10:40:54 | ||
图片预览

文档简介
第一单元 氯气及氯的化合物
第1课时 氯气的发现与制备
【夯实基础】
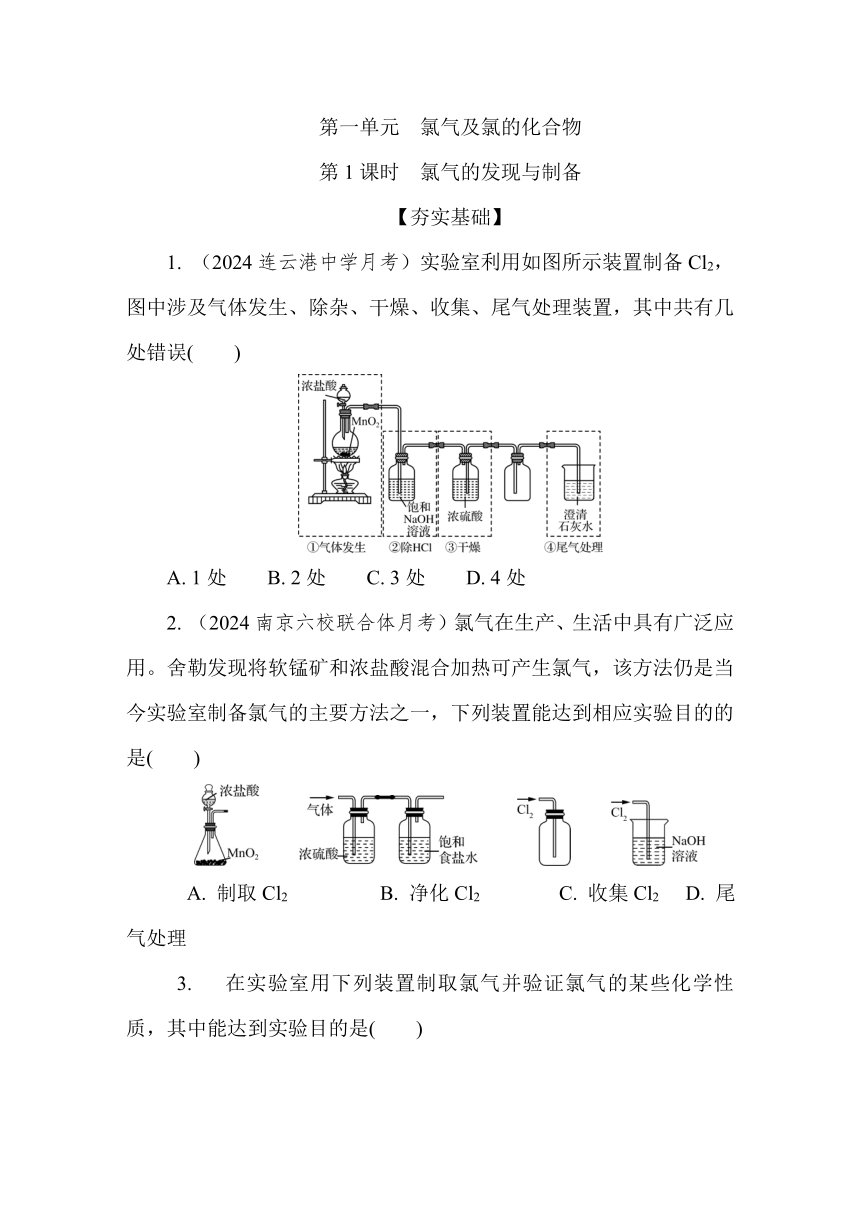
1. (2024连云港中学月考)实验室利用如图所示装置制备Cl2,图中涉及气体发生、除杂、干燥、收集、尾气处理装置,其中共有几处错误( )
A. 1处 B. 2处 C. 3处 D. 4处
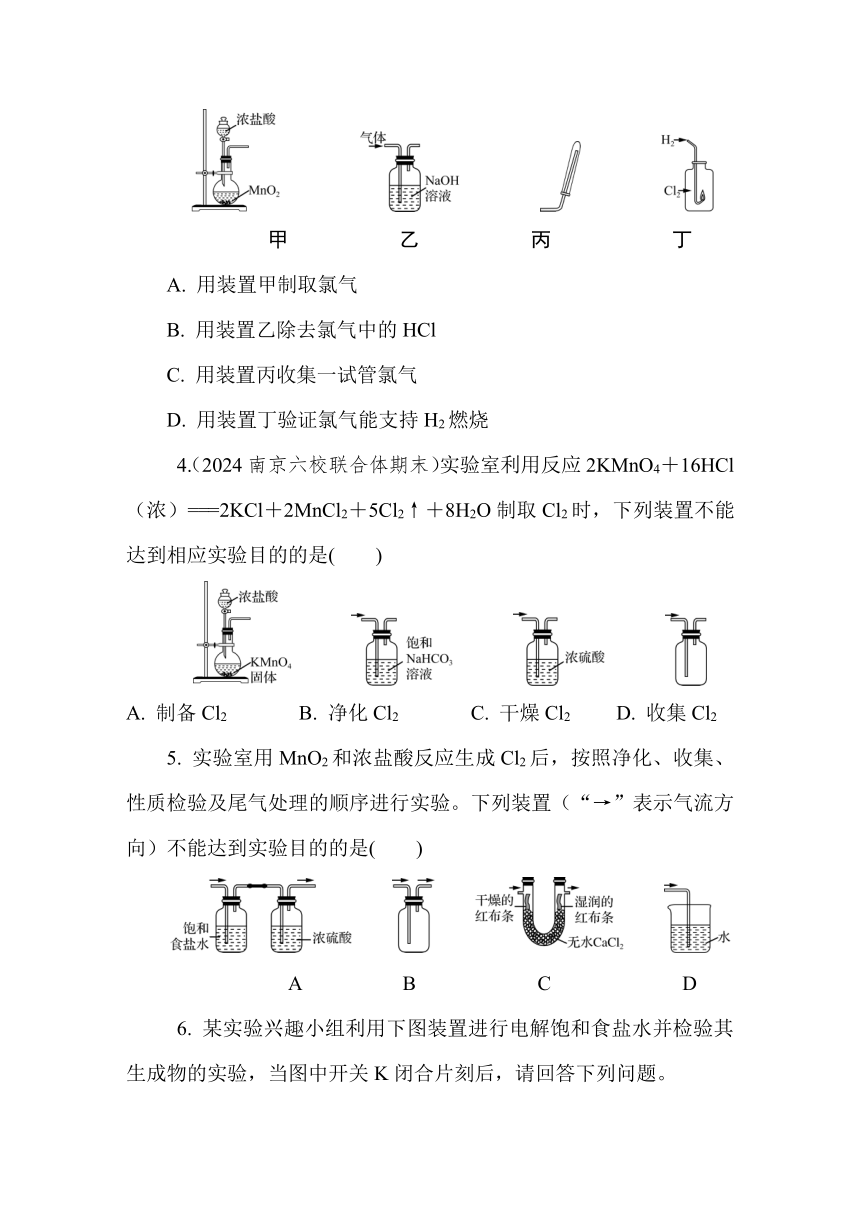
2. (2024南京六校联合体月考)氯气在生产、生活中具有广泛应用。舍勒发现将软锰矿和浓盐酸混合加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一,下列装置能达到相应实验目的的是( )
A. 制取Cl2 B. 净化Cl2 C. 收集Cl2 D. 尾气处理
3. 在实验室用下列装置制取氯气并验证氯气的某些化学性质,其中能达到实验目的是( )
甲 乙 丙 丁
A. 用装置甲制取氯气
B. 用装置乙除去氯气中的HCl
C. 用装置丙收集一试管氯气
D. 用装置丁验证氯气能支持H2燃烧
4.(2024南京六校联合体期末)实验室利用反应2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O制取Cl2时,下列装置不能达到相应实验目的的是( )
A. 制备Cl2 B. 净化Cl2 C. 干燥Cl2 D. 收集Cl2
5. 实验室用MnO2和浓盐酸反应生成Cl2后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
A B C D
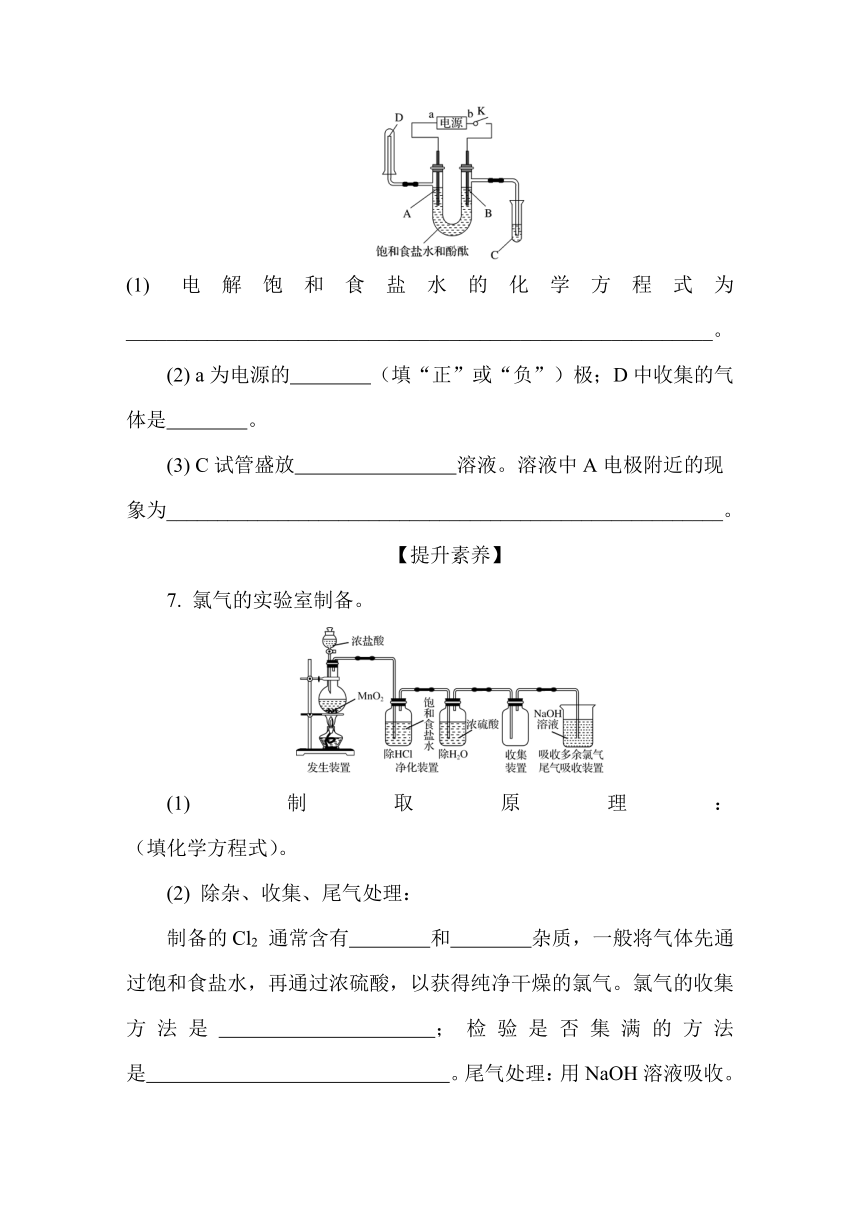
6. 某实验兴趣小组利用下图装置进行电解饱和食盐水并检验其生成物的实验,当图中开关K闭合片刻后,请回答下列问题。
(1) 电解饱和食盐水的化学方程式为__________________________________________________________。
(2) a为电源的 (填“正”或“负”)极;D中收集的气体是 。
(3) C试管盛放 溶液。溶液中A电极附近的现象为_______________________________________________________。
【提升素养】
7. 氯气的实验室制备。
(1) 制取原理: (填化学方程式)。
(2) 除杂、收集、尾气处理:
制备的Cl2 通常含有 和 杂质,一般将气体先通过饱和食盐水,再通过浓硫酸,以获得纯净干燥的氯气。氯气的收集方法是 ;检验是否集满的方法是 。尾气处理:用NaOH溶液吸收。
(3) 实验室中若无MnO2,可用固体KMnO4 代替,发生反应:2KMnO4+16HCl(浓)===2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的气体发生装置是 (填字母)。
a b c
8. 某研究性学习小组设计了用浓盐酸与二氧化锰反应制取氯气的实验,其实验装置如图所示。
(1) 如果将过量的二氧化锰与20 mL 12 mol/L的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要的原因有:
①____________________________________________;
②__________________________________________。
(2) L的作用是 ;B的作用是_____________________________________________________。
(3) 为了提高浓盐酸的利用率,你对实验的建议是________________________________________________。
第1课时 氯气的发现与制备
1. C 应选饱和食盐水除去HCl,②错误;用浓硫酸干燥气体时,气体应“长进短出”,③错误;澄清石灰水的浓度较低,处理Cl2的能力有限,可改用NaOH溶液,④错误。故选C。
由于浓盐酸易挥发,Cl2中的杂质气体有HCl、水蒸气,故无法收集到纯净干燥的Cl2。因为HCl极易溶于水,而Cl2在饱和食盐水中溶解度很小,故先用饱和食盐水除去HCl,再用浓硫酸进行干燥,就可获得纯净干燥的Cl2。除杂装置如图所示:
2. D 二氧化锰和浓盐酸在加热条件下制取Cl2,A错误;Cl2应该先除杂后干燥,B错误;装置为密闭装置,气体不能顺利进入,C错误;Cl2有毒,可以使用碱液吸收,D正确。
3. D 实验室用浓盐酸和二氧化锰制取氯气时需要加热,该装置中没有加热装置,A错误;除去氯气中的HCl气体用饱和食盐水,NaOH能与氯气反应,B错误;氯气的密度大于空气的,选用向上排空气法,C错误;装置丁可以用于验证氯气能支持氢气燃烧,发生反应H2+Cl22HCl,D正确。
4. B KMnO4和浓盐酸是固液不加热类型,可用该装置制备Cl2,A正确;浓盐酸易挥发出HCl杂质气体,盐酸和碳酸氢钠溶液反应生成二氧化碳气体,应用饱和食盐水洗气,B错误;浓硫酸具有吸水性,可干燥酸性气体,可用来干燥氯气,C正确;氯气的密度比空气的大,能溶于水且发生化学反应,可用向上排空气法收集氯气,D正确。
实验室制取Cl2的其他方法
可用KMnO4、K2Cr2O7、KClO3等氧化剂代替MnO2与浓盐酸反应(不需加热)。方程式如下:
2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O;
K2Cr2O7+14HCl(浓)===2KCl+2CrCl3+3Cl2↑+7H2O;
KClO3+6HCl(浓)KCl+3Cl2↑+3H2O。
5. D 浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl2可用浓硫酸干燥,A装置能达到实验目的,A不符合题意;氯气的密度大于空气的,用向上排空气法收集,B装置能收集氯气,B不符合题意;湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,C不符合题意;氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目的,D符合题意。
6. (1) 2NaCl+2H2O2NaOH+H2↑+Cl2↑
(2) 负 氢气(或H2) (3) 淀粉KI(或淀粉NaI等其他答案合理均可) 有气泡产生,溶液由无色变为红色
7. (1) MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O (2) HCl气体 水蒸气 向上排空气法 用湿润的淀粉-KI试纸置于集气瓶口,若试纸变蓝,则已收集满 (3) a
8. (1) ①反应中随着盐酸消耗,盐酸的浓度变稀,稀盐酸不能与MnO2反应 ②加热时有部分HCl挥发而损失 (2) 恒压条件下确保浓盐酸顺利滴下 利用Cl2在饱和食盐水中溶解度很小的性质来除去混有的HCl (3) 使浓盐酸慢慢滴下;加热时用小火慢慢加热等
实验室用MnO2和浓盐酸制Cl2时的注意事项
(1) 为了减少制得的Cl2中HCl的含量,加热温度不宜过高,以减少HCl的挥发。
(2) 因Cl-浓度越小,其还原性越弱,故必须用浓盐酸加热才可反应,稀盐酸不反应。
(3) 实验结束后,先使反应停止并排出残留的Cl2后,再拆卸装置,避免污染空气。
(4) 尾气吸收时,用NaOH溶液吸收Cl2,不能用澄清石灰水吸收,因为溶液中Ca(OH)2的含量少,吸收不完全。
第1课时 氯气的发现与制备
【夯实基础】
1. (2024连云港中学月考)实验室利用如图所示装置制备Cl2,图中涉及气体发生、除杂、干燥、收集、尾气处理装置,其中共有几处错误( )
A. 1处 B. 2处 C. 3处 D. 4处
2. (2024南京六校联合体月考)氯气在生产、生活中具有广泛应用。舍勒发现将软锰矿和浓盐酸混合加热可产生氯气,该方法仍是当今实验室制备氯气的主要方法之一,下列装置能达到相应实验目的的是( )
A. 制取Cl2 B. 净化Cl2 C. 收集Cl2 D. 尾气处理
3. 在实验室用下列装置制取氯气并验证氯气的某些化学性质,其中能达到实验目的是( )
甲 乙 丙 丁
A. 用装置甲制取氯气
B. 用装置乙除去氯气中的HCl
C. 用装置丙收集一试管氯气
D. 用装置丁验证氯气能支持H2燃烧
4.(2024南京六校联合体期末)实验室利用反应2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O制取Cl2时,下列装置不能达到相应实验目的的是( )
A. 制备Cl2 B. 净化Cl2 C. 干燥Cl2 D. 收集Cl2
5. 实验室用MnO2和浓盐酸反应生成Cl2后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
A B C D
6. 某实验兴趣小组利用下图装置进行电解饱和食盐水并检验其生成物的实验,当图中开关K闭合片刻后,请回答下列问题。
(1) 电解饱和食盐水的化学方程式为__________________________________________________________。
(2) a为电源的 (填“正”或“负”)极;D中收集的气体是 。
(3) C试管盛放 溶液。溶液中A电极附近的现象为_______________________________________________________。
【提升素养】
7. 氯气的实验室制备。
(1) 制取原理: (填化学方程式)。
(2) 除杂、收集、尾气处理:
制备的Cl2 通常含有 和 杂质,一般将气体先通过饱和食盐水,再通过浓硫酸,以获得纯净干燥的氯气。氯气的收集方法是 ;检验是否集满的方法是 。尾气处理:用NaOH溶液吸收。
(3) 实验室中若无MnO2,可用固体KMnO4 代替,发生反应:2KMnO4+16HCl(浓)===2MnCl2+2KCl+5Cl2↑+8H2O,则可选择的气体发生装置是 (填字母)。
a b c
8. 某研究性学习小组设计了用浓盐酸与二氧化锰反应制取氯气的实验,其实验装置如图所示。
(1) 如果将过量的二氧化锰与20 mL 12 mol/L的盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。其主要的原因有:
①____________________________________________;
②__________________________________________。
(2) L的作用是 ;B的作用是_____________________________________________________。
(3) 为了提高浓盐酸的利用率,你对实验的建议是________________________________________________。
第1课时 氯气的发现与制备
1. C 应选饱和食盐水除去HCl,②错误;用浓硫酸干燥气体时,气体应“长进短出”,③错误;澄清石灰水的浓度较低,处理Cl2的能力有限,可改用NaOH溶液,④错误。故选C。
由于浓盐酸易挥发,Cl2中的杂质气体有HCl、水蒸气,故无法收集到纯净干燥的Cl2。因为HCl极易溶于水,而Cl2在饱和食盐水中溶解度很小,故先用饱和食盐水除去HCl,再用浓硫酸进行干燥,就可获得纯净干燥的Cl2。除杂装置如图所示:
2. D 二氧化锰和浓盐酸在加热条件下制取Cl2,A错误;Cl2应该先除杂后干燥,B错误;装置为密闭装置,气体不能顺利进入,C错误;Cl2有毒,可以使用碱液吸收,D正确。
3. D 实验室用浓盐酸和二氧化锰制取氯气时需要加热,该装置中没有加热装置,A错误;除去氯气中的HCl气体用饱和食盐水,NaOH能与氯气反应,B错误;氯气的密度大于空气的,选用向上排空气法,C错误;装置丁可以用于验证氯气能支持氢气燃烧,发生反应H2+Cl22HCl,D正确。
4. B KMnO4和浓盐酸是固液不加热类型,可用该装置制备Cl2,A正确;浓盐酸易挥发出HCl杂质气体,盐酸和碳酸氢钠溶液反应生成二氧化碳气体,应用饱和食盐水洗气,B错误;浓硫酸具有吸水性,可干燥酸性气体,可用来干燥氯气,C正确;氯气的密度比空气的大,能溶于水且发生化学反应,可用向上排空气法收集氯气,D正确。
实验室制取Cl2的其他方法
可用KMnO4、K2Cr2O7、KClO3等氧化剂代替MnO2与浓盐酸反应(不需加热)。方程式如下:
2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O;
K2Cr2O7+14HCl(浓)===2KCl+2CrCl3+3Cl2↑+7H2O;
KClO3+6HCl(浓)KCl+3Cl2↑+3H2O。
5. D 浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl2可用浓硫酸干燥,A装置能达到实验目的,A不符合题意;氯气的密度大于空气的,用向上排空气法收集,B装置能收集氯气,B不符合题意;湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,C不符合题意;氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目的,D符合题意。
6. (1) 2NaCl+2H2O2NaOH+H2↑+Cl2↑
(2) 负 氢气(或H2) (3) 淀粉KI(或淀粉NaI等其他答案合理均可) 有气泡产生,溶液由无色变为红色
7. (1) MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O (2) HCl气体 水蒸气 向上排空气法 用湿润的淀粉-KI试纸置于集气瓶口,若试纸变蓝,则已收集满 (3) a
8. (1) ①反应中随着盐酸消耗,盐酸的浓度变稀,稀盐酸不能与MnO2反应 ②加热时有部分HCl挥发而损失 (2) 恒压条件下确保浓盐酸顺利滴下 利用Cl2在饱和食盐水中溶解度很小的性质来除去混有的HCl (3) 使浓盐酸慢慢滴下;加热时用小火慢慢加热等
实验室用MnO2和浓盐酸制Cl2时的注意事项
(1) 为了减少制得的Cl2中HCl的含量,加热温度不宜过高,以减少HCl的挥发。
(2) 因Cl-浓度越小,其还原性越弱,故必须用浓盐酸加热才可反应,稀盐酸不反应。
(3) 实验结束后,先使反应停止并排出残留的Cl2后,再拆卸装置,避免污染空气。
(4) 尾气吸收时,用NaOH溶液吸收Cl2,不能用澄清石灰水吸收,因为溶液中Ca(OH)2的含量少,吸收不完全。
