2025-2026学年厦门一中《化学》初高中衔接课件:灵活多变的新法——化学计算
文档属性
| 名称 | 2025-2026学年厦门一中《化学》初高中衔接课件:灵活多变的新法——化学计算 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-04 00:00:00 | ||
图片预览




文档简介
(共12张PPT)
灵活多变的新法——化学计算
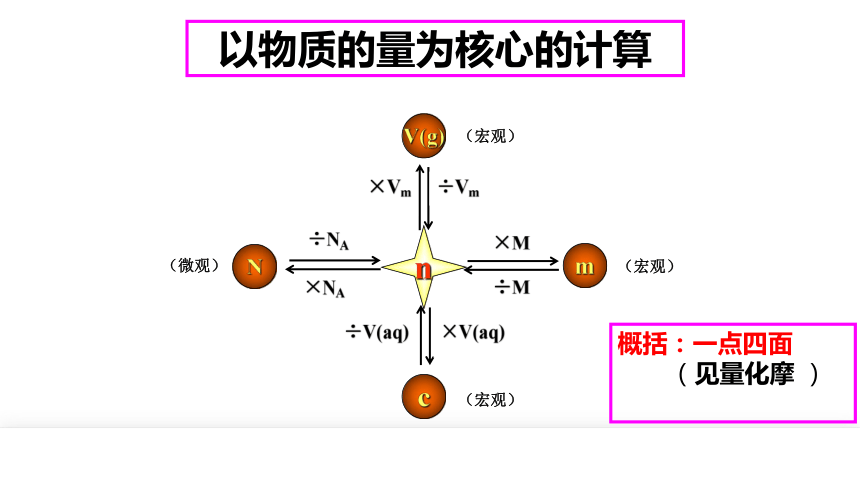
以物质的量为核心的计算
n
m
V(g)
N
c
×NA
×Vm
÷Vm
÷NA
×V(aq)
÷V(aq)
×M
÷M
(宏观)
(宏观)
(宏观)
(微观)
概括:一点四面
(见量化摩 )
1、物 质 的 量
2、阿伏伽德罗常数
3、摩 尔 质 量
4、气体摩尔体积
5、物质的量浓度
基本概念
一、理清概念体系,重在理解记忆
二、物质的量与微粒之间的相互关系计算
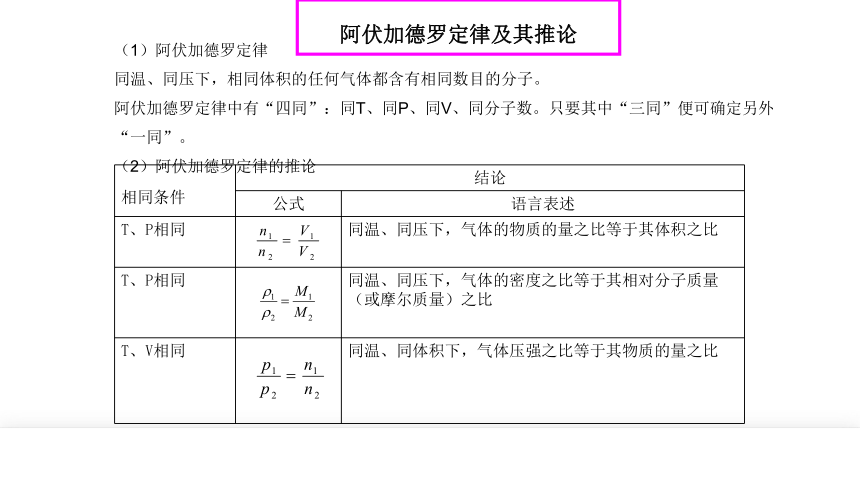
(1)阿伏加德罗定律
同温、同压下,相同体积的任何气体都含有相同数目的分子。
阿伏加德罗定律中有“四同”:同T、同P、同V、同分子数。只要其中“三同”便可确定另外“一同”。
(2)阿伏加德罗定律的推论
相同条件 结论 公式 语言表述
T、P相同 同温、同压下,气体的物质的量之比等于其体积之比
T、P相同 同温、同压下,气体的密度之比等于其相对分子质量(或摩尔质量)之比
T、V相同 同温、同体积下,气体压强之比等于其物质的量之比
阿伏加德罗定律及其推论
化学计量数(γ ) 之比
扩大NA倍
物质的量(n)之比
2Na+2H2O=2NaOH+H2↑
2
2
2
:
:
:
1
2NA
2NA
2NA
:
:
NA
:
2mol
2mol
2mol
:
:
1mol
:
化 学 计 量 数 之 比
物 质 的 量 之 比
=
微粒数之比
2个 : 2个 : 2个 : 1个
二、物质的量应用于化学方程式的计算
二、物质的量应用于化学方程式的计算
根据化学方程式计算的步骤
设
设未知数
写
写化学方程式
标
标出已知量和未知量
列
列比例式
解
解出未知数
答
简明地写出答案
三、思维建模:
二、物质的量应用于化学方程式的计算
(1)根据化学方程式确定关系式。
3CO+Fe2O3 2Fe+3CO2,
CO2+Ca(OH)2 == CaCO3↓+H2O
则3CO~3CO2~3CaCO3,即CO~CaCO3。
(2)根据原子守恒确定关系式。 根据碳原子守恒得出CO~CaCO3。
△
====
1.关系式法
当已知物和未知物之间是靠多个反应来联系时,只需直接确定已知量和未知量之间的比例关系。
四、化学计算方法简介
2.守恒法
质 量 守 恒
反应前后元素质量、原子个数不变
得失电子守恒
还原剂失电子总数=氧化剂得电子总数
电 荷 守 恒
阳离子所带正电荷总数=阴离子所带负电荷总数
根据化学反应前后物质的有关物理量发生的变化,找出所谓“理论差量”,如反应前后的质量、物质的量、气体体积等。
该差量的大小与反应物质的有关量成正比。
3.差量法
灵活多变的新法——化学计算
以物质的量为核心的计算
n
m
V(g)
N
c
×NA
×Vm
÷Vm
÷NA
×V(aq)
÷V(aq)
×M
÷M
(宏观)
(宏观)
(宏观)
(微观)
概括:一点四面
(见量化摩 )
1、物 质 的 量
2、阿伏伽德罗常数
3、摩 尔 质 量
4、气体摩尔体积
5、物质的量浓度
基本概念
一、理清概念体系,重在理解记忆
二、物质的量与微粒之间的相互关系计算
(1)阿伏加德罗定律
同温、同压下,相同体积的任何气体都含有相同数目的分子。
阿伏加德罗定律中有“四同”:同T、同P、同V、同分子数。只要其中“三同”便可确定另外“一同”。
(2)阿伏加德罗定律的推论
相同条件 结论 公式 语言表述
T、P相同 同温、同压下,气体的物质的量之比等于其体积之比
T、P相同 同温、同压下,气体的密度之比等于其相对分子质量(或摩尔质量)之比
T、V相同 同温、同体积下,气体压强之比等于其物质的量之比
阿伏加德罗定律及其推论
化学计量数(γ ) 之比
扩大NA倍
物质的量(n)之比
2Na+2H2O=2NaOH+H2↑
2
2
2
:
:
:
1
2NA
2NA
2NA
:
:
NA
:
2mol
2mol
2mol
:
:
1mol
:
化 学 计 量 数 之 比
物 质 的 量 之 比
=
微粒数之比
2个 : 2个 : 2个 : 1个
二、物质的量应用于化学方程式的计算
二、物质的量应用于化学方程式的计算
根据化学方程式计算的步骤
设
设未知数
写
写化学方程式
标
标出已知量和未知量
列
列比例式
解
解出未知数
答
简明地写出答案
三、思维建模:
二、物质的量应用于化学方程式的计算
(1)根据化学方程式确定关系式。
3CO+Fe2O3 2Fe+3CO2,
CO2+Ca(OH)2 == CaCO3↓+H2O
则3CO~3CO2~3CaCO3,即CO~CaCO3。
(2)根据原子守恒确定关系式。 根据碳原子守恒得出CO~CaCO3。
△
====
1.关系式法
当已知物和未知物之间是靠多个反应来联系时,只需直接确定已知量和未知量之间的比例关系。
四、化学计算方法简介
2.守恒法
质 量 守 恒
反应前后元素质量、原子个数不变
得失电子守恒
还原剂失电子总数=氧化剂得电子总数
电 荷 守 恒
阳离子所带正电荷总数=阴离子所带负电荷总数
根据化学反应前后物质的有关物理量发生的变化,找出所谓“理论差量”,如反应前后的质量、物质的量、气体体积等。
该差量的大小与反应物质的有关量成正比。
3.差量法
同课章节目录
