1.1物质的分类及转化 练习 (含解析) 高中化学 人教版(2019) 必修 第一册
文档属性
| 名称 | 1.1物质的分类及转化 练习 (含解析) 高中化学 人教版(2019) 必修 第一册 |

|
|
| 格式 | doc | ||
| 文件大小 | 3.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-04 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第一单元 物质的分类及转化(含答案)
测试时间:75 分钟 满分:100分
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32
一、选择题(本题包括15个小题,每小题3分,共45分,除标明外,每小题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案
1.[2025·黄冈中学月考]下列物质可与其他物质直接反应生成盐的是 ( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A.①②③ B.①④⑥ C.②⑤⑥ D.①②③④⑤⑥
2.[2025·成都外国语学校期中]X、Y、Z、W各代表一种物质,若它们之间能发生反应 X+Y→ 则X 与 Y 发生的不可能是 ( )
A.酸与碱的反应 B.碱性氧化物与酸的反应
C.盐与盐的反应 D.酸性氧化物与水的反应
3.已知由 溶液和稍过量的KI溶液可制得 AgI胶体,当它与 胶体相混合时,能析出 AgI 和 Fe(OH) 的混合沉淀,由此可知 ( )
A.该 AgI胶粒能通过半透膜 B.该AgI胶体带负电荷
C.该AgI胶体发生电泳时,胶粒向某一极移动 D.该AgI胶体是一种纯净物
4.[2022 杭州二中高一检测]用激光笔照射果冻,会形成一条光亮的“通路”,说明果冻属于 ( )
A.溶液 B.胶体 C.悬浊液 D.乳浊液
5. 生产生活中的许多现象或应用都与化学知识有关。下列现象或应用与胶体性质无关的是( )
A.将盐卤或石膏加入豆浆中,制成豆腐
B.冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
C.泡沫灭火器中将. 与 溶液混合后,喷出大量泡沫,起到灭火作用
D.清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象
6.[2022辽宁省沈阳市高一期末]如图所示,根据分散质粒子的直径大小可以对分散系进行分类。下列分散系中不属于分散系Ⅱ的是 ( )
A、氢氧化铜悬浊液 B.云 C.有色玻璃 D.雾
7.[2025·怀仁一中期中]甲、乙、丙三种物质间通过一步反应能实现如图所示的转化,下列选项中符合转化关系的是 ( )
A.甲为NaOH,乙为NaCl,丙为
B.甲为CuO,乙为 丙为
C.甲为 乙为 丙为
D.甲为 乙为 丙为
8.[2025·宝鸡中学月考]下图中相邻两种物质均可归为一类,甲、乙、丙、丁为物质的四种类别,下列分类正确的是 ( )
A.甲类两种物质的水溶液都呈碱性
B.乙类两种物质都是碱性氧化物
C.丙类两种物质都是钠盐
D.丁类两种物质都是硫酸盐
9.[2025·深圳中学月考]下列说法中正确的是 ( )
A.由一种元素组成的物质一定是纯净物
是混合物
C.酸性氧化物一定是非金属氧化物,非金属氧化物不一定是酸性氧化物
D.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
10.[双选][名师改编]晋代炼丹家葛洪所著《抱朴子》是中国为世界科技花园贡献出的一颗璀璨明珠,书中有记载:“丹砂烧之成水银,积变又还成丹砂。”这句话中的丹砂指的是HgS,下列关于这句话的说法正确的是( )
A.该过程只涉及物理变化 B.“积变又还成丹砂”是化合反应
C.该过程中发生了复分解反应 D.“丹砂烧之成水银”过程中产生S
11.[2025·天津静海区模拟]以下表示的是碳及其化合物的相互转化关系(部分反应条件已略去): 其中涉及的基本反应类型依次为 ( )
A.置换反应、化合反应、分解反应、复分解反应
B.置换反应、化合反应、复分解反应、分解反应
C.化合反应、置换反应、分解反应、复分解反应
D.化合反应、置换反应、复分解反应、分解反应
12.[双选][名师改编]如图是小红学习《常见的碱》课题后,总结出的氢氧化钙化学性质的部分内容。下列说法不正确的是 ( )
A.①中不能使酚酞溶液变色
B.②中与 HCl反应的化学方程式为
C.③中能与 溶液发生反应
D.④可解释久置的澄清石灰水变质的原因
13.下列有关物质的分类及反应均正确的是( )
A.碳酸钙属于盐,可用于实验室制
B.铁属于活泼金属单质,可用于实验室制
C.纯碱属于碱,可与稀盐酸发生反应:
D.烧碱属于碱,可与稀硫酸发生反应:
14.[2025·成都一中期中]下列关于胶体的叙述不正确的是 ( )
A.胶体区别于其他分散系的本质特征是具有丁达尔效应
B.用渗析法可以除去 胶体中的NaCl
C.往 胶体中逐滴加入稀硫酸,开始时会出现沉淀,再继续滴加稀硫酸,沉淀又会溶解直至消失
D.用盐卤点豆腐、河海交汇处可沉积成沙洲、血液透析等都与胶体性质有关
15.[2022 武汉二中高一月考]人体中99%的钙储存在骨骼、牙齿中,还有1%的钙储存在血液和软组织等中。血液和软组织中的钙非常重要,参与生理活动。部分钙及其化合物之间的转化关系如图所示,下列说法正确的是( )
A.图中的物质中有三种属于氧化物
B.电解熔融氯化钙得到钙的反应属于化合反应
C.④、⑤中一定有水生成
D. Ca能在 Cl 中燃烧,该反应说明燃烧不一定需要氧气
二、非选择题(本题包含7小题,共55分)
16.(12分)[2025·亳州一中月考]硫酸、碳酸钠、二氧化碳、铜片、氢氧化钡、氢氧化钠、铁片、
生石灰和木炭粉9种物质中的几种存在如图所示的关系,选择适当的物质,使连线的两种物质能发生反应(酸、碱、盐均配制成稀溶液)。
(1)写出下列物质的化学式。
① ;② ;③ ;④ 。
(2)写出下列序号对应物质之间发生反应的化学方程式。
①与②: ;
②与④: ;
②与⑤: ;
④与⑤: 。
17.(6分)现有如下各实验:
①将1g KCl加入99g水中;
②将1g可溶性淀粉加入100g水中,搅拌均匀后煮沸;
③将 粉末加入 100 g水中,充分振荡;
④将0.1g 植物油加入10g水中,充分振荡混匀;
⑤将96 mL酒精与5 mL水充分混合。
其中所得到的分散系,属于溶液的有 (填序号,下同),属于胶体的有 ,
属于浊液的有 。
18.(6分)[2025·苏州中学月考]某课外活动小组进行 胶体的制备实验并检验其性质。
(1)若将 饱和溶液分别滴入下列物质中,能形成胶体的是 (填字母)。
A.冷水 B.沸水
C.浓 NaOH溶液 D.饱和食盐水
(2)写出制备 胶体的化学方程式: 。
(3)怎样检验所得的分散系是胶体 。
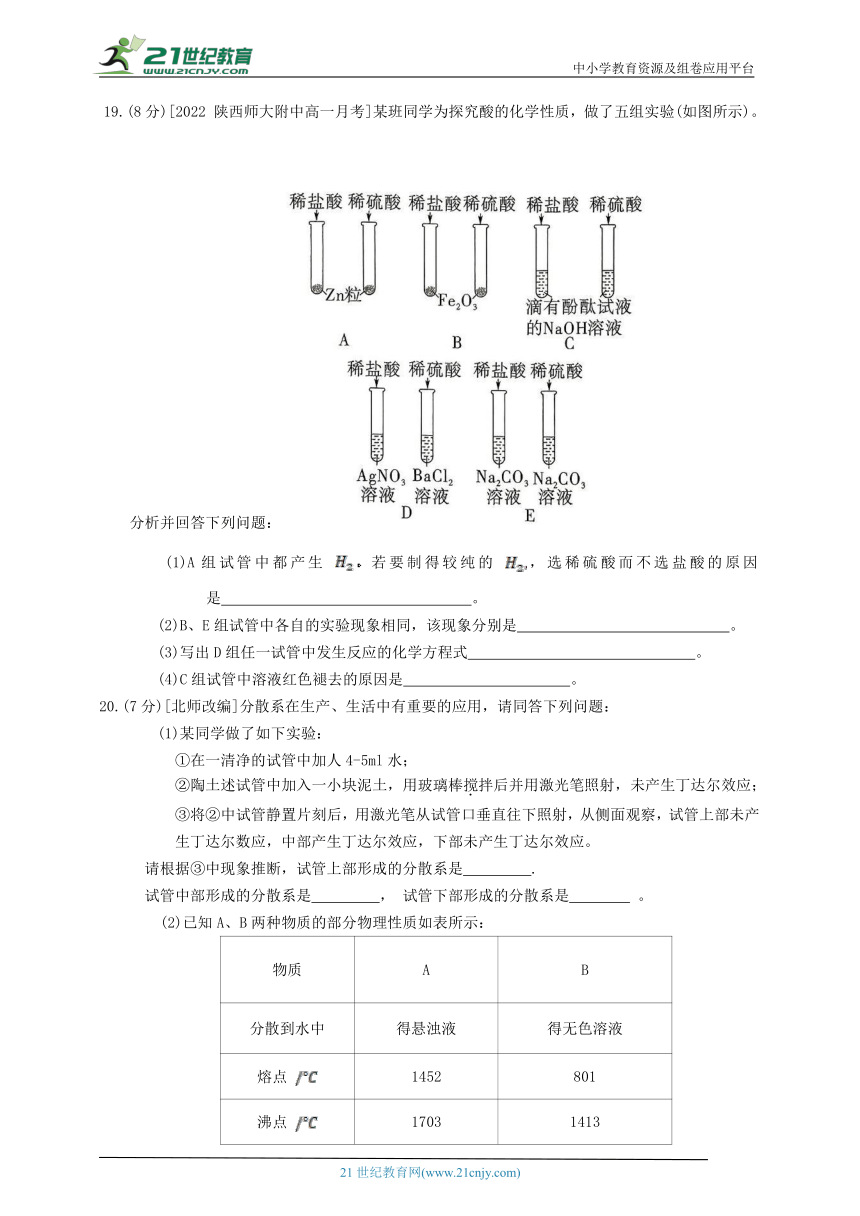
19.(8分)[2022 陕西师大附中高一月考]某班同学为探究酸的化学性质,做了五组实验(如图所示)。
分析并回答下列问题:
(1)A组试管中都产生 若要制得较纯的 ,选稀硫酸而不选盐酸的原因是 。
(2)B、E组试管中各自的实验现象相同,该现象分别是 。
(3)写出D组任一试管中发生反应的化学方程式 。
(4)C组试管中溶液红色褪去的原因是 。
20.(7分)[北师改编]分散系在生产、生活中有重要的应用,请同答下列问题:
(1)某同学做了如下实验:
①在一清净的试管中加人4-5ml水;
②陶土述试管中加入一小块泥土,用玻璃棒搅拌后并用激光笔照射,未产生丁达尔效应;③将②中试管静置片刻后,用激光笔从试管口垂直往下照射,从侧面观察,试管上部未产生丁达尔数应,中部产生丁达尔效应,下部未产生丁达尔效应。
请根据③中现象推断,试管上部形成的分散系是 .
试管中部形成的分散系是 , 试管下部形成的分散系是 。
(2)已知A、B两种物质的部分物理性质如表所示:
物质 A B
分散到水中 得悬浊液 得无色溶液
熔点 1452 801
沸点 1703 1413
①已知A与B不能反应,且 A、B均不能与水反应。欲从 A、B的混合物中分离出B,需进行的三步操作是:a.溶解;
b. (填操 作 名 称,下同 );
c. .
②上述a、b、c操作过程中均需用到的一种玻璃仪器为 。
③将 A、B分别加入水中,所得分散系中分散质粒子直径较大的是 (填“A”或“B”)。
21.(8分)[2022 重庆八中高一月考]氢氧化钙俗称熟石灰或消石灰,是一种白色粉末状固体,将石灰乳(主要成分为氢氧化均铜溶液按照一定的比例混合可配制农药波尔多液。
如图1.树木过冬防虫,树木根部以上可涂石灰浆。如图2,工业上常利用石灰窑制备氢氧化钙、具体过程如下:
将石灰石煅烧成氧化钙后,经精选,与水按1:(3~3.5)的比例混合,生成氢氧化钙料液,经净化分离除渣,再经离心脱水,干燥,即得氢氧化钙成品。
根据上述材料,回答下列问题:
(1)选择上述短文中提供的物质,完成下表(每空仅填一种物质)。
类别 混合物 碱 碱性氧化物
名称
化学式 —
(2)制波尔多液时 (填“能”或“不能”)用铁桶作容器。
(3)写出工业上制备氢氧化钙的化学方程式,并注明
物质类别: 。
示例:A(氧化物)· (氧化物)══C(盐)
(4)请写出与题中不同的制备氢氧化钙的方法,并说明题中工业生产方法的优点。
制备方法: (用化学方程式表示)。
优点: (写一个即可)。
22.(8分)[2025·珠海一中月考]A、B、C、D、E五种物质均为中学化学中常见的化合物,已知A、B、C、D、E五种物质里含有相同的一种金属元素,并且A、B、C、D都可与物质M反应生成E,物质之间按箭头方向都可通过一步反应实现转化。实验室通常用碱B的澄清溶液检验
回答下列问题:
(1)写出物质的化学式:A为 、B为 、C为 。
(2)M属于 (选填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
(3)写出正盐C转化为酸式盐D的化学方程式: 。
(4)写出碱 B转化为酸式盐D的化学方程式: 。
第一单元 物质的分类及转化参考答案
1.D 【解析】非金属单质和酸分别与金属单质反应、碱性氧化物和碱分别与酸反应、酸性氧化物和酸分别与碱反应都可以生成盐。
2.D 【解析】酸与碱反应生成盐和水,碱性氧化物与酸反应生成盐和水,盐与盐可能发生复分解反应生成两种盐,均符合反应特征;酸性氧化物与水发生化合反应生成酸,不符合反应特征,故选D项。
3. C 【解析】AgI胶体与 Fe(OH) 胶体相混合时,能析出AgI和 Fe(OH) 的混合沉淀,这是发生了胶体的聚沉,说明AgI和 Fe(OH) 的胶粒带相反电荷,因为 Fe(OH) 胶粒带正电,所以 AgI胶粒带负电。AgI胶粒直径为1~100mm,不能通过半透膜,A不符合题意;结合以上分析可知,AgI胶粒带负电,胶体不带电荷,B不符合题意;AgI胶粒带负电,发生电泳时,胶粒向阳极移动,C符合题意;AgI胶体是一种分散系,为混合物,D不符合题意。
4. B 【解析】 胶体能产生丁达尔效应,即用激光笔照射胶体,可看到一条光亮的“通路”,故果冻属于胶体,B项正确。
5. C 【解析】豆浆属于胶体,在电解质盐卤或石膏的作用下发生凝聚制成豆腐,A不符合题意;烟尘为气溶胶,其中胶粒带电荷,在电流作用下移向电极,B不符合题意;泡沫灭火器中将. 与 两溶液混合后, 与 水解且互相促进至水解完全: 在 的作用下喷出大量泡沫,起到灭火作用,与胶体性质无关,C符合题意;该景象是胶体的丁达尔效应,D不符合题意。
6. A 【解析】 根据分散质粒子的直径大小可以将分散系分为溶液、胶体和浊液,分散质粒子的直径为1 ~100 nm 的分散系为胶体,即为分散系Ⅱ,分散质粒子的直径小于1 nm的分散系为溶液,即为分散系Ⅰ,分散质粒子的直径大于100 nm的分散系为浊液,即为分散系Ⅲ。氢氧化铜悬浊液为浊液,属于分散系Ⅲ,云、有色玻璃、雾均为胶体,属于分散系Ⅱ,则不属于分散系Ⅱ的是氢氧化铜悬浊液,本题选 A。
7. C 【解析】NaOH 属于碱,NaCl 和 属于盐,与对应的酸发生反应可使碱转化为盐,要使盐转化为另一种盐,需要满足复分解反应发生的条件,即生成沉淀、放出气体或生成水,NaCl与. 反应生成AgCl沉淀和 可以实现 NaCl到 的转化,但是 不能与其他物质反应生成NaCl,无法实现图示的转化,故A不符合题意; 可通过与碱反应转化为( 而CuO 不能一步转化成 故B不符合题意; 与稀盐酸反应可生成( 或 与 反应可生成 高温分解生成 能通过一步反应实现图示的转化,故C符合题意; 可与 溶液反应生成 但 不能一步转化为 ,故D不符合题意。
8. D 【解析】甲类物质中NH 的水溶液呈碱性,SO 的水溶液呈酸性,A不正确;乙类物质中 Na O是碱性氧化物,SO 是酸性氧化物,B不正确;丙类物质中Na O是钠的氧化物, 是钠盐,C不正确;丁类物质中 是硫酸的钠盐, 是硫酸的钾盐,两种物质都是硫酸盐,D正确。
9. D 【解析】A项,如O 与O 均由一种元素组成,但由它们组成的物质是混合物,错误。B项,带有结晶水的盐属于纯净物, 是纯净物,错误。C项,酸性氧化物不一定是非金属氧化物,如 是酸性氧化物,非金属氧化物不一定是酸性氧化物,如CO不是酸性氧化物,错误。D项,碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物,如 是酸性氧化物,正确。
10. BD 【解析】 “丹砂烧之成水银”过程中HgS 分解为S和 Hg,为分解反应;“积变又还成丹砂”过程中S和 Hg反应生成HgS,为化合反应,据此分析解答。
HgS 的分解和生成都是化学变化,A项错误;由全景分析可知,B、D项正确,C项错误。
11. B 【解析】碳与氧化铜发生置换反应生成铜和二氧化碳;二氧化碳溶于水,并与水发生化合反应生成碳酸:碳酸与氢氧化钙发生复分解反应生成碳酸钙和水:碳酸钙高温分解生成氧化钙和二氧化碳,或碳酸钙与盐酸发生复分解反应生成氯化钙、水和二氧化碳,故B项符合题意。
12. AC 【解析】
选项 分析 结论
A 属于碱,能使酚酞溶液变红 错误
B 与 HCl发生酸碱中和反应: 正确
C 与 溶液不反应 错误
D 与非金属氧化物( 发生反应而变质: 正确
13.D 【解析】A项,实验室制 是利用碳酸钙与盐酸反应;B项,铁与 HCl反应的化学方程式为 H ↑;C项,纯碱属于盐,不属于碱。
14. A 【解析】胶体区别于其他分散系的本质特征是分散质粒子大小不同,故A 错误;胶体粒子不能通过半透膜,用渗析法可以除去 胶体中的 NaCl,故 B 正确;
Fe(OH) 胶体中逐滴加入稀硫酸,开始时发生聚沉出现氢氧化铁沉淀,再继续滴加稀硫酸,氢氧化铁与硫酸反应生成硫酸铁和水,所以沉淀又会溶解直至消失.故C 正确;用盐卤点豆腐、河海交汇处可沉积成沙洲与胶体聚沉有关,血液透析利用的是胶体渗析原理,故D正确。
15. D 【解析】 图中的物质中只有氧化钙属于氧化物,A项错误;电解熔融氯化钙得到钙和氯气的反应属于分解反应,B项错误;④可以通过氢氧化钙与碳酸钠反应实现,生成物是
碳酸钙和氢氧化钠,没有水生成,⑤可以通过氢氧化钙和氯化镁反应实现,生成物是氯化钙和氢氧化镁,也没有水生成,C项错误;钙在氯气中燃烧生成氯化钙,此燃烧过程中没有氧气参与,说明燃烧不一定需要氧气,D项正确。
16.
【解析】9种物质中只有一种酸,其化学式为 H SO ,Cu、Fe、C三种单质中,只有 Fe能与稀硫酸反应,二者反应生成 和 ,故①为 Fe,②为 ; 碱 有 NaOH、 只有 属于盐,而NaOH不能与 反应,故④为 ⑤为 ③应该为酸性氧化物,则为
17. ①⑤ ② ③④
【解析】①分散质KCl 溶于水后以离子形式存在,粒子直径小于1 nm,属于溶液;②淀粉分子大,溶于水并煮沸后,形成的是胶体;( 不溶于水,加入水中振荡所形成的是不稳定的体系,放置后生成沉淀,所以属于悬浊液;④植物油不溶于水,形成的是乳浊液;⑤分散质是酒精,分散剂是水,二者以任意比混溶,形成溶液。
18. (1)B
(胶体)+3HCl
(3)用激光笔照射,若有一条光亮的通路,则制得的分散系是胶体
19. (Ⅰ)反应放出的热会使盐酸挥发出 HCl 气体,使制得的1 ,不纯
(2)固体逐渐消失,溶液变为棕黄色;有气泡产生
(或
(4)NaOH与酸发生中和反应
【解析】 (1)反应放出的热会使盐酸挥发出 HCl气体,使制得的 不纯净,而反应放出的热不能使稀硫酸挥发,因此要制得较纯的 ,应选稀硫酸。 ( 属于碱性氧化物,能与稀盐酸反应生成 和 ,与稀硫酸反应生成 和 生成的 溶液、 溶液均显棕黄色,因此会观察到固体逐渐消失,溶液变成棕黄色; 能与稀盐酸或稀硫酸反应生成( ,因此会观察到有气泡产生。(3)稀盐酸与 溶液反应产生AgCl白色沉淀,反应的化学方程式为 稀硫酸与 溶液反应产生 白色沉淀,反应的化学方程式为 (4)NaOH与稀盐酸或稀硫酸发生中和反应,碱被消耗,溶液红色褪去。
20. (1)溶液 胶体 悬浊液
(2)①过滤 蒸发 ②玻璃棒 ③A
【解析】 (1)将泥土加入水中,搅拌,静置一段时间后,上部为澄清的溶液,其分散质粒子的直径小于1 nm,不能产生丁达尔效应;中部为胶体,其分散质粒子的直径为1 ~100 nm,能产生丁达尔效应;下部为悬浊液,其分散质粒子的直径大于 100 nm,不能产生丁达尔效应。
(2)①根据A与B的性质可知,A、B均为固体,A不溶于水,而B 能溶于水,所以从 A 与B的混合物中分离出B,可以先加水溶解,再过滤出A,然后通过蒸发即可得到 B。②在溶解、过滤和蒸发时都需要用到玻璃棒。③分散质粒子的直径:悬浊液>溶液。
21.(1)(合理即可)
类别 混合物 碱 碱性氧化物
名称 石灰乳 氢氧化钙 氧化钙
化学式 —— CaO
(2)不能
(盐) (氧化物) (氧化物)↑,
CaO(氧化物) (氧化物)=== Ca(OH) (碱)
2CaO (其他合理答案也可, 原料来源丰富、原料价格低廉或生产成本低等(写一个即可)
【解析】(Ⅰ)短文中提供了多种混合物,如波尔多液、石灰乳等,氮氧化钙为碱,氧化钙为碱性氧化物。(2)制波尔多液的原料中有 溶液,而Fe能与发生置换反应,故不能用铁桶作容器。(3)工业上制备 的反应为
为盐,CaO、 均为氧化物,为碱。
(4)分析可知,题中工业制法有原料(石灰石)来源丰富、原料价格低廉、生产成本低等优点。
22 .(1)CaO Ca(OH) CaCO CaCl 或
(2)酸
【解析】实验室通常用碱 B的澄清溶液检验( ,即 B 为 则A为CaO;D为酸式盐,说明D为( 则C为( 都可以与盐酸(或硝酸)反应生成氯化钙(或硝酸钙),故E 为氯化钙或硝酸钙。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
第一单元 物质的分类及转化(含答案)
测试时间:75 分钟 满分:100分
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32
一、选择题(本题包括15个小题,每小题3分,共45分,除标明外,每小题只有一个选项符合题意)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案
1.[2025·黄冈中学月考]下列物质可与其他物质直接反应生成盐的是 ( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A.①②③ B.①④⑥ C.②⑤⑥ D.①②③④⑤⑥
2.[2025·成都外国语学校期中]X、Y、Z、W各代表一种物质,若它们之间能发生反应 X+Y→ 则X 与 Y 发生的不可能是 ( )
A.酸与碱的反应 B.碱性氧化物与酸的反应
C.盐与盐的反应 D.酸性氧化物与水的反应
3.已知由 溶液和稍过量的KI溶液可制得 AgI胶体,当它与 胶体相混合时,能析出 AgI 和 Fe(OH) 的混合沉淀,由此可知 ( )
A.该 AgI胶粒能通过半透膜 B.该AgI胶体带负电荷
C.该AgI胶体发生电泳时,胶粒向某一极移动 D.该AgI胶体是一种纯净物
4.[2022 杭州二中高一检测]用激光笔照射果冻,会形成一条光亮的“通路”,说明果冻属于 ( )
A.溶液 B.胶体 C.悬浊液 D.乳浊液
5. 生产生活中的许多现象或应用都与化学知识有关。下列现象或应用与胶体性质无关的是( )
A.将盐卤或石膏加入豆浆中,制成豆腐
B.冶金厂常用高压电除去烟尘,是因为烟尘微粒带电荷
C.泡沫灭火器中将. 与 溶液混合后,喷出大量泡沫,起到灭火作用
D.清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象
6.[2022辽宁省沈阳市高一期末]如图所示,根据分散质粒子的直径大小可以对分散系进行分类。下列分散系中不属于分散系Ⅱ的是 ( )
A、氢氧化铜悬浊液 B.云 C.有色玻璃 D.雾
7.[2025·怀仁一中期中]甲、乙、丙三种物质间通过一步反应能实现如图所示的转化,下列选项中符合转化关系的是 ( )
A.甲为NaOH,乙为NaCl,丙为
B.甲为CuO,乙为 丙为
C.甲为 乙为 丙为
D.甲为 乙为 丙为
8.[2025·宝鸡中学月考]下图中相邻两种物质均可归为一类,甲、乙、丙、丁为物质的四种类别,下列分类正确的是 ( )
A.甲类两种物质的水溶液都呈碱性
B.乙类两种物质都是碱性氧化物
C.丙类两种物质都是钠盐
D.丁类两种物质都是硫酸盐
9.[2025·深圳中学月考]下列说法中正确的是 ( )
A.由一种元素组成的物质一定是纯净物
是混合物
C.酸性氧化物一定是非金属氧化物,非金属氧化物不一定是酸性氧化物
D.碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物
10.[双选][名师改编]晋代炼丹家葛洪所著《抱朴子》是中国为世界科技花园贡献出的一颗璀璨明珠,书中有记载:“丹砂烧之成水银,积变又还成丹砂。”这句话中的丹砂指的是HgS,下列关于这句话的说法正确的是( )
A.该过程只涉及物理变化 B.“积变又还成丹砂”是化合反应
C.该过程中发生了复分解反应 D.“丹砂烧之成水银”过程中产生S
11.[2025·天津静海区模拟]以下表示的是碳及其化合物的相互转化关系(部分反应条件已略去): 其中涉及的基本反应类型依次为 ( )
A.置换反应、化合反应、分解反应、复分解反应
B.置换反应、化合反应、复分解反应、分解反应
C.化合反应、置换反应、分解反应、复分解反应
D.化合反应、置换反应、复分解反应、分解反应
12.[双选][名师改编]如图是小红学习《常见的碱》课题后,总结出的氢氧化钙化学性质的部分内容。下列说法不正确的是 ( )
A.①中不能使酚酞溶液变色
B.②中与 HCl反应的化学方程式为
C.③中能与 溶液发生反应
D.④可解释久置的澄清石灰水变质的原因
13.下列有关物质的分类及反应均正确的是( )
A.碳酸钙属于盐,可用于实验室制
B.铁属于活泼金属单质,可用于实验室制
C.纯碱属于碱,可与稀盐酸发生反应:
D.烧碱属于碱,可与稀硫酸发生反应:
14.[2025·成都一中期中]下列关于胶体的叙述不正确的是 ( )
A.胶体区别于其他分散系的本质特征是具有丁达尔效应
B.用渗析法可以除去 胶体中的NaCl
C.往 胶体中逐滴加入稀硫酸,开始时会出现沉淀,再继续滴加稀硫酸,沉淀又会溶解直至消失
D.用盐卤点豆腐、河海交汇处可沉积成沙洲、血液透析等都与胶体性质有关
15.[2022 武汉二中高一月考]人体中99%的钙储存在骨骼、牙齿中,还有1%的钙储存在血液和软组织等中。血液和软组织中的钙非常重要,参与生理活动。部分钙及其化合物之间的转化关系如图所示,下列说法正确的是( )
A.图中的物质中有三种属于氧化物
B.电解熔融氯化钙得到钙的反应属于化合反应
C.④、⑤中一定有水生成
D. Ca能在 Cl 中燃烧,该反应说明燃烧不一定需要氧气
二、非选择题(本题包含7小题,共55分)
16.(12分)[2025·亳州一中月考]硫酸、碳酸钠、二氧化碳、铜片、氢氧化钡、氢氧化钠、铁片、
生石灰和木炭粉9种物质中的几种存在如图所示的关系,选择适当的物质,使连线的两种物质能发生反应(酸、碱、盐均配制成稀溶液)。
(1)写出下列物质的化学式。
① ;② ;③ ;④ 。
(2)写出下列序号对应物质之间发生反应的化学方程式。
①与②: ;
②与④: ;
②与⑤: ;
④与⑤: 。
17.(6分)现有如下各实验:
①将1g KCl加入99g水中;
②将1g可溶性淀粉加入100g水中,搅拌均匀后煮沸;
③将 粉末加入 100 g水中,充分振荡;
④将0.1g 植物油加入10g水中,充分振荡混匀;
⑤将96 mL酒精与5 mL水充分混合。
其中所得到的分散系,属于溶液的有 (填序号,下同),属于胶体的有 ,
属于浊液的有 。
18.(6分)[2025·苏州中学月考]某课外活动小组进行 胶体的制备实验并检验其性质。
(1)若将 饱和溶液分别滴入下列物质中,能形成胶体的是 (填字母)。
A.冷水 B.沸水
C.浓 NaOH溶液 D.饱和食盐水
(2)写出制备 胶体的化学方程式: 。
(3)怎样检验所得的分散系是胶体 。
19.(8分)[2022 陕西师大附中高一月考]某班同学为探究酸的化学性质,做了五组实验(如图所示)。
分析并回答下列问题:
(1)A组试管中都产生 若要制得较纯的 ,选稀硫酸而不选盐酸的原因是 。
(2)B、E组试管中各自的实验现象相同,该现象分别是 。
(3)写出D组任一试管中发生反应的化学方程式 。
(4)C组试管中溶液红色褪去的原因是 。
20.(7分)[北师改编]分散系在生产、生活中有重要的应用,请同答下列问题:
(1)某同学做了如下实验:
①在一清净的试管中加人4-5ml水;
②陶土述试管中加入一小块泥土,用玻璃棒搅拌后并用激光笔照射,未产生丁达尔效应;③将②中试管静置片刻后,用激光笔从试管口垂直往下照射,从侧面观察,试管上部未产生丁达尔数应,中部产生丁达尔效应,下部未产生丁达尔效应。
请根据③中现象推断,试管上部形成的分散系是 .
试管中部形成的分散系是 , 试管下部形成的分散系是 。
(2)已知A、B两种物质的部分物理性质如表所示:
物质 A B
分散到水中 得悬浊液 得无色溶液
熔点 1452 801
沸点 1703 1413
①已知A与B不能反应,且 A、B均不能与水反应。欲从 A、B的混合物中分离出B,需进行的三步操作是:a.溶解;
b. (填操 作 名 称,下同 );
c. .
②上述a、b、c操作过程中均需用到的一种玻璃仪器为 。
③将 A、B分别加入水中,所得分散系中分散质粒子直径较大的是 (填“A”或“B”)。
21.(8分)[2022 重庆八中高一月考]氢氧化钙俗称熟石灰或消石灰,是一种白色粉末状固体,将石灰乳(主要成分为氢氧化均铜溶液按照一定的比例混合可配制农药波尔多液。
如图1.树木过冬防虫,树木根部以上可涂石灰浆。如图2,工业上常利用石灰窑制备氢氧化钙、具体过程如下:
将石灰石煅烧成氧化钙后,经精选,与水按1:(3~3.5)的比例混合,生成氢氧化钙料液,经净化分离除渣,再经离心脱水,干燥,即得氢氧化钙成品。
根据上述材料,回答下列问题:
(1)选择上述短文中提供的物质,完成下表(每空仅填一种物质)。
类别 混合物 碱 碱性氧化物
名称
化学式 —
(2)制波尔多液时 (填“能”或“不能”)用铁桶作容器。
(3)写出工业上制备氢氧化钙的化学方程式,并注明
物质类别: 。
示例:A(氧化物)· (氧化物)══C(盐)
(4)请写出与题中不同的制备氢氧化钙的方法,并说明题中工业生产方法的优点。
制备方法: (用化学方程式表示)。
优点: (写一个即可)。
22.(8分)[2025·珠海一中月考]A、B、C、D、E五种物质均为中学化学中常见的化合物,已知A、B、C、D、E五种物质里含有相同的一种金属元素,并且A、B、C、D都可与物质M反应生成E,物质之间按箭头方向都可通过一步反应实现转化。实验室通常用碱B的澄清溶液检验
回答下列问题:
(1)写出物质的化学式:A为 、B为 、C为 。
(2)M属于 (选填“酸”“碱”“盐”“酸性氧化物”或“碱性氧化物”)。
(3)写出正盐C转化为酸式盐D的化学方程式: 。
(4)写出碱 B转化为酸式盐D的化学方程式: 。
第一单元 物质的分类及转化参考答案
1.D 【解析】非金属单质和酸分别与金属单质反应、碱性氧化物和碱分别与酸反应、酸性氧化物和酸分别与碱反应都可以生成盐。
2.D 【解析】酸与碱反应生成盐和水,碱性氧化物与酸反应生成盐和水,盐与盐可能发生复分解反应生成两种盐,均符合反应特征;酸性氧化物与水发生化合反应生成酸,不符合反应特征,故选D项。
3. C 【解析】AgI胶体与 Fe(OH) 胶体相混合时,能析出AgI和 Fe(OH) 的混合沉淀,这是发生了胶体的聚沉,说明AgI和 Fe(OH) 的胶粒带相反电荷,因为 Fe(OH) 胶粒带正电,所以 AgI胶粒带负电。AgI胶粒直径为1~100mm,不能通过半透膜,A不符合题意;结合以上分析可知,AgI胶粒带负电,胶体不带电荷,B不符合题意;AgI胶粒带负电,发生电泳时,胶粒向阳极移动,C符合题意;AgI胶体是一种分散系,为混合物,D不符合题意。
4. B 【解析】 胶体能产生丁达尔效应,即用激光笔照射胶体,可看到一条光亮的“通路”,故果冻属于胶体,B项正确。
5. C 【解析】豆浆属于胶体,在电解质盐卤或石膏的作用下发生凝聚制成豆腐,A不符合题意;烟尘为气溶胶,其中胶粒带电荷,在电流作用下移向电极,B不符合题意;泡沫灭火器中将. 与 两溶液混合后, 与 水解且互相促进至水解完全: 在 的作用下喷出大量泡沫,起到灭火作用,与胶体性质无关,C符合题意;该景象是胶体的丁达尔效应,D不符合题意。
6. A 【解析】 根据分散质粒子的直径大小可以将分散系分为溶液、胶体和浊液,分散质粒子的直径为1 ~100 nm 的分散系为胶体,即为分散系Ⅱ,分散质粒子的直径小于1 nm的分散系为溶液,即为分散系Ⅰ,分散质粒子的直径大于100 nm的分散系为浊液,即为分散系Ⅲ。氢氧化铜悬浊液为浊液,属于分散系Ⅲ,云、有色玻璃、雾均为胶体,属于分散系Ⅱ,则不属于分散系Ⅱ的是氢氧化铜悬浊液,本题选 A。
7. C 【解析】NaOH 属于碱,NaCl 和 属于盐,与对应的酸发生反应可使碱转化为盐,要使盐转化为另一种盐,需要满足复分解反应发生的条件,即生成沉淀、放出气体或生成水,NaCl与. 反应生成AgCl沉淀和 可以实现 NaCl到 的转化,但是 不能与其他物质反应生成NaCl,无法实现图示的转化,故A不符合题意; 可通过与碱反应转化为( 而CuO 不能一步转化成 故B不符合题意; 与稀盐酸反应可生成( 或 与 反应可生成 高温分解生成 能通过一步反应实现图示的转化,故C符合题意; 可与 溶液反应生成 但 不能一步转化为 ,故D不符合题意。
8. D 【解析】甲类物质中NH 的水溶液呈碱性,SO 的水溶液呈酸性,A不正确;乙类物质中 Na O是碱性氧化物,SO 是酸性氧化物,B不正确;丙类物质中Na O是钠的氧化物, 是钠盐,C不正确;丁类物质中 是硫酸的钠盐, 是硫酸的钾盐,两种物质都是硫酸盐,D正确。
9. D 【解析】A项,如O 与O 均由一种元素组成,但由它们组成的物质是混合物,错误。B项,带有结晶水的盐属于纯净物, 是纯净物,错误。C项,酸性氧化物不一定是非金属氧化物,如 是酸性氧化物,非金属氧化物不一定是酸性氧化物,如CO不是酸性氧化物,错误。D项,碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物,如 是酸性氧化物,正确。
10. BD 【解析】 “丹砂烧之成水银”过程中HgS 分解为S和 Hg,为分解反应;“积变又还成丹砂”过程中S和 Hg反应生成HgS,为化合反应,据此分析解答。
HgS 的分解和生成都是化学变化,A项错误;由全景分析可知,B、D项正确,C项错误。
11. B 【解析】碳与氧化铜发生置换反应生成铜和二氧化碳;二氧化碳溶于水,并与水发生化合反应生成碳酸:碳酸与氢氧化钙发生复分解反应生成碳酸钙和水:碳酸钙高温分解生成氧化钙和二氧化碳,或碳酸钙与盐酸发生复分解反应生成氯化钙、水和二氧化碳,故B项符合题意。
12. AC 【解析】
选项 分析 结论
A 属于碱,能使酚酞溶液变红 错误
B 与 HCl发生酸碱中和反应: 正确
C 与 溶液不反应 错误
D 与非金属氧化物( 发生反应而变质: 正确
13.D 【解析】A项,实验室制 是利用碳酸钙与盐酸反应;B项,铁与 HCl反应的化学方程式为 H ↑;C项,纯碱属于盐,不属于碱。
14. A 【解析】胶体区别于其他分散系的本质特征是分散质粒子大小不同,故A 错误;胶体粒子不能通过半透膜,用渗析法可以除去 胶体中的 NaCl,故 B 正确;
Fe(OH) 胶体中逐滴加入稀硫酸,开始时发生聚沉出现氢氧化铁沉淀,再继续滴加稀硫酸,氢氧化铁与硫酸反应生成硫酸铁和水,所以沉淀又会溶解直至消失.故C 正确;用盐卤点豆腐、河海交汇处可沉积成沙洲与胶体聚沉有关,血液透析利用的是胶体渗析原理,故D正确。
15. D 【解析】 图中的物质中只有氧化钙属于氧化物,A项错误;电解熔融氯化钙得到钙和氯气的反应属于分解反应,B项错误;④可以通过氢氧化钙与碳酸钠反应实现,生成物是
碳酸钙和氢氧化钠,没有水生成,⑤可以通过氢氧化钙和氯化镁反应实现,生成物是氯化钙和氢氧化镁,也没有水生成,C项错误;钙在氯气中燃烧生成氯化钙,此燃烧过程中没有氧气参与,说明燃烧不一定需要氧气,D项正确。
16.
【解析】9种物质中只有一种酸,其化学式为 H SO ,Cu、Fe、C三种单质中,只有 Fe能与稀硫酸反应,二者反应生成 和 ,故①为 Fe,②为 ; 碱 有 NaOH、 只有 属于盐,而NaOH不能与 反应,故④为 ⑤为 ③应该为酸性氧化物,则为
17. ①⑤ ② ③④
【解析】①分散质KCl 溶于水后以离子形式存在,粒子直径小于1 nm,属于溶液;②淀粉分子大,溶于水并煮沸后,形成的是胶体;( 不溶于水,加入水中振荡所形成的是不稳定的体系,放置后生成沉淀,所以属于悬浊液;④植物油不溶于水,形成的是乳浊液;⑤分散质是酒精,分散剂是水,二者以任意比混溶,形成溶液。
18. (1)B
(胶体)+3HCl
(3)用激光笔照射,若有一条光亮的通路,则制得的分散系是胶体
19. (Ⅰ)反应放出的热会使盐酸挥发出 HCl 气体,使制得的1 ,不纯
(2)固体逐渐消失,溶液变为棕黄色;有气泡产生
(或
(4)NaOH与酸发生中和反应
【解析】 (1)反应放出的热会使盐酸挥发出 HCl气体,使制得的 不纯净,而反应放出的热不能使稀硫酸挥发,因此要制得较纯的 ,应选稀硫酸。 ( 属于碱性氧化物,能与稀盐酸反应生成 和 ,与稀硫酸反应生成 和 生成的 溶液、 溶液均显棕黄色,因此会观察到固体逐渐消失,溶液变成棕黄色; 能与稀盐酸或稀硫酸反应生成( ,因此会观察到有气泡产生。(3)稀盐酸与 溶液反应产生AgCl白色沉淀,反应的化学方程式为 稀硫酸与 溶液反应产生 白色沉淀,反应的化学方程式为 (4)NaOH与稀盐酸或稀硫酸发生中和反应,碱被消耗,溶液红色褪去。
20. (1)溶液 胶体 悬浊液
(2)①过滤 蒸发 ②玻璃棒 ③A
【解析】 (1)将泥土加入水中,搅拌,静置一段时间后,上部为澄清的溶液,其分散质粒子的直径小于1 nm,不能产生丁达尔效应;中部为胶体,其分散质粒子的直径为1 ~100 nm,能产生丁达尔效应;下部为悬浊液,其分散质粒子的直径大于 100 nm,不能产生丁达尔效应。
(2)①根据A与B的性质可知,A、B均为固体,A不溶于水,而B 能溶于水,所以从 A 与B的混合物中分离出B,可以先加水溶解,再过滤出A,然后通过蒸发即可得到 B。②在溶解、过滤和蒸发时都需要用到玻璃棒。③分散质粒子的直径:悬浊液>溶液。
21.(1)(合理即可)
类别 混合物 碱 碱性氧化物
名称 石灰乳 氢氧化钙 氧化钙
化学式 —— CaO
(2)不能
(盐) (氧化物) (氧化物)↑,
CaO(氧化物) (氧化物)=== Ca(OH) (碱)
2CaO (其他合理答案也可, 原料来源丰富、原料价格低廉或生产成本低等(写一个即可)
【解析】(Ⅰ)短文中提供了多种混合物,如波尔多液、石灰乳等,氮氧化钙为碱,氧化钙为碱性氧化物。(2)制波尔多液的原料中有 溶液,而Fe能与发生置换反应,故不能用铁桶作容器。(3)工业上制备 的反应为
为盐,CaO、 均为氧化物,为碱。
(4)分析可知,题中工业制法有原料(石灰石)来源丰富、原料价格低廉、生产成本低等优点。
22 .(1)CaO Ca(OH) CaCO CaCl 或
(2)酸
【解析】实验室通常用碱 B的澄清溶液检验( ,即 B 为 则A为CaO;D为酸式盐,说明D为( 则C为( 都可以与盐酸(或硝酸)反应生成氯化钙(或硝酸钙),故E 为氯化钙或硝酸钙。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
