第五章 第三节 无机非金属材料--人教版高中化学必修第二册教学课件(共26张PPT)
文档属性
| 名称 | 第五章 第三节 无机非金属材料--人教版高中化学必修第二册教学课件(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
无机非金属材料
第五章第三节
化学
第五章 化工生产中的重要非金属元素
第三节 无机非金属材料
1.通过了解陶瓷、玻璃、水泥等传统硅酸盐材料的生产原料、性能和主要用途,知道普通玻璃的主要成分,能从结构角度分析硅酸盐的特性。
2.通过对新型无机非金属材料硅芯片的认识,能够从“位—构—性”的角度预测硅与二氧化硅的一般性质,了解并掌握硅、二氧化硅的特性与二者在生产、生活中的应用。感受新型无机非金属材料的特殊性能及其在高科技领域所发挥的重要作用。
3.通过对新型陶瓷、碳纳米材料认识材料的认识,了解材料对人类文明的推动作用,知道化学科学对新材料研发的重要作用,感受化学对社会发展和人类生活的巨大贡献,提升自身“科学态度与社会责任”等学科核心素养。
学习目标
一、传统无机非金属材料——硅酸盐材料
兵马俑
天津大剧院
珠港澳大桥
【问题1.1】陶瓷历史悠久,玻璃使用广泛,水泥是建筑与水利工程的必需品,请思考这些材料都具有什么特性?
传统无机非金属材料具有硬度高、难溶于水、耐高温、耐腐蚀的特点
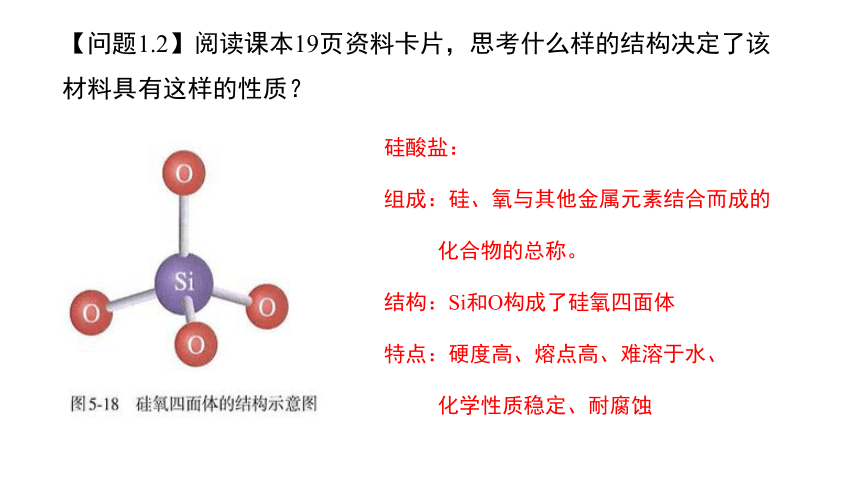
硅酸盐:
组成:硅、氧与其他金属元素结合而成的
化合物的总称。
结构:Si和O构成了硅氧四面体
特点:硬度高、熔点高、难溶于水、
化学性质稳定、耐腐蚀
【问题1.2】阅读课本19页资料卡片,思考什么样的结构决定了该材料具有这样的性质?
主要原料:黏土(主要成分为含水的铝硅酸盐)
特点:抗氧化、耐酸碱腐蚀、耐高温、绝缘
用途:建筑材料、绝缘材料、日用器皿、卫生洁具等
1.陶瓷
2.玻璃
主要原料:纯碱、石灰石和石英砂(主要成分是SiO2)
生产设备:玻璃窑
反应原理:SiO2 + CaCO3 CaSiO3 + CO2 ↑
SiO2 + Na2CO3 Na2SiO3 + CO2↑
主要成分:Na2SiO3、CaSiO3和SiO2
特点:无固定熔点,在一定温度范围内软化,可加工成玻璃制品
用途:建筑材料、光学仪器、各种器皿,还可制造玻璃纤维用于高强度复合材料等
含铅的光学玻璃
加入硼酸盐的玻璃仪器
加入金属氧化物的彩色玻璃
3.水泥
主要原料:黏土和石灰石
生产设备:水泥回转窑
用途:水泥、沙子和碎石等与水混合可以得到混凝土,
大量用于建筑和水利工程
三峡大坝
1.硅
(1)原子结构:如左图
(2)元素周期表位置:第三周期、第ⅣA族,正好处于金属与非金属的过渡位置
(3)性能:其单质的导电性介于导体与绝缘体之间,是应用广泛的半导体材料
二、新型无机非金属材料
【问题2.1】硅是应用最为广泛的半导体材料,从元素周期表中找到硅元素,思考硅单质可以作为半导体的原因?
【提问】自然界中硅以什么形态存在?
在自然界中主要以硅酸盐(如地壳中的大多数矿物)和氧化物(如水晶、玛瑙、石英砂)的形式存在。
【问题2.2】同主族元素性质具有一定的相似性,通过类比,思考硅单质可能具有哪些性质?你的推测依据是?
(1)物理性质:
晶体硅是灰黑色固体,有金属光泽,熔点高,硬度大,质脆,导电性介于导体与绝缘体之间,是良好的半导体材料。
(2)化学性质:
常温下“三反应”
加热(高温)“三反应”
Si + F2 ===SiF4
Si+4HF===SiF4↑+2H2↑
Si+2NaOH+H2O===Na2SiO3 +2H2↑
Si+O2 SiO2
Si+2Cl2 SiCl4
Si+C SiC
高纯硅的制取和用途
【问题2.3】自然界中没有游离态的硅,如何来制备高纯硅?阅读课本22页资料卡片,写出相应反应的化学方程式
粗硅的制备
SiO2 + 2C Si + 2CO↑
粗硅
粗硅变高纯硅
Si + 3HCl SiHCl3 + H2
SiHCl3 + H2 Si + 3HCl
高纯硅的制取和用途
硅单质的用途
硅芯片
硅太阳能电池
【问题2.4】二氧化硅用来生产光导纤维的原因是什么?二氧化硅的物理性质
(1)二氧化硅的物理性质
硬度大,熔、沸点高,常温下为固体,难溶于水,不导电
沙子
水晶
光导纤维
【问题2.5】类比二氧化碳预测二氧化硅的化学性质
C
CO2
H2CO3
Na2CO3
Si
SiO2
H2SiO3
Na2SiO3
SiO2具有酸性氧化物的通性
SiO2的化学性质
a.酸性氧化物
①与碱溶液反应:SiO2 + 2NaOH===Na2SiO3 + H2O
已知:Na2SiO3的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,
可以用作黏合剂和防火剂。
思考:实验室盛放碱溶液的试剂瓶应使用橡胶塞,还是玻璃塞?为什么?
回答:应使用橡胶塞。
因为玻璃中含有SiO2,与NaOH溶液反应生成的Na2SiO3水溶液有黏性,会使玻璃塞与瓶口内侧发生粘连而无法打开。
SiO2的化学性质
a.酸性氧化物
①与碱溶液反应:SiO2 + 2NaOH===Na2SiO3 + H2O
②与碱性氧化物反应:SiO2 + CaO CaSiO3
③与某些盐反应: SiO2 + CaCO3 CaSiO3 + CO2 ↑
SiO2 + Na2CO3 Na2SiO3 + CO2↑
以上两个反应为工业制玻璃的主要反应
b.特性
氢氟酸是HF的水溶液,可与SiO2发生反应生成SiF4和H2O。请写出该反应的化学方程式。想一想为什么可以用氢氟酸溶蚀玻璃生产磨砂玻璃?氢氟酸用什么样的试剂瓶存放?
SiO2 + 4HF===SiF4↑ + 2H2O
玻璃中有SiO2,可与氢氟酸反应而使部分玻璃溶解,使玻璃表面呈现磨砂状。
氢氟酸应该用塑料瓶盛装
SiO2的化学性质
光导纤维
SiO2的用途
光导纤维的通信容量大,抗干扰性能好,传输的信号不易衰减,能有效提高通信效率
3.新型陶瓷
(1)碳化硅(SiC)俗称金刚砂
①硬度很大,可用作砂纸和砂轮的磨料
②还具有优异的高温抗氧化性能,可以用作耐高温结构材料、耐高温半导体材料等。
(2)其他新型陶瓷:
①高温结构陶瓷
②压电陶瓷
③透明陶瓷
④超导陶瓷
富勒烯
石墨烯
碳纳米管(单壁)
碳纳米管(多壁)
4.碳纳米材料
石墨烯是只有一个碳原子直径厚度的单层石墨,其独特的结构使其电阻率低、热导率高,具有很高的强度。作为一种具有优异性能的新型材料,石墨烯在光电器件、超级电容器、电池和复合材料等方面的应用研究正在不断深入。
分类 名称 性能 主要用途
传统无机 非金属材料 陶瓷 熔点高、硬度大、耐腐蚀、性质稳定 建筑材料、日常器皿、
卫生洁具等
玻璃 透光性好、硬度大、 无固定熔点 建筑材料、各种器皿、
光学仪器等
水泥 遇水逐渐变硬(水硬性)、硬化后性质稳定 大量用于建筑、水利、
道路等工程中
分类 名称 性能 主要用途
新型无机非金属材料 晶体硅 导电性介于导体和绝缘体 之间 半导体材料、计算机芯片、太阳能电池等
二氧化硅 性质稳定,透光性好 光导纤维、玻璃仪器、
装饰品
新型陶瓷 分别具有光学、热学、电学、磁学等方面的特性 分别用于激光、火箭发动机、压电陶瓷(点火器)、
磁悬浮技术
石墨烯 电阻率低、热导率高、 强度高 光电器件、超级电容器、电池、复合材料
碳纳米管 比表面积大、电学性能好、强度高 传感器、电池、复合材料
课堂总结
谢谢大家
无机非金属材料
第五章第三节
化学
第五章 化工生产中的重要非金属元素
第三节 无机非金属材料
1.通过了解陶瓷、玻璃、水泥等传统硅酸盐材料的生产原料、性能和主要用途,知道普通玻璃的主要成分,能从结构角度分析硅酸盐的特性。
2.通过对新型无机非金属材料硅芯片的认识,能够从“位—构—性”的角度预测硅与二氧化硅的一般性质,了解并掌握硅、二氧化硅的特性与二者在生产、生活中的应用。感受新型无机非金属材料的特殊性能及其在高科技领域所发挥的重要作用。
3.通过对新型陶瓷、碳纳米材料认识材料的认识,了解材料对人类文明的推动作用,知道化学科学对新材料研发的重要作用,感受化学对社会发展和人类生活的巨大贡献,提升自身“科学态度与社会责任”等学科核心素养。
学习目标
一、传统无机非金属材料——硅酸盐材料
兵马俑
天津大剧院
珠港澳大桥
【问题1.1】陶瓷历史悠久,玻璃使用广泛,水泥是建筑与水利工程的必需品,请思考这些材料都具有什么特性?
传统无机非金属材料具有硬度高、难溶于水、耐高温、耐腐蚀的特点
硅酸盐:
组成:硅、氧与其他金属元素结合而成的
化合物的总称。
结构:Si和O构成了硅氧四面体
特点:硬度高、熔点高、难溶于水、
化学性质稳定、耐腐蚀
【问题1.2】阅读课本19页资料卡片,思考什么样的结构决定了该材料具有这样的性质?
主要原料:黏土(主要成分为含水的铝硅酸盐)
特点:抗氧化、耐酸碱腐蚀、耐高温、绝缘
用途:建筑材料、绝缘材料、日用器皿、卫生洁具等
1.陶瓷
2.玻璃
主要原料:纯碱、石灰石和石英砂(主要成分是SiO2)
生产设备:玻璃窑
反应原理:SiO2 + CaCO3 CaSiO3 + CO2 ↑
SiO2 + Na2CO3 Na2SiO3 + CO2↑
主要成分:Na2SiO3、CaSiO3和SiO2
特点:无固定熔点,在一定温度范围内软化,可加工成玻璃制品
用途:建筑材料、光学仪器、各种器皿,还可制造玻璃纤维用于高强度复合材料等
含铅的光学玻璃
加入硼酸盐的玻璃仪器
加入金属氧化物的彩色玻璃
3.水泥
主要原料:黏土和石灰石
生产设备:水泥回转窑
用途:水泥、沙子和碎石等与水混合可以得到混凝土,
大量用于建筑和水利工程
三峡大坝
1.硅
(1)原子结构:如左图
(2)元素周期表位置:第三周期、第ⅣA族,正好处于金属与非金属的过渡位置
(3)性能:其单质的导电性介于导体与绝缘体之间,是应用广泛的半导体材料
二、新型无机非金属材料
【问题2.1】硅是应用最为广泛的半导体材料,从元素周期表中找到硅元素,思考硅单质可以作为半导体的原因?
【提问】自然界中硅以什么形态存在?
在自然界中主要以硅酸盐(如地壳中的大多数矿物)和氧化物(如水晶、玛瑙、石英砂)的形式存在。
【问题2.2】同主族元素性质具有一定的相似性,通过类比,思考硅单质可能具有哪些性质?你的推测依据是?
(1)物理性质:
晶体硅是灰黑色固体,有金属光泽,熔点高,硬度大,质脆,导电性介于导体与绝缘体之间,是良好的半导体材料。
(2)化学性质:
常温下“三反应”
加热(高温)“三反应”
Si + F2 ===SiF4
Si+4HF===SiF4↑+2H2↑
Si+2NaOH+H2O===Na2SiO3 +2H2↑
Si+O2 SiO2
Si+2Cl2 SiCl4
Si+C SiC
高纯硅的制取和用途
【问题2.3】自然界中没有游离态的硅,如何来制备高纯硅?阅读课本22页资料卡片,写出相应反应的化学方程式
粗硅的制备
SiO2 + 2C Si + 2CO↑
粗硅
粗硅变高纯硅
Si + 3HCl SiHCl3 + H2
SiHCl3 + H2 Si + 3HCl
高纯硅的制取和用途
硅单质的用途
硅芯片
硅太阳能电池
【问题2.4】二氧化硅用来生产光导纤维的原因是什么?二氧化硅的物理性质
(1)二氧化硅的物理性质
硬度大,熔、沸点高,常温下为固体,难溶于水,不导电
沙子
水晶
光导纤维
【问题2.5】类比二氧化碳预测二氧化硅的化学性质
C
CO2
H2CO3
Na2CO3
Si
SiO2
H2SiO3
Na2SiO3
SiO2具有酸性氧化物的通性
SiO2的化学性质
a.酸性氧化物
①与碱溶液反应:SiO2 + 2NaOH===Na2SiO3 + H2O
已知:Na2SiO3的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,
可以用作黏合剂和防火剂。
思考:实验室盛放碱溶液的试剂瓶应使用橡胶塞,还是玻璃塞?为什么?
回答:应使用橡胶塞。
因为玻璃中含有SiO2,与NaOH溶液反应生成的Na2SiO3水溶液有黏性,会使玻璃塞与瓶口内侧发生粘连而无法打开。
SiO2的化学性质
a.酸性氧化物
①与碱溶液反应:SiO2 + 2NaOH===Na2SiO3 + H2O
②与碱性氧化物反应:SiO2 + CaO CaSiO3
③与某些盐反应: SiO2 + CaCO3 CaSiO3 + CO2 ↑
SiO2 + Na2CO3 Na2SiO3 + CO2↑
以上两个反应为工业制玻璃的主要反应
b.特性
氢氟酸是HF的水溶液,可与SiO2发生反应生成SiF4和H2O。请写出该反应的化学方程式。想一想为什么可以用氢氟酸溶蚀玻璃生产磨砂玻璃?氢氟酸用什么样的试剂瓶存放?
SiO2 + 4HF===SiF4↑ + 2H2O
玻璃中有SiO2,可与氢氟酸反应而使部分玻璃溶解,使玻璃表面呈现磨砂状。
氢氟酸应该用塑料瓶盛装
SiO2的化学性质
光导纤维
SiO2的用途
光导纤维的通信容量大,抗干扰性能好,传输的信号不易衰减,能有效提高通信效率
3.新型陶瓷
(1)碳化硅(SiC)俗称金刚砂
①硬度很大,可用作砂纸和砂轮的磨料
②还具有优异的高温抗氧化性能,可以用作耐高温结构材料、耐高温半导体材料等。
(2)其他新型陶瓷:
①高温结构陶瓷
②压电陶瓷
③透明陶瓷
④超导陶瓷
富勒烯
石墨烯
碳纳米管(单壁)
碳纳米管(多壁)
4.碳纳米材料
石墨烯是只有一个碳原子直径厚度的单层石墨,其独特的结构使其电阻率低、热导率高,具有很高的强度。作为一种具有优异性能的新型材料,石墨烯在光电器件、超级电容器、电池和复合材料等方面的应用研究正在不断深入。
分类 名称 性能 主要用途
传统无机 非金属材料 陶瓷 熔点高、硬度大、耐腐蚀、性质稳定 建筑材料、日常器皿、
卫生洁具等
玻璃 透光性好、硬度大、 无固定熔点 建筑材料、各种器皿、
光学仪器等
水泥 遇水逐渐变硬(水硬性)、硬化后性质稳定 大量用于建筑、水利、
道路等工程中
分类 名称 性能 主要用途
新型无机非金属材料 晶体硅 导电性介于导体和绝缘体 之间 半导体材料、计算机芯片、太阳能电池等
二氧化硅 性质稳定,透光性好 光导纤维、玻璃仪器、
装饰品
新型陶瓷 分别具有光学、热学、电学、磁学等方面的特性 分别用于激光、火箭发动机、压电陶瓷(点火器)、
磁悬浮技术
石墨烯 电阻率低、热导率高、 强度高 光电器件、超级电容器、电池、复合材料
碳纳米管 比表面积大、电学性能好、强度高 传感器、电池、复合材料
课堂总结
谢谢大家
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
