第八章 第一节 自然资源的开发利用 第2课时--人教版高中化学必修第二册教学课件(共25张PPT)
文档属性
| 名称 | 第八章 第一节 自然资源的开发利用 第2课时--人教版高中化学必修第二册教学课件(共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
第2课时 海水资源的开发利用
第一节 自然资源的开发利用
化学
1. 通过阅读理解、原理分析,了解海水资源的利用方法和从海水中获得化学物质的方法,初步认识海水资源的广泛性和多样性。
2. 通过讨论交流、原理分析,认识海水提溴工艺流程图的设计与分析,形成工业上提取物质的一般思路和方法,培养模型认知和证据推理的能力。
学习目标
3. 通过思考交流、问题探究,能从化学的角度分析从自然资源到产品的转化途径,认识化学方法在实现物质转化中的作用和贡献,感受化学科学在生产、生活中的应用价值。
重点:
以海水提镁、海水提溴为例,用化学视角找到物质转化、元素富集的途径。
难点:
海水提溴工艺流程图的绘制,提炼形成工业提取物质的一般思路和方法。
学习重难点
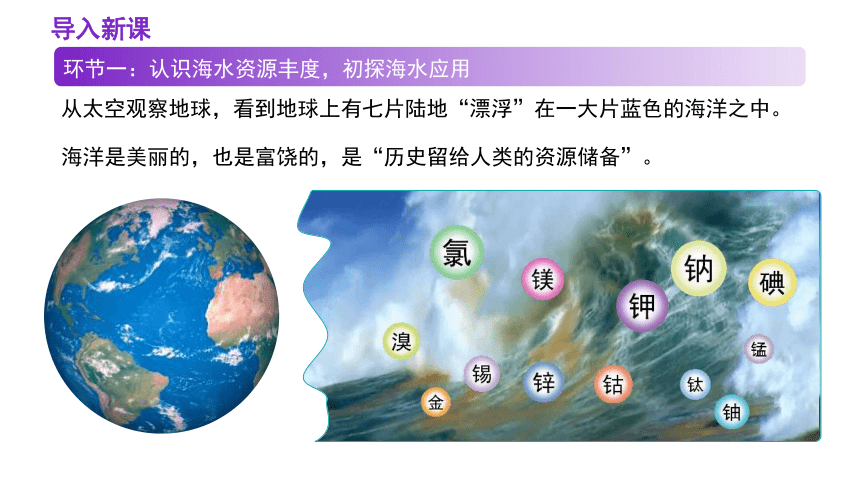
从太空观察地球,看到地球上有七片陆地“漂浮”在一大片蓝色的海洋之中。
海洋是美丽的,也是富饶的,是“历史留给人类的资源储备”。
导入新课
环节一:认识海水资源丰度,初探海水应用
导入新课
水资源
生物资源
能源资源
化学资源
地球表面海洋面积占到71%,海洋是人类千万年来的巨大资源宝库,其中的水资源和其他化学资源具有十分巨大的开发潜力。
结合教材和资料请同学们思考,从海水中能获得哪些产品或资源
环节一:认识海水资源丰度,初探海水应用
海水中大多数元素总量很大,如海水中金元素总含量约为 50000000t(5千万吨)
资源丰富
01
海水中资源分散 ,含量极微少,如一吨海水中只含金元素0.000004g。
资源分散
02
导入新课
从海水中获得产品的过程中可能会遇到哪些困难
环节一:认识海水资源丰度,初探海水应用
课堂探究
环节二:海水淡化,认识蒸馏装置
海洋约占地球表面积的71%,海水中水的储量约为1.3×1018吨,约占全球总水量的97%(3%是陆地上的淡水)。
利用途径
海水水资源的利用主要包括海水的淡化和直接利用海水进行循环冷却(作冷却用水)。
海水淡化
通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。
海水淡化方法
蒸馏法
电渗析法
离子交换法
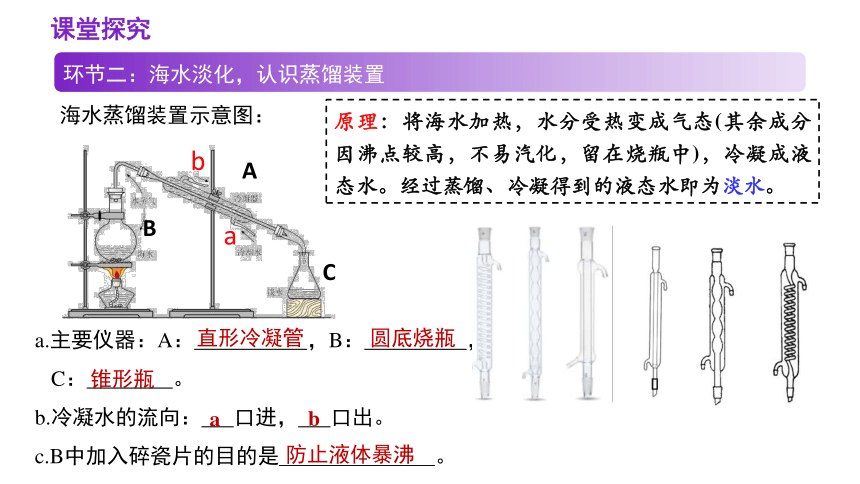
a.主要仪器:A: ,B: ,
C: 。
b.冷凝水的流向: 口进, 口出。
c.B中加入碎瓷片的目的是 。
直形冷凝管
圆底烧瓶
锥形瓶
a
b
防止液体暴沸
原理:将海水加热,水分受热变成气态(其余成分因沸点较高,不易汽化,留在烧瓶中),冷凝成液态水。经过蒸馏、冷凝得到的液态水即为淡水。
海水蒸馏装置示意图:
A
B
a
b
C
课堂探究
环节二:海水淡化,认识蒸馏装置
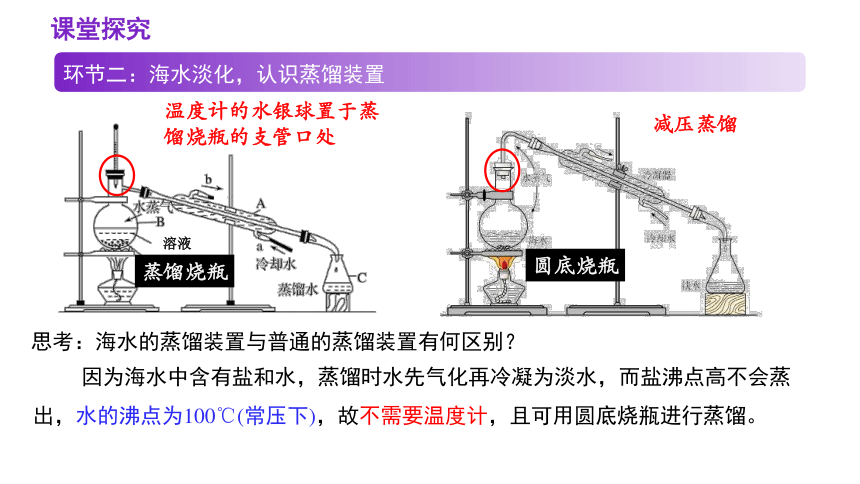
思考:海水的蒸馏装置与普通的蒸馏装置有何区别?
因为海水中含有盐和水,蒸馏时水先气化再冷凝为淡水,而盐沸点高不会蒸出,水的沸点为100℃(常压下),故不需要温度计,且可用圆底烧瓶进行蒸馏。
减压蒸馏
溶液
温度计的水银球置于蒸馏烧瓶的支管口处
蒸馏烧瓶
圆底烧瓶
课堂探究
环节二:海水淡化,认识蒸馏装置
结论:海中含有的盐主要是
_____________
含量最多的非金属离子
含量前两位的金属离子
NaCl、MgCl2
课堂探究
环节三:海水制盐,初识海水化学资源
目前,从海水中提取食盐的方法主要为“盐田法”(也称“太阳能蒸发法”),这是一种古老而至今仍广泛沿用的方法。
先将海水(或海边地下卤水)引入蒸发池,经日晒蒸发水分到一定程度时,导入结晶池,再晒就会逐渐析出食盐来。这时得到的晶体就是我们常见的“粗盐”。剩余的液体称为母液(也称“苦卤”) 。
海水
蒸发池
结晶池
粗盐
母液
课堂探究
环节三:海水制盐,初识海水化学资源
从海水中制得的氯化钠除了供食用,还作为化工原料用于生产烧碱、纯碱、钠、氯气、盐酸等。
氯碱工业
侯氏制碱法
氯化钠
钠
氢氧化钠
盐酸
Na2CO3
氯气
氢气
漂白剂
NaHCO3
课堂探究
环节三:海水制盐,初识海水化学资源
海水提溴
海
水
浓缩海水
(Br-)
吸收塔用SO2吸收
浓缩海水
(Cl-、Br2)
Br-
SO42-
浓缩
(酸化)
通入Cl2
(氧化)
通入热空气或水蒸气(吹出)
反应后
富集溴
通入Cl2
(提取)
Br2、Cl-
蒸馏
分离
溴单质
Cl2+2Br- =2Cl-+Br2
Br2+SO2+2H2O = H2SO4+2HBr
海水晒盐和海水淡化的过程中Br-得到浓缩
向经过酸化的浓缩海水中通入Cl2,将Br-氧化为Br2
利用溴的挥发性,通入热空气或水蒸气,吹出的溴蒸气用SO2吸收
Cl2+2Br- = 2Cl-+Br2
课堂探究
环节四:苦卤的利用——海水提溴与提镁
人们提取海水中的化学元素,来制备有多种用途的物质。如广泛用于火箭、导弹和飞机制造业的金属镁,是利用从海水中提取的镁盐制取的
导弹
火箭
飞机
国防金属
课堂探究
环节四:苦卤的利用——海水提溴与提镁
MgCl2(熔融) Mg+Cl2↑
通电
MgCl2+Ca(OH)2 =Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl = MgCl2+2H2O
海水或卤水
MgCl2
氢氧化镁
Mg(OH)2
MgCl2溶液
MgCl2
盐酸
脱水
镁
电
解
石灰乳
MgCl2 6H2O
由MgCl2·6H2O制备无水MgCl2,必须在HCl气流中加热,以防 MgCl2 水解
因镁在高温下与O2、N2、CO2等气体发生反应,故工业电解得到的镁,在 H2氛围中冷却
工艺流程
海水制镁
课堂探究
环节四:苦卤的利用——海水提溴与提镁
2.所加盐酸是否要过量 目的是什么 如果过量,如何除去
1.海水中本来就有氯化镁,为什么不直接通电 而是要经过“MgCl2→Mg(OH)2→ MgCl2”这样的过程来获取MgCl2呢
要过量,目的是保证Mg(OH)2完全反应,过量的稀盐酸加热蒸发即可除去
除去其他杂质,将MgCl2富集起来
NaOH价格贵,Ca(OH)2 价格便宜且容易得到。工业上可以利用高温煅烧贝壳得到所需要的Ca(OH)2。
贝壳(含CaCO3)
CaO
流程图:
高温煅烧
水
石灰乳
3.为什么不用NaOH代替Ca(OH)2,怎样得到Ca(OH)2 流程图
课堂探究
环节四:苦卤的利用——海水提溴与提镁
海洋生物品种繁多,通过养殖、增殖等途径可实现可持续利用。
课堂探究
拓展:海水资源的多样性——生物资源(海洋生物)
海水运动中蕴藏着巨大的能量,包括潮汐能、波浪能、海流能、温差能和盐差能资源等海上水能资源,它们都属于可再生能源,而且没有污染,具有商业开发价值的。
此外,铀和重水是目前核能开发的重要原料。
课堂探究
拓展:海水资源的多样性——能源资源
大陆架的浅海海底有石油、天然气、煤、硫、磷等;多数近岸带的滨海海盆中有锰结核、可燃冰、砂和砾石,用于冶金、燃料、建筑、石英砂用制玻璃等。
课堂探究
拓展:海水资源的多样性——能源资源
海洋可利用空间包括海上、海中、海底三个部分。海洋空间利用已从传统的交通运输扩大到生产、通信、电力输送、储藏、文化娱乐等诸多领域。
我国拥有18000公里的大陆海岸线,管辖的海域面积近300万平方公里。
课堂探究
拓展:海水资源的多样性——空间资源
课堂练习
【练习1】
1.关于海水资源的综合利用,下列说法错误的是( )
A.海水中含量最高的盐是NaCl
B.电解饱和食盐水可以制得金属钠
C.从海水中提取的镁可用于制造火箭、飞机
D.食用含碘丰富的海产品可防治甲状腺肿大
B
课堂练习
【练习2】
2.水资源是发展国民经济不可缺少的重要自然资源。在世界许多地方,对水的需求已经超过水资源所能负荷的程度,同时有许多地区也存在水资源利用不平衡。下列关于水的说法错误的是( )
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0℃以上,温度越高,水的密度越小
D
课堂练习
【练习3】
A
3.除去粗盐中的杂质MgCl2、CaCl2和Na2SO4,过程如下:
下列有关说法中,不正确的是( )
A.试剂①②③依次加入过量的Na2CO3、NaOH、BaCl2溶液
B.溶解、过滤都用到玻璃棒,其作用是搅拌使加速溶解和引流
C.除去Ca2+的主要反应:Ca2++CO32- ==CaCO3↓
D.向滤液中加入盐酸是为了除去过量的氢氧化钠和碳酸钠
布置作业
预习下节学案。
完成本节素养专练。
谢谢大家
第2课时 海水资源的开发利用
第一节 自然资源的开发利用
化学
1. 通过阅读理解、原理分析,了解海水资源的利用方法和从海水中获得化学物质的方法,初步认识海水资源的广泛性和多样性。
2. 通过讨论交流、原理分析,认识海水提溴工艺流程图的设计与分析,形成工业上提取物质的一般思路和方法,培养模型认知和证据推理的能力。
学习目标
3. 通过思考交流、问题探究,能从化学的角度分析从自然资源到产品的转化途径,认识化学方法在实现物质转化中的作用和贡献,感受化学科学在生产、生活中的应用价值。
重点:
以海水提镁、海水提溴为例,用化学视角找到物质转化、元素富集的途径。
难点:
海水提溴工艺流程图的绘制,提炼形成工业提取物质的一般思路和方法。
学习重难点
从太空观察地球,看到地球上有七片陆地“漂浮”在一大片蓝色的海洋之中。
海洋是美丽的,也是富饶的,是“历史留给人类的资源储备”。
导入新课
环节一:认识海水资源丰度,初探海水应用
导入新课
水资源
生物资源
能源资源
化学资源
地球表面海洋面积占到71%,海洋是人类千万年来的巨大资源宝库,其中的水资源和其他化学资源具有十分巨大的开发潜力。
结合教材和资料请同学们思考,从海水中能获得哪些产品或资源
环节一:认识海水资源丰度,初探海水应用
海水中大多数元素总量很大,如海水中金元素总含量约为 50000000t(5千万吨)
资源丰富
01
海水中资源分散 ,含量极微少,如一吨海水中只含金元素0.000004g。
资源分散
02
导入新课
从海水中获得产品的过程中可能会遇到哪些困难
环节一:认识海水资源丰度,初探海水应用
课堂探究
环节二:海水淡化,认识蒸馏装置
海洋约占地球表面积的71%,海水中水的储量约为1.3×1018吨,约占全球总水量的97%(3%是陆地上的淡水)。
利用途径
海水水资源的利用主要包括海水的淡化和直接利用海水进行循环冷却(作冷却用水)。
海水淡化
通过从海水中提取淡水或从海水中把盐分离出去,都可以达到淡化海水的目的。
海水淡化方法
蒸馏法
电渗析法
离子交换法
a.主要仪器:A: ,B: ,
C: 。
b.冷凝水的流向: 口进, 口出。
c.B中加入碎瓷片的目的是 。
直形冷凝管
圆底烧瓶
锥形瓶
a
b
防止液体暴沸
原理:将海水加热,水分受热变成气态(其余成分因沸点较高,不易汽化,留在烧瓶中),冷凝成液态水。经过蒸馏、冷凝得到的液态水即为淡水。
海水蒸馏装置示意图:
A
B
a
b
C
课堂探究
环节二:海水淡化,认识蒸馏装置
思考:海水的蒸馏装置与普通的蒸馏装置有何区别?
因为海水中含有盐和水,蒸馏时水先气化再冷凝为淡水,而盐沸点高不会蒸出,水的沸点为100℃(常压下),故不需要温度计,且可用圆底烧瓶进行蒸馏。
减压蒸馏
溶液
温度计的水银球置于蒸馏烧瓶的支管口处
蒸馏烧瓶
圆底烧瓶
课堂探究
环节二:海水淡化,认识蒸馏装置
结论:海中含有的盐主要是
_____________
含量最多的非金属离子
含量前两位的金属离子
NaCl、MgCl2
课堂探究
环节三:海水制盐,初识海水化学资源
目前,从海水中提取食盐的方法主要为“盐田法”(也称“太阳能蒸发法”),这是一种古老而至今仍广泛沿用的方法。
先将海水(或海边地下卤水)引入蒸发池,经日晒蒸发水分到一定程度时,导入结晶池,再晒就会逐渐析出食盐来。这时得到的晶体就是我们常见的“粗盐”。剩余的液体称为母液(也称“苦卤”) 。
海水
蒸发池
结晶池
粗盐
母液
课堂探究
环节三:海水制盐,初识海水化学资源
从海水中制得的氯化钠除了供食用,还作为化工原料用于生产烧碱、纯碱、钠、氯气、盐酸等。
氯碱工业
侯氏制碱法
氯化钠
钠
氢氧化钠
盐酸
Na2CO3
氯气
氢气
漂白剂
NaHCO3
课堂探究
环节三:海水制盐,初识海水化学资源
海水提溴
海
水
浓缩海水
(Br-)
吸收塔用SO2吸收
浓缩海水
(Cl-、Br2)
Br-
SO42-
浓缩
(酸化)
通入Cl2
(氧化)
通入热空气或水蒸气(吹出)
反应后
富集溴
通入Cl2
(提取)
Br2、Cl-
蒸馏
分离
溴单质
Cl2+2Br- =2Cl-+Br2
Br2+SO2+2H2O = H2SO4+2HBr
海水晒盐和海水淡化的过程中Br-得到浓缩
向经过酸化的浓缩海水中通入Cl2,将Br-氧化为Br2
利用溴的挥发性,通入热空气或水蒸气,吹出的溴蒸气用SO2吸收
Cl2+2Br- = 2Cl-+Br2
课堂探究
环节四:苦卤的利用——海水提溴与提镁
人们提取海水中的化学元素,来制备有多种用途的物质。如广泛用于火箭、导弹和飞机制造业的金属镁,是利用从海水中提取的镁盐制取的
导弹
火箭
飞机
国防金属
课堂探究
环节四:苦卤的利用——海水提溴与提镁
MgCl2(熔融) Mg+Cl2↑
通电
MgCl2+Ca(OH)2 =Mg(OH)2↓+CaCl2
Mg(OH)2+2HCl = MgCl2+2H2O
海水或卤水
MgCl2
氢氧化镁
Mg(OH)2
MgCl2溶液
MgCl2
盐酸
脱水
镁
电
解
石灰乳
MgCl2 6H2O
由MgCl2·6H2O制备无水MgCl2,必须在HCl气流中加热,以防 MgCl2 水解
因镁在高温下与O2、N2、CO2等气体发生反应,故工业电解得到的镁,在 H2氛围中冷却
工艺流程
海水制镁
课堂探究
环节四:苦卤的利用——海水提溴与提镁
2.所加盐酸是否要过量 目的是什么 如果过量,如何除去
1.海水中本来就有氯化镁,为什么不直接通电 而是要经过“MgCl2→Mg(OH)2→ MgCl2”这样的过程来获取MgCl2呢
要过量,目的是保证Mg(OH)2完全反应,过量的稀盐酸加热蒸发即可除去
除去其他杂质,将MgCl2富集起来
NaOH价格贵,Ca(OH)2 价格便宜且容易得到。工业上可以利用高温煅烧贝壳得到所需要的Ca(OH)2。
贝壳(含CaCO3)
CaO
流程图:
高温煅烧
水
石灰乳
3.为什么不用NaOH代替Ca(OH)2,怎样得到Ca(OH)2 流程图
课堂探究
环节四:苦卤的利用——海水提溴与提镁
海洋生物品种繁多,通过养殖、增殖等途径可实现可持续利用。
课堂探究
拓展:海水资源的多样性——生物资源(海洋生物)
海水运动中蕴藏着巨大的能量,包括潮汐能、波浪能、海流能、温差能和盐差能资源等海上水能资源,它们都属于可再生能源,而且没有污染,具有商业开发价值的。
此外,铀和重水是目前核能开发的重要原料。
课堂探究
拓展:海水资源的多样性——能源资源
大陆架的浅海海底有石油、天然气、煤、硫、磷等;多数近岸带的滨海海盆中有锰结核、可燃冰、砂和砾石,用于冶金、燃料、建筑、石英砂用制玻璃等。
课堂探究
拓展:海水资源的多样性——能源资源
海洋可利用空间包括海上、海中、海底三个部分。海洋空间利用已从传统的交通运输扩大到生产、通信、电力输送、储藏、文化娱乐等诸多领域。
我国拥有18000公里的大陆海岸线,管辖的海域面积近300万平方公里。
课堂探究
拓展:海水资源的多样性——空间资源
课堂练习
【练习1】
1.关于海水资源的综合利用,下列说法错误的是( )
A.海水中含量最高的盐是NaCl
B.电解饱和食盐水可以制得金属钠
C.从海水中提取的镁可用于制造火箭、飞机
D.食用含碘丰富的海产品可防治甲状腺肿大
B
课堂练习
【练习2】
2.水资源是发展国民经济不可缺少的重要自然资源。在世界许多地方,对水的需求已经超过水资源所能负荷的程度,同时有许多地区也存在水资源利用不平衡。下列关于水的说法错误的是( )
A.蒸馏法是海水淡化的方法之一
B.淡水的密度小于海水的密度
C.融化的雪水中矿物质含量比深井水中的少
D.0℃以上,温度越高,水的密度越小
D
课堂练习
【练习3】
A
3.除去粗盐中的杂质MgCl2、CaCl2和Na2SO4,过程如下:
下列有关说法中,不正确的是( )
A.试剂①②③依次加入过量的Na2CO3、NaOH、BaCl2溶液
B.溶解、过滤都用到玻璃棒,其作用是搅拌使加速溶解和引流
C.除去Ca2+的主要反应:Ca2++CO32- ==CaCO3↓
D.向滤液中加入盐酸是为了除去过量的氢氧化钠和碳酸钠
布置作业
预习下节学案。
完成本节素养专练。
谢谢大家
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
