第七章 第四节 基本营养物质 第2课时--人教版高中化学必修第二册教学课件(共26张PPT)
文档属性
| 名称 | 第七章 第四节 基本营养物质 第2课时--人教版高中化学必修第二册教学课件(共26张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 09:10:15 | ||
图片预览






文档简介
(共26张PPT)
第2课时 蛋白质 油脂
第四节 基本营养物质
化学
1.通过日常生活中常见的蛋白质分析蛋白质的水溶性。
2.通过分析氨基酸的官能团,知道氨基酸具有两性,可以发生取代反应和聚合反应。
3.通过实验探究,掌握蛋白质的盐析、变性,并能说出二者的区别;会判断蛋白质分离提纯的方法,知道蛋白质变性的应用;能说出蛋白质的检验方法。
学习目标
4.通过阅读教材所给资料,通过问题的引导,掌握油脂的成分和化学性质。
重点:
蛋白质的性质、油脂的结构与性质。
难点:
利用蛋白质的性质、油脂的结构与性质解释生产生活中的实例。
学习重难点
导入新课
结晶牛胰岛素的合成
我国科学家于1965年在世界上首次完成了具有生命活力的蛋白质——结晶牛胰岛素的全合成,对蛋白质的研究作出了重要贡献。
课堂探究
一、蛋白质
◆蛋白质存在
课堂探究
一、蛋白质
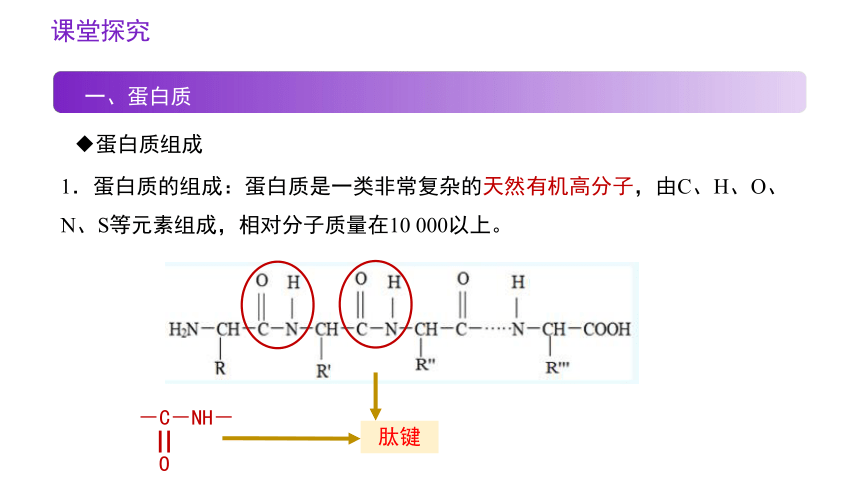
◆蛋白质组成
O
-C-NH-
1.蛋白质的组成:蛋白质是一类非常复杂的天然有机高分子,由C、H、O、N、S等元素组成,相对分子质量在10 000以上。
肽键
课堂探究
一、蛋白质
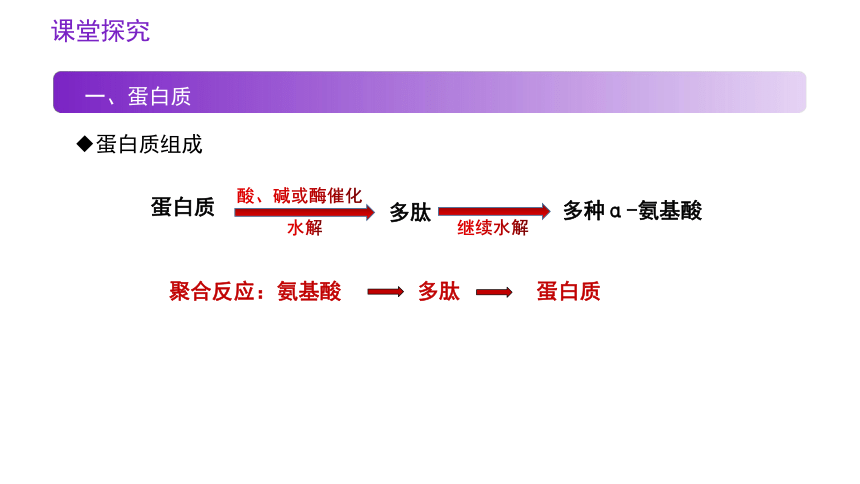
◆蛋白质组成
蛋白质
多肽
多种α-氨基酸
继续水解
水解
酸、碱或酶催化
聚合反应:氨基酸 多肽 蛋白质
课堂探究
一、蛋白质
◆氨基酸的性质
【思考与讨论】观察甘氨酸和苯丙氨酸的结构简式,辨认其中的官能团,并说明其结构的共同点。
CH2—COOH
NH2
甘氨酸
苯丙氨酸
含有共同的官能团:氨基-NH2 、 羧基 -COOH
且两个官能团连在同一个碳原子上。
【思考】由官能团分析氨基酸有哪些化学性质?
课堂探究
一、蛋白质
◆氨基酸的性质
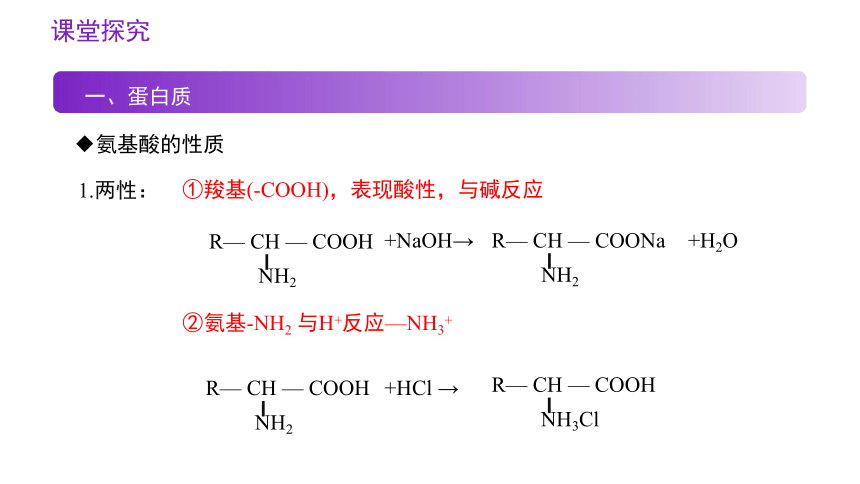
1.两性:
②氨基-NH2 与H+反应—NH3+
NH2
R— CH — COOH
①羧基(-COOH),表现酸性,与碱反应
+NaOH→
NH2
R— CH — COONa
+H2O
NH2
R— CH — COOH
+HCl →
NH3Cl
R— CH — COOH
课堂探究
一、蛋白质
◆氨基酸的性质
2.成肽反应:
R`
+ H-NH— CH — COOH
(酸脱羟基,氨脱氢)
NH2
R— CH — COOH
R`
— NH— CH — COOH+H2O
NH2
R— CH — C
O
二肽
3.聚合反应:
n个氨基酸结合
脱去n-1个H2O
形成n-1个肽键
课堂探究
一、蛋白质
◆蛋白质的性质
(1)向盛有鸡蛋清溶液的试管中加入几滴(CH3COO)2Pb溶液,观察现象。
(2)向盛有鸡蛋清溶液的试管中滴入几滴浓硝酸,加热,观察现象。
(3)在酒精灯的火焰上分别灼烧一小段头发和丝织品,小心地闻气味。
实验现象:
(1)试管内生成白色沉淀。
(2)试管内产生黄色沉淀。
(3)有烧焦羽毛的气味。
课堂探究
一、蛋白质
◆蛋白质的性质
1.变性:某些条件下,蛋白质的分子内部结构和性质发生改变,溶解度下降,失去生理活性。
化学变化,不可逆,即变性后不会恢复
能使蛋白质变性的因素有:
物理因素:加热、加压、搅拌、振荡、紫外线照射、超声波等;
化学因素:强酸、强碱、重金属盐(醋酸铅、硫酸铜、氯化钡)、某些有机物(甲醛、乙醇等)。
课堂探究
一、蛋白质
思考1.①想一想,新型冠状病毒爆发,医院里用高温蒸煮、紫外线照射或涂抹医用酒精等方法进行消毒,原理是什么?
病毒是活的蛋白质,高温、紫外线和酒精都能使蛋白质变性死亡。
课堂探究
一、蛋白质
②在生物实验室,常用甲醛溶液(福尔马林)保存动物标本。
③在农业上,可以用硫酸铜、生石灰和水制成波尔多液防治农作物病害。为什么?
波尔多液既含有重金属离子,又呈强碱性,能够使导致农作物病害的活的蛋白质变性死亡。
福尔马林能使让动物标本腐败的微生物变性死亡,起到防腐的作用,实现长期保存。
课堂探究
一、蛋白质
◆蛋白质的性质
2、盐析
定义:
条件:
过程:
应用:
蛋白质在浓的轻金属盐如Na2SO4、(NH4)2SO4等盐的浓溶液中,由于溶解度的降低而析出
钠盐、铵盐等轻金属盐的浓溶液
可逆的物理变化
分离和提纯蛋白质
课堂探究
一、蛋白质
硝酸可以使含有苯环蛋白质变黄称为蛋白质的显色反应
应用: 检验蛋白质
3、显色反应:
4、灼烧:
蛋白质灼烧时会产生特殊的焦羽毛气味
应用: 鉴别蛋白质产品如真假羊毛衫、蚕丝被
◆蛋白质的性质
课堂探究
一、蛋白质
思考2.钡盐属于重金属盐,医院在做胃透视时要服用“钡餐”BaSO4为何不会中毒?能否改服BaCO3
BaSO4是一种不溶性的重金属盐且不与胃酸反应,BaCO3在胃酸的作用下会溶解,重金属离子Ba2+会使人体蛋白质变性而中毒,所以不能服用BaCO3。
课堂探究
一、蛋白质
思考3.使用浓硝酸时如果不慎溅到皮肤上,皮肤会有什么变化 为什么
皮肤变黄色且最终会脱皮,浓硝酸可以与蛋白质发生显色反应,且能使蛋白质变性。
课堂探究
二、油脂
油(花生油、豆油、茶油、棉籽油、油菜籽油呈液态)
脂肪(猪油、牛油、羊油呈固态)
阅读教材P87内容,完成以下问题。
1.油脂是人类的主要食物之一,也是一种重要的工业原料,我们日常食用的猪油、牛油、羊油、花生油、豆油、茶油、棉籽油、油菜籽油等都是油脂。
以上列举的几种油脂在常温下分别呈什么状态?
◆油脂的状态与结构
课堂探究
二、油脂
2.油脂是由什么组成的?油脂的状态与油脂的分子结构有何关系
油脂是高级脂肪酸与甘油生成的酯。
从分子组成方面来看,油脂可看作是高级脂肪酸和甘油(丙三醇)经酯化反应生成的酯。
当油脂的分子结构中碳链上含有碳碳双键时,其沸点低,常温下呈液态;当油脂的分子结构中碳链全为碳碳单键时,其沸点高,常温下呈固态。
◆油脂的状态与结构
课堂探究
二、油脂
◆油脂的化学性质
1.氢化植物油是普通植物油在一定的温度和压力下加入氢催化而成。植物油氢化的反应属于哪一类有机化学反应?为什么氢化植物油可以延长食物的保质期?
+3H2
①油酯的氢化(硬化)
加成反应
含有碳碳双键的植物油容易被空气中的氧气氧化,碳碳双键被加成后变成碳碳单键,不易被氧化变质。
课堂探究
二、油脂
◆油脂的化学性质
2.人们经常用热的纯碱溶液洗涤炊具上的油污,其原理是什么
炊具上的油污一般是油脂,它属于酯类物质,不溶于水,在碱性条件下水解生成易溶于水的高级脂肪酸盐和甘油。
②油脂的水解反应(皂化反应)
油脂在碱性条件下的水解又叫皂化反应,工业常用来制取肥皂。
油脂+ H2O
高级脂肪酸+甘油
酸或酶
油脂+ H2O
高级脂肪酸盐+甘油
碱性条件
课堂探究
二、油脂
◆油脂在生产、生活中的应用
油脂
是产生能量最高的营养物质
具有保持体温和保护内脏器官的作用
能增加食物的滋味,增进食欲,保证机体的正常生理功能
工业上生产高级脂肪酸和甘油,制肥皂等
课堂小结
蛋白质和油脂
蛋白质
油脂
组成:由碳、氢、氧、氮、硫等元素组成
油脂是高级脂肪酸与甘油生成的酯。由C、H、O三种元素组成
能水解为氨基酸
蛋白质变性、盐析
鉴别蛋白质:显色反应
用于区别合成纤维与蛋白质:灼烧
油:植物油、液体
脂肪:动物油、固体
油酯的氢化:不易变质
油脂的水解反应:生成甘油、高级脂肪酸
布置作业
预习下节学案。
完成本节素养专练。
谢谢大家
第2课时 蛋白质 油脂
第四节 基本营养物质
化学
1.通过日常生活中常见的蛋白质分析蛋白质的水溶性。
2.通过分析氨基酸的官能团,知道氨基酸具有两性,可以发生取代反应和聚合反应。
3.通过实验探究,掌握蛋白质的盐析、变性,并能说出二者的区别;会判断蛋白质分离提纯的方法,知道蛋白质变性的应用;能说出蛋白质的检验方法。
学习目标
4.通过阅读教材所给资料,通过问题的引导,掌握油脂的成分和化学性质。
重点:
蛋白质的性质、油脂的结构与性质。
难点:
利用蛋白质的性质、油脂的结构与性质解释生产生活中的实例。
学习重难点
导入新课
结晶牛胰岛素的合成
我国科学家于1965年在世界上首次完成了具有生命活力的蛋白质——结晶牛胰岛素的全合成,对蛋白质的研究作出了重要贡献。
课堂探究
一、蛋白质
◆蛋白质存在
课堂探究
一、蛋白质
◆蛋白质组成
O
-C-NH-
1.蛋白质的组成:蛋白质是一类非常复杂的天然有机高分子,由C、H、O、N、S等元素组成,相对分子质量在10 000以上。
肽键
课堂探究
一、蛋白质
◆蛋白质组成
蛋白质
多肽
多种α-氨基酸
继续水解
水解
酸、碱或酶催化
聚合反应:氨基酸 多肽 蛋白质
课堂探究
一、蛋白质
◆氨基酸的性质
【思考与讨论】观察甘氨酸和苯丙氨酸的结构简式,辨认其中的官能团,并说明其结构的共同点。
CH2—COOH
NH2
甘氨酸
苯丙氨酸
含有共同的官能团:氨基-NH2 、 羧基 -COOH
且两个官能团连在同一个碳原子上。
【思考】由官能团分析氨基酸有哪些化学性质?
课堂探究
一、蛋白质
◆氨基酸的性质
1.两性:
②氨基-NH2 与H+反应—NH3+
NH2
R— CH — COOH
①羧基(-COOH),表现酸性,与碱反应
+NaOH→
NH2
R— CH — COONa
+H2O
NH2
R— CH — COOH
+HCl →
NH3Cl
R— CH — COOH
课堂探究
一、蛋白质
◆氨基酸的性质
2.成肽反应:
R`
+ H-NH— CH — COOH
(酸脱羟基,氨脱氢)
NH2
R— CH — COOH
R`
— NH— CH — COOH+H2O
NH2
R— CH — C
O
二肽
3.聚合反应:
n个氨基酸结合
脱去n-1个H2O
形成n-1个肽键
课堂探究
一、蛋白质
◆蛋白质的性质
(1)向盛有鸡蛋清溶液的试管中加入几滴(CH3COO)2Pb溶液,观察现象。
(2)向盛有鸡蛋清溶液的试管中滴入几滴浓硝酸,加热,观察现象。
(3)在酒精灯的火焰上分别灼烧一小段头发和丝织品,小心地闻气味。
实验现象:
(1)试管内生成白色沉淀。
(2)试管内产生黄色沉淀。
(3)有烧焦羽毛的气味。
课堂探究
一、蛋白质
◆蛋白质的性质
1.变性:某些条件下,蛋白质的分子内部结构和性质发生改变,溶解度下降,失去生理活性。
化学变化,不可逆,即变性后不会恢复
能使蛋白质变性的因素有:
物理因素:加热、加压、搅拌、振荡、紫外线照射、超声波等;
化学因素:强酸、强碱、重金属盐(醋酸铅、硫酸铜、氯化钡)、某些有机物(甲醛、乙醇等)。
课堂探究
一、蛋白质
思考1.①想一想,新型冠状病毒爆发,医院里用高温蒸煮、紫外线照射或涂抹医用酒精等方法进行消毒,原理是什么?
病毒是活的蛋白质,高温、紫外线和酒精都能使蛋白质变性死亡。
课堂探究
一、蛋白质
②在生物实验室,常用甲醛溶液(福尔马林)保存动物标本。
③在农业上,可以用硫酸铜、生石灰和水制成波尔多液防治农作物病害。为什么?
波尔多液既含有重金属离子,又呈强碱性,能够使导致农作物病害的活的蛋白质变性死亡。
福尔马林能使让动物标本腐败的微生物变性死亡,起到防腐的作用,实现长期保存。
课堂探究
一、蛋白质
◆蛋白质的性质
2、盐析
定义:
条件:
过程:
应用:
蛋白质在浓的轻金属盐如Na2SO4、(NH4)2SO4等盐的浓溶液中,由于溶解度的降低而析出
钠盐、铵盐等轻金属盐的浓溶液
可逆的物理变化
分离和提纯蛋白质
课堂探究
一、蛋白质
硝酸可以使含有苯环蛋白质变黄称为蛋白质的显色反应
应用: 检验蛋白质
3、显色反应:
4、灼烧:
蛋白质灼烧时会产生特殊的焦羽毛气味
应用: 鉴别蛋白质产品如真假羊毛衫、蚕丝被
◆蛋白质的性质
课堂探究
一、蛋白质
思考2.钡盐属于重金属盐,医院在做胃透视时要服用“钡餐”BaSO4为何不会中毒?能否改服BaCO3
BaSO4是一种不溶性的重金属盐且不与胃酸反应,BaCO3在胃酸的作用下会溶解,重金属离子Ba2+会使人体蛋白质变性而中毒,所以不能服用BaCO3。
课堂探究
一、蛋白质
思考3.使用浓硝酸时如果不慎溅到皮肤上,皮肤会有什么变化 为什么
皮肤变黄色且最终会脱皮,浓硝酸可以与蛋白质发生显色反应,且能使蛋白质变性。
课堂探究
二、油脂
油(花生油、豆油、茶油、棉籽油、油菜籽油呈液态)
脂肪(猪油、牛油、羊油呈固态)
阅读教材P87内容,完成以下问题。
1.油脂是人类的主要食物之一,也是一种重要的工业原料,我们日常食用的猪油、牛油、羊油、花生油、豆油、茶油、棉籽油、油菜籽油等都是油脂。
以上列举的几种油脂在常温下分别呈什么状态?
◆油脂的状态与结构
课堂探究
二、油脂
2.油脂是由什么组成的?油脂的状态与油脂的分子结构有何关系
油脂是高级脂肪酸与甘油生成的酯。
从分子组成方面来看,油脂可看作是高级脂肪酸和甘油(丙三醇)经酯化反应生成的酯。
当油脂的分子结构中碳链上含有碳碳双键时,其沸点低,常温下呈液态;当油脂的分子结构中碳链全为碳碳单键时,其沸点高,常温下呈固态。
◆油脂的状态与结构
课堂探究
二、油脂
◆油脂的化学性质
1.氢化植物油是普通植物油在一定的温度和压力下加入氢催化而成。植物油氢化的反应属于哪一类有机化学反应?为什么氢化植物油可以延长食物的保质期?
+3H2
①油酯的氢化(硬化)
加成反应
含有碳碳双键的植物油容易被空气中的氧气氧化,碳碳双键被加成后变成碳碳单键,不易被氧化变质。
课堂探究
二、油脂
◆油脂的化学性质
2.人们经常用热的纯碱溶液洗涤炊具上的油污,其原理是什么
炊具上的油污一般是油脂,它属于酯类物质,不溶于水,在碱性条件下水解生成易溶于水的高级脂肪酸盐和甘油。
②油脂的水解反应(皂化反应)
油脂在碱性条件下的水解又叫皂化反应,工业常用来制取肥皂。
油脂+ H2O
高级脂肪酸+甘油
酸或酶
油脂+ H2O
高级脂肪酸盐+甘油
碱性条件
课堂探究
二、油脂
◆油脂在生产、生活中的应用
油脂
是产生能量最高的营养物质
具有保持体温和保护内脏器官的作用
能增加食物的滋味,增进食欲,保证机体的正常生理功能
工业上生产高级脂肪酸和甘油,制肥皂等
课堂小结
蛋白质和油脂
蛋白质
油脂
组成:由碳、氢、氧、氮、硫等元素组成
油脂是高级脂肪酸与甘油生成的酯。由C、H、O三种元素组成
能水解为氨基酸
蛋白质变性、盐析
鉴别蛋白质:显色反应
用于区别合成纤维与蛋白质:灼烧
油:植物油、液体
脂肪:动物油、固体
油酯的氢化:不易变质
油脂的水解反应:生成甘油、高级脂肪酸
布置作业
预习下节学案。
完成本节素养专练。
谢谢大家
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
