第二章 第二节 烯烃 炔烃 第1课时--人教版高中化学选择性必修第三册教学课件(共28张PPT)
文档属性
| 名称 | 第二章 第二节 烯烃 炔烃 第1课时--人教版高中化学选择性必修第三册教学课件(共28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 983.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 00:00:00 | ||
图片预览






文档简介
(共28张PPT)
第1课时 烯烃
第二节 烯烃、炔烃
化学
1.激发兴趣与思维培养:结合生活实例引入烯烃,培养从化学角度分析生活问题的思维,引导其通过提问归纳掌握烯烃结构与同系物概念。
2.性质规律总结:分析数据,掌握烯烃物理性质规律,基于乙烯性质推导烯烃化学性质,学会运用马氏规则,提升知识迁移与分析归纳能力。
学习目标
3.突破知识难点:阐释顺反异构原理,理解相关概念,突破异构体辨识难点,培养空间想象能力。
重点:
烯烃结构与性质的关系。
难点:
烯烃的立体异构。
学习重难点
情境导入
三天后
四天后
1、熟苹果可以大大缩短青橘子变熟的时间,你知道为什么吗
乙烯-催熟剂
2、天猫超市买到的水果,在水果箱中放入一些用0.2%的KMnO4溶液浸泡过的纸,封严,能延长水果的保质期,你知道原因吗
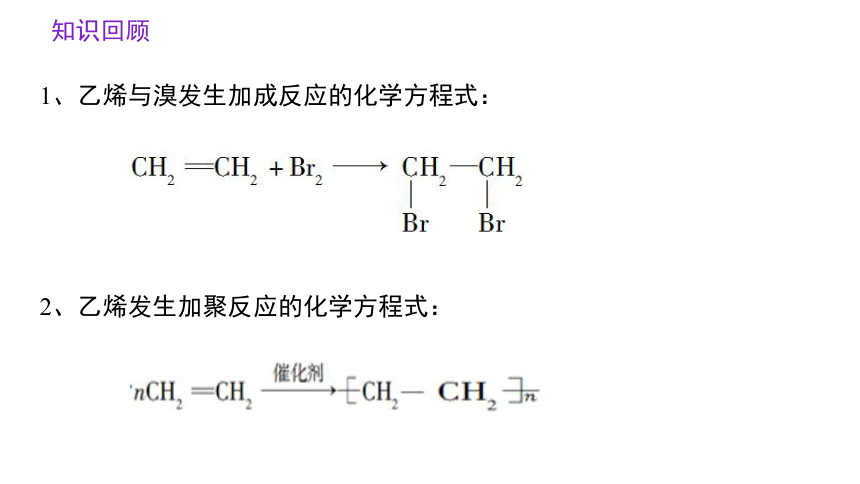
1、乙烯与溴发生加成反应的化学方程式:
2、乙烯发生加聚反应的化学方程式:
知识回顾
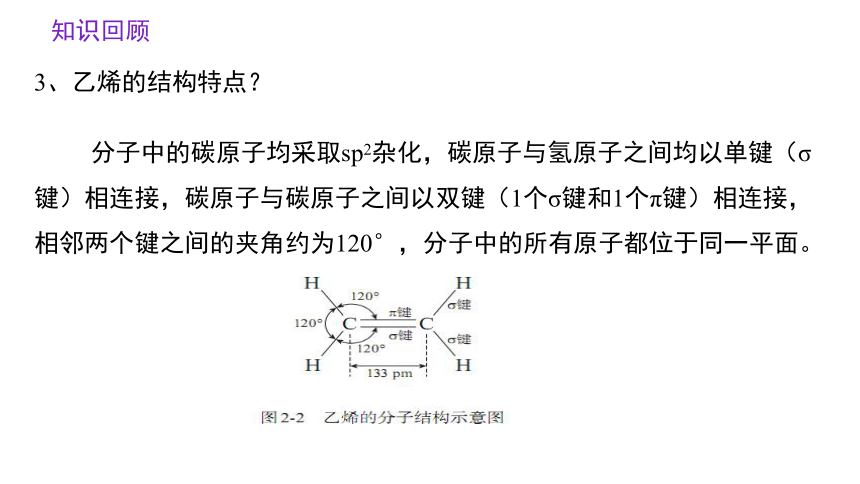
3、乙烯的结构特点?
分子中的碳原子均采取sp2杂化,碳原子与氢原子之间均以单键(σ键)相连接,碳原子与碳原子之间以双键(1个σ键和1个π键)相连接,相邻两个键之间的夹角约为120°,分子中的所有原子都位于同一平面。
知识回顾
1、烯烃中所含官能团名称是什么?
2、烯烃的概念是什么?
3、烯烃的通式是CnH2n(n≥2)?
4、烯烃中碳原子杂化方式是什么?
碳碳双键
含有碳碳双键的烃类有机物
含一个 的链状烯烃的通式为CnH2n(n≥2)
链状烯烃(除乙烯外)分子内碳原子一般存在两种杂化方式:sp2和sp3。
课堂探究
一、烯烃的组成与结构
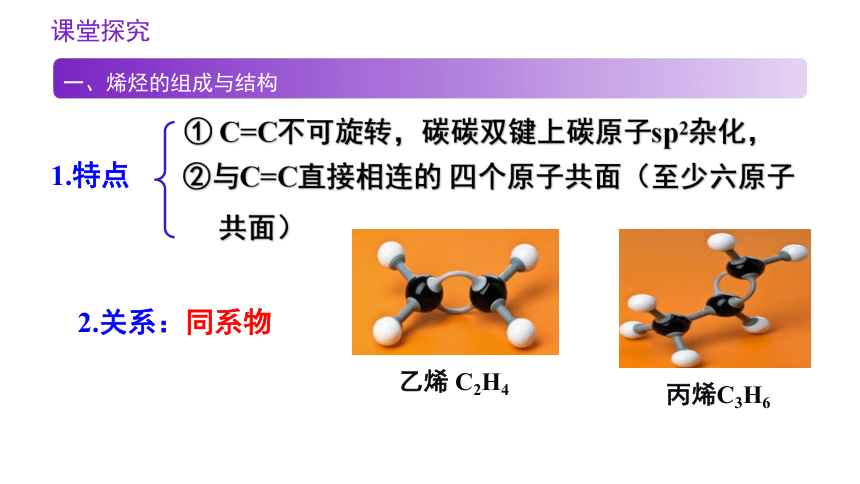
1.特点
① C=C不可旋转,碳碳双键上碳原子sp2杂化,
②与C=C直接相连的 四个原子共面(至少六原子
共面)
2.关系:同系物
乙烯 C2H4
丙烯C3H6
课堂探究
一、烯烃的组成与结构
【课堂练习】
关于2-丁烯的说法不正确的是( )
B
A: 四个C原子一定在同一平面上
B: 2-丁烯与C3H6是同系物
C: 2-丁烯的C原子的杂化方式是sp2和sp3
D: 2-丁烯一定共面的原子有6个
课堂探究
名称 结构简式 沸点 相对密度
乙烯 CH2=CH2 -103.7 0.566
丙烯 CH2=CHCH3 -47.4 0.519
1-丁烯 CH2=CHCH2CH3 -6.3 0.595
1-戊烯 CH2=CH(CH2) 2CH3 30 0.640
1-己烯 CH2=CH(CH2)3CH3 63.3 0.673
1-庚烯 CH2=CH(CH2)4CH3 93.6 0.697
问题1:烯烃沸点和密度的变化规律?
随着碳原子数目的增多,烷烃和烯烃的同系物的沸点逐渐升高,密度逐渐增大。常温下的状态由气体到液态到固体。同分异构体支链越多,沸点越低。
课堂探究
二、烯烃的物理性质
名称 结构简式 沸点 相对密度
乙烯 CH2=CH2 -103.7 0.566
丙烯 CH2=CHCH3 -47.4 0.519
1-丁烯 CH2=CHCH2CH3 -6.3 0.595
1-戊烯 CH2=CH(CH2) 2CH3 30 0.640
1-己烯 CH2=CH(CH2)3CH3 63.3 0.673
1-庚烯 CH2=CH(CH2)4CH3 93.6 0.697
问题2:上述沸点变化的原因?
结构相似的分子,相对分子质量越大,范德华力越大,熔沸点越高。
课堂探究
二、烯烃的物理性质
名称 结构简式 沸点 相对密度
乙烯 CH2=CH2 -103.7 0.566
丙烯 CH2=CHCH3 -47.4 0.519
1-丁烯 CH2=CHCH2CH3 -6.3 0.595
1-戊烯 CH2=CH(CH2) 2CH3 30 0.640
1-己烯 CH2=CH(CH2)3CH3 63.3 0.673
1-庚烯 CH2=CH(CH2)4CH3 93.6 0.697
问题3 :烯烃状态的变化情况?
C1~C4气态; 4 以上为液态或固态
课堂探究
二、烯烃的物理性质
■熔沸点:
随着C个数增加,熔沸点逐渐升高
C个数相同,支链越多反而越低
■状态:
C1~C4气态; 4 以上为液态或固态,
■密度:
随着C个数增加,密度逐渐增加,但都比水小
■水溶性:
都难溶于水,但易溶于有机溶剂
课堂探究
二、烯烃的物理性质
答案: > >
课堂探究
二、烯烃的物理性质
思考:根据乙烯的性质预测烯烃有哪些化学性质?
烯烃由于有官能团“碳碳双键”,均可发生氧化反应、加成反应、加聚反应
课堂探究
三、烯烃的化学性质
(1)氧化反应
①燃烧:
火焰明亮,冒黑烟
②与酸性KMnO4的作用:
使KMnO4溶液褪色
课堂探究
三、烯烃的化学性质
(2)加成反应 ( 与H2、Br2、HX、H2O、HCN等)
试剂 乙烯 丙烯
溴水
氯化氢
水
CH2===CH2+Br2→CH2Br—CH2Br
CH2===CH2+HCl→CH3CH2Cl
CH2===CH2+H2O→CH3CH2OH
CH3CH===CH2+Br2→CH3CHBrCH2Br
CH3CH===CH2+HCl→CH3CH2CH2Cl
CH3CH===CH2+HCl→CH3CHClCH3
CH3—CH===CH2+H2O→CH3CH2CH2OH
课堂探究
三、烯烃的化学性质
例:丙烯与氯化氢、H2O加成时哪种产物更多
大量实验事实表明:凡是不对称结构的烯烃和卤化氢(HX)加成时,卤素原子主要加到含氢原子较少的双键碳原子上,这称为马尔科夫尼科夫规则,也就是马氏规则。(氢上加氢)
课堂探究
三、烯烃的化学性质
【评价任务1】根据已有的知识设计制备氯乙烷的实验方案。
课堂探究
三、烯烃的化学性质
方案1:乙烯和氯化氢的加成反应制备
方案2:利用乙烷和氯气发生取代反应制备
原子利用率达到100%(没有副产物)
除了生成一氯乙烷,还会有氯化氢、二氯乙烷、三氯乙烷……,副产物多,产率低,物质的分离提纯也难。
【评价任务2】现有两种无色气体丙烷和丙烯,如何鉴别?
课堂探究
三、烯烃的化学性质
分别将其通入KMnO4溶液中,能使其褪色的为乙烯
分别将其通入Br2的CCl4溶液中,能使其褪色的为乙烯
【评价任务3】现有两种无色气体丙烷和丙烯,如何除去丙烯?
将混合气体通入溴水中洗气
【评价任务4】1-丁烯与氯化氢的反应
CH2=CHCH2CH3 + HCl CH3CHCl CH2CH3
CH2=CHCH2CH3 + HCl CH2ClCH2 CH2CH3
课堂探究
三、烯烃的化学性质
单体
链节
聚合度
(3)加聚反应
课堂探究
三、烯烃的化学性质
课堂探究
三、烯烃的化学性质
练习:分别写出氯乙烯发生加聚反应,异丁烯发生加聚反应的化学方程式。
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象,称为顺反异构。
产生顺反异构体的条件:
双键两端的同一个碳原子上不能连有相同基团只有这样才会产生顺反异构体。即:a' b'且a b 。
课堂探究
四、烯烃的顺反异构
两个相同的原子或原子团排列在双键的同一侧的称为顺式结构。
两个相同的原子或原子团排列在双键的两侧的称为反式结构。
课堂探究
四、烯烃的顺反异构
思考:互为顺反异构体的有机物物理性质和化学性质相同么?
化学性质基本相同,物理性质有一定的差异。
课堂探究
四、烯烃的顺反异构
A
B
C
D
练习:下列存在顺反异构的分子是( )
A、B
课堂练习
谢谢大家
第1课时 烯烃
第二节 烯烃、炔烃
化学
1.激发兴趣与思维培养:结合生活实例引入烯烃,培养从化学角度分析生活问题的思维,引导其通过提问归纳掌握烯烃结构与同系物概念。
2.性质规律总结:分析数据,掌握烯烃物理性质规律,基于乙烯性质推导烯烃化学性质,学会运用马氏规则,提升知识迁移与分析归纳能力。
学习目标
3.突破知识难点:阐释顺反异构原理,理解相关概念,突破异构体辨识难点,培养空间想象能力。
重点:
烯烃结构与性质的关系。
难点:
烯烃的立体异构。
学习重难点
情境导入
三天后
四天后
1、熟苹果可以大大缩短青橘子变熟的时间,你知道为什么吗
乙烯-催熟剂
2、天猫超市买到的水果,在水果箱中放入一些用0.2%的KMnO4溶液浸泡过的纸,封严,能延长水果的保质期,你知道原因吗
1、乙烯与溴发生加成反应的化学方程式:
2、乙烯发生加聚反应的化学方程式:
知识回顾
3、乙烯的结构特点?
分子中的碳原子均采取sp2杂化,碳原子与氢原子之间均以单键(σ键)相连接,碳原子与碳原子之间以双键(1个σ键和1个π键)相连接,相邻两个键之间的夹角约为120°,分子中的所有原子都位于同一平面。
知识回顾
1、烯烃中所含官能团名称是什么?
2、烯烃的概念是什么?
3、烯烃的通式是CnH2n(n≥2)?
4、烯烃中碳原子杂化方式是什么?
碳碳双键
含有碳碳双键的烃类有机物
含一个 的链状烯烃的通式为CnH2n(n≥2)
链状烯烃(除乙烯外)分子内碳原子一般存在两种杂化方式:sp2和sp3。
课堂探究
一、烯烃的组成与结构
1.特点
① C=C不可旋转,碳碳双键上碳原子sp2杂化,
②与C=C直接相连的 四个原子共面(至少六原子
共面)
2.关系:同系物
乙烯 C2H4
丙烯C3H6
课堂探究
一、烯烃的组成与结构
【课堂练习】
关于2-丁烯的说法不正确的是( )
B
A: 四个C原子一定在同一平面上
B: 2-丁烯与C3H6是同系物
C: 2-丁烯的C原子的杂化方式是sp2和sp3
D: 2-丁烯一定共面的原子有6个
课堂探究
名称 结构简式 沸点 相对密度
乙烯 CH2=CH2 -103.7 0.566
丙烯 CH2=CHCH3 -47.4 0.519
1-丁烯 CH2=CHCH2CH3 -6.3 0.595
1-戊烯 CH2=CH(CH2) 2CH3 30 0.640
1-己烯 CH2=CH(CH2)3CH3 63.3 0.673
1-庚烯 CH2=CH(CH2)4CH3 93.6 0.697
问题1:烯烃沸点和密度的变化规律?
随着碳原子数目的增多,烷烃和烯烃的同系物的沸点逐渐升高,密度逐渐增大。常温下的状态由气体到液态到固体。同分异构体支链越多,沸点越低。
课堂探究
二、烯烃的物理性质
名称 结构简式 沸点 相对密度
乙烯 CH2=CH2 -103.7 0.566
丙烯 CH2=CHCH3 -47.4 0.519
1-丁烯 CH2=CHCH2CH3 -6.3 0.595
1-戊烯 CH2=CH(CH2) 2CH3 30 0.640
1-己烯 CH2=CH(CH2)3CH3 63.3 0.673
1-庚烯 CH2=CH(CH2)4CH3 93.6 0.697
问题2:上述沸点变化的原因?
结构相似的分子,相对分子质量越大,范德华力越大,熔沸点越高。
课堂探究
二、烯烃的物理性质
名称 结构简式 沸点 相对密度
乙烯 CH2=CH2 -103.7 0.566
丙烯 CH2=CHCH3 -47.4 0.519
1-丁烯 CH2=CHCH2CH3 -6.3 0.595
1-戊烯 CH2=CH(CH2) 2CH3 30 0.640
1-己烯 CH2=CH(CH2)3CH3 63.3 0.673
1-庚烯 CH2=CH(CH2)4CH3 93.6 0.697
问题3 :烯烃状态的变化情况?
C1~C4气态; 4 以上为液态或固态
课堂探究
二、烯烃的物理性质
■熔沸点:
随着C个数增加,熔沸点逐渐升高
C个数相同,支链越多反而越低
■状态:
C1~C4气态; 4 以上为液态或固态,
■密度:
随着C个数增加,密度逐渐增加,但都比水小
■水溶性:
都难溶于水,但易溶于有机溶剂
课堂探究
二、烯烃的物理性质
答案: > >
课堂探究
二、烯烃的物理性质
思考:根据乙烯的性质预测烯烃有哪些化学性质?
烯烃由于有官能团“碳碳双键”,均可发生氧化反应、加成反应、加聚反应
课堂探究
三、烯烃的化学性质
(1)氧化反应
①燃烧:
火焰明亮,冒黑烟
②与酸性KMnO4的作用:
使KMnO4溶液褪色
课堂探究
三、烯烃的化学性质
(2)加成反应 ( 与H2、Br2、HX、H2O、HCN等)
试剂 乙烯 丙烯
溴水
氯化氢
水
CH2===CH2+Br2→CH2Br—CH2Br
CH2===CH2+HCl→CH3CH2Cl
CH2===CH2+H2O→CH3CH2OH
CH3CH===CH2+Br2→CH3CHBrCH2Br
CH3CH===CH2+HCl→CH3CH2CH2Cl
CH3CH===CH2+HCl→CH3CHClCH3
CH3—CH===CH2+H2O→CH3CH2CH2OH
课堂探究
三、烯烃的化学性质
例:丙烯与氯化氢、H2O加成时哪种产物更多
大量实验事实表明:凡是不对称结构的烯烃和卤化氢(HX)加成时,卤素原子主要加到含氢原子较少的双键碳原子上,这称为马尔科夫尼科夫规则,也就是马氏规则。(氢上加氢)
课堂探究
三、烯烃的化学性质
【评价任务1】根据已有的知识设计制备氯乙烷的实验方案。
课堂探究
三、烯烃的化学性质
方案1:乙烯和氯化氢的加成反应制备
方案2:利用乙烷和氯气发生取代反应制备
原子利用率达到100%(没有副产物)
除了生成一氯乙烷,还会有氯化氢、二氯乙烷、三氯乙烷……,副产物多,产率低,物质的分离提纯也难。
【评价任务2】现有两种无色气体丙烷和丙烯,如何鉴别?
课堂探究
三、烯烃的化学性质
分别将其通入KMnO4溶液中,能使其褪色的为乙烯
分别将其通入Br2的CCl4溶液中,能使其褪色的为乙烯
【评价任务3】现有两种无色气体丙烷和丙烯,如何除去丙烯?
将混合气体通入溴水中洗气
【评价任务4】1-丁烯与氯化氢的反应
CH2=CHCH2CH3 + HCl CH3CHCl CH2CH3
CH2=CHCH2CH3 + HCl CH2ClCH2 CH2CH3
课堂探究
三、烯烃的化学性质
单体
链节
聚合度
(3)加聚反应
课堂探究
三、烯烃的化学性质
课堂探究
三、烯烃的化学性质
练习:分别写出氯乙烯发生加聚反应,异丁烯发生加聚反应的化学方程式。
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排列方式不同所产生的异构现象,称为顺反异构。
产生顺反异构体的条件:
双键两端的同一个碳原子上不能连有相同基团只有这样才会产生顺反异构体。即:a' b'且a b 。
课堂探究
四、烯烃的顺反异构
两个相同的原子或原子团排列在双键的同一侧的称为顺式结构。
两个相同的原子或原子团排列在双键的两侧的称为反式结构。
课堂探究
四、烯烃的顺反异构
思考:互为顺反异构体的有机物物理性质和化学性质相同么?
化学性质基本相同,物理性质有一定的差异。
课堂探究
四、烯烃的顺反异构
A
B
C
D
练习:下列存在顺反异构的分子是( )
A、B
课堂练习
谢谢大家
