第三章 第三节 醛 酮 第1课时--人教版高中化学选择性必修第三册教学课件(共19张PPT)
文档属性
| 名称 | 第三章 第三节 醛 酮 第1课时--人教版高中化学选择性必修第三册教学课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 09:10:15 | ||
图片预览





文档简介
(共19张PPT)
第1课时 乙醛
第三节 醛 酮
化学
1.能够阐述酒精转化为乙醛的反应过程,理解醛在生活中的常见存在形式及其用途,形成 “化学与生活紧密相关” 的认知,培养 “科学态度与社会责任” 的学科核心素养。
2.通过观察分析醛的结构特点,准确识别醛类物质的碳骨架结构和官能团,学会从结构角度分析有机物性质,强化 “宏观辨识与微观探析” 的学科核心素养,树立 “结构决定性质” 的化学观念。
学习目标
3.根据对醛类物质性质的预测,自主设计并完成给定试剂的实验,熟练掌握实验操作技能,学会观察、记录和分析实验现象,提高 “科学探究与创新意识” 的学科核心素养。
重点:
从物质结构分析得出模型,建立认识有机物化学性质的预测模型,进而总结研究有机物性质的一般思路。
难点:
通过乙醛性质的学习,实现从有机物官能团深入到化学键水平的认识。
学习重难点
课前预习
1. 乙醛的物理性质
乙醛是一种无色,有刺激性气味的液体,密度比水的小,沸点20.8℃,易挥发,易燃烧,易溶于水(氢键的作用)及乙醇、乙醚、氯仿等有机溶剂。
课前预习
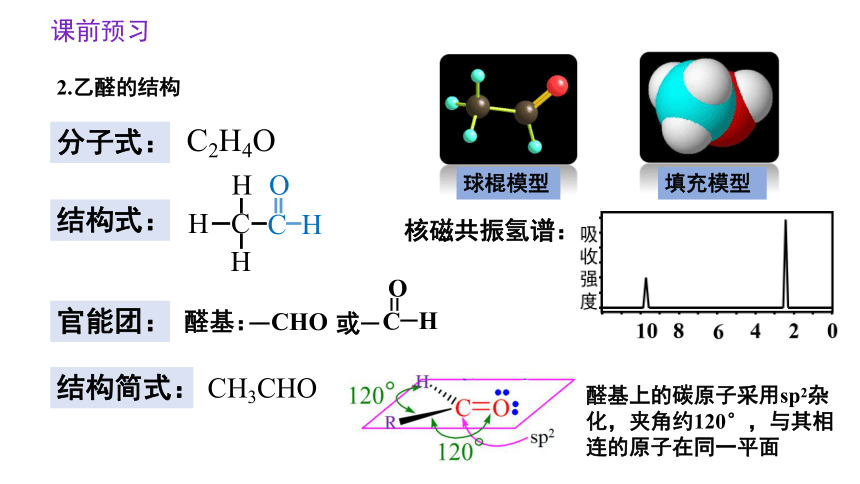
分子式:
结构简式:
结构式:
C2H4O
H
H
H
H
C
C
O
CH3CHO
球棍模型
填充模型
核磁共振氢谱:
醛基上的碳原子采用sp2杂化,夹角约120°,与其相连的原子在同一平面
2.乙醛的结构
官能团:
醛基:
CHO
或
C
H
O
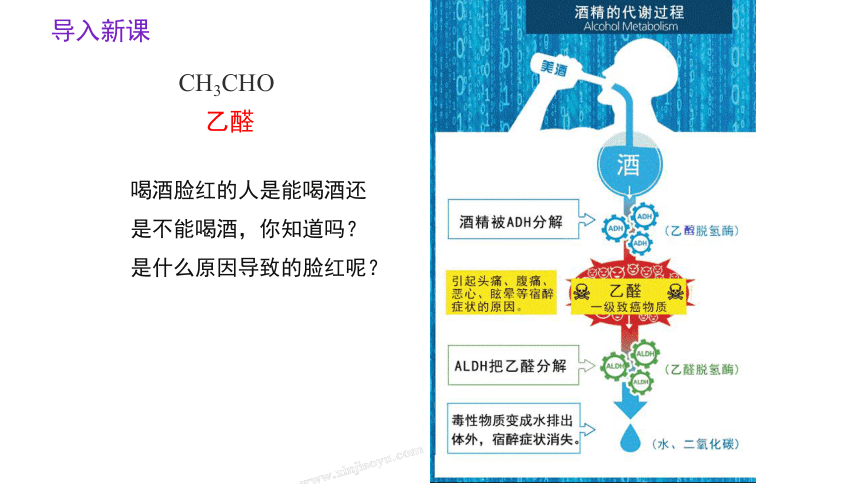
导入新课
喝酒脸红的人是能喝酒还是不能喝酒,你知道吗?是什么原因导致的脸红呢?
乙醛
CH3CHO
课堂探究
一、认识乙醛——危害健康的元凶
1.酒精如何转化为乙醛?
乙醇 乙醛 乙酸
氧化(去H) 氧化(加O)
课堂探究
二、分析结构,推测断键部位
2. 思考身边哪些物质属于醛,并说说它们的用途。
身边的化学
苯甲醛
肉桂醛
柠檬醛
蜜蜂传递警戒信息的激素中含有的2-庚酮
2-庚酮
课堂探究
二、分析结构,推测断键部位
3. 通过观察各种醛的结构特点,分析醛的碳骨架结构和官能团的特点。
以乙醛为例:
课堂探究
二、分析结构,推测断键部位
4. 乙醛的加成反应
a.催化加氢:
催化剂
C
C
O
H
H
H
H
+ H—H
C
C
O
H
H
H
H
H
H
CH3CHO+H2
CH3CH2OH
催化剂
注意:
①C=O(醛基/羰基)和C=C双键不同的是,通常情况下,C=O(醛基/羰基)不能和HX、X2、H2O发生加成反应。
②酯基(-COO-)和羧基 (-COOH) 中的C=O不能与H2发生加成反应
(还原反应)
课堂探究
二、分析结构,推测断键部位
在醛基中,由于氧原子电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,碳原子带部分正电荷,从而使醛基具有较强的极性。醛基/羰基能和极性试剂(如H CN、H NH2、H NHR、H OCH3等)发生加成反应。
+
C
O
δ+
δ-
B — A
δ+
δ-
O
—A
C
B
双键变单键
异性相吸
δ+
δ-
δ+
δ-
b.与极性试剂加成
课堂探究
二、分析结构,推测断键部位
与HCN加成
δ+
δ-
+H—CN →
—C—CN
OH
α-羟基腈
应用:醛与氢氰酸加成,在有机合成中可以用来增长碳链。
CH3─C─H
O
+ H─CN→
CH3─CH─CN
OH
2 羟基丙腈
5.分析醛基结构,推测醛类物质反应时可能的断键部位和反应类型,并说明其依据。
课堂探究
二、分析结构,推测断键部位
课堂探究
二、分析结构,推测断键部位
【思考交流】
对于一个陌生的有机物分子如何分析其结构?试分析总结有机化合物结构的一般思路。
从结构角度分析有机化合物化学性质的思路:
课堂探究
三、证据探究,实验求证
6. 各小组展开组内讨论,根据断键部位推测反应类型,选择合适试剂预测可能的产物,形成实验方案后汇报,利用提供的仪器和试剂进行探究,以小组为单位完成实验。
试剂和仪器:乙醛溶液,AgNO3溶液,氨水,酸性KMnO4溶液,CuSO4溶液,NaOH溶液,蒸馏水;酒精灯,烧杯,玻璃棒,试管,胶头滴管等。
实验过程及记录:
①预测实验产物;②实验步骤;③实验现象;④实验结论。
【问题思考】
展示出每一种探究实验的基本思路及所依据的反应机理。
课堂探究
三、证据探究,实验求证
实验内容 实验操作 实验现象 化学方程式
1.乙醛与酸性高锰酸钾溶液反应 取适量乙醛溶液于试管中,加入酸性高锰酸钾溶液,振荡,观察现象 酸性高锰酸钾溶液褪色 —
2.乙醛与银氨溶液反应 向新配制的银氨溶液中加入3滴乙醛溶液,水浴加热 洁净的试管内壁形成光亮的银镜 CH3CHO+2[Ag(NH3)2]OH
CH3COONH4+2Ag↓+3NH3+H2O
3.乙醛与新制氢氧化铜反应 向 2 mL 10% 的氢氧化钠溶液中加入5滴 5% 的硫酸铜溶液,振荡后加入 0.5 mL乙醛溶液,用酒精灯加热,观察实验现象 有砖红色沉淀生成 CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
四、总结提升,构建模型
课堂小结
7. 根据以上结构分析、性质预测、实验验证,你认为研究有机化合物性质的一般思路方法是什么?试归纳总结。
认识有机物性质的一般思路:
布置作业
制作手抄报:每个小组制作一个以“饮酒与健康”为主题的手抄报,提醒人们要关注健康,远离酒精。
完成学案中的素养专练。
谢谢大家
第1课时 乙醛
第三节 醛 酮
化学
1.能够阐述酒精转化为乙醛的反应过程,理解醛在生活中的常见存在形式及其用途,形成 “化学与生活紧密相关” 的认知,培养 “科学态度与社会责任” 的学科核心素养。
2.通过观察分析醛的结构特点,准确识别醛类物质的碳骨架结构和官能团,学会从结构角度分析有机物性质,强化 “宏观辨识与微观探析” 的学科核心素养,树立 “结构决定性质” 的化学观念。
学习目标
3.根据对醛类物质性质的预测,自主设计并完成给定试剂的实验,熟练掌握实验操作技能,学会观察、记录和分析实验现象,提高 “科学探究与创新意识” 的学科核心素养。
重点:
从物质结构分析得出模型,建立认识有机物化学性质的预测模型,进而总结研究有机物性质的一般思路。
难点:
通过乙醛性质的学习,实现从有机物官能团深入到化学键水平的认识。
学习重难点
课前预习
1. 乙醛的物理性质
乙醛是一种无色,有刺激性气味的液体,密度比水的小,沸点20.8℃,易挥发,易燃烧,易溶于水(氢键的作用)及乙醇、乙醚、氯仿等有机溶剂。
课前预习
分子式:
结构简式:
结构式:
C2H4O
H
H
H
H
C
C
O
CH3CHO
球棍模型
填充模型
核磁共振氢谱:
醛基上的碳原子采用sp2杂化,夹角约120°,与其相连的原子在同一平面
2.乙醛的结构
官能团:
醛基:
CHO
或
C
H
O
导入新课
喝酒脸红的人是能喝酒还是不能喝酒,你知道吗?是什么原因导致的脸红呢?
乙醛
CH3CHO
课堂探究
一、认识乙醛——危害健康的元凶
1.酒精如何转化为乙醛?
乙醇 乙醛 乙酸
氧化(去H) 氧化(加O)
课堂探究
二、分析结构,推测断键部位
2. 思考身边哪些物质属于醛,并说说它们的用途。
身边的化学
苯甲醛
肉桂醛
柠檬醛
蜜蜂传递警戒信息的激素中含有的2-庚酮
2-庚酮
课堂探究
二、分析结构,推测断键部位
3. 通过观察各种醛的结构特点,分析醛的碳骨架结构和官能团的特点。
以乙醛为例:
课堂探究
二、分析结构,推测断键部位
4. 乙醛的加成反应
a.催化加氢:
催化剂
C
C
O
H
H
H
H
+ H—H
C
C
O
H
H
H
H
H
H
CH3CHO+H2
CH3CH2OH
催化剂
注意:
①C=O(醛基/羰基)和C=C双键不同的是,通常情况下,C=O(醛基/羰基)不能和HX、X2、H2O发生加成反应。
②酯基(-COO-)和羧基 (-COOH) 中的C=O不能与H2发生加成反应
(还原反应)
课堂探究
二、分析结构,推测断键部位
在醛基中,由于氧原子电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,碳原子带部分正电荷,从而使醛基具有较强的极性。醛基/羰基能和极性试剂(如H CN、H NH2、H NHR、H OCH3等)发生加成反应。
+
C
O
δ+
δ-
B — A
δ+
δ-
O
—A
C
B
双键变单键
异性相吸
δ+
δ-
δ+
δ-
b.与极性试剂加成
课堂探究
二、分析结构,推测断键部位
与HCN加成
δ+
δ-
+H—CN →
—C—CN
OH
α-羟基腈
应用:醛与氢氰酸加成,在有机合成中可以用来增长碳链。
CH3─C─H
O
+ H─CN→
CH3─CH─CN
OH
2 羟基丙腈
5.分析醛基结构,推测醛类物质反应时可能的断键部位和反应类型,并说明其依据。
课堂探究
二、分析结构,推测断键部位
课堂探究
二、分析结构,推测断键部位
【思考交流】
对于一个陌生的有机物分子如何分析其结构?试分析总结有机化合物结构的一般思路。
从结构角度分析有机化合物化学性质的思路:
课堂探究
三、证据探究,实验求证
6. 各小组展开组内讨论,根据断键部位推测反应类型,选择合适试剂预测可能的产物,形成实验方案后汇报,利用提供的仪器和试剂进行探究,以小组为单位完成实验。
试剂和仪器:乙醛溶液,AgNO3溶液,氨水,酸性KMnO4溶液,CuSO4溶液,NaOH溶液,蒸馏水;酒精灯,烧杯,玻璃棒,试管,胶头滴管等。
实验过程及记录:
①预测实验产物;②实验步骤;③实验现象;④实验结论。
【问题思考】
展示出每一种探究实验的基本思路及所依据的反应机理。
课堂探究
三、证据探究,实验求证
实验内容 实验操作 实验现象 化学方程式
1.乙醛与酸性高锰酸钾溶液反应 取适量乙醛溶液于试管中,加入酸性高锰酸钾溶液,振荡,观察现象 酸性高锰酸钾溶液褪色 —
2.乙醛与银氨溶液反应 向新配制的银氨溶液中加入3滴乙醛溶液,水浴加热 洁净的试管内壁形成光亮的银镜 CH3CHO+2[Ag(NH3)2]OH
CH3COONH4+2Ag↓+3NH3+H2O
3.乙醛与新制氢氧化铜反应 向 2 mL 10% 的氢氧化钠溶液中加入5滴 5% 的硫酸铜溶液,振荡后加入 0.5 mL乙醛溶液,用酒精灯加热,观察实验现象 有砖红色沉淀生成 CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
四、总结提升,构建模型
课堂小结
7. 根据以上结构分析、性质预测、实验验证,你认为研究有机化合物性质的一般思路方法是什么?试归纳总结。
认识有机物性质的一般思路:
布置作业
制作手抄报:每个小组制作一个以“饮酒与健康”为主题的手抄报,提醒人们要关注健康,远离酒精。
完成学案中的素养专练。
谢谢大家
