第三章 章末复习 第1、2课时--人教版高中化学选择性必修第三册教学课件(共26张PPT)
文档属性
| 名称 | 第三章 章末复习 第1、2课时--人教版高中化学选择性必修第三册教学课件(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 357.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 00:00:00 | ||
图片预览








文档简介
(共26张PPT)
第1、2课时
第三章 烃的衍生物 章末复习
化学
1.通过小组合作学习,总结归纳以反应类型为载体的物质转化关系,并以思维导图的形式进行呈现,建立结构变化与反应类型的对应关系,丰富结构决定性质的认识角度。
2.通过对各步物质转化的反应条件、碳骨架的变化及官能团的转化的分析,巩固基础,强化反应条件与物质转化的联系,建立由条件推测反应类型及官能团转化的基本思维模型。
3.通过小组竞赛的方式交流讨论引入各种常见官能团的方法,激发学生的学习主动性,并能应用解决部分实际问题。
学习目标
4.通过以乙醇为原料合成对羟基苯甲酸乙酯和离子导体材料中的有机溶剂,巩固官能团引入的方法,体会有机合成中官能团的定位和保护,巩固正、逆合成分析法。
重点、难点:
以反应类型为载体的物质转化关系,官能团的引入和保护,逆合成分析法。
学习重难点
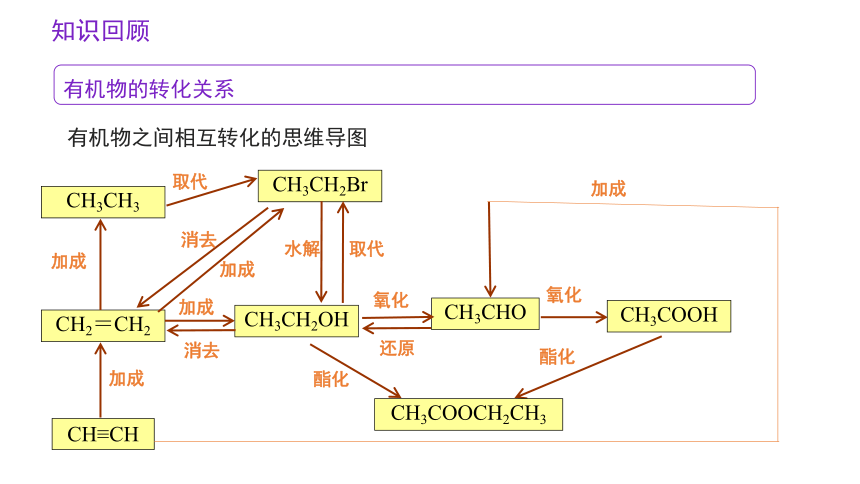
有机物的转化关系
有机物之间相互转化的思维导图
知识回顾
CH≡CH
加成
CH2=CH2
加成
CH3CH3
加成
CH3CH2OH
CH3CHO
CH3CH2Br
取代
消去
水解
取代
氧化
氧化
CH3COOH
CH3COOCH2CH3
酯化
消去
加成
还原
酯化
加成
课堂探究
一、有机反应类型总结
【问题1】“结构决定性质,性质体现应用”是我们学习有机化学的重要认识思路,请梳理乙醇能发生的反应类型及可制得的物质种类,从结构角度分析乙醇为什么会成为科学家进行合成的重要原料。
乙醇的官能团-OH可发生取代反应、消去反应、氧化反应等多种反应类型,生成卤代烃、醚、酯、烯烃、醛等多类物质。
课堂探究
【问题2】有机反应常见的反应类型有哪些,并准确描述其概念。
①取代反应:有机物化合物分子中任何一个原子或原子团被试剂中同类型的其他原子或原子团所替代的反应 。
②加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
③消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含有不饱和键的化合物的反应。
④氧化反应和还原反应:通常把有机化合物分子中失去氢原子或加入氧原子的反应叫氧化反应;通常把有机化合物分子中失去氧原子或加入氢原子的反应叫还原反应。
课堂探究
【问题3】
①独立思考能发生取代反应的有机物及官能团的种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示, 用时3分钟。
二、取代反应
课堂探究
能发生取代反应的有机物的种类:卤代烃、醇、酚、羧酸、酯、酰胺。
卤代烃的水解反应条件:NaOH溶液、加热;
醇与氢卤酸的反应条件:加热;
醇之间的成醚反应条件:浓硫酸、加热;
醇与羧酸之间的酯化反应条件:浓硫酸、加热;
酚与溴水的反应条件:饱和溴水。
酯的水解反应条件:稀硫酸或NaOH溶液、加热;
酰胺的水解反应条件:盐酸或NaOH溶液、加热。
二、取代反应
课堂探究
【问题4】
①独立思考能发生加成反应的有机物及官能团种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示,用时3分钟。
三、加成反应
课堂探究
能发生加成反应的有机物的种类:烯烃、炔烃、苯、醛、酮、油脂。
烯烃、炔烃、苯、醛、酮、油脂与H2的反应条件:催化剂、加热;
醛与HCN的反应:催化剂。
三、加成反应
【问题5】
与氢气的加成反应还可以看成什么反应类型?
还原反应
课堂探究
【问题6】
①独立思考能发生消去反应的有机物及官能团的种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示,用时3分钟。
能发生消去反应的有机物种类:卤代烃、醇。
卤代烃的消去反应条件:NaOH的醇溶液、加热;
醇的消去反应条件:浓硫酸、加热。
四、消去反应
课堂探究
【问题7】
①独立思考能发生氧化反应(不含有机物的燃烧反应)的有机物及官能团的种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示,用时3分钟。
五、氧化反应(不含有机物的燃烧反应)
课堂探究
能发生氧化反应(不含有机物的燃烧反应)的有机物的种类:醇、酚、醛。
醇的氧化反应 (不含有机物的燃烧反应):O2、催化剂、加热或酸性K2Cr2O7溶液;
酚的氧化反应 (不含有机物的燃烧反应):O2或酸性K2Cr2O7溶液;
醛的氧化反应 (不含有机物的燃烧反应):银氨溶液、水浴加热或氢氧化铜悬浊液、加热或酸性K2Cr2O7溶液或O2、催化剂、加热。
五、氧化反应(不含有机物的燃烧反应)
课堂探究
六、引入官能团的方法
【问题8】小组竞赛活动:
独立思考总结引入—X、 — OH、 — CHO、 — COOH、 — COOR、 — CONHR等官能团的方法,用时2分钟;小组合作完善,先完成的小组,在黑板上展示引入各种常见官能团的方法,合作与展示共5分钟。
课堂探究
六、引入官能团的方法
—X的引入方法:烷烃与X2的取代反应;烯烃、炔烃与HX的加成反应;醇与HX的取代反应。
—OH的引入方法:烯烃与H2O的加成反应;卤代烃的水解反应;酯的水解反应;醛、酮与H2的加成反应。
—CHO的引入方法:醇的氧化反应。
—COOH的引入方法:醛的氧化反应;酯的水解反应;酰胺的水解反应;苯的同系物的氧化反应。
—COOR的引入方法:醇和酸的酯化反应。
—CONHR的引入方法:酸和胺的取代反应。
课堂探究
七、制备对羟基苯甲酸乙酯
【问题9】 科学家在荒岛进行合成工作,必备原料有乙醇。乙醇可发生多种有机反应,是重要的基础有机原料。让我们试着用乙醇和甲苯为原料制备对羟基苯甲酸乙酯。
课堂探究
七、制备对羟基苯甲酸乙酯
【问题10】 根据逆向合成思路,分析生成对羟基苯甲酸乙酯需要的物质。
对羟基苯甲酸乙酯易由对羟基苯甲酸和乙醇经过酯化反应得到。
课堂探究
【问题11】 由甲苯制得中间产物对羟基苯甲酸时,—COOH和—OH分别怎么引入?
甲苯侧链的氧化反应易引入—COOH;苯环上甲基是邻、对位取代基,可先在苯环对位引入—X,再通过卤代烃的水解反应实现—OH的引入:
课堂探究
【问题12】 酚羟基易被空气中的氧气氧化,也易被KMnO4溶液氧化,若先引入 — OH,易被氧化,得不到目标产物;若先引入 — COOH,又难以在对位引入官能团,应该怎么处理?
已知:
根据已知信息,可先将酚羟基保护起来,引入 — COOH后再重新得到 — OH;
中间产物对羟基苯甲酸与乙醇酯化反应即可得到目标产物。
课堂探究
八、设计手机新型电池中离子导体材料的合成路线
【情境材料】某锂离子电池的负极材料为石墨,正极材料为过渡金属氧化物,离子导体由锂盐掺杂在液态的有机溶剂中形成。电池在放电时,外电路中电子从负极移动到正极,内电路中锂离子通过有机溶剂的传导从负极移动到正极,形成闭合回路;充电时,内电路中锂离子同样通过有机溶剂的传导从正极移动到负极。我国科学家研究出与锂盐复合可以形成良好的聚合物离子导体材料,将固态新型聚合物锂离子电池的发展向前推进了一步。共聚物基体的原料之一是丙烯酸丁酯( )。
)。
课堂探究
【问题13】 继续以乙醇为基础原料(其他无机试剂任选)合成 ,写出合成路线。
1.先根据逆向分析思路和官能团的引入方法,拆分骨架,分析合成目标产物所需要的物质有哪些。
逆向分析,拆分骨架:
+
八、设计手机新型电池中离子导体材料的合成路线
课堂探究
【问题14】 结合资料信息,分析如何由乙醇增长碳链得到CH2CH2CH2CH2OH所需要的物质。资料:
根据信息,乙醛之间发生反应,可增长碳链得到含4个碳原子的物质。合成的关键中间产物为乙醛,由原料乙醇很容易得到乙醛。反应的化学方程式为
2CH3CH2OH+O2 2CH3CHO+2H2O
课堂探究
【问题15】 结合资料信息,分析如何由乙醇增长碳链得到CH2=CHCOOH。资料:
根据信息分析,根据信息分析,R—CN水解可引入—COOH;乙醛和HCN可发生加成反应引入—CN,且起到了增长碳链的作用。CH3CHOH—CN消去可引入碳碳双键,CH2=CH—CN水解可引入—COOH。
课堂小结
布置作业
预习下节学案。
完成本节素养专练。
谢谢大家
第1、2课时
第三章 烃的衍生物 章末复习
化学
1.通过小组合作学习,总结归纳以反应类型为载体的物质转化关系,并以思维导图的形式进行呈现,建立结构变化与反应类型的对应关系,丰富结构决定性质的认识角度。
2.通过对各步物质转化的反应条件、碳骨架的变化及官能团的转化的分析,巩固基础,强化反应条件与物质转化的联系,建立由条件推测反应类型及官能团转化的基本思维模型。
3.通过小组竞赛的方式交流讨论引入各种常见官能团的方法,激发学生的学习主动性,并能应用解决部分实际问题。
学习目标
4.通过以乙醇为原料合成对羟基苯甲酸乙酯和离子导体材料中的有机溶剂,巩固官能团引入的方法,体会有机合成中官能团的定位和保护,巩固正、逆合成分析法。
重点、难点:
以反应类型为载体的物质转化关系,官能团的引入和保护,逆合成分析法。
学习重难点
有机物的转化关系
有机物之间相互转化的思维导图
知识回顾
CH≡CH
加成
CH2=CH2
加成
CH3CH3
加成
CH3CH2OH
CH3CHO
CH3CH2Br
取代
消去
水解
取代
氧化
氧化
CH3COOH
CH3COOCH2CH3
酯化
消去
加成
还原
酯化
加成
课堂探究
一、有机反应类型总结
【问题1】“结构决定性质,性质体现应用”是我们学习有机化学的重要认识思路,请梳理乙醇能发生的反应类型及可制得的物质种类,从结构角度分析乙醇为什么会成为科学家进行合成的重要原料。
乙醇的官能团-OH可发生取代反应、消去反应、氧化反应等多种反应类型,生成卤代烃、醚、酯、烯烃、醛等多类物质。
课堂探究
【问题2】有机反应常见的反应类型有哪些,并准确描述其概念。
①取代反应:有机物化合物分子中任何一个原子或原子团被试剂中同类型的其他原子或原子团所替代的反应 。
②加成反应:有机物分子中的不饱和碳原子与其他原子或原子团直接结合生成新的化合物的反应。
③消去反应:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HX等),而生成含有不饱和键的化合物的反应。
④氧化反应和还原反应:通常把有机化合物分子中失去氢原子或加入氧原子的反应叫氧化反应;通常把有机化合物分子中失去氧原子或加入氢原子的反应叫还原反应。
课堂探究
【问题3】
①独立思考能发生取代反应的有机物及官能团的种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示, 用时3分钟。
二、取代反应
课堂探究
能发生取代反应的有机物的种类:卤代烃、醇、酚、羧酸、酯、酰胺。
卤代烃的水解反应条件:NaOH溶液、加热;
醇与氢卤酸的反应条件:加热;
醇之间的成醚反应条件:浓硫酸、加热;
醇与羧酸之间的酯化反应条件:浓硫酸、加热;
酚与溴水的反应条件:饱和溴水。
酯的水解反应条件:稀硫酸或NaOH溶液、加热;
酰胺的水解反应条件:盐酸或NaOH溶液、加热。
二、取代反应
课堂探究
【问题4】
①独立思考能发生加成反应的有机物及官能团种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示,用时3分钟。
三、加成反应
课堂探究
能发生加成反应的有机物的种类:烯烃、炔烃、苯、醛、酮、油脂。
烯烃、炔烃、苯、醛、酮、油脂与H2的反应条件:催化剂、加热;
醛与HCN的反应:催化剂。
三、加成反应
【问题5】
与氢气的加成反应还可以看成什么反应类型?
还原反应
课堂探究
【问题6】
①独立思考能发生消去反应的有机物及官能团的种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示,用时3分钟。
能发生消去反应的有机物种类:卤代烃、醇。
卤代烃的消去反应条件:NaOH的醇溶液、加热;
醇的消去反应条件:浓硫酸、加热。
四、消去反应
课堂探究
【问题7】
①独立思考能发生氧化反应(不含有机物的燃烧反应)的有机物及官能团的种类,写出典型代表物发生反应的所有的有机化学方程式,注明反应条件,用时3分钟;
②小组相互补充完善,用时2分钟;
③小组代表在黑板上以思维导图形式展示,用时3分钟。
五、氧化反应(不含有机物的燃烧反应)
课堂探究
能发生氧化反应(不含有机物的燃烧反应)的有机物的种类:醇、酚、醛。
醇的氧化反应 (不含有机物的燃烧反应):O2、催化剂、加热或酸性K2Cr2O7溶液;
酚的氧化反应 (不含有机物的燃烧反应):O2或酸性K2Cr2O7溶液;
醛的氧化反应 (不含有机物的燃烧反应):银氨溶液、水浴加热或氢氧化铜悬浊液、加热或酸性K2Cr2O7溶液或O2、催化剂、加热。
五、氧化反应(不含有机物的燃烧反应)
课堂探究
六、引入官能团的方法
【问题8】小组竞赛活动:
独立思考总结引入—X、 — OH、 — CHO、 — COOH、 — COOR、 — CONHR等官能团的方法,用时2分钟;小组合作完善,先完成的小组,在黑板上展示引入各种常见官能团的方法,合作与展示共5分钟。
课堂探究
六、引入官能团的方法
—X的引入方法:烷烃与X2的取代反应;烯烃、炔烃与HX的加成反应;醇与HX的取代反应。
—OH的引入方法:烯烃与H2O的加成反应;卤代烃的水解反应;酯的水解反应;醛、酮与H2的加成反应。
—CHO的引入方法:醇的氧化反应。
—COOH的引入方法:醛的氧化反应;酯的水解反应;酰胺的水解反应;苯的同系物的氧化反应。
—COOR的引入方法:醇和酸的酯化反应。
—CONHR的引入方法:酸和胺的取代反应。
课堂探究
七、制备对羟基苯甲酸乙酯
【问题9】 科学家在荒岛进行合成工作,必备原料有乙醇。乙醇可发生多种有机反应,是重要的基础有机原料。让我们试着用乙醇和甲苯为原料制备对羟基苯甲酸乙酯。
课堂探究
七、制备对羟基苯甲酸乙酯
【问题10】 根据逆向合成思路,分析生成对羟基苯甲酸乙酯需要的物质。
对羟基苯甲酸乙酯易由对羟基苯甲酸和乙醇经过酯化反应得到。
课堂探究
【问题11】 由甲苯制得中间产物对羟基苯甲酸时,—COOH和—OH分别怎么引入?
甲苯侧链的氧化反应易引入—COOH;苯环上甲基是邻、对位取代基,可先在苯环对位引入—X,再通过卤代烃的水解反应实现—OH的引入:
课堂探究
【问题12】 酚羟基易被空气中的氧气氧化,也易被KMnO4溶液氧化,若先引入 — OH,易被氧化,得不到目标产物;若先引入 — COOH,又难以在对位引入官能团,应该怎么处理?
已知:
根据已知信息,可先将酚羟基保护起来,引入 — COOH后再重新得到 — OH;
中间产物对羟基苯甲酸与乙醇酯化反应即可得到目标产物。
课堂探究
八、设计手机新型电池中离子导体材料的合成路线
【情境材料】某锂离子电池的负极材料为石墨,正极材料为过渡金属氧化物,离子导体由锂盐掺杂在液态的有机溶剂中形成。电池在放电时,外电路中电子从负极移动到正极,内电路中锂离子通过有机溶剂的传导从负极移动到正极,形成闭合回路;充电时,内电路中锂离子同样通过有机溶剂的传导从正极移动到负极。我国科学家研究出与锂盐复合可以形成良好的聚合物离子导体材料,将固态新型聚合物锂离子电池的发展向前推进了一步。共聚物基体的原料之一是丙烯酸丁酯( )。
)。
课堂探究
【问题13】 继续以乙醇为基础原料(其他无机试剂任选)合成 ,写出合成路线。
1.先根据逆向分析思路和官能团的引入方法,拆分骨架,分析合成目标产物所需要的物质有哪些。
逆向分析,拆分骨架:
+
八、设计手机新型电池中离子导体材料的合成路线
课堂探究
【问题14】 结合资料信息,分析如何由乙醇增长碳链得到CH2CH2CH2CH2OH所需要的物质。资料:
根据信息,乙醛之间发生反应,可增长碳链得到含4个碳原子的物质。合成的关键中间产物为乙醛,由原料乙醇很容易得到乙醛。反应的化学方程式为
2CH3CH2OH+O2 2CH3CHO+2H2O
课堂探究
【问题15】 结合资料信息,分析如何由乙醇增长碳链得到CH2=CHCOOH。资料:
根据信息分析,根据信息分析,R—CN水解可引入—COOH;乙醛和HCN可发生加成反应引入—CN,且起到了增长碳链的作用。CH3CHOH—CN消去可引入碳碳双键,CH2=CH—CN水解可引入—COOH。
课堂小结
布置作业
预习下节学案。
完成本节素养专练。
谢谢大家
