第四章 第一节 糖类 第1课时--人教版高中化学选择性必修第三册教学课件(共23张PPT)
文档属性
| 名称 | 第四章 第一节 糖类 第1课时--人教版高中化学选择性必修第三册教学课件(共23张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第1课时 糖类的组成
和分类 单糖
第一节 糖类
化学
1.了解糖类的概念、分类及结构特点,加强对糖类物质的宏观辨识与微观探析。
2.通过类比醇类和醛类有机物的结构特点,掌握葡萄糖的结构和性质,培养“结构决定性质”的学习思维,学会用变化观念进行科学探究。
学习目标
3.通过学习葡萄糖的检验方法,培养严谨的科学态度。
学习重难点
重点:
葡萄糖的组成、典型性质及应用。
难点:
从官能团角度分析葡萄糖的多重化学性质,并设计实验验证。
糖类是一类重要的有机化合物,在自然界中分布广泛。糖类在生命活动中起着重要作用,是生物体所需能量的主要来源,也是重要的能量储存物质,糖类还是很多生物体的结构成分,如植物细胞壁的主要成分为纤维素。
日常食用的蔗糖
粮食中的淀粉
植物茎叶中的纤维素
人体血液中的葡萄糖
导入新课
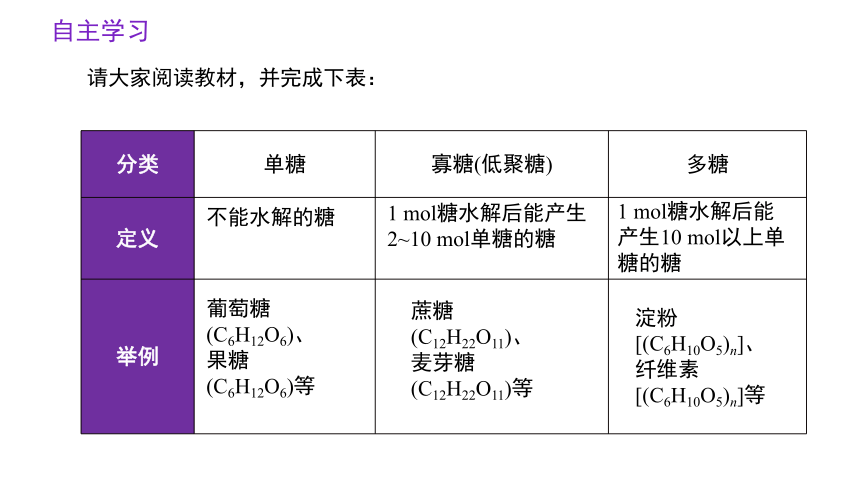
请大家阅读教材,并完成下表:
分类 单糖 寡糖(低聚糖) 多糖
定义
举例
自主学习
不能水解的糖
1 mol糖水解后能产生2~10 mol单糖的糖
1 mol糖水解后能 产生10 mol以上单糖的糖
葡萄糖
(C6H12O6)、
果糖
(C6H12O6)等
蔗糖
(C12H22O11)、
麦芽糖
(C12H22O11)等
淀粉
[(C6H10O5)n]、
纤维素
[(C6H10O5)n]等
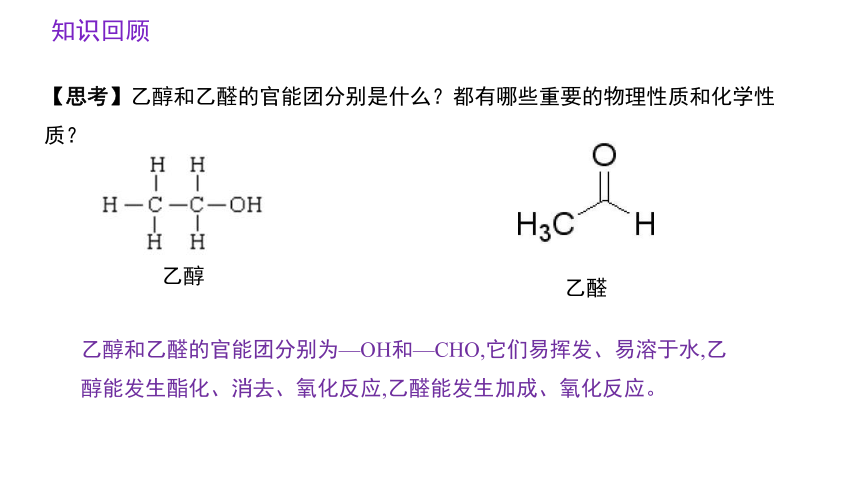
【思考】乙醇和乙醛的官能团分别是什么?都有哪些重要的物理性质和化学性质?
乙醇
乙醛
知识回顾
乙醇和乙醛的官能团分别为—OH和—CHO,它们易挥发、易溶于水,乙醇能发生酯化、消去、氧化反应,乙醛能发生加成、氧化反应。
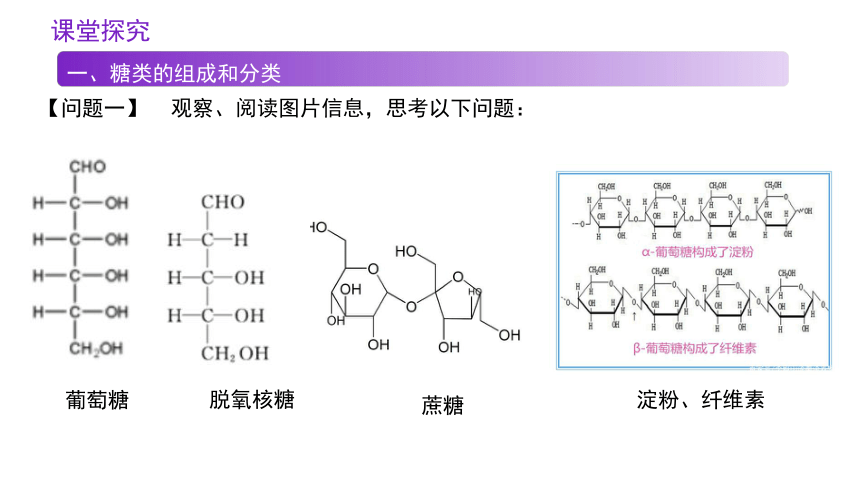
【问题一】
观察、阅读图片信息,思考以下问题:
葡萄糖
蔗糖
淀粉、纤维素
课堂探究
一、糖类的组成和分类
脱氧核糖
【问题一】
1.观察葡萄糖、脱氧核糖、蔗糖、纤维素、淀粉的结构,分析糖类的组成有什么特点?
2.糖类与碳水化合物有怎样的关系?
3.概括糖类的定义。
4.糖类的分类依据是什么?
观察、阅读图片信息,思考以下问题:
课堂探究
一、糖类的组成和分类
【问题一】
1.糖类化合物一般由碳、氢、氧三种元素组成。
2.很多糖类分子中氢原子和氧原子的数目比恰好为2∶1,其组成可以用通式Cm(H2O)n表示,所以糖类也被称为碳水化合物,但不是所有糖的组成都符合上述通式,如脱氧核糖(C5H10O4),而某些符合此通式的物质却不属于糖类,如乙酸(C2H4O2)。因此,用碳水化合物这一名称表示糖类并不准确。
3.从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
4.可依据糖类的水解情况以及产物的多少进行分类。
观察、阅读图片信息,思考以下问题:
课堂探究
一、糖类的组成和分类
【概括归纳】
糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
糖类
是否
水解
不水解:单糖
水解
寡糖(低聚糖):2~10个单糖
多糖:>10个单糖
课堂探究
一、糖类的组成和分类
【问题二】阅读教材,并结合葡萄糖的分子结构,思考以下问题:
1.葡萄糖在自然界中的分布情况是怎样的?
2.从结构角度分析葡萄糖在水中的溶解度和熔、沸点高低情况,总结葡萄糖的物理性质。
3. 葡萄糖有哪些官能团?预测它有哪些化学性质。
课堂探究
二、单糖——葡萄糖
1. 葡萄糖存在于水果、蜂蜜,以及植物的种子、叶、根、花中。动物的血液和淋巴液中也含有葡萄糖。
2.葡萄糖含有多个羟基,易与水分子形成氢键,易溶于水;葡萄糖属于分子晶体,可以形成分子间氢键,熔、沸点相对较高。葡萄糖是易溶于水的无色晶体,熔点为146 ℃,有甜味,但甜度不如蔗糖。
3.葡萄糖含有羟基和醛基。能发生酯化、氧化、加成反应。
课堂探究
二、单糖——葡萄糖
实验序号 操作 现象 实验结论及解释
1 在一支洁净的试管中配制约2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡,然后在水浴中加热。观察实验现象
2 在另一支试管中加入2 mL 10%NaOH溶液,加入5滴5% CuSO4溶液,再加入2 mL 10%葡萄糖溶液,加热。观察实验现象 产生砖红色沉淀
试管壁上形成光亮的银镜
葡萄糖具有还原性,属于还原糖。
(1)CH2OH(CHOH)4CHO+
2[Ag(NH3)2]OH
CH2OH(CHOH)4COONH4+
2Ag↓+3NH3+H2O;
(2)CH2OH(CHOH)4CHO+
2Cu(OH)2+NaOH
CH2OH(CHOH)4COONa+
Cu2O↓+3H2O。
课堂探究
二、单糖——葡萄糖
【实验探究】
【归纳总结】葡萄糖的结构、性质、用途
葡萄糖的结构式 官能团 反应类型 试剂或条件
醛基 加成反应 H2/Ni
氧化反应 银氨溶液
新制Cu(OH)2
使溴水褪色
生理氧化
羟基 酯化反应 与乙酸等
课堂探究
二、单糖——葡萄糖
课堂探究
二、单糖——葡萄糖
1.葡萄糖是一种重要的营养物质,动物需要的能量来源;低血糖的患者可利用静脉注射葡萄糖溶液的方式来迅速补充营养。
2.糖果制造业。
3.制镜业。
4.制药工业。
5.制酒工业。
【问题三】结合葡萄糖的化学性质讨论葡萄糖在实际生产和生活中都有哪些用途
【问题四】阅读教材P104,结合果糖的结构,思考果糖有哪些化学性质?果糖与葡萄糖有什么关系?完成表格。
物质 果糖
分子式
结构简式
物理性质
化学性质
与葡萄糖的关系
①能和酸发生酯化反应
②与H2加成生成醇
互为同分异构体
课堂探究
三、单糖——果糖
C6H12O6
无色晶体,有甜味,易溶于水,吸湿性强
【问题五】写出核糖与脱氧核糖的结构简式,其结构有哪些异同点?它们有哪些主要的化学性质?
课堂探究
四、单糖——核糖与脱氧核糖
书写分子结构:
组成相差一个O原子,都有羟基和醛基,能发生酯化反应,能与H2发生加成反应,具有还原性,属于还原糖。
【概括】在分子中连有4个不同的原子或原子团的碳原子叫不对称碳原子,也叫手性碳原子。含有手性碳原子,存在不能重叠、互为镜像的对映异构体的分子称手性分子。
课堂探究
四、单糖——核糖与脱氧核糖
【问题六】请用“*”标注出核糖与脱氧核糖结构中的手性碳原子。
1.木糖醇是一种理想的蔗糖代替品,它具有甜味足、溶解性好、防龋齿的优点。木糖醇为白色晶体或结晶性粉末,分子式为C5H12O5,结构简式为CH2OH(CHOH)3CH2OH。下列有关木糖醇的叙述中不正确的是( )
A.木糖醇不属于单糖
B.木糖醇不能跟新制的氢氧化铜反应生成砖红色沉淀
C.木糖醇与乙醇互为同系物
D.木糖醇是一种五元醇,可以与羧酸在一定条件下发生酯化反应
课堂练习
C
解析 单糖是多羟基醛或多羟基酮,而木糖醇为五元醇,不含醛基,也不含酮羰基,乙醇为一元醇,故A、B、D正确,C不正确。
2.下列有关葡萄糖与果糖的说法中,不正确的是( )
①二者互为同分异构体 ②二者都易溶于水 ③二者都能发生银镜反应,都能与新制的Cu(OH)2反应生成砖红色沉淀 ④葡萄糖能发生酯化反应,而果糖不能 ⑤都能与H2发生加成反应生成六元醇 ⑥果糖是最甜的糖,而葡萄糖并不甜
A.①②③ B.④⑤ C.④⑥ D.⑥
课堂练习
C
解析 葡萄糖与果糖的分子式相同,结构不同,①正确;葡萄糖与果糖都易溶于水,②正确;果糖虽无醛基,但仍能同葡萄糖一样发生银镜反应,能与新制的Cu(OH)2反应,③正确;葡萄糖与果糖都含有羟基,所以都能发生酯化反应,④错误;葡萄糖与果糖都能与H2发生加成反应生成六元醇,⑤正确;葡萄糖也有甜味,⑥错误。
课堂小结
布置作业
完成学案中的素养专练。
谢谢大家
第1课时 糖类的组成
和分类 单糖
第一节 糖类
化学
1.了解糖类的概念、分类及结构特点,加强对糖类物质的宏观辨识与微观探析。
2.通过类比醇类和醛类有机物的结构特点,掌握葡萄糖的结构和性质,培养“结构决定性质”的学习思维,学会用变化观念进行科学探究。
学习目标
3.通过学习葡萄糖的检验方法,培养严谨的科学态度。
学习重难点
重点:
葡萄糖的组成、典型性质及应用。
难点:
从官能团角度分析葡萄糖的多重化学性质,并设计实验验证。
糖类是一类重要的有机化合物,在自然界中分布广泛。糖类在生命活动中起着重要作用,是生物体所需能量的主要来源,也是重要的能量储存物质,糖类还是很多生物体的结构成分,如植物细胞壁的主要成分为纤维素。
日常食用的蔗糖
粮食中的淀粉
植物茎叶中的纤维素
人体血液中的葡萄糖
导入新课
请大家阅读教材,并完成下表:
分类 单糖 寡糖(低聚糖) 多糖
定义
举例
自主学习
不能水解的糖
1 mol糖水解后能产生2~10 mol单糖的糖
1 mol糖水解后能 产生10 mol以上单糖的糖
葡萄糖
(C6H12O6)、
果糖
(C6H12O6)等
蔗糖
(C12H22O11)、
麦芽糖
(C12H22O11)等
淀粉
[(C6H10O5)n]、
纤维素
[(C6H10O5)n]等
【思考】乙醇和乙醛的官能团分别是什么?都有哪些重要的物理性质和化学性质?
乙醇
乙醛
知识回顾
乙醇和乙醛的官能团分别为—OH和—CHO,它们易挥发、易溶于水,乙醇能发生酯化、消去、氧化反应,乙醛能发生加成、氧化反应。
【问题一】
观察、阅读图片信息,思考以下问题:
葡萄糖
蔗糖
淀粉、纤维素
课堂探究
一、糖类的组成和分类
脱氧核糖
【问题一】
1.观察葡萄糖、脱氧核糖、蔗糖、纤维素、淀粉的结构,分析糖类的组成有什么特点?
2.糖类与碳水化合物有怎样的关系?
3.概括糖类的定义。
4.糖类的分类依据是什么?
观察、阅读图片信息,思考以下问题:
课堂探究
一、糖类的组成和分类
【问题一】
1.糖类化合物一般由碳、氢、氧三种元素组成。
2.很多糖类分子中氢原子和氧原子的数目比恰好为2∶1,其组成可以用通式Cm(H2O)n表示,所以糖类也被称为碳水化合物,但不是所有糖的组成都符合上述通式,如脱氧核糖(C5H10O4),而某些符合此通式的物质却不属于糖类,如乙酸(C2H4O2)。因此,用碳水化合物这一名称表示糖类并不准确。
3.从分子结构上看,糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
4.可依据糖类的水解情况以及产物的多少进行分类。
观察、阅读图片信息,思考以下问题:
课堂探究
一、糖类的组成和分类
【概括归纳】
糖类是多羟基醛、多羟基酮和它们的脱水缩合物。
糖类
是否
水解
不水解:单糖
水解
寡糖(低聚糖):2~10个单糖
多糖:>10个单糖
课堂探究
一、糖类的组成和分类
【问题二】阅读教材,并结合葡萄糖的分子结构,思考以下问题:
1.葡萄糖在自然界中的分布情况是怎样的?
2.从结构角度分析葡萄糖在水中的溶解度和熔、沸点高低情况,总结葡萄糖的物理性质。
3. 葡萄糖有哪些官能团?预测它有哪些化学性质。
课堂探究
二、单糖——葡萄糖
1. 葡萄糖存在于水果、蜂蜜,以及植物的种子、叶、根、花中。动物的血液和淋巴液中也含有葡萄糖。
2.葡萄糖含有多个羟基,易与水分子形成氢键,易溶于水;葡萄糖属于分子晶体,可以形成分子间氢键,熔、沸点相对较高。葡萄糖是易溶于水的无色晶体,熔点为146 ℃,有甜味,但甜度不如蔗糖。
3.葡萄糖含有羟基和醛基。能发生酯化、氧化、加成反应。
课堂探究
二、单糖——葡萄糖
实验序号 操作 现象 实验结论及解释
1 在一支洁净的试管中配制约2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡,然后在水浴中加热。观察实验现象
2 在另一支试管中加入2 mL 10%NaOH溶液,加入5滴5% CuSO4溶液,再加入2 mL 10%葡萄糖溶液,加热。观察实验现象 产生砖红色沉淀
试管壁上形成光亮的银镜
葡萄糖具有还原性,属于还原糖。
(1)CH2OH(CHOH)4CHO+
2[Ag(NH3)2]OH
CH2OH(CHOH)4COONH4+
2Ag↓+3NH3+H2O;
(2)CH2OH(CHOH)4CHO+
2Cu(OH)2+NaOH
CH2OH(CHOH)4COONa+
Cu2O↓+3H2O。
课堂探究
二、单糖——葡萄糖
【实验探究】
【归纳总结】葡萄糖的结构、性质、用途
葡萄糖的结构式 官能团 反应类型 试剂或条件
醛基 加成反应 H2/Ni
氧化反应 银氨溶液
新制Cu(OH)2
使溴水褪色
生理氧化
羟基 酯化反应 与乙酸等
课堂探究
二、单糖——葡萄糖
课堂探究
二、单糖——葡萄糖
1.葡萄糖是一种重要的营养物质,动物需要的能量来源;低血糖的患者可利用静脉注射葡萄糖溶液的方式来迅速补充营养。
2.糖果制造业。
3.制镜业。
4.制药工业。
5.制酒工业。
【问题三】结合葡萄糖的化学性质讨论葡萄糖在实际生产和生活中都有哪些用途
【问题四】阅读教材P104,结合果糖的结构,思考果糖有哪些化学性质?果糖与葡萄糖有什么关系?完成表格。
物质 果糖
分子式
结构简式
物理性质
化学性质
与葡萄糖的关系
①能和酸发生酯化反应
②与H2加成生成醇
互为同分异构体
课堂探究
三、单糖——果糖
C6H12O6
无色晶体,有甜味,易溶于水,吸湿性强
【问题五】写出核糖与脱氧核糖的结构简式,其结构有哪些异同点?它们有哪些主要的化学性质?
课堂探究
四、单糖——核糖与脱氧核糖
书写分子结构:
组成相差一个O原子,都有羟基和醛基,能发生酯化反应,能与H2发生加成反应,具有还原性,属于还原糖。
【概括】在分子中连有4个不同的原子或原子团的碳原子叫不对称碳原子,也叫手性碳原子。含有手性碳原子,存在不能重叠、互为镜像的对映异构体的分子称手性分子。
课堂探究
四、单糖——核糖与脱氧核糖
【问题六】请用“*”标注出核糖与脱氧核糖结构中的手性碳原子。
1.木糖醇是一种理想的蔗糖代替品,它具有甜味足、溶解性好、防龋齿的优点。木糖醇为白色晶体或结晶性粉末,分子式为C5H12O5,结构简式为CH2OH(CHOH)3CH2OH。下列有关木糖醇的叙述中不正确的是( )
A.木糖醇不属于单糖
B.木糖醇不能跟新制的氢氧化铜反应生成砖红色沉淀
C.木糖醇与乙醇互为同系物
D.木糖醇是一种五元醇,可以与羧酸在一定条件下发生酯化反应
课堂练习
C
解析 单糖是多羟基醛或多羟基酮,而木糖醇为五元醇,不含醛基,也不含酮羰基,乙醇为一元醇,故A、B、D正确,C不正确。
2.下列有关葡萄糖与果糖的说法中,不正确的是( )
①二者互为同分异构体 ②二者都易溶于水 ③二者都能发生银镜反应,都能与新制的Cu(OH)2反应生成砖红色沉淀 ④葡萄糖能发生酯化反应,而果糖不能 ⑤都能与H2发生加成反应生成六元醇 ⑥果糖是最甜的糖,而葡萄糖并不甜
A.①②③ B.④⑤ C.④⑥ D.⑥
课堂练习
C
解析 葡萄糖与果糖的分子式相同,结构不同,①正确;葡萄糖与果糖都易溶于水,②正确;果糖虽无醛基,但仍能同葡萄糖一样发生银镜反应,能与新制的Cu(OH)2反应,③正确;葡萄糖与果糖都含有羟基,所以都能发生酯化反应,④错误;葡萄糖与果糖都能与H2发生加成反应生成六元醇,⑤正确;葡萄糖也有甜味,⑥错误。
课堂小结
布置作业
完成学案中的素养专练。
谢谢大家
