第四章 实验活动3 糖类的性质--人教版高中化学选择性必修第三册教学课件(共12张PPT)
文档属性
| 名称 | 第四章 实验活动3 糖类的性质--人教版高中化学选择性必修第三册教学课件(共12张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 395.6KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-08 00:00:00 | ||
图片预览





文档简介
(共12张PPT)
糖类的性质
实验活动3
化学
1.通过探究实验,能够准确配制银氨溶液、新制氢氧化铜并验证糖类的还原性,记录实验现象,分析出实验结论。发展设计实验、分析解释、科学探究的核心素养。
2.通过糖类性质对比分析,能建立有机物官能团与性质的关联认知,形成 "结构决定性质" 的化学思维。
学习目标
重点:
验证糖类的还原性、糖类水解反应及水解产物检验的实验操作。
难点:
实验的条件控制及实验现象的分析。
学习重难点
导入新课
【问题1】如何检验葡萄糖的还原性?
利用银氨溶液或者新制氢氧化铜检验葡萄糖的还原性。
【问题2】如何配置银氨溶液、新制氢氧化铜。
配制银氨溶液:在洁净的试管中加入1 mL 2% AgNO3溶液,然后一边振荡试管,一边逐滴加入2%氨水,直到最初产生的沉淀恰好溶解为止,得到银氨溶液。
配制新制氢氧化铜:在试管中加入2 mL 10% NaOH溶液,滴加5滴 5% CuSO4溶液,振荡,得到新制氢氧化铜。
课堂探究
一、探究糖类的性质
任务1:葡萄糖的还原性验证。
实验目标:通过银镜反应和新制氢氧化铜检验葡萄糖的还原性。
实验内容 实验现象 实验结论
取少量葡萄糖,观察状态,将其加入试管后加水振荡,观察其溶解状况
在洁净的试管中配制约2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡。然后水浴加热,观察现象
在另一支试管中加入2 mL 10% NaOH溶液,滴入5滴 5% CuSO4溶液,振荡。再加入 2 mL 10%葡萄糖溶液,加热,观察现象
葡萄糖为无色晶体,迅速溶解于水
有银镜生成
先有蓝色絮状沉淀生成,后有砖红色沉淀生成
常温常压下葡萄糖为无色晶体;易溶于水
说明葡萄糖是还原糖
说明葡萄糖是还原糖
NaOH过量
课堂探究
一、探究糖类的性质
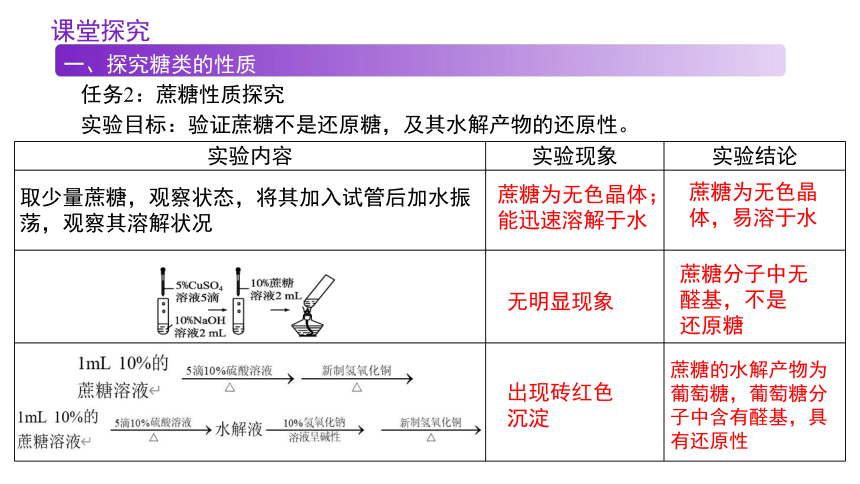
任务2:蔗糖性质探究
实验目标:验证蔗糖不是还原糖,及其水解产物的还原性。
实验内容 实验现象 实验结论
取少量蔗糖,观察状态,将其加入试管后加水振荡,观察其溶解状况
无明显现象
蔗糖为无色晶体;能迅速溶解于水
蔗糖为无色晶体,易溶于水
出现砖红色
沉淀
蔗糖的水解产物为葡萄糖,葡萄糖分子中含有醛基,具有还原性
蔗糖分子中无醛基,不是
还原糖
课堂探究
一、探究糖类的性质
任务3:淀粉性质探究
实验目标:探究淀粉的溶解性,及其水解前后物质还原性的变化。
实验内容 实验现象 实验结论
取少量淀粉,观察状态,将其加入试管后加水振荡,再加热煮沸,观察其溶解状况
淀粉不溶于冷水;在热水中淀粉会部分溶解
无明显现象
出现砖红色沉淀
淀粉是白色粉末状物质,没有甜味,不溶于冷水。在热水中淀粉会部分溶解,形成胶状的淀粉糊
淀粉的水解产物为葡萄糖,葡萄糖分子中含有醛基,具有还原性
淀粉分子中无醛基,不是还原糖
课堂探究
二、问题讨论
讨论任务:
1.根据上述实验现象,葡萄糖、蔗糖和淀粉中,哪种物质是还原糖 为什么
2.在检验蔗糖和淀粉水解产物时,均需在水解液中加NaOH溶液使之呈碱性,为什么
葡萄糖是还原糖,能被弱氧化剂银氨溶液或新制Cu(OH)2氧化;蔗糖、淀粉为非还原糖,不能被弱氧化剂银氨溶液、新制Cu(OH)2氧化。
NaOH溶液可中和水解时加入的酸,若未加NaOH溶液,银氨溶液或新制Cu(OH)2会与酸反应,影响检测结果的准确性。
课堂探究
二、问题讨论
讨论任务:
3.请结合糖类的性质,推测急救患者补充能量时,一般使用葡萄糖溶液,而不选择其他糖类溶液的可能原因。
4.若证明淀粉没有水解完全,则需要什么试剂 现象是什么
葡萄糖具有较的强还原性,易被氧化,能快速给人体提供能量,同时葡萄糖在消化道中更易被直接吸收。
碘水溶液,淀粉溶液变蓝。
课堂小结
整理本节课的知识点,用图示呈现相关概念间的关系。
1.葡萄糖
(还原糖)
银镜反应
与新制Cu(OH)2反应:
2.蔗糖(非还原糖):
1mL10%蔗糖溶液
5滴10% H2SO4溶液
△
10% NaOH溶液至碱性
新制Cu(OH)2
砖红色沉淀
3.淀粉(非还原糖):
1mL淀粉溶液
2mL10% H2SO4溶液
△
10% NaOH溶液至碱性
新制Cu(OH)2
砖红色沉淀
布置作业
完成学案中的素养专练。
谢谢大家
糖类的性质
实验活动3
化学
1.通过探究实验,能够准确配制银氨溶液、新制氢氧化铜并验证糖类的还原性,记录实验现象,分析出实验结论。发展设计实验、分析解释、科学探究的核心素养。
2.通过糖类性质对比分析,能建立有机物官能团与性质的关联认知,形成 "结构决定性质" 的化学思维。
学习目标
重点:
验证糖类的还原性、糖类水解反应及水解产物检验的实验操作。
难点:
实验的条件控制及实验现象的分析。
学习重难点
导入新课
【问题1】如何检验葡萄糖的还原性?
利用银氨溶液或者新制氢氧化铜检验葡萄糖的还原性。
【问题2】如何配置银氨溶液、新制氢氧化铜。
配制银氨溶液:在洁净的试管中加入1 mL 2% AgNO3溶液,然后一边振荡试管,一边逐滴加入2%氨水,直到最初产生的沉淀恰好溶解为止,得到银氨溶液。
配制新制氢氧化铜:在试管中加入2 mL 10% NaOH溶液,滴加5滴 5% CuSO4溶液,振荡,得到新制氢氧化铜。
课堂探究
一、探究糖类的性质
任务1:葡萄糖的还原性验证。
实验目标:通过银镜反应和新制氢氧化铜检验葡萄糖的还原性。
实验内容 实验现象 实验结论
取少量葡萄糖,观察状态,将其加入试管后加水振荡,观察其溶解状况
在洁净的试管中配制约2 mL银氨溶液,加入1 mL 10%葡萄糖溶液,振荡。然后水浴加热,观察现象
在另一支试管中加入2 mL 10% NaOH溶液,滴入5滴 5% CuSO4溶液,振荡。再加入 2 mL 10%葡萄糖溶液,加热,观察现象
葡萄糖为无色晶体,迅速溶解于水
有银镜生成
先有蓝色絮状沉淀生成,后有砖红色沉淀生成
常温常压下葡萄糖为无色晶体;易溶于水
说明葡萄糖是还原糖
说明葡萄糖是还原糖
NaOH过量
课堂探究
一、探究糖类的性质
任务2:蔗糖性质探究
实验目标:验证蔗糖不是还原糖,及其水解产物的还原性。
实验内容 实验现象 实验结论
取少量蔗糖,观察状态,将其加入试管后加水振荡,观察其溶解状况
无明显现象
蔗糖为无色晶体;能迅速溶解于水
蔗糖为无色晶体,易溶于水
出现砖红色
沉淀
蔗糖的水解产物为葡萄糖,葡萄糖分子中含有醛基,具有还原性
蔗糖分子中无醛基,不是
还原糖
课堂探究
一、探究糖类的性质
任务3:淀粉性质探究
实验目标:探究淀粉的溶解性,及其水解前后物质还原性的变化。
实验内容 实验现象 实验结论
取少量淀粉,观察状态,将其加入试管后加水振荡,再加热煮沸,观察其溶解状况
淀粉不溶于冷水;在热水中淀粉会部分溶解
无明显现象
出现砖红色沉淀
淀粉是白色粉末状物质,没有甜味,不溶于冷水。在热水中淀粉会部分溶解,形成胶状的淀粉糊
淀粉的水解产物为葡萄糖,葡萄糖分子中含有醛基,具有还原性
淀粉分子中无醛基,不是还原糖
课堂探究
二、问题讨论
讨论任务:
1.根据上述实验现象,葡萄糖、蔗糖和淀粉中,哪种物质是还原糖 为什么
2.在检验蔗糖和淀粉水解产物时,均需在水解液中加NaOH溶液使之呈碱性,为什么
葡萄糖是还原糖,能被弱氧化剂银氨溶液或新制Cu(OH)2氧化;蔗糖、淀粉为非还原糖,不能被弱氧化剂银氨溶液、新制Cu(OH)2氧化。
NaOH溶液可中和水解时加入的酸,若未加NaOH溶液,银氨溶液或新制Cu(OH)2会与酸反应,影响检测结果的准确性。
课堂探究
二、问题讨论
讨论任务:
3.请结合糖类的性质,推测急救患者补充能量时,一般使用葡萄糖溶液,而不选择其他糖类溶液的可能原因。
4.若证明淀粉没有水解完全,则需要什么试剂 现象是什么
葡萄糖具有较的强还原性,易被氧化,能快速给人体提供能量,同时葡萄糖在消化道中更易被直接吸收。
碘水溶液,淀粉溶液变蓝。
课堂小结
整理本节课的知识点,用图示呈现相关概念间的关系。
1.葡萄糖
(还原糖)
银镜反应
与新制Cu(OH)2反应:
2.蔗糖(非还原糖):
1mL10%蔗糖溶液
5滴10% H2SO4溶液
△
10% NaOH溶液至碱性
新制Cu(OH)2
砖红色沉淀
3.淀粉(非还原糖):
1mL淀粉溶液
2mL10% H2SO4溶液
△
10% NaOH溶液至碱性
新制Cu(OH)2
砖红色沉淀
布置作业
完成学案中的素养专练。
谢谢大家
