2025年福建省龙岩市新罗区中考模拟考试 化学试卷(含答案)
文档属性
| 名称 | 2025年福建省龙岩市新罗区中考模拟考试 化学试卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-06 00:00:00 | ||
图片预览




文档简介
2024-2025学年中考模拟测试一
九年级化学试题
(考试时间:60分钟;满分100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ca-40
一、选择题(共10题,各3分,共30分。在每题给出四个选项中,只有一项符合题目要求)
1.2025年3月5日,李强总理在政府工作报告中提出“协同推进降碳减污扩绿增长,加快经济社会发展全面绿色转型”,下列做法不符合该主题的是
A.推广火力发电 B.发展清洁能源 C.完善绿色政策 D.开展节能行动
2.中国科学家发明了世界上超薄的光学晶体——菱方氮化硼晶体。氮化硼()属于
A.单质 B.氧化物 C.化合物 D.混合物
3.玉米是三大粮食作物之一。我国科学家破解了铁元素进入玉米籽粒的路径,有望低成本改善大范围人群的铁营养状况。下列说法错误的是
A.玉米含淀粉等营养物质 B.铁元素是人体必需的常量元素
C.人体缺铁会引起贫血 D.该研究利于提高玉米的铁含量
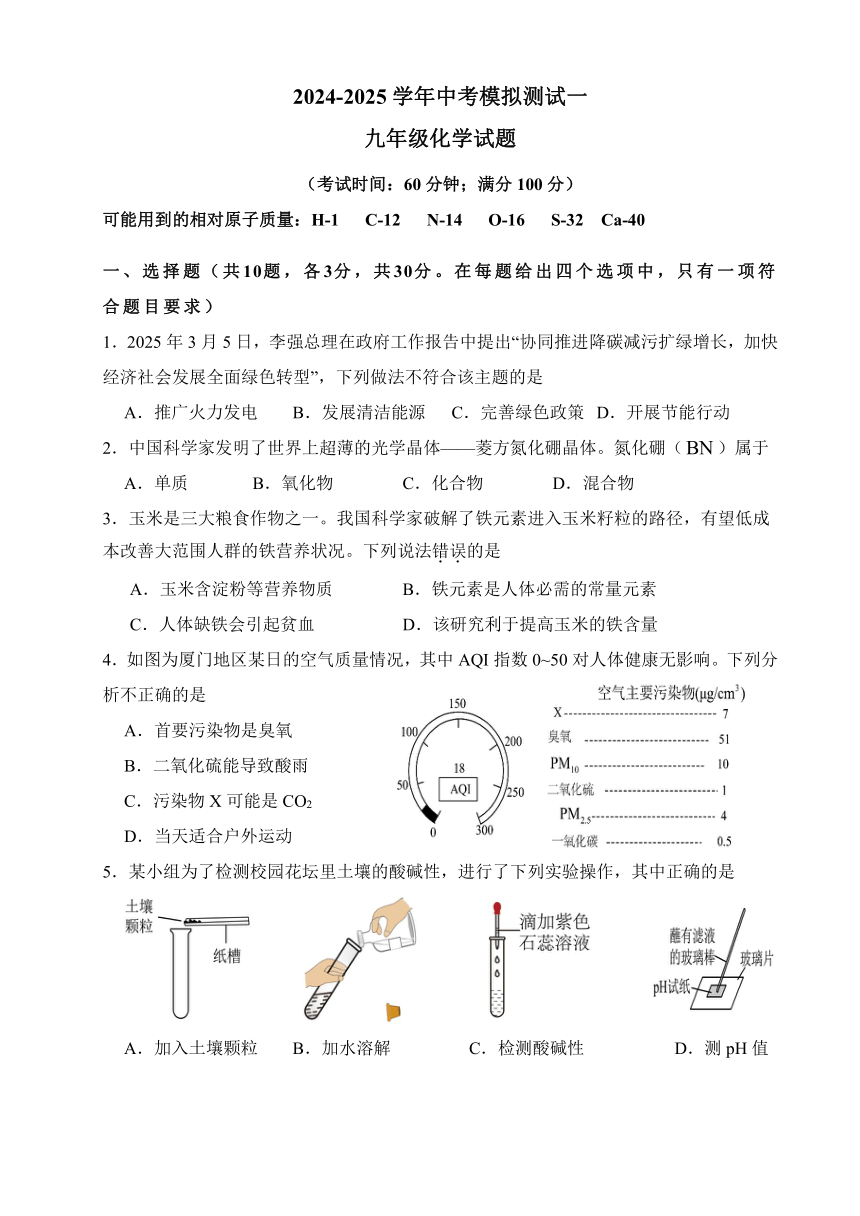
4.如图为厦门地区某日的空气质量情况,其中AQI指数0~50对人体健康无影响。下列分析不正确的是
A.首要污染物是臭氧
B.二氧化硫能导致酸雨
C.污染物X可能是CO2
D.当天适合户外运动
5.某小组为了检测校园花坛里土壤的酸碱性,进行了下列实验操作,其中正确的是
A.加入土壤颗粒 B.加水溶解 C.检测酸碱性 D.测pH值
6.钷可为航天器提供动力。钷元素在元素周期表中的信息如图所示,下列说法错误的是
A.钷为金属元素
B.钷的元素符号为Pm
C.钷原子的中子数为61
D.钷元素的相对原子质量为145
7.下列实践活动涉及的化学知识正确的是
选项 实践活动 化学知识
A 制作氨(NH3)分子结构模型 氨气由氮、氢原子构成
B 基于特定需求制氧气 O2可以供给呼吸
C 消防演练使用水基型灭火器 纸质文件档案可用水基型灭火器扑灭
D 调查家用燃料的变迁与使用 燃气灶火焰呈黄色时调小空气进风口
8.茶树适宜在pH为5-6的土壤中生长,茶叶中含锌、硒、茶氨酸(化学式为)等多种成分,下列说法错误的是
A.茶氨酸由碳、氢、氧、氮四种元素组成
B.茶氨酸中碳元素与氢元素质量比为
C.茶氨酸中氮元素的质量分数最大
D.可以用熟石灰改良茶树土壤,使其更好生长
9.如图所示,将缠有铁丝绒的粗铜丝插入U型管的右端,往管中注入溶质质量分数为6%的硫酸铜溶液(呈酸性),液面距管口有2~3cm。一段时间后可观察到的现象是
A.铁丝绒表面覆盖一层白色固体
B.U型管右端产生气体
C.U型管两边的液面出现左低右高
D.U型管中溶液颜色由蓝色变无色
10.室温下,某化学兴趣小组的同学设计如图甲所示装置对氢氧化钠溶液和稀盐酸反应进行探究。他们在盛有一定量X溶液的烧杯中放置pH传感器和温度传感器,并滴入3滴酚酞试液,然后开启电磁搅拌器,用滴管逐滴加入Y溶液,计算机显示两种传感器所得的数据曲线如图乙和图丙、下列表述正确的是
A.滴加Y溶液的全过程中,持续发生反应并放出热量
B.烧杯中的X溶液是稀盐酸
C.a点溶液中溶质的成分为HCl,此时烧杯中溶液呈现无色
D.滴加Y溶液的全过程中,氯化钠的溶解度逐渐增大
二、非选择题(共7题,共70分)
11.(5分)《天工开物》中记载了铜镜(如图)的制作过程:“凡铸镜,模用灰沙,铜用锡和……开面成光,则水银附体而成,非铜有光明如许也。”
(1)“铜用锡和”是指在铜中加入锡,制成青铜。青铜属于 材料(填“金属”或“合成”),与用纯铜相比,青铜制得的铜镜的优点是 (写一条)。
(2)经过氧化处理后,铜镜表面会形成一层耐腐蚀的二氧化锡(SnO2)薄膜。SnO2中锡元素的化合价为 。
(3)“阳燧”是古代照日取火用的凹面铜镜。取火时将凹面镜对着阳光,把艾绒放于焦点部位引火。从燃烧条件分析,“阳燧”的作用是 。
12.(6分)水和溶液在生产生活中有广泛的用途。
(1)人体需要持续补充水分以维持正常的生理功能,生活中常用活性炭除去水中 。
(2)如图所示的创可贴可快速止血,其原理是凸起的小囊区挤破后,水和某固体混合后降温,从而起到止血效果。该固体可能是______(填字母)。
A.氯化钠 B.硝酸铵 C.氢氧化钠 D.蔗糖
(3)个人口腔鼻腔消毒常使用盐水(氯化钠溶液),现用5%的盐水30g配制3%的盐水,需要加水的质量为 g,若使用的5%的盐水因放置时间过长导致水分蒸发了一部分,则配制的3%的盐水的溶质质量分数 (填“偏大”“偏小”或“无影响”)。
(4)目前有城市已经开始实施“阶梯水价”方案,“阶梯水价”的基本特点是用水越多,水价越贵。实施“阶梯水价”的目的是 。
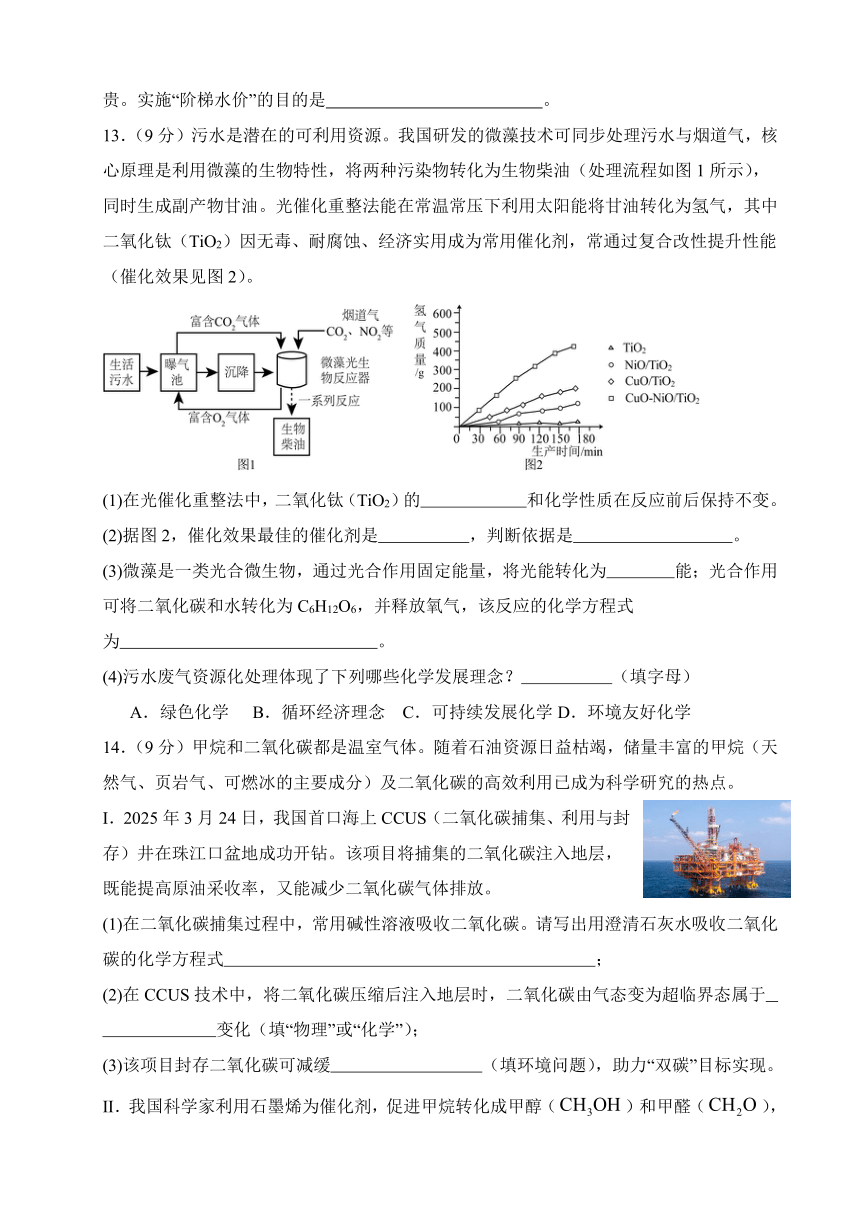
13.(9分)污水是潜在的可利用资源。我国研发的微藻技术可同步处理污水与烟道气,核心原理是利用微藻的生物特性,将两种污染物转化为生物柴油(处理流程如图1所示),同时生成副产物甘油。光催化重整法能在常温常压下利用太阳能将甘油转化为氢气,其中二氧化钛(TiO2)因无毒、耐腐蚀、经济实用成为常用催化剂,常通过复合改性提升性能(催化效果见图2)。
(1)在光催化重整法中,二氧化钛(TiO2)的 和化学性质在反应前后保持不变。
(2)据图2,催化效果最佳的催化剂是 ,判断依据是 。
(3)微藻是一类光合微生物,通过光合作用固定能量,将光能转化为 能;光合作用可将二氧化碳和水转化为C6H12O6,并释放氧气,该反应的化学方程式为 。
(4)污水废气资源化处理体现了下列哪些化学发展理念? (填字母)
A.绿色化学 B.循环经济理念 C.可持续发展化学 D.环境友好化学
14.(9分)甲烷和二氧化碳都是温室气体。随着石油资源日益枯竭,储量丰富的甲烷(天然气、页岩气、可燃冰的主要成分)及二氧化碳的高效利用已成为科学研究的热点。
I.2025年3月24日,我国首口海上CCUS(二氧化碳捕集、利用与封存)井在珠江口盆地成功开钻。该项目将捕集的二氧化碳注入地层,既能提高原油采收率,又能减少二氧化碳气体排放。
(1)在二氧化碳捕集过程中,常用碱性溶液吸收二氧化碳。请写出用澄清石灰水吸收二氧化碳的化学方程式 ;
(2)在CCUS技术中,将二氧化碳压缩后注入地层时,二氧化碳由气态变为超临界态属于
变化(填“物理”或“化学”);
(3)该项目封存二氧化碳可减缓 (填环境问题),助力“双碳”目标实现。
II.我国科学家利用石墨烯为催化剂,促进甲烷转化成甲醇()和甲醛(),主要原理如图。请结合示意图回答下列问题:
(4) 主要成分为甲烷的化石燃料是_______________(填一种)。
(5)等质量的甲醇和甲醛,___________(填“甲醇”或“甲醛”)的分子个数多。
(6)过程Ⅳ中各粒子数目比为1:1:1:1:2,则X的化学式为_________。
15.(13分)我国运城盐湖(湖水富含、)地区是世界上最早采用人工治畦、利用日光晒盐的地方。当地开创的“垦畦浇晒”产盐法,发展成熟于隋唐时期,至今仍在沿用。“垦畦浇晒”的工艺流程见图1,和的溶解度曲线见图2。
Ⅰ.古法制盐分析
(1) 当蒸发畦中的盐湖水变得“模糊”时,工人将盐湖水经沟渠引入结晶畦,为防止泥沙等杂质进入结晶畦,工人会在沟渠不同位置设置多个表面带有许多小孔的盐板,这一过程称为“过箩”除杂,“过箩”除杂与实验室中的 操作原理相似。
(2)该工艺最终所得卤水中一定含有的阴离子为 (写出其中一个离子符号)。
(3)80℃时,饱和硫酸钠溶液的溶质质量分数为 (只列式)。
当气温较低时,所制得的粗盐中含量较高,这是因为 。为除去粗盐中的,可使用 溶液对粗盐进行淋洗。
Ⅱ.实验室制盐
化学实践小组的同学们取某区域的盐湖水样品(主要含、及少量和),他们从中获取和的主要过程如下:
(4)除Mg2+、Ca2+时依次加入氢氧化钠溶液和碳酸钠溶液,发生反应的化学方程式为_______________________________。(写出其中一个)
(5)将“溶液A”在80℃蒸发浓缩,至有少量固体析出。小华同学分析溶解度曲线,推测析出的少量固体是,但检验后却发现是。请作出合理解释 。
(6)小华同学停止蒸发浓缩,经 、过滤得到大量固体及母液。后续从母液中获取固体。
16.(12分)铜箔在新能源汽车电池制造等领域有重要应用。一种制造铜箔工艺的主要工序如图1所示。
(1)“溶铜”前,粉碎处理铜原料的目的是 。
(2)“溶铜”中,存在Cu与O2生成CuO的反应,该反应属于 (填基本反应类型)。
(3)“制箔”中,发生反应的化学方程式:2CuSO4+2H2O2Cu+O2↑+2X,X的化学式为 。物质X可用于 和 工序。
(4)“制箔”中,需生产抗拉强度大于355MPa且延伸率大于13.5%的铜箔,据图2可知,温度应控制在 内(填字母)。
a.45~49℃ b.50~52℃
c.53~55℃ d.56~60℃
(5)“酸洗”后,常用熟石灰中和酸性废液,其反应原理为:。
若要中和含9.8t硫酸的酸性废液,理论上需要的熟石灰的质量是多少?(利用化学方程式计算,写出完整计算过程。)
17.( 16分)氢能是一种清洁能源,氢气的制备方法受到广泛的关注和研究。
(一)实验室用锌粒和稀硫酸反应制取H2.
(1)反应的化学方程式为 。
(2)下列仪器中,制备并收集H2时不一定需要选用的是 (填字母),仪器M的名称为 。
(二)暗发酵制氢是生物制氢的一种方法,温度在40-60℃为宜。扬州地区主要粮食作物为小麦和水稻,小麦和水稻的秸秆中木质素紧密包围纤维素,纤维素在暗发酵细菌和酶的作用下先转化为葡萄糖,葡萄糖再转化为甲酸、乙醇等,最后转化为氢气。
Ⅰ.用小麦和水稻的秸秆为发酵物进行暗发酵制氢实验,产氢量和能量转化率如表所示。
发酵物 木质素/% 产氢量/mL 能量转化率/%
小麦秸秆 22.1 292 5.2
水稻秸秆 17.3 446 6.1
(3)由表可知,与小麦秸秆相比,水稻秸秆作为发酵物的优点是 。
(4)甲酸(HCOOH)在氢化酶的催化下生成CO2和H2反应的化学方程式为 。
Ⅱ.为了探究影响水稻秸秆暗发酵制氢的因素,进行以下实验,装置如左图所示。
①实验1,向三个锥形瓶中分别加入5g水稻秸秆、一定质量的酶,一定温度下,初始pH设置为4.5、5.5和6.5,加入产氢培养基溶液使最终的发酵体积为200mL。每隔一段时间抽取发酵液的代谢产物进行检测,得到累积产氢量[V(H2)]与时间的关系如右图所示。
(5)设计实验1的目的是 。
②温度能影响酶和微生物的活性以及反应的快慢。
(6)为了确定水稻秸秆暗发酵制氢的最佳温度,请参照实验1,设计实验2的方案为 。
③发酵物的能量转化效率(E)计算公式为:
已知:。
(7)实验1的初始pH设置为6.5时,水稻秸秆的E= 。
(三)未来制氢的方向是利用地球上普遍存在的太阳能和水制氢。
光催化分解制是目前研究的热点之一,它利用半导体材料作催化剂,其原理如图所示。
(8)该方法与电解制相比有优点也有不足,选择其中一个视角,写出一点: 。
《模拟卷一》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 A C B C D C B C B B
11. (1) 金属 硬度更大/抗腐蚀性更好(合理即可)
(2)+4
(3)使温度达到可燃物的着火点
12.(1)色素和异味 (2)B
(3) 20 偏大
(4)提醒人们节约用水(合理即可)
13.(1)质量
(2) CuO-NiO/TiO2 在生产时间相同时,二氧化钛产生的氢气质量最多
(3) 化学 ;
(4)ABCD
14.I.(1)
(2)物理
(3)温室效应/全球变暖
II.(4)天然气 (5)甲醛 (6)H2O2
15.(1)过滤 (2) Cl-或
(3) ×100%
硫酸钠的溶解度随温度降低而减小 饱和氯化钠
2NaOH+MgSO4== Na2SO4+ Mg(OH)2 ↓
或Na2CO3+CaSO4== Na2SO4+ CaCO3 ↓
(5)溶液中硫酸钠的浓度较高,优先达到饱和析出
(6)降温结晶
16.(1)增大反应物之间的接触面积,使反应更快更充分
(2) 化合反应
(3) H2SO4 溶铜 酸洗
(4)c
(5)解:设理论上需要的熟石灰的质量为x,则
。
74 98
X 9.8t
x=7.4t
答:理论上需要的熟石灰的质量为7.4t。
17.(1)
(2) B 分液漏斗
(3) 水稻秸秆产氢量高、能量转化率高、木质素含量低
(4)
(5)探究pH对水稻秸秆暗发酵产氢量的影响
(6)向三个锥形瓶中分别加入5g水稻秸秆、一定质量的酶,初始pH为5.5,设置温度为40℃、45℃、50℃(或40℃、50℃、60℃),加入产氢培养基溶液使最终的发酵体积为200mL。每隔一段时间抽取发酵液的代谢产物进行检测,根据累积产氢量V(H2)确定水稻秸秆暗发酵制氢的最佳温度。[或保持与实验1相同条件下,初始pH为5.5,设置温度为40℃、45℃、50℃(或40℃、50℃、60℃)时,根据累积产氢量V(H2)确定水稻秸秆暗发酵制氢的最佳温度]
(7)4.8%
(8)利用太阳能,降低能耗和成本等/产物中H2和O2混合在一起易发生爆炸(合理即可)
九年级化学试题
(考试时间:60分钟;满分100分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ca-40
一、选择题(共10题,各3分,共30分。在每题给出四个选项中,只有一项符合题目要求)
1.2025年3月5日,李强总理在政府工作报告中提出“协同推进降碳减污扩绿增长,加快经济社会发展全面绿色转型”,下列做法不符合该主题的是
A.推广火力发电 B.发展清洁能源 C.完善绿色政策 D.开展节能行动
2.中国科学家发明了世界上超薄的光学晶体——菱方氮化硼晶体。氮化硼()属于
A.单质 B.氧化物 C.化合物 D.混合物
3.玉米是三大粮食作物之一。我国科学家破解了铁元素进入玉米籽粒的路径,有望低成本改善大范围人群的铁营养状况。下列说法错误的是
A.玉米含淀粉等营养物质 B.铁元素是人体必需的常量元素
C.人体缺铁会引起贫血 D.该研究利于提高玉米的铁含量
4.如图为厦门地区某日的空气质量情况,其中AQI指数0~50对人体健康无影响。下列分析不正确的是
A.首要污染物是臭氧
B.二氧化硫能导致酸雨
C.污染物X可能是CO2
D.当天适合户外运动
5.某小组为了检测校园花坛里土壤的酸碱性,进行了下列实验操作,其中正确的是
A.加入土壤颗粒 B.加水溶解 C.检测酸碱性 D.测pH值
6.钷可为航天器提供动力。钷元素在元素周期表中的信息如图所示,下列说法错误的是
A.钷为金属元素
B.钷的元素符号为Pm
C.钷原子的中子数为61
D.钷元素的相对原子质量为145
7.下列实践活动涉及的化学知识正确的是
选项 实践活动 化学知识
A 制作氨(NH3)分子结构模型 氨气由氮、氢原子构成
B 基于特定需求制氧气 O2可以供给呼吸
C 消防演练使用水基型灭火器 纸质文件档案可用水基型灭火器扑灭
D 调查家用燃料的变迁与使用 燃气灶火焰呈黄色时调小空气进风口
8.茶树适宜在pH为5-6的土壤中生长,茶叶中含锌、硒、茶氨酸(化学式为)等多种成分,下列说法错误的是
A.茶氨酸由碳、氢、氧、氮四种元素组成
B.茶氨酸中碳元素与氢元素质量比为
C.茶氨酸中氮元素的质量分数最大
D.可以用熟石灰改良茶树土壤,使其更好生长
9.如图所示,将缠有铁丝绒的粗铜丝插入U型管的右端,往管中注入溶质质量分数为6%的硫酸铜溶液(呈酸性),液面距管口有2~3cm。一段时间后可观察到的现象是
A.铁丝绒表面覆盖一层白色固体
B.U型管右端产生气体
C.U型管两边的液面出现左低右高
D.U型管中溶液颜色由蓝色变无色
10.室温下,某化学兴趣小组的同学设计如图甲所示装置对氢氧化钠溶液和稀盐酸反应进行探究。他们在盛有一定量X溶液的烧杯中放置pH传感器和温度传感器,并滴入3滴酚酞试液,然后开启电磁搅拌器,用滴管逐滴加入Y溶液,计算机显示两种传感器所得的数据曲线如图乙和图丙、下列表述正确的是
A.滴加Y溶液的全过程中,持续发生反应并放出热量
B.烧杯中的X溶液是稀盐酸
C.a点溶液中溶质的成分为HCl,此时烧杯中溶液呈现无色
D.滴加Y溶液的全过程中,氯化钠的溶解度逐渐增大
二、非选择题(共7题,共70分)
11.(5分)《天工开物》中记载了铜镜(如图)的制作过程:“凡铸镜,模用灰沙,铜用锡和……开面成光,则水银附体而成,非铜有光明如许也。”
(1)“铜用锡和”是指在铜中加入锡,制成青铜。青铜属于 材料(填“金属”或“合成”),与用纯铜相比,青铜制得的铜镜的优点是 (写一条)。
(2)经过氧化处理后,铜镜表面会形成一层耐腐蚀的二氧化锡(SnO2)薄膜。SnO2中锡元素的化合价为 。
(3)“阳燧”是古代照日取火用的凹面铜镜。取火时将凹面镜对着阳光,把艾绒放于焦点部位引火。从燃烧条件分析,“阳燧”的作用是 。
12.(6分)水和溶液在生产生活中有广泛的用途。
(1)人体需要持续补充水分以维持正常的生理功能,生活中常用活性炭除去水中 。
(2)如图所示的创可贴可快速止血,其原理是凸起的小囊区挤破后,水和某固体混合后降温,从而起到止血效果。该固体可能是______(填字母)。
A.氯化钠 B.硝酸铵 C.氢氧化钠 D.蔗糖
(3)个人口腔鼻腔消毒常使用盐水(氯化钠溶液),现用5%的盐水30g配制3%的盐水,需要加水的质量为 g,若使用的5%的盐水因放置时间过长导致水分蒸发了一部分,则配制的3%的盐水的溶质质量分数 (填“偏大”“偏小”或“无影响”)。
(4)目前有城市已经开始实施“阶梯水价”方案,“阶梯水价”的基本特点是用水越多,水价越贵。实施“阶梯水价”的目的是 。
13.(9分)污水是潜在的可利用资源。我国研发的微藻技术可同步处理污水与烟道气,核心原理是利用微藻的生物特性,将两种污染物转化为生物柴油(处理流程如图1所示),同时生成副产物甘油。光催化重整法能在常温常压下利用太阳能将甘油转化为氢气,其中二氧化钛(TiO2)因无毒、耐腐蚀、经济实用成为常用催化剂,常通过复合改性提升性能(催化效果见图2)。
(1)在光催化重整法中,二氧化钛(TiO2)的 和化学性质在反应前后保持不变。
(2)据图2,催化效果最佳的催化剂是 ,判断依据是 。
(3)微藻是一类光合微生物,通过光合作用固定能量,将光能转化为 能;光合作用可将二氧化碳和水转化为C6H12O6,并释放氧气,该反应的化学方程式为 。
(4)污水废气资源化处理体现了下列哪些化学发展理念? (填字母)
A.绿色化学 B.循环经济理念 C.可持续发展化学 D.环境友好化学
14.(9分)甲烷和二氧化碳都是温室气体。随着石油资源日益枯竭,储量丰富的甲烷(天然气、页岩气、可燃冰的主要成分)及二氧化碳的高效利用已成为科学研究的热点。
I.2025年3月24日,我国首口海上CCUS(二氧化碳捕集、利用与封存)井在珠江口盆地成功开钻。该项目将捕集的二氧化碳注入地层,既能提高原油采收率,又能减少二氧化碳气体排放。
(1)在二氧化碳捕集过程中,常用碱性溶液吸收二氧化碳。请写出用澄清石灰水吸收二氧化碳的化学方程式 ;
(2)在CCUS技术中,将二氧化碳压缩后注入地层时,二氧化碳由气态变为超临界态属于
变化(填“物理”或“化学”);
(3)该项目封存二氧化碳可减缓 (填环境问题),助力“双碳”目标实现。
II.我国科学家利用石墨烯为催化剂,促进甲烷转化成甲醇()和甲醛(),主要原理如图。请结合示意图回答下列问题:
(4) 主要成分为甲烷的化石燃料是_______________(填一种)。
(5)等质量的甲醇和甲醛,___________(填“甲醇”或“甲醛”)的分子个数多。
(6)过程Ⅳ中各粒子数目比为1:1:1:1:2,则X的化学式为_________。
15.(13分)我国运城盐湖(湖水富含、)地区是世界上最早采用人工治畦、利用日光晒盐的地方。当地开创的“垦畦浇晒”产盐法,发展成熟于隋唐时期,至今仍在沿用。“垦畦浇晒”的工艺流程见图1,和的溶解度曲线见图2。
Ⅰ.古法制盐分析
(1) 当蒸发畦中的盐湖水变得“模糊”时,工人将盐湖水经沟渠引入结晶畦,为防止泥沙等杂质进入结晶畦,工人会在沟渠不同位置设置多个表面带有许多小孔的盐板,这一过程称为“过箩”除杂,“过箩”除杂与实验室中的 操作原理相似。
(2)该工艺最终所得卤水中一定含有的阴离子为 (写出其中一个离子符号)。
(3)80℃时,饱和硫酸钠溶液的溶质质量分数为 (只列式)。
当气温较低时,所制得的粗盐中含量较高,这是因为 。为除去粗盐中的,可使用 溶液对粗盐进行淋洗。
Ⅱ.实验室制盐
化学实践小组的同学们取某区域的盐湖水样品(主要含、及少量和),他们从中获取和的主要过程如下:
(4)除Mg2+、Ca2+时依次加入氢氧化钠溶液和碳酸钠溶液,发生反应的化学方程式为_______________________________。(写出其中一个)
(5)将“溶液A”在80℃蒸发浓缩,至有少量固体析出。小华同学分析溶解度曲线,推测析出的少量固体是,但检验后却发现是。请作出合理解释 。
(6)小华同学停止蒸发浓缩,经 、过滤得到大量固体及母液。后续从母液中获取固体。
16.(12分)铜箔在新能源汽车电池制造等领域有重要应用。一种制造铜箔工艺的主要工序如图1所示。
(1)“溶铜”前,粉碎处理铜原料的目的是 。
(2)“溶铜”中,存在Cu与O2生成CuO的反应,该反应属于 (填基本反应类型)。
(3)“制箔”中,发生反应的化学方程式:2CuSO4+2H2O2Cu+O2↑+2X,X的化学式为 。物质X可用于 和 工序。
(4)“制箔”中,需生产抗拉强度大于355MPa且延伸率大于13.5%的铜箔,据图2可知,温度应控制在 内(填字母)。
a.45~49℃ b.50~52℃
c.53~55℃ d.56~60℃
(5)“酸洗”后,常用熟石灰中和酸性废液,其反应原理为:。
若要中和含9.8t硫酸的酸性废液,理论上需要的熟石灰的质量是多少?(利用化学方程式计算,写出完整计算过程。)
17.( 16分)氢能是一种清洁能源,氢气的制备方法受到广泛的关注和研究。
(一)实验室用锌粒和稀硫酸反应制取H2.
(1)反应的化学方程式为 。
(2)下列仪器中,制备并收集H2时不一定需要选用的是 (填字母),仪器M的名称为 。
(二)暗发酵制氢是生物制氢的一种方法,温度在40-60℃为宜。扬州地区主要粮食作物为小麦和水稻,小麦和水稻的秸秆中木质素紧密包围纤维素,纤维素在暗发酵细菌和酶的作用下先转化为葡萄糖,葡萄糖再转化为甲酸、乙醇等,最后转化为氢气。
Ⅰ.用小麦和水稻的秸秆为发酵物进行暗发酵制氢实验,产氢量和能量转化率如表所示。
发酵物 木质素/% 产氢量/mL 能量转化率/%
小麦秸秆 22.1 292 5.2
水稻秸秆 17.3 446 6.1
(3)由表可知,与小麦秸秆相比,水稻秸秆作为发酵物的优点是 。
(4)甲酸(HCOOH)在氢化酶的催化下生成CO2和H2反应的化学方程式为 。
Ⅱ.为了探究影响水稻秸秆暗发酵制氢的因素,进行以下实验,装置如左图所示。
①实验1,向三个锥形瓶中分别加入5g水稻秸秆、一定质量的酶,一定温度下,初始pH设置为4.5、5.5和6.5,加入产氢培养基溶液使最终的发酵体积为200mL。每隔一段时间抽取发酵液的代谢产物进行检测,得到累积产氢量[V(H2)]与时间的关系如右图所示。
(5)设计实验1的目的是 。
②温度能影响酶和微生物的活性以及反应的快慢。
(6)为了确定水稻秸秆暗发酵制氢的最佳温度,请参照实验1,设计实验2的方案为 。
③发酵物的能量转化效率(E)计算公式为:
已知:。
(7)实验1的初始pH设置为6.5时,水稻秸秆的E= 。
(三)未来制氢的方向是利用地球上普遍存在的太阳能和水制氢。
光催化分解制是目前研究的热点之一,它利用半导体材料作催化剂,其原理如图所示。
(8)该方法与电解制相比有优点也有不足,选择其中一个视角,写出一点: 。
《模拟卷一》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 A C B C D C B C B B
11. (1) 金属 硬度更大/抗腐蚀性更好(合理即可)
(2)+4
(3)使温度达到可燃物的着火点
12.(1)色素和异味 (2)B
(3) 20 偏大
(4)提醒人们节约用水(合理即可)
13.(1)质量
(2) CuO-NiO/TiO2 在生产时间相同时,二氧化钛产生的氢气质量最多
(3) 化学 ;
(4)ABCD
14.I.(1)
(2)物理
(3)温室效应/全球变暖
II.(4)天然气 (5)甲醛 (6)H2O2
15.(1)过滤 (2) Cl-或
(3) ×100%
硫酸钠的溶解度随温度降低而减小 饱和氯化钠
2NaOH+MgSO4== Na2SO4+ Mg(OH)2 ↓
或Na2CO3+CaSO4== Na2SO4+ CaCO3 ↓
(5)溶液中硫酸钠的浓度较高,优先达到饱和析出
(6)降温结晶
16.(1)增大反应物之间的接触面积,使反应更快更充分
(2) 化合反应
(3) H2SO4 溶铜 酸洗
(4)c
(5)解:设理论上需要的熟石灰的质量为x,则
。
74 98
X 9.8t
x=7.4t
答:理论上需要的熟石灰的质量为7.4t。
17.(1)
(2) B 分液漏斗
(3) 水稻秸秆产氢量高、能量转化率高、木质素含量低
(4)
(5)探究pH对水稻秸秆暗发酵产氢量的影响
(6)向三个锥形瓶中分别加入5g水稻秸秆、一定质量的酶,初始pH为5.5,设置温度为40℃、45℃、50℃(或40℃、50℃、60℃),加入产氢培养基溶液使最终的发酵体积为200mL。每隔一段时间抽取发酵液的代谢产物进行检测,根据累积产氢量V(H2)确定水稻秸秆暗发酵制氢的最佳温度。[或保持与实验1相同条件下,初始pH为5.5,设置温度为40℃、45℃、50℃(或40℃、50℃、60℃)时,根据累积产氢量V(H2)确定水稻秸秆暗发酵制氢的最佳温度]
(7)4.8%
(8)利用太阳能,降低能耗和成本等/产物中H2和O2混合在一起易发生爆炸(合理即可)
同课章节目录
