2025年江苏省宿迁市沭阳县中考三模 化学试题(含答案)
文档属性
| 名称 | 2025年江苏省宿迁市沭阳县中考三模 化学试题(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 894.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-07-06 00:00:00 | ||
图片预览



文档简介
化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5
一、选择题(共10小题,每小题只有一个选项符合题意,每小题2分,共20分。)
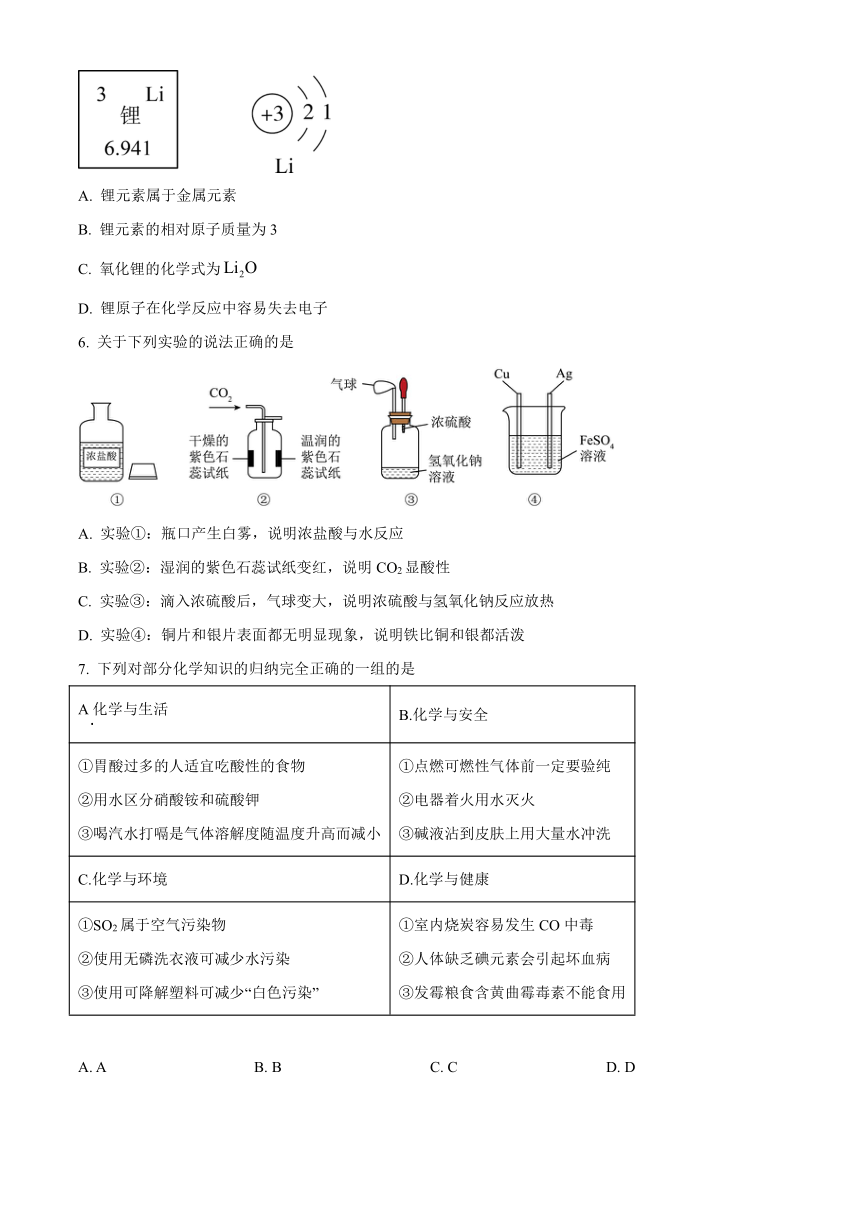
1. 下列过程中发生了化学变化的是
A. 呼吸作用 B. 酒精挥发 C. 摩擦生热 D. 湿衣晾干
2. 下列实验操作不正确的是
A. 测定pH B. 比较火焰各层温度
C. 读出液体体积 D. 检查气密性
3. 下列记录的实验现象,不符合实验事实的是
A. 镁条在空气中燃烧,产生大量的黑色固体
B. 氢氧化钠固体溶于水,溶液温度升高
C. 蜡烛在氧气中燃烧发出白光、放出热量
D. 生锈的铁钉加入稀硫酸中,溶液由无色变为黄色,然后有气泡冒出
4. 甲醛是室内装修材料释放出来的污染空气的有毒物质,利用催化剂可消除,该反应前后的微观示意图如图,则下列说法不正确的是
A. 该反应前后分子数目不变 B. 原子是化学变化中的最小粒子
C. 甲属于氧化物 D. 生成物丙和丁中氧元素的化合价相同
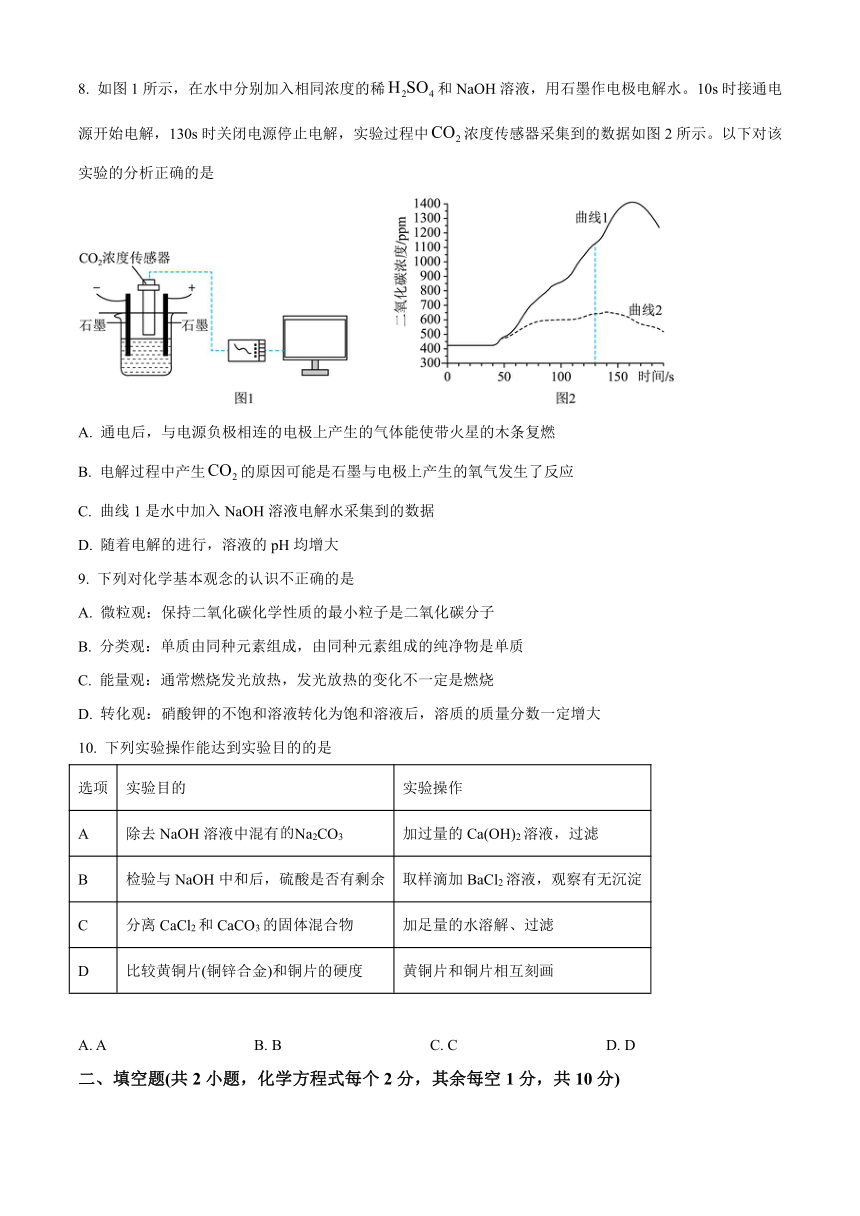
5. 有“锂”走遍天下,无“锂”寸步难行。科学不断进步,锂电池应用日益广泛。下图是锂元素在元素周期表中的部分信息及原子结构示意图,下列说法不正确的是
A. 锂元素属于金属元素
B. 锂元素的相对原子质量为3
C. 氧化锂的化学式为
D. 锂原子在化学反应中容易失去电子
6. 关于下列实验的说法正确的是
A. 实验①:瓶口产生白雾,说明浓盐酸与水反应
B. 实验②:湿润的紫色石蕊试纸变红,说明CO2显酸性
C. 实验③:滴入浓硫酸后,气球变大,说明浓硫酸与氢氧化钠反应放热
D. 实验④:铜片和银片表面都无明显现象,说明铁比铜和银都活泼
7. 下列对部分化学知识的归纳完全正确的一组的是
A化学与生活 B.化学与安全
①胃酸过多的人适宜吃酸性的食物 ②用水区分硝酸铵和硫酸钾 ③喝汽水打嗝是气体溶解度随温度升高而减小 ①点燃可燃性气体前一定要验纯 ②电器着火用水灭火 ③碱液沾到皮肤上用大量水冲洗
C.化学与环境 D.化学与健康
①SO2属于空气污染物 ②使用无磷洗衣液可减少水污染 ③使用可降解塑料可减少“白色污染” ①室内烧炭容易发生CO中毒 ②人体缺乏碘元素会引起坏血病 ③发霉粮食含黄曲霉毒素不能食用
A. A B. B C. C D. D
8. 如图1所示,在水中分别加入相同浓度的稀和NaOH溶液,用石墨作电极电解水。10s时接通电源开始电解,130s时关闭电源停止电解,实验过程中浓度传感器采集到的数据如图2所示。以下对该实验的分析正确的是
A. 通电后,与电源负极相连的电极上产生的气体能使带火星的木条复燃
B. 电解过程中产生的原因可能是石墨与电极上产生的氧气发生了反应
C. 曲线1是水中加入NaOH溶液电解水采集到的数据
D. 随着电解的进行,溶液的pH均增大
9. 下列对化学基本观念的认识不正确的是
A. 微粒观:保持二氧化碳化学性质的最小粒子是二氧化碳分子
B. 分类观:单质由同种元素组成,由同种元素组成的纯净物是单质
C. 能量观:通常燃烧发光放热,发光放热的变化不一定是燃烧
D. 转化观:硝酸钾的不饱和溶液转化为饱和溶液后,溶质的质量分数一定增大
10. 下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 除去NaOH溶液中混有Na2CO3 加过量的Ca(OH)2溶液,过滤
B 检验与NaOH中和后,硫酸是否有剩余 取样滴加BaCl2溶液,观察有无沉淀
C 分离CaCl2和CaCO3的固体混合物 加足量的水溶解、过滤
D 比较黄铜片(铜锌合金)和铜片的硬度 黄铜片和铜片相互刻画
A. A B. B C. C D. D
二、填空题(共2小题,化学方程式每个2分,其余每空1分,共10分)
11. 2024龙年春晚创意节目《年锦》织出一幅跨越千年的纹样变迁图卷。
(1)汉代袍服:选择了中国传统色彩中的黄色作为主色调。姜黄是一种黄色染料,含有姜黄素(C21H20O6),姜黄素中氢、氧元素的质量比为____(填最简整数比)。
(2)唐代襦裙:唐代的纹样运用到了花罗,真丝花罗面料属于_____(填“有机合成材料”或“天然材料”)。
(3)宋代褙子:服饰上的纹样为牡丹月桂纹。在远处能闻到牡丹花香,说明分子在____。
(4)明代袄裙:运用了刺绣工艺。手绷是一种刺绣用具,用薄竹片制成。竹子生长期需要追加化肥,下列不属于复合肥的是_____(填字母)。
A. KNO3 B. NH4H2PO4 C. CO(NH2)2
12. 将1600℃的铁水抛向高空,化为漫天华彩,遍地生金,这是来自中国传统民俗文化表演技艺—“打铁花”的浪漫。
(1)铁水氧化生成四氧化三铁的反应方程式为______。
(2)打铁花所用的铁水一般是含磷、硫等的铁合金,它是______(填纯净物或混合物)。其熔点比纯铁______(填“高”或“低”)。
(3)盛放在容器中的铁水不会燃烧,但打散在空中就会形成绚丽的铁花,这说明铁在空气中燃烧与______有关。
(4)冬季表演“打铁花”更安全,打开的铁花会迅速降温,这体现了铁具有良好的______性。
三、实验、探究题(共2小题,化学方程式每个2分,其余每空1分,共20分)
13. “支原体肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质和“富氧空气”差不多。某化学兴趣小组对气体制取开展以下实验。
(1)制取二氧化碳并要控制反应发生和停止可选用的发生装置______________。
(2)搭建如图A所示装置时,需要调整试管的倾斜度,可松开______________(选填“K1”、“K2”或“K3”)处的螺丝,待调整到所需倾斜度后再拧紧。
(3)若用B装置制取氧气,反应的化学方程式为______________。
(4)用纯氮气及上述实验制取的氧气混制“富氧空气”:使用图F装置(集气瓶容积为250mL,已装满水)和另一种仪器混制氧气体积分数为40%的“富氧空气”,则该仪器的名称为______________。从管d先通入氮气排出120mL水,再通入氧气排出______________mL水。
14. 保护环境和资源利用是人们共同关注的问题。某化学兴趣小组开启了以下项目性探究学习之旅。
项目一:探究塑料垃圾焚烧后的生成物中除了二氧化碳、氯化氢是否含有一氧化碳。
(1)【实验步骤】(试剂均足量)
①向装置A中通入燃烧后的气体一段时间后,点燃酒精灯集中加热前先需要预热,其具体操作是_______。
②然后继续通入燃烧后的气体,一段时间后观察现象;
③实验结束后,先熄灭酒精灯,固体冷却后停止通入气体。
(2)【实验分析】
装置A的作用是______。装置B中硬质玻璃管内可观察到的实验现象是______。装置C中发生反应的化学方程式为______。
【实验结论】燃烧后的气体中含有一氧化碳。
(3)【反思评价】
小组中有同学认为该实验装置存在缺陷不够严谨,你认为该装置需要改进的地方是______。塑料垃圾回收的好处远远大于焚烧处理。
项目二:海水是宝贵的自然资源。常用的海水淡化方法有蒸馏法和反渗透法。
(4)图1所示的蒸馏法过程为:海水水蒸气淡水。从能量角度看,a过程需要______(填“吸收”或“放出”)热量;图2所示加压一段时间后,剩余海水中氯化钠的质量分数_____(填“变大”或“变小”或“不变”)。
(5)提纯制盐:
同学们从某反渗透法净水厂购买了少量母液,在实验室模拟工业生产进一步提纯制盐。(母液中除含有大量的NaCl外,还含有CaCl2、MgCl2杂质)。
实验步骤 实验现象
①取少量母液于试管中,向其中滴加过量NaOH溶液 ______
②继续向①中加入过量______溶液 产生白色沉淀
③过滤,将滤液蒸发结晶 /
【反思评价】有同学认为通过以上步骤还不能得到精盐,需对步骤③进行改进,改进方案是______。
项目三:同学们对反渗透法淡化海水原理很感兴趣,进行了如图探究:
【查阅资料】鸡蛋膜有极其微小的孔隙。
【实验探究】
如图所示:向3个鸡蛋壳内分别加入表中的物质,放入盛有蒸馏水的小烧杯中,一段时间后取出鸡蛋壳,再向小烧杯中分别加入如表中的物质进行实验。
实验编号 ① ② ③
鸡蛋壳内加入的物质 NaCl溶液 NaOH溶液 淀粉溶液
小烧杯中加入的物质 AgNO3溶液 FeCl3溶液 碘水
小烧杯中的现象 白色沉淀 红褐色沉淀 无现象
【实验分析】
(6)由实验①②③小烧杯中现象得出______(填粒子符号)可以透过鸡蛋膜。
【实验结论】
综上实验探究可知:构成物质的基本粒子的体积大小不同。科学家可设计出与鸡蛋膜类似的“小筛子”分离提纯物质,如海水淡化。
【反思交流】
(7)小明同学认为上述实验③不能比较分子体积大小差异,在不增加新试剂的条件下,还应增加下列对比实验进行完善:将实验③______,重复上述实验操作,小烧杯中的现象是______,说明碘分子体积比淀粉分子小。
四、推理、计算题(共2小题,第15题5分,第16题5分,共10分)
15. 回收含铜废料(主要成分为Cu)中的铜,部分实验流程如图:回答下列问题:
(注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。)
(1)“灼烧”的主要目的是______。
(2)“酸溶”反应的化学方程式为______,基本反应类型为______。
(3)第二次过滤后滤液中的溶质为______(填化学式)。
16. 某氢氧化钠固体因保存不当部分变质生成了Na2CO3,取该样品10.0g逐滴加入一定量的稀盐酸,恰好完全反应时,得到75g溶液。反应中产生的气体的质量与稀盐酸的用量关系如图所示。试计算:
(1)x=______g。
(2)样品中NaOH的质量分数。(写出计算过程)
化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5
一、选择题(共10小题,每小题只有一个选项符合题意,每小题2分,共20分。)
【1题答案】
【答案】A
【2题答案】
【答案】A
【3题答案】
【答案】A
【4题答案】
【答案】C
【5题答案】
【答案】B
【6题答案】
【答案】D
【7题答案】
【答案】C
【8题答案】
【答案】B
【9题答案】
【答案】D
【10题答案】
【答案】D
二、填空题(共2小题,化学方程式每个2分,其余每空1分,共10分)
【11题答案】
【答案】(1)5:24
(2)天然材料 (3)不断运动 (4)C
【12题答案】
【答案】(1)
(2) ①.
混合物 ②
低 (3)
铁和氧气接触面积 (4)
导热
三、实验、探究题(共2小题,化学方程式每个2分,其余每空1分,共20分)
【13题答案】
【答案】(1)C (2)
(3)
(4) ①. 量筒 ②. 80
【14题答案】
【答案】(1)将酒精灯在酒精喷灯下方来回移动
(2) ①. 除尽燃烧产物中的二氧化碳 ②. 黑色粉末逐渐变红 ③. Ca(OH)2+CO2= CaCO3↓+H2O
(3)装置末端加一个燃着的酒精灯或用气球收集尾气等进行尾气处理
(4) ①. 吸收 ②. 变大
(5) ①. 产生白色沉淀 ②. Na2CO3 ③. 过滤后,向滤液中加入足量稀盐酸,蒸发结晶
(6)OH-、Cl- (7) ①. 鸡蛋壳内加入碘水,小烧杯中加入淀粉溶液 ②. 溶液变蓝
四、推理、计算题(共2小题,第15题5分,第16题5分,共10分)
【15题答案】
【答案】(1)将铜转化氧化铜
(2) ①. CuO+H2SO4=CuSO4+H2O ②. 复分解反应
(3)FeSO4
【16题答案】
【答案】(1)67.2
(2)解:设样品中碳酸钠的质量为x。
则样品中NaOH的质量分数为
答:样品中NaOH的质量分数为47%。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5
一、选择题(共10小题,每小题只有一个选项符合题意,每小题2分,共20分。)
1. 下列过程中发生了化学变化的是
A. 呼吸作用 B. 酒精挥发 C. 摩擦生热 D. 湿衣晾干
2. 下列实验操作不正确的是
A. 测定pH B. 比较火焰各层温度
C. 读出液体体积 D. 检查气密性
3. 下列记录的实验现象,不符合实验事实的是
A. 镁条在空气中燃烧,产生大量的黑色固体
B. 氢氧化钠固体溶于水,溶液温度升高
C. 蜡烛在氧气中燃烧发出白光、放出热量
D. 生锈的铁钉加入稀硫酸中,溶液由无色变为黄色,然后有气泡冒出
4. 甲醛是室内装修材料释放出来的污染空气的有毒物质,利用催化剂可消除,该反应前后的微观示意图如图,则下列说法不正确的是
A. 该反应前后分子数目不变 B. 原子是化学变化中的最小粒子
C. 甲属于氧化物 D. 生成物丙和丁中氧元素的化合价相同
5. 有“锂”走遍天下,无“锂”寸步难行。科学不断进步,锂电池应用日益广泛。下图是锂元素在元素周期表中的部分信息及原子结构示意图,下列说法不正确的是
A. 锂元素属于金属元素
B. 锂元素的相对原子质量为3
C. 氧化锂的化学式为
D. 锂原子在化学反应中容易失去电子
6. 关于下列实验的说法正确的是
A. 实验①:瓶口产生白雾,说明浓盐酸与水反应
B. 实验②:湿润的紫色石蕊试纸变红,说明CO2显酸性
C. 实验③:滴入浓硫酸后,气球变大,说明浓硫酸与氢氧化钠反应放热
D. 实验④:铜片和银片表面都无明显现象,说明铁比铜和银都活泼
7. 下列对部分化学知识的归纳完全正确的一组的是
A化学与生活 B.化学与安全
①胃酸过多的人适宜吃酸性的食物 ②用水区分硝酸铵和硫酸钾 ③喝汽水打嗝是气体溶解度随温度升高而减小 ①点燃可燃性气体前一定要验纯 ②电器着火用水灭火 ③碱液沾到皮肤上用大量水冲洗
C.化学与环境 D.化学与健康
①SO2属于空气污染物 ②使用无磷洗衣液可减少水污染 ③使用可降解塑料可减少“白色污染” ①室内烧炭容易发生CO中毒 ②人体缺乏碘元素会引起坏血病 ③发霉粮食含黄曲霉毒素不能食用
A. A B. B C. C D. D
8. 如图1所示,在水中分别加入相同浓度的稀和NaOH溶液,用石墨作电极电解水。10s时接通电源开始电解,130s时关闭电源停止电解,实验过程中浓度传感器采集到的数据如图2所示。以下对该实验的分析正确的是
A. 通电后,与电源负极相连的电极上产生的气体能使带火星的木条复燃
B. 电解过程中产生的原因可能是石墨与电极上产生的氧气发生了反应
C. 曲线1是水中加入NaOH溶液电解水采集到的数据
D. 随着电解的进行,溶液的pH均增大
9. 下列对化学基本观念的认识不正确的是
A. 微粒观:保持二氧化碳化学性质的最小粒子是二氧化碳分子
B. 分类观:单质由同种元素组成,由同种元素组成的纯净物是单质
C. 能量观:通常燃烧发光放热,发光放热的变化不一定是燃烧
D. 转化观:硝酸钾的不饱和溶液转化为饱和溶液后,溶质的质量分数一定增大
10. 下列实验操作能达到实验目的的是
选项 实验目的 实验操作
A 除去NaOH溶液中混有Na2CO3 加过量的Ca(OH)2溶液,过滤
B 检验与NaOH中和后,硫酸是否有剩余 取样滴加BaCl2溶液,观察有无沉淀
C 分离CaCl2和CaCO3的固体混合物 加足量的水溶解、过滤
D 比较黄铜片(铜锌合金)和铜片的硬度 黄铜片和铜片相互刻画
A. A B. B C. C D. D
二、填空题(共2小题,化学方程式每个2分,其余每空1分,共10分)
11. 2024龙年春晚创意节目《年锦》织出一幅跨越千年的纹样变迁图卷。
(1)汉代袍服:选择了中国传统色彩中的黄色作为主色调。姜黄是一种黄色染料,含有姜黄素(C21H20O6),姜黄素中氢、氧元素的质量比为____(填最简整数比)。
(2)唐代襦裙:唐代的纹样运用到了花罗,真丝花罗面料属于_____(填“有机合成材料”或“天然材料”)。
(3)宋代褙子:服饰上的纹样为牡丹月桂纹。在远处能闻到牡丹花香,说明分子在____。
(4)明代袄裙:运用了刺绣工艺。手绷是一种刺绣用具,用薄竹片制成。竹子生长期需要追加化肥,下列不属于复合肥的是_____(填字母)。
A. KNO3 B. NH4H2PO4 C. CO(NH2)2
12. 将1600℃的铁水抛向高空,化为漫天华彩,遍地生金,这是来自中国传统民俗文化表演技艺—“打铁花”的浪漫。
(1)铁水氧化生成四氧化三铁的反应方程式为______。
(2)打铁花所用的铁水一般是含磷、硫等的铁合金,它是______(填纯净物或混合物)。其熔点比纯铁______(填“高”或“低”)。
(3)盛放在容器中的铁水不会燃烧,但打散在空中就会形成绚丽的铁花,这说明铁在空气中燃烧与______有关。
(4)冬季表演“打铁花”更安全,打开的铁花会迅速降温,这体现了铁具有良好的______性。
三、实验、探究题(共2小题,化学方程式每个2分,其余每空1分,共20分)
13. “支原体肺炎”重症患者的治疗上有一个重要环节为“高流氧呼吸”,其本质和“富氧空气”差不多。某化学兴趣小组对气体制取开展以下实验。
(1)制取二氧化碳并要控制反应发生和停止可选用的发生装置______________。
(2)搭建如图A所示装置时,需要调整试管的倾斜度,可松开______________(选填“K1”、“K2”或“K3”)处的螺丝,待调整到所需倾斜度后再拧紧。
(3)若用B装置制取氧气,反应的化学方程式为______________。
(4)用纯氮气及上述实验制取的氧气混制“富氧空气”:使用图F装置(集气瓶容积为250mL,已装满水)和另一种仪器混制氧气体积分数为40%的“富氧空气”,则该仪器的名称为______________。从管d先通入氮气排出120mL水,再通入氧气排出______________mL水。
14. 保护环境和资源利用是人们共同关注的问题。某化学兴趣小组开启了以下项目性探究学习之旅。
项目一:探究塑料垃圾焚烧后的生成物中除了二氧化碳、氯化氢是否含有一氧化碳。
(1)【实验步骤】(试剂均足量)
①向装置A中通入燃烧后的气体一段时间后,点燃酒精灯集中加热前先需要预热,其具体操作是_______。
②然后继续通入燃烧后的气体,一段时间后观察现象;
③实验结束后,先熄灭酒精灯,固体冷却后停止通入气体。
(2)【实验分析】
装置A的作用是______。装置B中硬质玻璃管内可观察到的实验现象是______。装置C中发生反应的化学方程式为______。
【实验结论】燃烧后的气体中含有一氧化碳。
(3)【反思评价】
小组中有同学认为该实验装置存在缺陷不够严谨,你认为该装置需要改进的地方是______。塑料垃圾回收的好处远远大于焚烧处理。
项目二:海水是宝贵的自然资源。常用的海水淡化方法有蒸馏法和反渗透法。
(4)图1所示的蒸馏法过程为:海水水蒸气淡水。从能量角度看,a过程需要______(填“吸收”或“放出”)热量;图2所示加压一段时间后,剩余海水中氯化钠的质量分数_____(填“变大”或“变小”或“不变”)。
(5)提纯制盐:
同学们从某反渗透法净水厂购买了少量母液,在实验室模拟工业生产进一步提纯制盐。(母液中除含有大量的NaCl外,还含有CaCl2、MgCl2杂质)。
实验步骤 实验现象
①取少量母液于试管中,向其中滴加过量NaOH溶液 ______
②继续向①中加入过量______溶液 产生白色沉淀
③过滤,将滤液蒸发结晶 /
【反思评价】有同学认为通过以上步骤还不能得到精盐,需对步骤③进行改进,改进方案是______。
项目三:同学们对反渗透法淡化海水原理很感兴趣,进行了如图探究:
【查阅资料】鸡蛋膜有极其微小的孔隙。
【实验探究】
如图所示:向3个鸡蛋壳内分别加入表中的物质,放入盛有蒸馏水的小烧杯中,一段时间后取出鸡蛋壳,再向小烧杯中分别加入如表中的物质进行实验。
实验编号 ① ② ③
鸡蛋壳内加入的物质 NaCl溶液 NaOH溶液 淀粉溶液
小烧杯中加入的物质 AgNO3溶液 FeCl3溶液 碘水
小烧杯中的现象 白色沉淀 红褐色沉淀 无现象
【实验分析】
(6)由实验①②③小烧杯中现象得出______(填粒子符号)可以透过鸡蛋膜。
【实验结论】
综上实验探究可知:构成物质的基本粒子的体积大小不同。科学家可设计出与鸡蛋膜类似的“小筛子”分离提纯物质,如海水淡化。
【反思交流】
(7)小明同学认为上述实验③不能比较分子体积大小差异,在不增加新试剂的条件下,还应增加下列对比实验进行完善:将实验③______,重复上述实验操作,小烧杯中的现象是______,说明碘分子体积比淀粉分子小。
四、推理、计算题(共2小题,第15题5分,第16题5分,共10分)
15. 回收含铜废料(主要成分为Cu)中的铜,部分实验流程如图:回答下列问题:
(注:灼烧后得到黑色固体和残留物,残留物不溶于水和稀硫酸。)
(1)“灼烧”的主要目的是______。
(2)“酸溶”反应的化学方程式为______,基本反应类型为______。
(3)第二次过滤后滤液中的溶质为______(填化学式)。
16. 某氢氧化钠固体因保存不当部分变质生成了Na2CO3,取该样品10.0g逐滴加入一定量的稀盐酸,恰好完全反应时,得到75g溶液。反应中产生的气体的质量与稀盐酸的用量关系如图所示。试计算:
(1)x=______g。
(2)样品中NaOH的质量分数。(写出计算过程)
化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5
一、选择题(共10小题,每小题只有一个选项符合题意,每小题2分,共20分。)
【1题答案】
【答案】A
【2题答案】
【答案】A
【3题答案】
【答案】A
【4题答案】
【答案】C
【5题答案】
【答案】B
【6题答案】
【答案】D
【7题答案】
【答案】C
【8题答案】
【答案】B
【9题答案】
【答案】D
【10题答案】
【答案】D
二、填空题(共2小题,化学方程式每个2分,其余每空1分,共10分)
【11题答案】
【答案】(1)5:24
(2)天然材料 (3)不断运动 (4)C
【12题答案】
【答案】(1)
(2) ①.
混合物 ②
低 (3)
铁和氧气接触面积 (4)
导热
三、实验、探究题(共2小题,化学方程式每个2分,其余每空1分,共20分)
【13题答案】
【答案】(1)C (2)
(3)
(4) ①. 量筒 ②. 80
【14题答案】
【答案】(1)将酒精灯在酒精喷灯下方来回移动
(2) ①. 除尽燃烧产物中的二氧化碳 ②. 黑色粉末逐渐变红 ③. Ca(OH)2+CO2= CaCO3↓+H2O
(3)装置末端加一个燃着的酒精灯或用气球收集尾气等进行尾气处理
(4) ①. 吸收 ②. 变大
(5) ①. 产生白色沉淀 ②. Na2CO3 ③. 过滤后,向滤液中加入足量稀盐酸,蒸发结晶
(6)OH-、Cl- (7) ①. 鸡蛋壳内加入碘水,小烧杯中加入淀粉溶液 ②. 溶液变蓝
四、推理、计算题(共2小题,第15题5分,第16题5分,共10分)
【15题答案】
【答案】(1)将铜转化氧化铜
(2) ①. CuO+H2SO4=CuSO4+H2O ②. 复分解反应
(3)FeSO4
【16题答案】
【答案】(1)67.2
(2)解:设样品中碳酸钠的质量为x。
则样品中NaOH的质量分数为
答:样品中NaOH的质量分数为47%。
同课章节目录
