课题2溶解度 课件(共28张PPT)
图片预览





文档简介
(共28张PPT)
溶解度(第2课时)
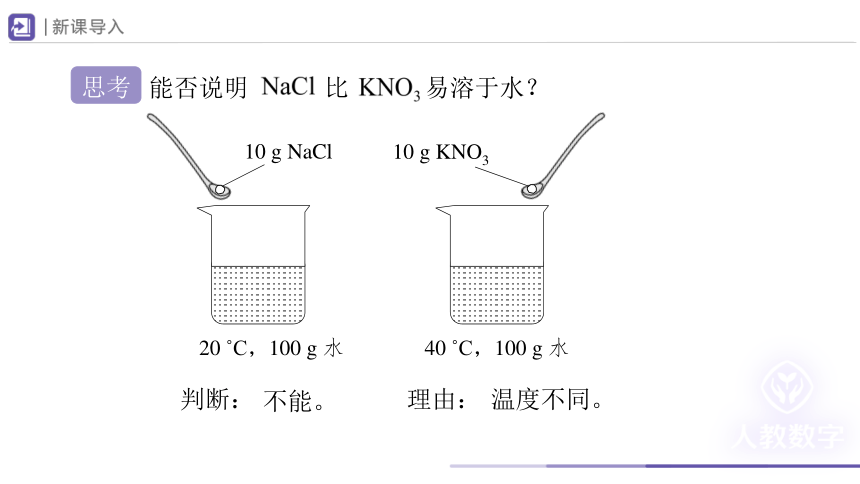
判断:
不能。
理由:
温度不同。
能否说明 比 易溶于水?
20 C,100 g 水
40 C,100 g 水
10 g NaCl
10 g KNO3
思考
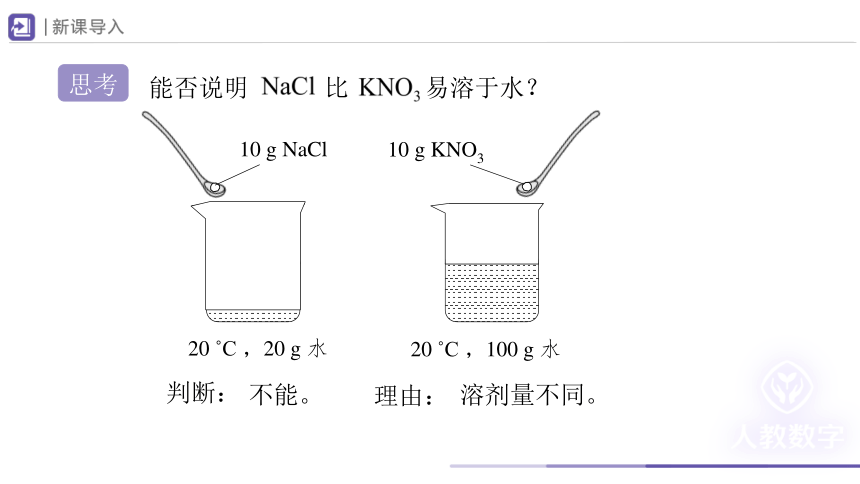
20 C ,20 g 水
20 C ,100 g 水
10 g NaCl
10 g KNO3
判断:
不能。
理由:
溶剂量不同。
思考
能否说明 比 易溶于水?
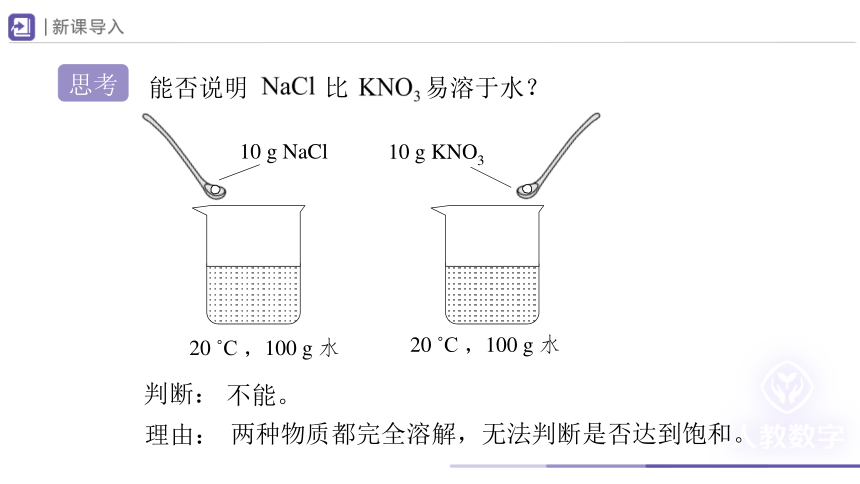
判断:
不能。
理由:
两种物质都完全溶解,无法判断是否达到饱和。
20 C ,100 g 水
20 C ,100 g 水
10 g NaCl
10 g KNO3
思考
能否说明 比 易溶于水?
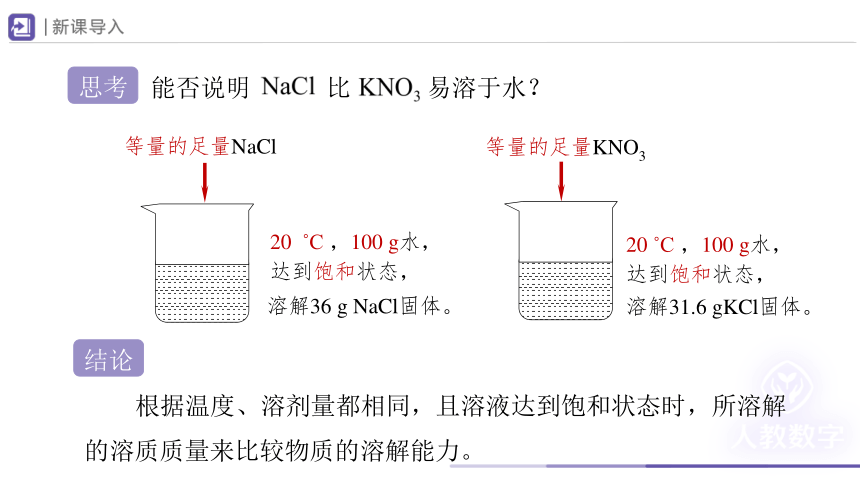
等量的足量NaCl
等量的足量KNO3
20 C ,100 g水,
达到饱和状态,
20 C ,100 g水,
达到饱和状态,
溶解36 g NaCl固体。
溶解31.6 gKCl固体。
根据温度、溶剂量都相同,且溶液达到饱和状态时,所溶解的溶质质量来比较物质的溶解能力。
思考
能否说明 比 易溶于水?
结论
固体的溶解度
在一定温度下,某固态物质在100 g 溶剂里达到饱和状态时所溶解的质量,叫作这种物质在这种溶剂中的溶解度。
概念
四要素
条件:一定温度
状态:饱和状态
标准:在100 g 溶剂里
单位:g
如果不指明溶剂,通常所说的溶解度是指物质在水里的溶解度。
四要素缺一不可!
温度 溶质的质量 溶剂的质量 溶液的质量
20 C时,硝酸钾的溶解度是 31.6 g。
20 C
31.6 g
100 g
131.6 g
概念的理解
20 C 时,100 g 水中最多能溶解硝酸钾的质量为 31.6 g。
20 C 时,100 g 水中溶解 31.6 g 硝酸钾达到饱和状态。
1.30 g 固体甲溶解在 100 g 水中恰好达到饱和状态,则固体甲的溶解度为 30 g。
2.20 C时,30 g 固体甲溶解在水中恰好达到饱和状态,则20 C时,固体甲的溶解度为30 g。
3.20 C时,30 g 固体甲可溶解在100 g 水中,则20 C时,固体甲的溶解度为 30 g。
不正确,未指明温度(t C )。
不正确,未指明一定量溶剂(100 g)。
不正确,未指明是否达到饱和状态。
判断下列说法是否正确,并说明原因。
讨论
溶解度的相对大小(20 C )
物质 碳酸钙 氯化钙
溶解度/g(20 C) 0.006 5 74.5
20 C时,碳酸钙和氯化钙在水中的溶解度如表所示,可知碳酸钙是 _____溶物质。分离碳酸钙和氯化钙的混合物可用什么方法?
难
溶解、过滤
溶解性与溶解度的关系
溶解度/g 一般称为
<0.01 难溶
0.01~1 微溶
1~10 可溶
>10 易溶
思考
资料卡片
温度/ C 0 10 20 30 40 50 60 70 80 90 100
溶解度 / g 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8
27.6 31.0 34.0 37.0 40.0 42.6 45.5 48.3 51.1 54.0 56.7
29.4 33.3 37.2 41.4 45.8 50.4 55.2 60.2 65.6 71.3 77.3
13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
溶解度曲线
几种物质在不同温度时的溶解度
探究
溶解度曲线
如何根据上表的数据推测表中物质在某一未测温度(如 25 C 、85 C 等)时的溶解度呢?
【问题】
【方案设计】
根据上表的数据绘制曲线,并获得所需要的信息。
【方案实施】
用纵坐标表示溶解度,横坐标表示温度,根据上表提供的数据,在坐标纸上(或利用计算机软件)绘制几种物质的溶解度随温度变化的曲线——溶解度曲线。
(1)绘制溶解度曲线。
温度/ C 25 85
溶解度 / g 36.2 38.5
35.6 52.4
39.7 68.7
37.2 183.7
(2)应用溶解度曲线。
在绘制的溶解度曲线上,查出上述几种物质在 25 C 和 85 C 时的溶解度。
几种固体的溶解度曲线
氢氧化钙的溶解度曲线
(2)分析溶解度曲线。
(1)这些固体的溶解度随温度的变化有什么规律?举例说明。
讨论
(2)从溶解度曲线中,你还能获得哪些信息?
多数固体的溶解度随温度升高而增大,如硝酸铵、硝酸钾、硝酸钠;少数固体的溶解度受温度变化的影响很小,如氯化钠;极少数固体的溶解度随温度升高而减小,如氢氧化钙。
某物质在指定温度下的溶解度;某物质溶解度受温度变化的影响趋势。
溶解度数据表和溶解度曲线都可以表示物质在不同温度时的溶解度,二者有什么区别 通过溶解度数据表和溶解度曲线所提供的不同信息,你能否体会到数据处理的方法不同,获得结果的形式和作用就不同 与同学交流。
思考与讨论
溶解度数据表的优点是以实验为基础,数据准确,但因温度是一个连续的量,无法在任意温度下都测定溶解度,故有一定的局限性;以一系列实验数据为依据绘制的溶解度曲线解决了这个问题,所呈现的温度范围比较宽,但曲线上查得的溶解度数据会有误差。
几种固体的溶解度曲线
1.点:溶解度曲线上的每个点表示的是某温度下某种物质的溶解度。
(2)比较相同温度下不同物质的溶解度。
(1)根据已知温度查出有关物质的溶解度,并判断溶解性。
溶解度曲线的意义
氢氧化钙的溶解度曲线
2.线:溶解度曲线表示某物质在不同温度下的溶解度和溶解度随温度的变化情况。
(3)极少数固体物质的溶解度随温度的升高而减小,如 。
(2)少数固体物质的溶解度受温度变化的影响很小,如 。
(1)大多数固体物质的溶解度随温度的升高而增大,如 。
几种固体的溶解度曲线
氢氧化钙的溶解度曲线
溶解度/g
温度/℃
A
B
C
3.面:
(1)曲线上的点表示该温度下该种物质的溶解度,所以此时的溶液恰好达到饱和状态,如 B 点。
(2)曲线下面的点表示该温度下的不饱和状态,如 C 点。
(3)曲线上面的点表示该温度下的饱和状态,而且有固体未溶解,如 A 点。
t2
S2
S1
S3
t1
O
4.交点:
两条溶解度曲线的交点表示该温度下两物质的溶解度相同。
t
S
A
溶解度/g
温度/℃
O
方法导引
数据处理
以表格或曲线的形式呈现物质的溶解度及其变化,就是对实验测得的溶解度的原始数据进行处理的结果。
数据处理是对已有数据进行加工的过程,目的是从大量的、可能是无序的数据中,抽取出有价值、有意义的数据,通过处理、分析,发现规律。列表和作图是常用的数据处理方法。数据处理在科学研究、工农业生产和经济活动等领域有广泛的应用。
通常用的气体溶解度,是指该气体的压强为101 kPa和一定温度时,溶解在1体积水里达到饱和状态时的气体体积。
定义
例如:氮气的压强为101 kPa 、温度为 0 ℃时,1 体积水里最多能溶解 0.024 体积的氮气,则在 0 ℃时,氮气的溶解度为 0.024。
气体溶解度
1.打开汽水(含有二氧化碳气体的饮料)瓶盖时,汽水有时会喷出来。请分析原因并与同学交流。
打开瓶盖,瓶内压强减小,气体的溶解度减小,气体从溶液中逸出。
思考与讨论
打开瓶盖后汽水自动喷出
结论:气体的溶解度与外界压强有关。
2 .为什么不能用煮沸后的凉开水养鱼
由于气体的溶解度随温度的升高而减小,温度升高,水中溶解的氧气减少,煮沸后的凉开水中氧气含量太低,不适合养鱼。
思考与讨论
结论:气体的溶解度与外界温度有关。
影响因素
气体溶解度
压强
温度
1.夏天鱼常常浮出水面,而冬天则少见,说明了什么?
2.雷阵雨前,鱼常常将头浮出水面,说明了什么?
把水喷向空中可以增加水中氧气的溶解量
讨论
溶解度
固体的溶解度
概念形成
四要素
概念的理解
溶解度曲线
定义
影响因素
气体的溶解度
溶解度曲线的意义
溶解度(第2课时)
判断:
不能。
理由:
温度不同。
能否说明 比 易溶于水?
20 C,100 g 水
40 C,100 g 水
10 g NaCl
10 g KNO3
思考
20 C ,20 g 水
20 C ,100 g 水
10 g NaCl
10 g KNO3
判断:
不能。
理由:
溶剂量不同。
思考
能否说明 比 易溶于水?
判断:
不能。
理由:
两种物质都完全溶解,无法判断是否达到饱和。
20 C ,100 g 水
20 C ,100 g 水
10 g NaCl
10 g KNO3
思考
能否说明 比 易溶于水?
等量的足量NaCl
等量的足量KNO3
20 C ,100 g水,
达到饱和状态,
20 C ,100 g水,
达到饱和状态,
溶解36 g NaCl固体。
溶解31.6 gKCl固体。
根据温度、溶剂量都相同,且溶液达到饱和状态时,所溶解的溶质质量来比较物质的溶解能力。
思考
能否说明 比 易溶于水?
结论
固体的溶解度
在一定温度下,某固态物质在100 g 溶剂里达到饱和状态时所溶解的质量,叫作这种物质在这种溶剂中的溶解度。
概念
四要素
条件:一定温度
状态:饱和状态
标准:在100 g 溶剂里
单位:g
如果不指明溶剂,通常所说的溶解度是指物质在水里的溶解度。
四要素缺一不可!
温度 溶质的质量 溶剂的质量 溶液的质量
20 C时,硝酸钾的溶解度是 31.6 g。
20 C
31.6 g
100 g
131.6 g
概念的理解
20 C 时,100 g 水中最多能溶解硝酸钾的质量为 31.6 g。
20 C 时,100 g 水中溶解 31.6 g 硝酸钾达到饱和状态。
1.30 g 固体甲溶解在 100 g 水中恰好达到饱和状态,则固体甲的溶解度为 30 g。
2.20 C时,30 g 固体甲溶解在水中恰好达到饱和状态,则20 C时,固体甲的溶解度为30 g。
3.20 C时,30 g 固体甲可溶解在100 g 水中,则20 C时,固体甲的溶解度为 30 g。
不正确,未指明温度(t C )。
不正确,未指明一定量溶剂(100 g)。
不正确,未指明是否达到饱和状态。
判断下列说法是否正确,并说明原因。
讨论
溶解度的相对大小(20 C )
物质 碳酸钙 氯化钙
溶解度/g(20 C) 0.006 5 74.5
20 C时,碳酸钙和氯化钙在水中的溶解度如表所示,可知碳酸钙是 _____溶物质。分离碳酸钙和氯化钙的混合物可用什么方法?
难
溶解、过滤
溶解性与溶解度的关系
溶解度/g 一般称为
<0.01 难溶
0.01~1 微溶
1~10 可溶
>10 易溶
思考
资料卡片
温度/ C 0 10 20 30 40 50 60 70 80 90 100
溶解度 / g 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8
27.6 31.0 34.0 37.0 40.0 42.6 45.5 48.3 51.1 54.0 56.7
29.4 33.3 37.2 41.4 45.8 50.4 55.2 60.2 65.6 71.3 77.3
13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
溶解度曲线
几种物质在不同温度时的溶解度
探究
溶解度曲线
如何根据上表的数据推测表中物质在某一未测温度(如 25 C 、85 C 等)时的溶解度呢?
【问题】
【方案设计】
根据上表的数据绘制曲线,并获得所需要的信息。
【方案实施】
用纵坐标表示溶解度,横坐标表示温度,根据上表提供的数据,在坐标纸上(或利用计算机软件)绘制几种物质的溶解度随温度变化的曲线——溶解度曲线。
(1)绘制溶解度曲线。
温度/ C 25 85
溶解度 / g 36.2 38.5
35.6 52.4
39.7 68.7
37.2 183.7
(2)应用溶解度曲线。
在绘制的溶解度曲线上,查出上述几种物质在 25 C 和 85 C 时的溶解度。
几种固体的溶解度曲线
氢氧化钙的溶解度曲线
(2)分析溶解度曲线。
(1)这些固体的溶解度随温度的变化有什么规律?举例说明。
讨论
(2)从溶解度曲线中,你还能获得哪些信息?
多数固体的溶解度随温度升高而增大,如硝酸铵、硝酸钾、硝酸钠;少数固体的溶解度受温度变化的影响很小,如氯化钠;极少数固体的溶解度随温度升高而减小,如氢氧化钙。
某物质在指定温度下的溶解度;某物质溶解度受温度变化的影响趋势。
溶解度数据表和溶解度曲线都可以表示物质在不同温度时的溶解度,二者有什么区别 通过溶解度数据表和溶解度曲线所提供的不同信息,你能否体会到数据处理的方法不同,获得结果的形式和作用就不同 与同学交流。
思考与讨论
溶解度数据表的优点是以实验为基础,数据准确,但因温度是一个连续的量,无法在任意温度下都测定溶解度,故有一定的局限性;以一系列实验数据为依据绘制的溶解度曲线解决了这个问题,所呈现的温度范围比较宽,但曲线上查得的溶解度数据会有误差。
几种固体的溶解度曲线
1.点:溶解度曲线上的每个点表示的是某温度下某种物质的溶解度。
(2)比较相同温度下不同物质的溶解度。
(1)根据已知温度查出有关物质的溶解度,并判断溶解性。
溶解度曲线的意义
氢氧化钙的溶解度曲线
2.线:溶解度曲线表示某物质在不同温度下的溶解度和溶解度随温度的变化情况。
(3)极少数固体物质的溶解度随温度的升高而减小,如 。
(2)少数固体物质的溶解度受温度变化的影响很小,如 。
(1)大多数固体物质的溶解度随温度的升高而增大,如 。
几种固体的溶解度曲线
氢氧化钙的溶解度曲线
溶解度/g
温度/℃
A
B
C
3.面:
(1)曲线上的点表示该温度下该种物质的溶解度,所以此时的溶液恰好达到饱和状态,如 B 点。
(2)曲线下面的点表示该温度下的不饱和状态,如 C 点。
(3)曲线上面的点表示该温度下的饱和状态,而且有固体未溶解,如 A 点。
t2
S2
S1
S3
t1
O
4.交点:
两条溶解度曲线的交点表示该温度下两物质的溶解度相同。
t
S
A
溶解度/g
温度/℃
O
方法导引
数据处理
以表格或曲线的形式呈现物质的溶解度及其变化,就是对实验测得的溶解度的原始数据进行处理的结果。
数据处理是对已有数据进行加工的过程,目的是从大量的、可能是无序的数据中,抽取出有价值、有意义的数据,通过处理、分析,发现规律。列表和作图是常用的数据处理方法。数据处理在科学研究、工农业生产和经济活动等领域有广泛的应用。
通常用的气体溶解度,是指该气体的压强为101 kPa和一定温度时,溶解在1体积水里达到饱和状态时的气体体积。
定义
例如:氮气的压强为101 kPa 、温度为 0 ℃时,1 体积水里最多能溶解 0.024 体积的氮气,则在 0 ℃时,氮气的溶解度为 0.024。
气体溶解度
1.打开汽水(含有二氧化碳气体的饮料)瓶盖时,汽水有时会喷出来。请分析原因并与同学交流。
打开瓶盖,瓶内压强减小,气体的溶解度减小,气体从溶液中逸出。
思考与讨论
打开瓶盖后汽水自动喷出
结论:气体的溶解度与外界压强有关。
2 .为什么不能用煮沸后的凉开水养鱼
由于气体的溶解度随温度的升高而减小,温度升高,水中溶解的氧气减少,煮沸后的凉开水中氧气含量太低,不适合养鱼。
思考与讨论
结论:气体的溶解度与外界温度有关。
影响因素
气体溶解度
压强
温度
1.夏天鱼常常浮出水面,而冬天则少见,说明了什么?
2.雷阵雨前,鱼常常将头浮出水面,说明了什么?
把水喷向空中可以增加水中氧气的溶解量
讨论
溶解度
固体的溶解度
概念形成
四要素
概念的理解
溶解度曲线
定义
影响因素
气体的溶解度
溶解度曲线的意义
同课章节目录
