母题必读 命题区间十二化学实验基础知识--《高考快车道》2026版高考化学母题必读及衍生卷
文档属性
| 名称 | 母题必读 命题区间十二化学实验基础知识--《高考快车道》2026版高考化学母题必读及衍生卷 |
|
|
| 格式 | DOCX | ||
| 文件大小 | 444.3KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-10-20 00:00:00 | ||
图片预览


文档简介
化学实验基础知识
命题角度 3年考题分布 考情预测
化学实验基本操作 2024·山东卷T6;2024·安徽卷T2;2024·湖北卷T3;2023·山东卷T4;2023·全国甲卷T9;2022·海南卷T2、T3;2022·湖南卷T4 化学实验基础是历年高考的必考内容,近几年高考试题多以论述形式、表格形式、装置图的形式出现,以中学化学所涉及的重要物质的性质为载体,突出考查基本仪器的使用、化学实验操作的规范性、物质的检验分离提纯、气体的制备等,试题常涉及物质的分离提纯,气体的制取、除杂、收集、尾气处理,溶液的配制等操作。试题考查点多,在稳定的基础上追求创新,题目具有较强的综合性。
“装置—目的”一致性判断 2024·广东卷T8;2024·甘肃卷T6;2023·北京卷T8;2023·湖南卷T3;2023·全国乙卷T9;2023·湖北卷T13;2022·湖北卷T6
“操作—现象—结论”一致性判断 2024·河北卷T6;2024·山东卷T12;2023·浙江6月卷T16;2023·新课标卷T11
综合实验分析 2024·黑吉辽卷T19;2024·甘肃卷T15;2024·湖南卷T16;2023·山东卷T18;2023·湖南卷T15;2022·湖北卷T16;2022·浙江6月卷T30
化学实验基本操作
高考真题 构建解题模型
(2023·山东卷,T4)实验室安全至关重要,下列实验室事故处理方法错误的是( ) A.眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗 B.皮肤溅上碱液,先用大量水冲洗,再用2%的硼酸溶液冲洗 C.电器起火,先切断电源,再用二氧化碳灭火器灭火 D.活泼金属燃烧起火,用灭火毯(石棉布)灭火 眼睛溅进酸液,先用大量水冲洗,边洗边眨眼,尽可能减少酸对眼睛的伤害,再用3%~5%的碳酸氢钠溶液冲洗,A错误;皮肤溅上碱液,应立即用大量水冲洗,再用2%的硼酸中和残余的碱,B正确;电器起火,先切断电源,再用二氧化碳灭火器灭火,C正确;活泼金属会与水反应,所以燃烧起火,用灭火毯(石棉布)灭火,D正确。 A
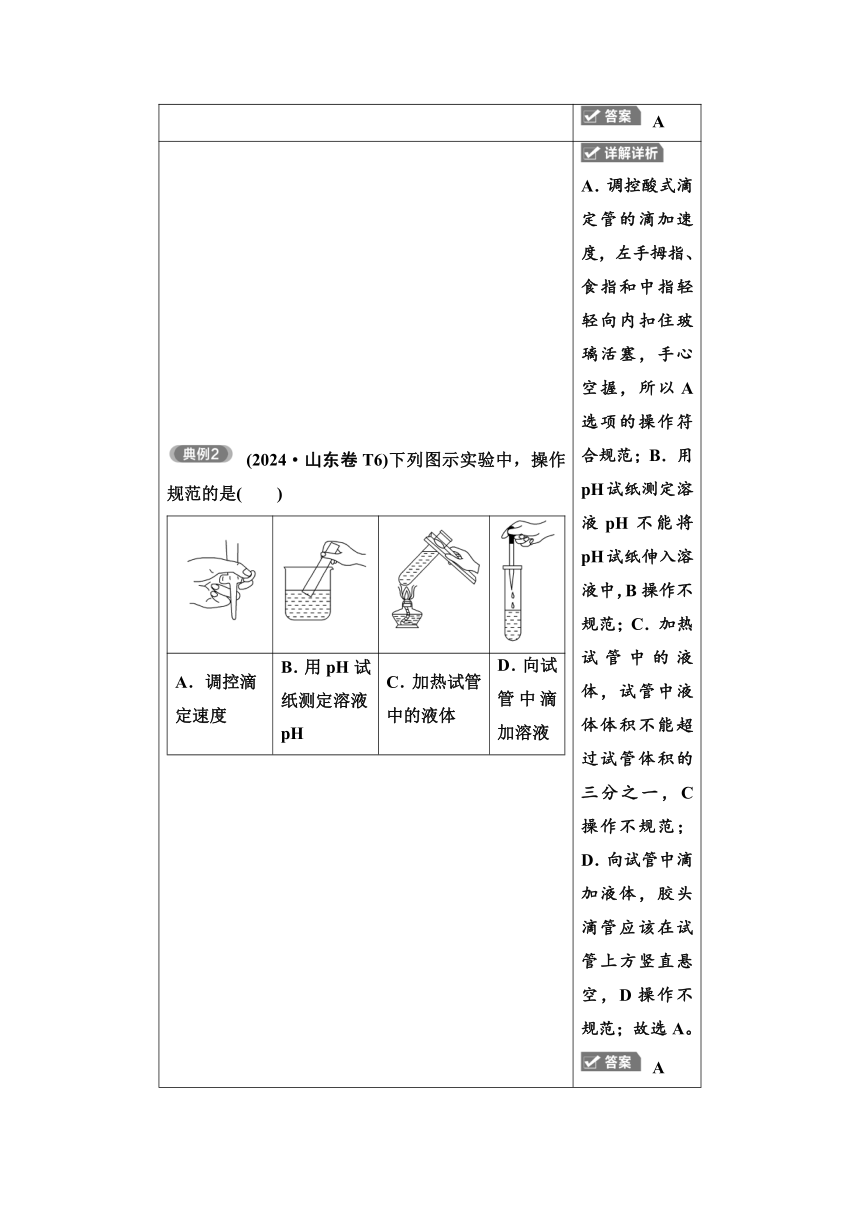
(2024·山东卷T6)下列图示实验中,操作规范的是( ) A.调控滴 定速度B.用pH试纸测定溶液pHC.加热试管 中的液体D.向试管中滴加溶液
A.调控酸式滴定管的滴加速度,左手拇指、食指和中指轻轻向内扣住玻璃活塞,手心空握,所以A选项的操作符合规范;B.用pH试纸测定溶液pH不能将pH试纸伸入溶液中,B操作不规范;C.加热试管中的液体,试管中液体体积不能超过试管体积的三分之一,C操作不规范;D.向试管中滴加液体,胶头滴管应该在试管上方竖直悬空,D操作不规范;故选A。 A
“装置—目的”一致性判断
高考真题 构建解题模型
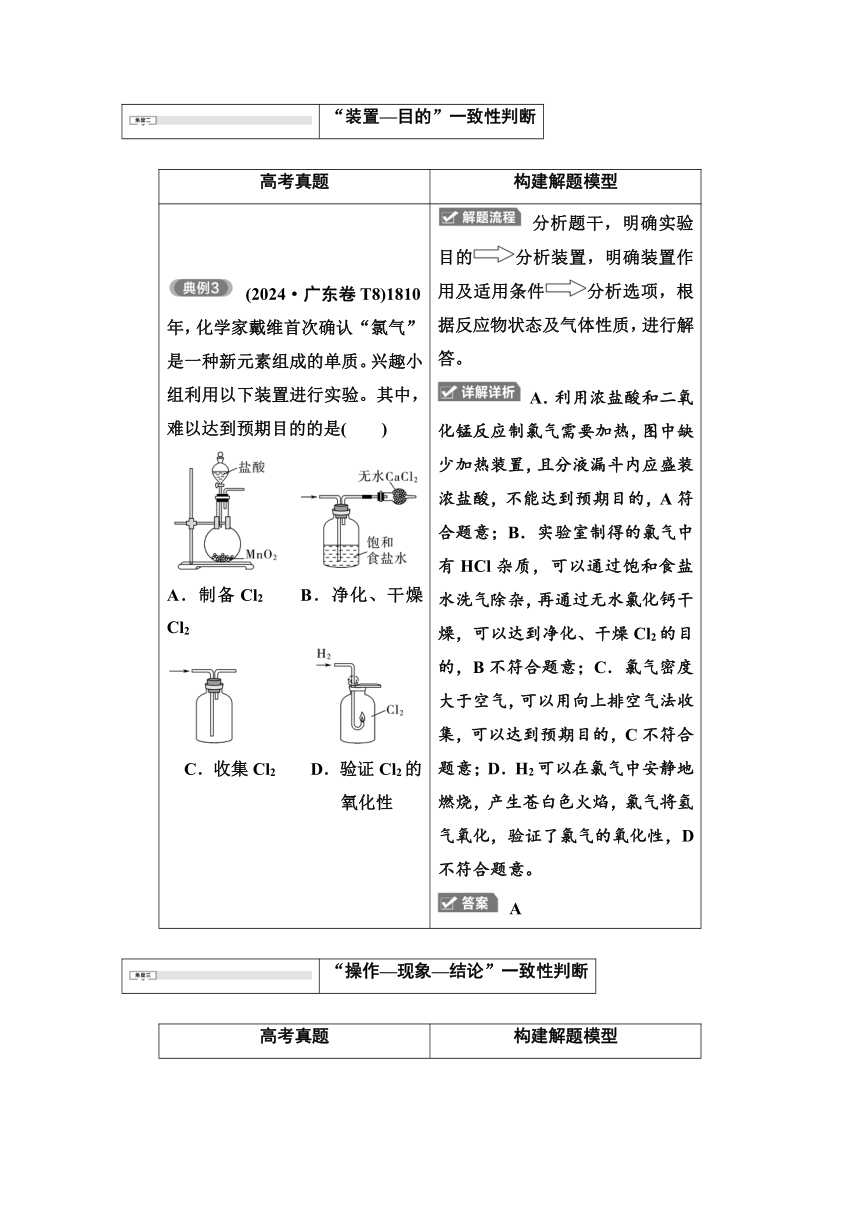
(2024·广东卷T8)1810年,化学家戴维首次确认“氯气”是一种新元素组成的单质。兴趣小组利用以下装置进行实验。其中,难以达到预期目的的是( ) A.制备Cl2 B.净化、干燥Cl2 C.收集Cl2 D.验证Cl2的 氧化性 分析题干,明确实验目的分析装置,明确装置作用及适用条件分析选项,根据反应物状态及气体性质,进行解答。 A.利用浓盐酸和二氧化锰反应制氯气需要加热,图中缺少加热装置,且分液漏斗内应盛装浓盐酸,不能达到预期目的,A符合题意;B.实验室制得的氯气中有HCl杂质,可以通过饱和食盐水洗气除杂,再通过无水氯化钙干燥,可以达到净化、干燥Cl2的目的,B不符合题意;C.氯气密度大于空气,可以用向上排空气法收集,可以达到预期目的,C不符合题意;D.H2可以在氯气中安静地燃烧,产生苍白色火焰,氯气将氢气氧化,验证了氯气的氧化性,D不符合题意。 A
“操作—现象—结论”一致性判断
高考真题 构建解题模型
(2024·河北卷T6)下列实验操作及现象能得出相应结论的是( ) 选项实验操作及现象结论A还原铁粉与水蒸气反应生成的气体点燃后有爆鸣声H2O具有还原性B待测液中滴加BaCl2溶液,生成白色沉淀待测液含有CMg(OH)2和Al(OH)3中均分别加入NaOH溶液和盐酸,Mg(OH)2只溶于盐酸,Al(OH)3都能溶Mg(OH)2比 Al(OH)3碱性强DK2Cr2O7溶液中滴加NaOH溶液,溶液由橙色变为黄色增大生成物的浓度,平衡向逆反应方向移动
铁与水蒸气反应生成的气体是H2,该反应中H由+1价变成0价,被还原,体现了H2O的氧化性,A错误;如果待测液中含有Ag+,Ag+与Cl-反应也能产生白色沉淀,通过该实验不能得出待测液中含有的结论,B错误;Mg(OH)2溶液能与盐酸反应,不能与NaOH溶液反应,与NaOH溶液和盐酸都能反应,说明Mg(OH)2的碱性比Al(OH)3的强,C正确;K2Cr2O7溶液中存在平衡:(橙色(黄色)+2H+,加入NaOH溶液后,OH-与H+反应,生成物浓度减小,使平衡正向移动,导致溶液由橙色变为黄色,题给结论错误,D错误。 C
解答“操作—现象—结论”类实验题的操作步骤 第一步:明确题干要求,确定判断类别。首先判断题干要求的一致性关系,确定属于“因果关系型”“结论与操作相关型”“方法原理应用型”等的哪一类型。第二步:认真阅读表格要素,细研表格各栏目信息。(1)判断原理与现象或结论解释的关系。 (2)判断“目的—仪器—试剂”的合理性。 (3)判断“仪器(或用品)”与“实验”的对应性。 (4)判断“分离、提纯方法”与“原理”的合理性等。第三步:逐项判断,不遗漏任何信息。抓住操作、现象、数据等关键点,充分利用排除法、特例法等解题技巧,迅速作答。
高考真题 构建解题模型
(2024·黑吉辽卷T17)某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验方案如下: Ⅰ.向50 mL烧瓶中分别加入5.7 mL乙酸(100 mmol)、8.8 mL乙醇(150 mmol)、1.4 g NaHSO4固体及4~6滴1‰甲基紫的乙醇溶液,向小孔冷凝柱中装入变色硅胶。 Ⅱ.加热回流50 min后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。 Ⅲ.冷却后,向烧瓶中缓慢加入饱和Na2CO3溶液至无CO2逸出,分离出有机相。 Ⅳ.洗涤有机相后,加入无水MgSO4,过滤。 Ⅴ.蒸馏滤液,收集73~78 ℃馏分,得无色液体6.60 g,色谱检测纯度为98.0%。 回答下列问题: (1)NaHSO4在反应中起 作用,用其代替浓硫酸的优点是 (答出一条即可)。 (2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可 。 (3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是 (填标号)。 A.无需分离 B.增大该反应平衡常数 C.起到沸石作用,防止暴沸 D.不影响甲基紫指示反应进程 乙酸与过量乙醇在一定温度下、硫酸氢钠作催化剂、甲基紫的乙醇溶液和变色硅胶作指示剂的条件下反应制取乙酸乙酯,用饱和碳酸钠溶液除去其中的乙酸至无二氧化碳逸出,分离出有机相、洗涤、加无水硫酸镁后过滤,滤液蒸馏时收集73~78 ℃馏分,得纯度为98.0%的乙酸乙酯6.60 g。 乙酸与过量乙醇在一定温度下、硫酸氢钠作催化剂、甲基紫的乙醇溶液和变色硅胶作指示剂的条件下反应制取乙酸乙酯,用饱和碳酸钠溶液除去其中的乙酸至无二氧化碳逸出,分离出有机相、洗涤、加无水硫酸镁后过滤,蒸馏滤液时收集73~78 ℃馏分,得6.60 g纯度为98.0%的乙酸乙酯。(1)该实验可实现乙酸乙酯的绿色制备及反应过程可视化,用浓硫酸时,浓硫酸的作用是作催化剂和吸水剂,所以NaHSO4在反应中起催化剂作用;浓硫酸还具有强氧化性和脱水性,用浓硫酸在加热条件下反应时,可能发生副反应,且浓硫酸的还原产物二氧化硫有毒,所以用其代替浓硫酸的优点是副产物少,可绿色制备乙酸乙酯,无有毒气体二氧化硫产生。(2)变色硅胶吸水,除指示反应进程外,还可吸收加热时生成的水,使平衡正向移动,提高乙酸乙酯的产率。(3)A.若向反应液中直接加入变色硅胶,则反应后需要过滤出硅胶,而使用小孔冷凝柱承载则无需分离,故A正确;B.反应的平衡常数只与温度有关,使用小孔冷凝柱承载不能增大该反应平衡常数,故B错误;C.小孔冷凝柱承载并没有投入溶液中,不能起到沸石作用,不能防止暴沸,故C错误;D.由题中“反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热”可知,若向反应液中直接加入变色硅胶,则变色硅胶由蓝色变为粉红色,会影响观察反应液由蓝色变为紫色,所以使用小孔冷凝柱承载不影响甲基紫指示反应进程,故D正确;故答案为AD。
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是 (填名称)。 (5)该实验乙酸乙酯的产率为 (精确至0.1%)。 (6)若改用OH作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为 (精确至1)。 (4)容量瓶用于配制一定物质的量浓度的溶液,分离有机相和洗涤有机相不需要容量瓶;漏斗用于固液分离,分离有机相和洗涤有机相不需要漏斗;分离液态有机相和洗涤液态有机相也不需要洗气瓶;分离有机相和洗涤有机相时均需使用的是分液漏斗。(5)由反应CH3COOH+CH3CH2OH CH3COOC2H5+H2O可知,100 mmol乙酸与150 mmol乙醇反应时,理论上可获得的乙酸乙酯的质量为0.1 mol×88 g·mol-1=8.8 g,则该实验乙酸乙酯的产率为×100%=73.5%。(6)若改用OH作为反应物进行反应,则因为OH CH3CO18OC2H5+H2O,生成的乙酸乙酯的摩尔质量为90 g·mol-1,所以质谱检测目标产物分子离子峰的质荷比数值应为90。 (1)催化剂 无有毒气体二氧化硫产生 (2)吸收生成的水,使平衡正向移动,提高乙酸乙酯的产率 (3)AD (4)分液漏斗 (5)73.5% (6)90
突破实验综合题的思路与方法 (1)巧审题,明确实验的目的和原理。实验原理遵循可靠性、简洁性、安全性的原则,确定符合实验目的、要求的方案。 (2)想过程,厘清实验操作的先后顺序。根据实验原理所确定的实验过程,确定实验操作的方法和步骤,把握各步实验操作的要点,厘清实验操作的先后顺序。 (3)看准图,分析各项实验装置的作用。认真细致地分析图中所示装置,并结合实验目的和原理,确定它们在实验中的作用。 (4)析问题,分析各个小题,确定问题的方向,结合所学知识回答问题。应注意答案的准确、规范。
命题角度 3年考题分布 考情预测
化学实验基本操作 2024·山东卷T6;2024·安徽卷T2;2024·湖北卷T3;2023·山东卷T4;2023·全国甲卷T9;2022·海南卷T2、T3;2022·湖南卷T4 化学实验基础是历年高考的必考内容,近几年高考试题多以论述形式、表格形式、装置图的形式出现,以中学化学所涉及的重要物质的性质为载体,突出考查基本仪器的使用、化学实验操作的规范性、物质的检验分离提纯、气体的制备等,试题常涉及物质的分离提纯,气体的制取、除杂、收集、尾气处理,溶液的配制等操作。试题考查点多,在稳定的基础上追求创新,题目具有较强的综合性。
“装置—目的”一致性判断 2024·广东卷T8;2024·甘肃卷T6;2023·北京卷T8;2023·湖南卷T3;2023·全国乙卷T9;2023·湖北卷T13;2022·湖北卷T6
“操作—现象—结论”一致性判断 2024·河北卷T6;2024·山东卷T12;2023·浙江6月卷T16;2023·新课标卷T11
综合实验分析 2024·黑吉辽卷T19;2024·甘肃卷T15;2024·湖南卷T16;2023·山东卷T18;2023·湖南卷T15;2022·湖北卷T16;2022·浙江6月卷T30
化学实验基本操作
高考真题 构建解题模型
(2023·山东卷,T4)实验室安全至关重要,下列实验室事故处理方法错误的是( ) A.眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗 B.皮肤溅上碱液,先用大量水冲洗,再用2%的硼酸溶液冲洗 C.电器起火,先切断电源,再用二氧化碳灭火器灭火 D.活泼金属燃烧起火,用灭火毯(石棉布)灭火 眼睛溅进酸液,先用大量水冲洗,边洗边眨眼,尽可能减少酸对眼睛的伤害,再用3%~5%的碳酸氢钠溶液冲洗,A错误;皮肤溅上碱液,应立即用大量水冲洗,再用2%的硼酸中和残余的碱,B正确;电器起火,先切断电源,再用二氧化碳灭火器灭火,C正确;活泼金属会与水反应,所以燃烧起火,用灭火毯(石棉布)灭火,D正确。 A
(2024·山东卷T6)下列图示实验中,操作规范的是( ) A.调控滴 定速度B.用pH试纸测定溶液pHC.加热试管 中的液体D.向试管中滴加溶液
A.调控酸式滴定管的滴加速度,左手拇指、食指和中指轻轻向内扣住玻璃活塞,手心空握,所以A选项的操作符合规范;B.用pH试纸测定溶液pH不能将pH试纸伸入溶液中,B操作不规范;C.加热试管中的液体,试管中液体体积不能超过试管体积的三分之一,C操作不规范;D.向试管中滴加液体,胶头滴管应该在试管上方竖直悬空,D操作不规范;故选A。 A
“装置—目的”一致性判断
高考真题 构建解题模型
(2024·广东卷T8)1810年,化学家戴维首次确认“氯气”是一种新元素组成的单质。兴趣小组利用以下装置进行实验。其中,难以达到预期目的的是( ) A.制备Cl2 B.净化、干燥Cl2 C.收集Cl2 D.验证Cl2的 氧化性 分析题干,明确实验目的分析装置,明确装置作用及适用条件分析选项,根据反应物状态及气体性质,进行解答。 A.利用浓盐酸和二氧化锰反应制氯气需要加热,图中缺少加热装置,且分液漏斗内应盛装浓盐酸,不能达到预期目的,A符合题意;B.实验室制得的氯气中有HCl杂质,可以通过饱和食盐水洗气除杂,再通过无水氯化钙干燥,可以达到净化、干燥Cl2的目的,B不符合题意;C.氯气密度大于空气,可以用向上排空气法收集,可以达到预期目的,C不符合题意;D.H2可以在氯气中安静地燃烧,产生苍白色火焰,氯气将氢气氧化,验证了氯气的氧化性,D不符合题意。 A
“操作—现象—结论”一致性判断
高考真题 构建解题模型
(2024·河北卷T6)下列实验操作及现象能得出相应结论的是( ) 选项实验操作及现象结论A还原铁粉与水蒸气反应生成的气体点燃后有爆鸣声H2O具有还原性B待测液中滴加BaCl2溶液,生成白色沉淀待测液含有CMg(OH)2和Al(OH)3中均分别加入NaOH溶液和盐酸,Mg(OH)2只溶于盐酸,Al(OH)3都能溶Mg(OH)2比 Al(OH)3碱性强DK2Cr2O7溶液中滴加NaOH溶液,溶液由橙色变为黄色增大生成物的浓度,平衡向逆反应方向移动
铁与水蒸气反应生成的气体是H2,该反应中H由+1价变成0价,被还原,体现了H2O的氧化性,A错误;如果待测液中含有Ag+,Ag+与Cl-反应也能产生白色沉淀,通过该实验不能得出待测液中含有的结论,B错误;Mg(OH)2溶液能与盐酸反应,不能与NaOH溶液反应,与NaOH溶液和盐酸都能反应,说明Mg(OH)2的碱性比Al(OH)3的强,C正确;K2Cr2O7溶液中存在平衡:(橙色(黄色)+2H+,加入NaOH溶液后,OH-与H+反应,生成物浓度减小,使平衡正向移动,导致溶液由橙色变为黄色,题给结论错误,D错误。 C
解答“操作—现象—结论”类实验题的操作步骤 第一步:明确题干要求,确定判断类别。首先判断题干要求的一致性关系,确定属于“因果关系型”“结论与操作相关型”“方法原理应用型”等的哪一类型。第二步:认真阅读表格要素,细研表格各栏目信息。(1)判断原理与现象或结论解释的关系。 (2)判断“目的—仪器—试剂”的合理性。 (3)判断“仪器(或用品)”与“实验”的对应性。 (4)判断“分离、提纯方法”与“原理”的合理性等。第三步:逐项判断,不遗漏任何信息。抓住操作、现象、数据等关键点,充分利用排除法、特例法等解题技巧,迅速作答。
高考真题 构建解题模型
(2024·黑吉辽卷T17)某实验小组为实现乙酸乙酯的绿色制备及反应过程可视化,设计实验方案如下: Ⅰ.向50 mL烧瓶中分别加入5.7 mL乙酸(100 mmol)、8.8 mL乙醇(150 mmol)、1.4 g NaHSO4固体及4~6滴1‰甲基紫的乙醇溶液,向小孔冷凝柱中装入变色硅胶。 Ⅱ.加热回流50 min后,反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热。 Ⅲ.冷却后,向烧瓶中缓慢加入饱和Na2CO3溶液至无CO2逸出,分离出有机相。 Ⅳ.洗涤有机相后,加入无水MgSO4,过滤。 Ⅴ.蒸馏滤液,收集73~78 ℃馏分,得无色液体6.60 g,色谱检测纯度为98.0%。 回答下列问题: (1)NaHSO4在反应中起 作用,用其代替浓硫酸的优点是 (答出一条即可)。 (2)甲基紫和变色硅胶的颜色变化均可指示反应进程。变色硅胶吸水,除指示反应进程外,还可 。 (3)使用小孔冷凝柱承载,而不向反应液中直接加入变色硅胶的优点是 (填标号)。 A.无需分离 B.增大该反应平衡常数 C.起到沸石作用,防止暴沸 D.不影响甲基紫指示反应进程 乙酸与过量乙醇在一定温度下、硫酸氢钠作催化剂、甲基紫的乙醇溶液和变色硅胶作指示剂的条件下反应制取乙酸乙酯,用饱和碳酸钠溶液除去其中的乙酸至无二氧化碳逸出,分离出有机相、洗涤、加无水硫酸镁后过滤,滤液蒸馏时收集73~78 ℃馏分,得纯度为98.0%的乙酸乙酯6.60 g。 乙酸与过量乙醇在一定温度下、硫酸氢钠作催化剂、甲基紫的乙醇溶液和变色硅胶作指示剂的条件下反应制取乙酸乙酯,用饱和碳酸钠溶液除去其中的乙酸至无二氧化碳逸出,分离出有机相、洗涤、加无水硫酸镁后过滤,蒸馏滤液时收集73~78 ℃馏分,得6.60 g纯度为98.0%的乙酸乙酯。(1)该实验可实现乙酸乙酯的绿色制备及反应过程可视化,用浓硫酸时,浓硫酸的作用是作催化剂和吸水剂,所以NaHSO4在反应中起催化剂作用;浓硫酸还具有强氧化性和脱水性,用浓硫酸在加热条件下反应时,可能发生副反应,且浓硫酸的还原产物二氧化硫有毒,所以用其代替浓硫酸的优点是副产物少,可绿色制备乙酸乙酯,无有毒气体二氧化硫产生。(2)变色硅胶吸水,除指示反应进程外,还可吸收加热时生成的水,使平衡正向移动,提高乙酸乙酯的产率。(3)A.若向反应液中直接加入变色硅胶,则反应后需要过滤出硅胶,而使用小孔冷凝柱承载则无需分离,故A正确;B.反应的平衡常数只与温度有关,使用小孔冷凝柱承载不能增大该反应平衡常数,故B错误;C.小孔冷凝柱承载并没有投入溶液中,不能起到沸石作用,不能防止暴沸,故C错误;D.由题中“反应液由蓝色变为紫色,变色硅胶由蓝色变为粉红色,停止加热”可知,若向反应液中直接加入变色硅胶,则变色硅胶由蓝色变为粉红色,会影响观察反应液由蓝色变为紫色,所以使用小孔冷凝柱承载不影响甲基紫指示反应进程,故D正确;故答案为AD。
(4)下列仪器中,分离有机相和洗涤有机相时均需使用的是 (填名称)。 (5)该实验乙酸乙酯的产率为 (精确至0.1%)。 (6)若改用OH作为反应物进行反应,质谱检测目标产物分子离子峰的质荷比数值应为 (精确至1)。 (4)容量瓶用于配制一定物质的量浓度的溶液,分离有机相和洗涤有机相不需要容量瓶;漏斗用于固液分离,分离有机相和洗涤有机相不需要漏斗;分离液态有机相和洗涤液态有机相也不需要洗气瓶;分离有机相和洗涤有机相时均需使用的是分液漏斗。(5)由反应CH3COOH+CH3CH2OH CH3COOC2H5+H2O可知,100 mmol乙酸与150 mmol乙醇反应时,理论上可获得的乙酸乙酯的质量为0.1 mol×88 g·mol-1=8.8 g,则该实验乙酸乙酯的产率为×100%=73.5%。(6)若改用OH作为反应物进行反应,则因为OH CH3CO18OC2H5+H2O,生成的乙酸乙酯的摩尔质量为90 g·mol-1,所以质谱检测目标产物分子离子峰的质荷比数值应为90。 (1)催化剂 无有毒气体二氧化硫产生 (2)吸收生成的水,使平衡正向移动,提高乙酸乙酯的产率 (3)AD (4)分液漏斗 (5)73.5% (6)90
突破实验综合题的思路与方法 (1)巧审题,明确实验的目的和原理。实验原理遵循可靠性、简洁性、安全性的原则,确定符合实验目的、要求的方案。 (2)想过程,厘清实验操作的先后顺序。根据实验原理所确定的实验过程,确定实验操作的方法和步骤,把握各步实验操作的要点,厘清实验操作的先后顺序。 (3)看准图,分析各项实验装置的作用。认真细致地分析图中所示装置,并结合实验目的和原理,确定它们在实验中的作用。 (4)析问题,分析各个小题,确定问题的方向,结合所学知识回答问题。应注意答案的准确、规范。
同课章节目录
